基于铈配合物信号探针的凝血酶电化学适体传感器
2023-10-19邹晓川黄远波邓明川
王 存 邹晓川 黄远波 胡 静 邓明川 冯 霞
(重庆第二师范学院生物与化学工程学院,重庆 400067)
0 引 言
凝血酶(TB)是一种丝氨酸蛋白酶,能够促进血液凝固,调节凝血功能,对揭示肿瘤发生机制、早期诊断和疗效具有重要意义[1-2]。由于血液中TB 的浓度非常低,检测困难,因此建立一种简单、快速、高灵敏度的TB 检测方法具有重要意义[3]。近年来,化学发光[4]、表面等离子体共振[5]、荧光[6]和电化学方法[7]等已被用于TB 的检测。然而,这些方法大多存在操作复杂、成本高、设备规模大、价格昂贵等问题。其中,电化学适体传感器因仪器小型化、成本低廉、响应迅速及灵敏度高等特点而备受关注。
电化学适体传感器有效结合了传感器的高灵敏度与生物识别的高特异性,能显著提高相关生物分子检测的灵敏度和选择性,在蛋白质检测和临床分析等研究中展现出广阔的应用前景[8]。信号探针的制备是电化学适体传感器应用推广的关键[9],然而传统信号探针的制备主要是以纳米材料如金属有机骨架(MOFs)、金属有机片层(MOLs)及一些碳纳米材料等作为支撑基质来固定信号分子(亚甲蓝、甲苯胺蓝或二茂铁等)。同时为进一步提高传感器的灵敏度,常需要酶和其他纳米材料标记[10]。然而,以上方法虽然可以在一定程度上放大信号,达到提高传感器灵敏度的目的,但不可避免地存在一些问题:(1)MOLs 比表面积相对较低,MOFs 孔径与信号分子尺寸不匹配,信号分子的固载量有限,甚至信号分子在检测过程中泄漏,导致传感器稳定性差[11];(2) MOFs 和MOLs 的配体一般为有机配体,具有一定的绝缘性,进而降低传感器的导电性[12];(3) 标记过程通常繁琐,特别是酶存在失活等问题[13]。因此,直接用于电化学适体传感器,且具有电化学活性的纳米材料的合成越来越受到关注。
配合物(COP)是一种多孔软杂化超分子材料,具有结构多样、孔隙可调、可设计和高比表面积等优点,被广泛应用于能源储存、气体吸附分离、催化等领域[3]。其中具有电化学活性的镧系配合物(Ln-COP)除具有上述优点外,还具有内在的氧化还原特性,能够直接用于电化学适体传感器的信号探针,因而备受关注[14]。如Zhang等[15]合成了用于色氨酸检测的壳聚糖负载的铈配合物(Ce-COP)。Ce-COP 合成方法绿色、经济、简便,同时壳聚糖和Ce-COP的结合不仅使修饰电极更加稳定,还可以防止Ce-COP 的聚积。然而,壳聚糖阻碍电子传递,传感器导电性差。Tu 等[16]采用简单、绿色的方法合成了一种还原氧化石墨烯(RGO)封装的Ce-COP 纳米复合材料。RGO 和Ce-COP 的结合显著提高了复合材料的导电性。因此,选择其他导电性好的功能材料如石墨烯[16]、碳纳米管[17]、金属纳米颗粒[18]等能够改善Ln-COP 的导电性,并推动其在适体传感器中的应用。
基于以上,我们以Ce3+为中心离子,N,N-二甲基甲酰胺(DMF)为有机配体,通过温度控制,合成了系列形貌不同和电化学信号不同的铈配合物(Ce-COPs)。筛选出电化学信号最强的多面体状Ce-COP,同时通过原位还原的方法将金(Au)纳米粒子包裹到Ce-COP表面形成Au@Ce-COP纳米复合材料。首先,Au 既起到改善Au@Ce-COP 导电性的作用,又起到固定TB 适体链(TBA)的作用;其次,电化学信号直接来自Ce-COP,电子在Ce3+和Ce4+之间转移,避免添加或标记其他氧化还原介质。最后,以Ce-COP 为信号探针,TB 为目标分析物,我们成功构建了一种用于TB 灵敏检测的适体传感器(图1)。结果表明,本工作中构建传感器具有检测限较低、线性范围较宽等优点,已经成功用于实际样品中TB高灵敏检测,有望为临床实际样品中TB的快速检测提供一个简单、高效的通用平台。
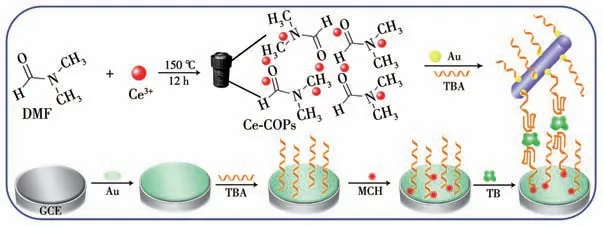
图1 Ce-COPs的制备及传感器构建过程Fig.1 Preparation of Ce-COPs and the biosensor construction process
1 实验部分
1.1 试剂与仪器
六水合硝酸铈(Ce(NO3)3·6H2O,99.99%)、DMF、凝血酶(TB,2 000 U·mg-1)和6-巯基-1-己醇(MCH,99%)购买于Sigma-Aldrich 公司(美国)。Na2HPO4、KH2PO4、四氯金酸(HAuCl4)和NaBH4购买于重庆钛新化工有限公司(中国)。不同pH 值的磷酸盐缓冲溶液(PBS,0.1 mol·L-1)由Na2HPO4和KH2PO4配制,支持电解质为0.1 mol·L-1KCl。0.1 mol·L-1pH 7.4 的Tris-HCl 缓冲液(包含140 mmol·L-1NaCl、5 mmol·L-1KCl 和1 mmol·L-1MgCl2)作为DNA 杂交和储存液。巯基修饰TBA(5′-GGTTGGTGTGGTTGGAGA AGAAGGTGTTTAAGTA-(CH3)6-SH-3′)购买于生工生物技术(上海)有限公司。实验用水为二次蒸馏水。
CHI660E 电化学工作站购自上海辰华仪器公司,三电极系统中工作电极为直径4 mm的玻碳电极(GCE),对电极为铂丝电极,参比电极为饱和甘汞电极。
1.2 系列Ce-COPs的制备[18]
系列Ce-COPs 制备过程如下:将0.434 4 mg Ce(NO3)3·6H2O加入到DMF/H2O(7∶3)混合溶液中,磁力搅拌30 min 得到均一透明溶液。将上述均一透明溶液转移到50 mL反应釜中,在烘箱中分别于90、120、150、180 和200 ℃下水热反应12 h。反应结束后,反应釜冷却至室温,离心收集产物并用DMF 和无水乙醇洗涤产物。最后在60 ℃烘箱中干燥,得系列Ce-COPs,不同温度合成样品分别记为Ce-COP-90、Ce-COP-120、Ce-COP-150、Ce-COP-180、Ce-COP-200。
1.3 Au@Ce-COP纳米复合材料的制备[19]
将1 mL 1%HAuCl4溶液迅速加入到2 mL Ce-COP(0.5 mg·mL-1)分散液中,持续搅拌30 min,然后加入1 mL NaBH4(0.1 mol·L-1,0 ℃)溶液,搅拌30 min,得Au@Ce-COP纳米复合材料。离心、洗涤后将Au@Ce-COP 重新分散于1 mL Tris-HCl 缓冲液中,4 ℃储存备用。
1.4 TBA/Au@Ce-COP复合物的制备
将100 μL TBA(4 μmol·L-1)加入到1 mL Au@Ce-COP(0.5 mg·mL-1)分散液中,4 ℃下搅拌至少16 h,TBA 通过Au—S 键作用固定到Au@Ce-COP 上。离心除去游离未结合的TBA,所得沉淀即为TBA/Au@Ce-COP 复合物。最后将TBA/Au@Ce-COP 重新分散于1 mL Tris-HCl缓冲液中,4 ℃储存备用。
1.5 TB适体传感器的构建
GCE(直径4 mm)依次用0.3和0.05 μm的氧化铝浆液反复抛光成镜面,然后依次用水和无水乙醇分别超声洗涤5次,室温晾干。为固定TBA,将晾干后的GCE浸入HAuCl4溶液(1%)中,-0.2 V电沉积30 s,得纳米金修饰的GCE(Au NPs/GCE)。蒸馏水冲洗电极之后,将10 μL TBA(2 μmol·L-1)滴涂至Au NPs/GCE 表面,4 ℃孵育过夜,通过Au—S 键将TBA 固定到Au NPs/GCE 表面。加入10 μL MCH(1 mmol·L-1)在4 ℃孵育30 min,封闭电极剩余的活性位点,记为TBA/Au NPs/GCE。随后,将10 μL 不同浓度目标物TB 标准溶液滴涂至TBA/Au NPs/GCE 表面,37 ℃孵育1 h。最后,将10 μL TBA/Au@Ce-COP 滴涂于上述电极表面,37 ℃孵育1 h后测其电化学信号。
1.6 表征仪器
主要仪器包括X 射线光电子能谱仪(XPS,ThermoFisher Scientific 公司,美国,单色AlKα(hν=1 486.6 eV),功率150 W,650 μm 束斑,电压14.8 kV,电流1.6 A)、S-4800 扫描电子显微镜(SEM,日立仪器有限公司,日本,加速电压20 kV,工作距离7.6 mm)、UNICUBE 有机元素分析仪(Elementar 公司,德国)、ICPoes730 电感耦合等离子光谱发生仪(ICP,Agilent 公司,美国,发射功率1.0 kW,载气为Ar,等离子气流量15 L·min-1,辅助气流量1.5 L·min-1,雾化器流量0.75 L·min-1)、D8 型X 射线衍射仪(XRD,布鲁克,德国,管电流40 mA,管电压40 kV,CuKα辐射,波长0.154 06 nm,扫描范围10°~80°,扫速6(°)·min-1)、托利多同步热分析仪TGA/DSC3+(梅特勒,美国,从室温升至600 ℃,升温速率10 ℃·min-1,气氛N2)。
1.7 电化学测试
循环伏安(CV)测试底液为0.1 mol·L-1PBS(pH 7.5),实验参数如下:初始电位-0.2 V,最高电位0.6 V,最低电位-0.2 V,最终电位0 V,扫描速率0.05 V·s-1,扫描4 圈,采样间隔0.001 V,静置时间2 s,灵敏度1×10-4A·V-1。电化学阻抗(EIS)测试底液为5 mmol·L-1[Fe(CN)6]3-/[Fe(CN)6]4-溶液,实验参数如下:频率范围0.012 12~1 000 Hz,电位幅度0.05 V,静止时间2 s。差分脉冲伏安(DPV)法测试底液为0.1 mol·L-1PBS(pH 7.5),实验参数如下:初始电位0 V,终止电位0.3 V,电位间隔0.004 V,电位幅度0.05 V,脉冲宽度0.016 7 s,脉冲周期0.2 s,静止时间2 s,选用的电流灵敏度为2×10-5A·V-1。
2 结果与讨论
2.1 系列Ce-COPs的表征
采用SEM 表征系列Ce-COPs 的形貌和尺寸。当水热温度由90 ℃逐渐变化到200 ℃时,Ce-COPs的形貌随之变化。如图2 所示,Ce-COP-90(图2a)、Ce-COP-120(图2b)、Ce-COP-150(图2c)、Ce-COP-180(图2d)、Ce-COP-200(图2e)的形貌分别为蜂窝状、四角星、棒状、多孔球状和不规则多面体状,其中Ce-COP-120 长约16 μm、厚约2 μm,Ce-COP-150 长约32.5 μm、厚约4 μm,Ce-COP-180 和Ce-COP-200 的直径分别约为0.2 和0.5 μm。此外,分别将Ce-COP-90、Ce-COP-120、Ce-COP-150、Ce-COP-180、Ce-COP-200 修饰到电极表面,发现Ce-COP-150 的电化学信号最强(图2f)。基于以上结果,选择Ce-COP-150 作为后续实验用材料。
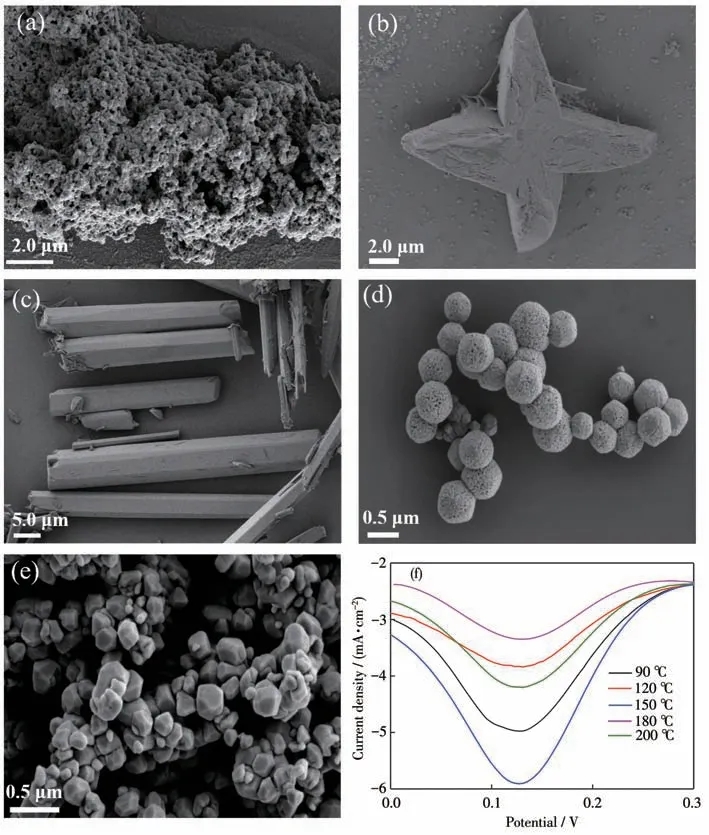
图2 (a)Ce-COP-90、(b)Ce-COP-120、(c)Ce-COP-150、(d)Ce-COP-180、(e)Ce-COP-200的SEM图;(f)不同温度下Ce-COPs的DPV曲线Fig.2 SEM images of(a)Ce-COP-90,(b)Ce-COP-120,(c)Ce-COP-150,(d)Ce-COP-180,and(e)Ce-COP-200;(f)DPV curves of Ce-COPs at different temperatures
ICP测试表明,Ce-COP-150中Ce的含量(质量分数)为42.51%,根据有机元素分析仪得出N、C和O的质量分数分别为0.09%、6.63%和14.82%。此外,采用能量色散X 射线光谱(EDX)表征Ce-COP-150 的组成,如图3 所示,Ce-COP-150 主要由C、N、O 和Ce 元素组成且各元素分布均匀。
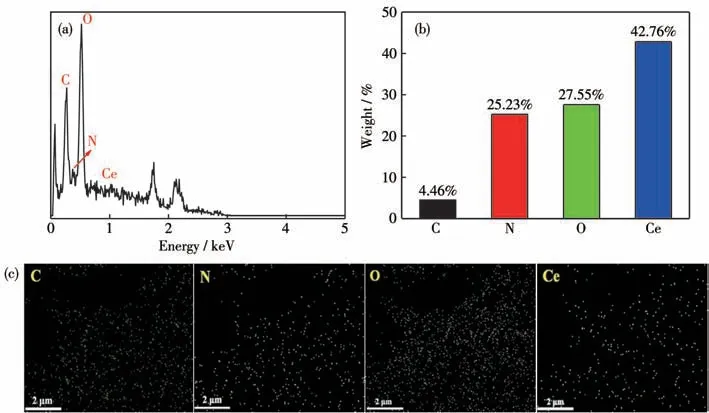
图3 Ce-COP-150的(a)EDX谱图和(b)元素含量及(c)元素分布图Fig.3 (a)EDX spectrum,(b)element contents,and(c)the elemental mapping images of C,N,O and Ce for Ce-COP-150
采用XPS 测定Ce-COP-150 的元素组成及其价态。如图4a 所示,284.3、399.2 和529.7 eV 处的峰分别对应C1s、N1s和O1s。由Ce3d谱图分峰可知(图4b),Ce-COP-150 表面存在Ce3+和Ce4+两种价态,且Ce4+面积占比较大,说明Ce 元素主要以+4 价为主,且Ce4+和Ce3+的比值约为1.7∶1。图4c 为Au@Ce-COP 纳米复合材料的XPS 谱图,由图可知,C、N、O、Ce 和Au 元素同时存在,表明Au@Ce-COP 纳米复合材料成功合成。XRD 图表明Ce-COP-150 的结晶度和晶体结构(图4d)相对较差,且与Ce(OH)3(PDF No.81-0792)和Ce2O3(PDF No.19-0284)标准卡差别较大。此外,采用FTIR 光谱研究Ce-COP-150 的组成。如图4e 所示,对于配体DMF,1 658 cm-1处为—C=O 伸缩振动,658 cm-1处为N—C=O 变形振动,1 503 cm-1处为N—C 伸缩振动,1 063 cm-1处为H—C=O 弯曲振动。然而,当Ce 与DMF 发生配位后,N—C=O 变形振动峰和H—C=O 弯曲振动峰消失,—C=O 伸缩振动和N—C 伸缩振动峰发生移动,这可能是Ce与N 和O 发生配位所致。结合XRD与FTIR 表征可知,Ce-COP-150 主要以配合物的形式存在。
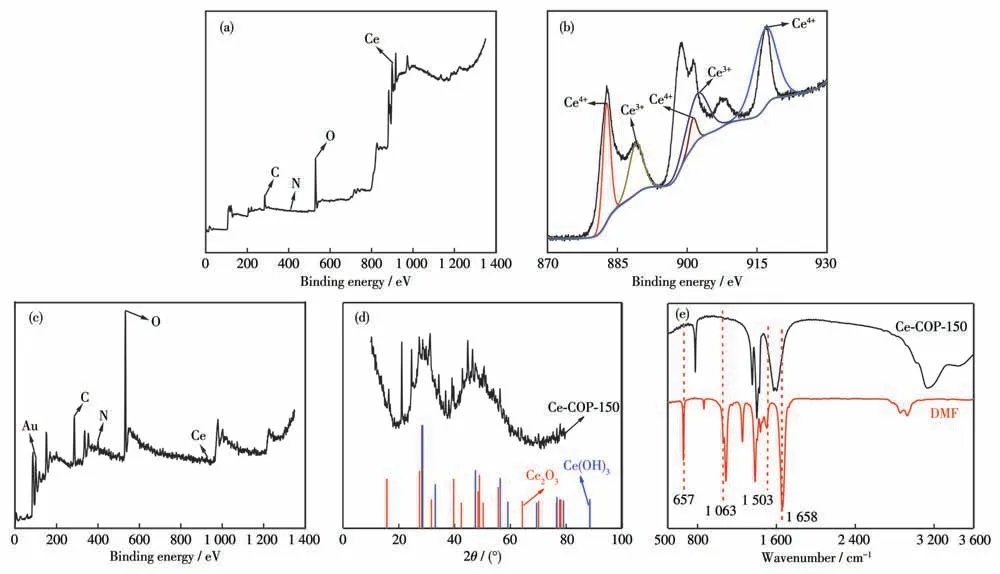
图4 Ce-COP-150的(a)XPS总谱图和(b)Ce3d谱图;(c)Au@Ce-COP-150的XPS总谱图;(d)Ce-COP-150的XRD图;(e)DMF和Ce-COP-150的FTIR谱图Fig.4 (a)XPS survey spectrum and(b)Ce3d spectrum for Ce-COP-150;(c)XPS survey spectrum for Au@Ce-COP-150;(d)XRD pattern for Ce-COP-150;(e)FTIR spectra of DMF and Ce-COP-150
采用热重分析法测试Ce-COP-150的热稳定性。如图5 所示,由热重(TG)和热重微分(DTG)曲线可知,Ce-COP-150 的初始分解温度为204.5 ℃,表明其具有一定的热稳定性。
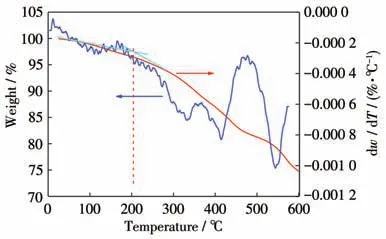
图5 Ce-COP-150的TG和DTG曲线Fig.5 TG and DTG curves of Ce-COP-150
2.2 修饰电极组装过程的表征
采用CV 和EIS 表征电极的组装过程。如图6A所示,当电极表面沉积Au NPs 后,其峰电流值(曲线b)相较于裸GCE(曲线a)明显增大,主要归功于Au NPs 增加了电极的有效比表面积,加快了电子的传递速率。当TBA(曲线c)、MCH(曲线d)、TB(曲线e)和TBA/Au@Ce-COP-150(曲线f)分别修饰到电极表面时,传感器峰电流值依次下降,主要归因于DNA 适体链、蛋白质及配合物阻碍了电子传递。图6B为电极组装过程的EIS 表征。EIS 中半圆直径大小对应电子转移电阻(Ret)。如图所示,Au NPs 修饰GCE 的Ret(曲线b)小于裸GCE 的Ret(曲线a)。当TBA(曲线c)、MCH(曲线d)、TB(曲线e)和TBA/Au@Ce-COP-150(曲线f)分别修饰到电极表面时,Ret值依次增大。EIS 表征结果与CV 曲线一致,表明传感器构建成功。
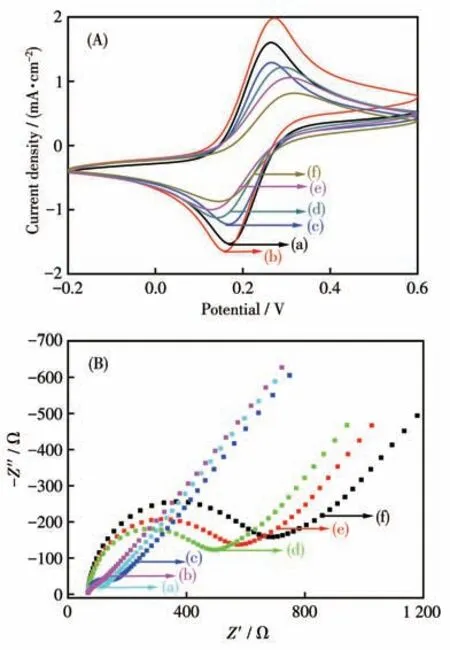
图6 传感器组装过程的(A)CV曲线和(B)EISFig.6 (A)CV curves and(B)EIS on the biosensor assembly process
2.3 TBA在Au NPs/GCE的表面覆盖量
在5 mmol·L-1Fe(CN)63-/Fe(CN)64-溶液中,采用CV 法分别在10、20、30、50、80、100、120、150、180、200、220、250、280、300 和320 mV·s-1扫速下研究Au NPs/GCE 的有效比表面积(A)。如图7A、7B 所示,根据Randles-Sevcik 方程[20],Au NPs/GCE 的有效比表面积为11.5 mm2。
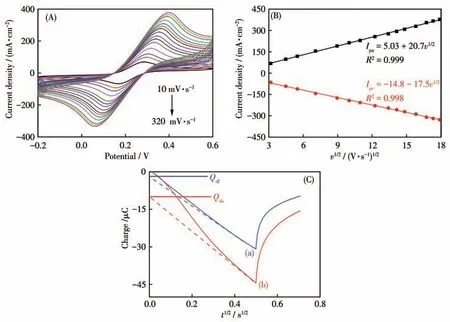
图7 (A)不同扫速下Au NPs/GCE在5 mmol·L-1 Fe(CN)63-/Fe(CN)64-溶液中的CV曲线;(B)Au NPs/GCE的阳极和阴极峰电流值与扫描速率平方根的线性关系;(C)不存在(曲线a)和存在(曲线b)5 0 μmol·L-1氯化六氨合钌时TBA/Au NPs/GCE 的计时电量曲线Fig.7 (A)CV curves of Au NPs/GCE in 5 mmol·L-1 Fe(CN)63-/Fe(CN)64-at different scan rates;(B)Linear relations of the Au NPs/GCE with the anodic and cathodic peak currents against the square root of scan rate;(C)Representative chronocoulometric curves for TBA/Au NPs/GCE in the absence(curve a)and presence(curve b)of 50 μmol·L-1 hexaammineruthenium(Ⅲ)chloride
其中,Ip为图7a 中不同扫速的下CV 峰电流值(mA·cm-2),n为氧化还原反应过程中电子转移的量,D为扩散系数(25 ℃,(6.70±0.02)×10-6cm2·s-1),c为Fe(CN)63-/Fe(CN)64-溶液浓度,v为扫速(mV·s-1)。
电荷补偿量与DNA 中碱基的数量直接相关,因此TBA 在Au NPs/GCE 上的表面覆盖量可以通过计时电量法求出。图7C为TBA/Au NPs/GCE 在不含有(曲线a)和含有(曲线b)50 μmol·L-1氯化六氨合钌的Tris-HCl 缓冲溶液中(10 mmol·L-1,pH 7.4)的电量曲线,电位范围-0.5~0.2 V。根据Cottrell 方程[21],TBA在Au NPs/GCE 上的表面覆盖量(ГTBA)为3.87×1016mol·cm-2。具体计算过程如下:
计时电量法测得的电量(Q)为时间t的函数:
其中n为电子转移数,F是法拉第常数(96 485 C·mol-1),A为Au NPs/GCE 的有效比表面积(cm2),Do为氯化六氨合钌的扩散系数(cm2·s-1),co*为氯化六氨合钌的浓度(mol·cm-2),Qdl为电容电量(C),nFAГo为电极表面吸附的氧化还原标记物还原的法拉第分量,Гo为表面过剩浓度或表面余量(mol·cm-2),表示限制在电极表面的氯化六氨合钌的量。t=0 时,计时库仑电量为双层电荷和表面余量之和。在氯化六氨合钌存在和不存在条件下,表面余量是由图7c中纵坐标截距的差值确定:
其中,Qdl和Qds分别为氯化六氨合钌存在和不存在时的电容电量。
氯化六氨合钌饱和的电极表面余量与DNA 表面密度的关系如下:
其中ГTBA为TBA 在Au NPs/GCE 的表面覆盖量(mol·cm-2),z为六氨合钌电荷,m为TBA中的碱基数量,NA为阿伏伽德罗常数。
2.4 可行性实验
为考察传感器检测TB的可行性,研究了传感器在存在和不存在TB 时的电化学响应。如图8 所示,当传感器没有孵育TB(曲线a)时,传感器无电化学响应峰,这主要是由于信号探针Ce-COP-150不能被引入到电极表面。相反,当传感器孵育不同浓度TB时,在0.127 和0.257 V 可以观察到一对明显的氧化还原峰,且随着目标物浓度由0.1 pmol·L-1增大到1.0 pmol·L-1,相应的峰电流也随之增强(曲线b和c)。这表明由于TB 与TBA 之间的特异性识别作用,随着TB 的浓度增加,引入到电极表面的信号探针Ce-COP-150 的量也随之增加,导致传感器电化学响应峰电流增强。以上结果表明,本方法可用于TB的灵敏和特异性检测。
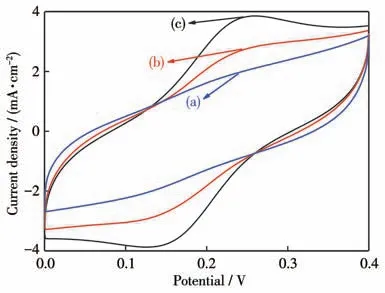
图8 在0.1 mol·L-1 PBS(pH 7.5)中(a)不存在和存在(b)0.1 pmol·L-1和(c)1.0 pmol·L-1 TB时传感器的CV响应Fig.8 CV responses of the biosensor in the(a)absence and presence of(b)0.1 pmol·L-1 and(c)1.0 pmol·L-1 TB in 0.1 mol·L-1 PBS(pH 7.5)
2.5 适体传感器的性能分析
由于差分脉冲伏安法(DPV)比CV 法具有更高的灵敏度,因此实验采用DPV 对不同浓度的TB 进行测定,结果如图9 所示。在最佳实验条件下(图9a),随着TB 浓度的增加,传感器峰电流值逐渐增大(图9b)。在1.0 fmol·L-1~1.0 nmol·L-1(0.1 fmol·L-1、1 fmol·L-1、10 fmol·L-1、0.1 pmol·L-1、1 pmol·L-1、10 pmol·L-1、0.1 nmol·L-1、1 nmol·L-1、10 nmol·L-1)浓度范围内,峰电流值与TB 浓度的对数成正比(图9c),线性方程为Ip=-11.61-0.320lgc(R=0.994),检测限为0.94 fmol·L-1。此外,与文献相比(表1),本文中构建的传感器具有相对较低的检测限和较宽的线性范围。
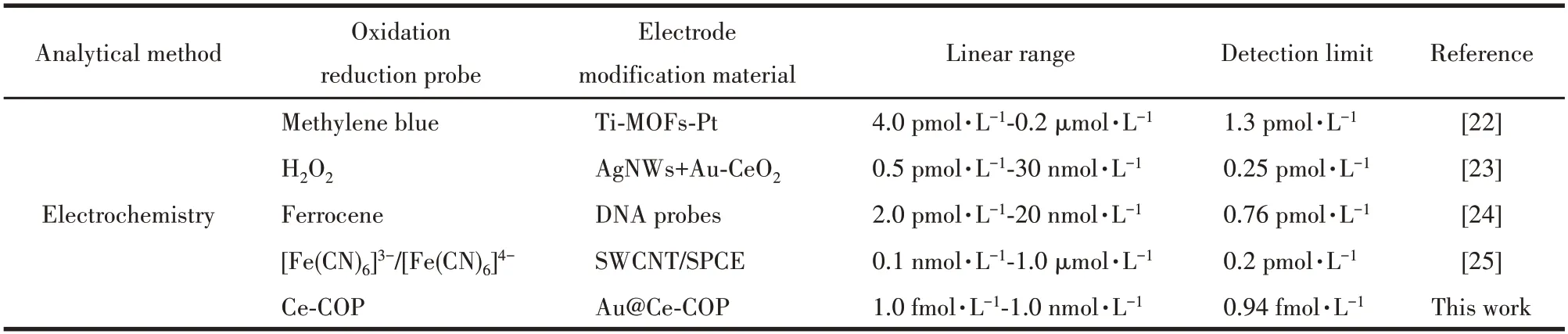
表1 TB检测方法比较Table 1 Comparison of TB detection methods
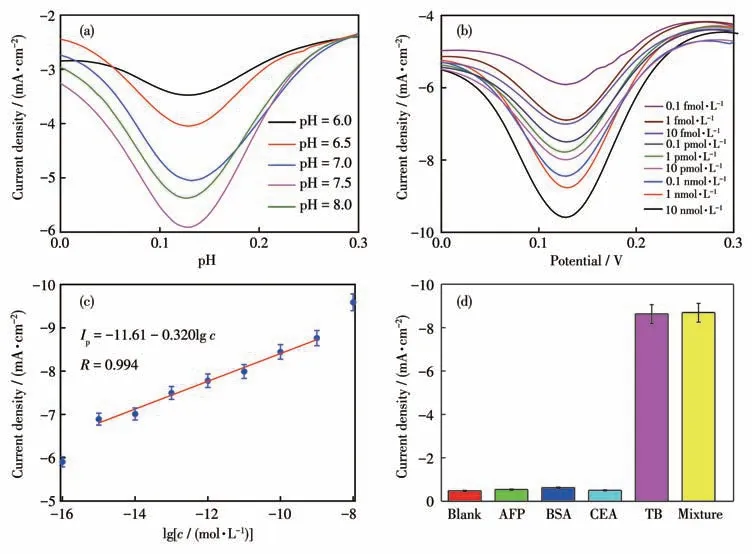
图9 (a)pH的影响;(b)生物传感器对不同浓度TB的DPV响应曲线;(c)峰电流值与相应TB浓度对数值的线性关系曲线;(d)传感器抗干扰能力Fig.9 (a)Effect of the pH;(b)DPV response curves of the biosensor with various concentrations of TB;(c)Linear relationship curve between peak current value and corresponding TB concentration logarithmic value;(d)Anti-interference ability
2.6 传感器的抗干扰能力和稳定性
抗干扰能力和稳定性是评估生物传感器性能的重要因素。因此,通过检测潜在干扰物质(10 pmol·L-1,目标物浓度的100 倍),如甲胎蛋白(AFP)、牛血清蛋白(BSA)和癌胚抗原(CEA)等其他蛋白来评估传感器的选择性,结果如图9d 所示,干扰物质与空白DPV 信号强度接近。然而,当目标物TB(0.1 pmol·L-1)孵育到电极表面,DPV 信号值远高于干扰物质和空白信号值。此外,目标物TB和干扰物组成的混合物的DPV 信号值与目标TB 的信号值接近。这表明开发的TB 适体传感策略具有高的选择性。传感器不用时将其盖帽储存(4 ℃)5 和10 d 后,传感器峰电流值仅分别下降0.3%和1.5%,相对标准偏差(RSD)分别为0.3%和0.5%。同时,同一只电极连续测量8 次后,传感器峰电流值没有明显变化,RSD为1.7%。以上表明,该传感策略具有相对较好的稳定性。
2.7 实际样品分析
为了评估本文中提出的传感器在临床应用的可行性,将制备的适体传感器用于检测人血清中TB的含量,患者血清来自重庆市第九人民医院。采用本实验方法和TM ELISA 试剂盒方法同时检测患者血清中TB 含量,结果如表2 所示。由表可知,本方案方法与商品TM ELISA 试剂盒检测结果相近,表明构建的生物传感器在临床分析中具有良好的应用潜力。
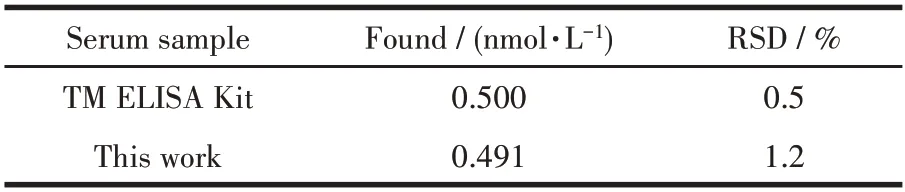
表2 不同检测方法的对比Table 2 Comparison of different detection methods
3 结 论
通过水热法成功合成了系列不同形貌和电化学信号不同的铈配合物(Ce-COPs)。传感器电化学信号直接源自Ce-COPs 内在的氧化还原特性,电子在Ce3+和Ce4+之间转移。同时,通过原位还原的方法将金纳米粒子包裹到Ce-COPs 表面,不仅改善了其导电性,还可以避免添加或标记其他氧化还原介质。通过TB 与TBA 之间的高特异性识别作用,成功实现了TB的高效、灵敏、准确检测。此外,人血清样品中TB实验表明,该传感器有望为临床血液样品中TB的检测提供参考和借鉴。
