急性淋巴细胞白血病患儿化疗相关性口腔黏膜炎的风险预测模型构建与验证
2023-10-18何小凤梁丽婵孟江南廖小妹王为杰黄佳颖张静史蕾
何小凤 梁丽婵 孟江南 廖小妹 王为杰 黄佳颖 张静 史蕾
(1.南方医科大学护理学院,广东 广州 510515;2.南方医科大学珠江医院儿科,广东 广州 510260;3.南方医科大学南方医院儿科,广东 广州 510515)
急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)为儿童最常见的恶性肿瘤[1],化疗是最主要的治疗手段[2],但20.00%~72.55%的ALL患儿会继发化疗相关性口腔黏膜炎(chemotherapy-induced oral mucositis,CTOM),为最常见的口腔并发症[3-5]。研究指出,血液系统肿瘤患儿相比其他肿瘤患儿化疗后发生口腔黏膜炎的概率高7.0~7.1倍[6],而ALL作为儿童血液系统肿瘤中占比最多的类型[6],ALL患儿的CTOM发生状况更值得关注。ALL患儿发生CTOM,易导致患儿继发感染,不仅影响正常化疗进程,严重者甚至危及生命[7-8]。同时,口腔黏膜炎会引起患儿口腔疼痛、吞咽障碍、进食困难,致使患儿出现不同程度的营养不良,且疼痛带来的不适,也会影响患儿的情绪健康[9]。早期识别高危人群并采取针对性预防措施,对于降低ALL患儿CTOM的发生率具有重要意义。风险预测模型能帮助医护人员早期识别高危人群、针对个体化危险因素实施预防干预[10],但目前鲜见适用于ALL患儿的CTOM风险预测模型。因此,本研究旨在构建并验证ALL患儿CTOM风险预测模型,以期为医护人员提供评估实用工具,为制定个性化干预措施提供参考。
1 对象与方法
1.1研究对象 采取便利抽样法,选择广东省2所三甲医院的470例ALL患儿为研究对象。将2020年1月-2022年4月一所广东省三甲医院收治的376例ALL患儿作为建模组,将2021年12月至2022年7月另一所广东省三甲医院收治的94例ALL患儿作为验证组。纳入标准:(1)患儿符合国际公认的儿童ALL诊断标准。(2)年龄0~18岁。(3)根据世界卫生组织发布的口腔黏膜炎分度标准确定患儿化疗前未发生口腔黏膜炎[11]。(4)病历资料完整。(5)患儿照顾者具备沟通能力,知情同意。(6)患儿照顾者为主要照顾者,知晓患儿的口腔卫生及进食情况。排除标准:(1)患儿合并其他肿瘤。(2)患儿合并重要器官严重疾病。样本量计算:采取logistic回归因变量事件数法[12],即因变量发生数应不少于模型中纳入的自变量乘以的倍数,本研究模型中纳入的自变量乘以的倍数取10,预计进入模型的自变量个数为10个,ALL患儿CTOM发生率根据文献调研结果取46%[3],考虑到15%的失访率,则模型构建至少需要样本量257例。根据风险预测模型外部验证样本量一般为建模组样本量的1/4~1/2[13],考虑到15%的失访率,模型外部验证至少需要样本量为76例。最终,纳入建模组样本量为376例,验证组样本量为94例。研究经南方医科大学伦理委员会审批,批件号(审批号:南医伦审[2022]第011号)。
1.2方法
1.2.1研究工具 根据前期系统评价结果,咨询相关专家,制作ALL患儿发生CTOM的影响因素调查表,包括:(1)一般人口学资料:患儿确诊时的年龄、性别、父亲受教育程度、母亲受教育程度、家庭月收入。(2)营养指标:此次化疗(指纳入研究的此次化疗)前年龄别身体质量指数(body mass index for age Z-score,BAZ)(取化疗前最近的一次测量值)。(3)病情及化疗资料:临床危险度分型、免疫学分型、患病时长、此次化疗是否同时伴随中枢或外周疾病、治疗阶段、是否复发、化疗周期、此次化疗药物是否含甲氨蝶呤(methotrexate,MTX)/柔红霉素(daunorubicin,DNR)/阿糖胞苷(cytarabine,Ara-C)。(4)血液生化指标:确诊时白细胞计数、此次化疗前白细胞计数、红细胞计数、血红蛋白计数、血小板计数、中性粒细胞计数(取化疗前1 d的值)。(5)微生物资料:既往或此次化疗是否携带单纯疱疹病毒1型(herpes virus type 1,HSV-1)、是否感染白色念珠菌。(6)口腔及进食资料:此次化疗前每天进行预防性漱口的频率(取化疗前平均每天使用漱口水漱口的频率值)、此次化疗每天进食的次数、此次化疗每天进食的主要食物类型、此次化疗使用的牙刷类型、既往有无口腔黏膜炎、龋齿、牙周炎、牙龈炎史。
1.2.2相关定义 (1)口腔黏膜炎分度标准:根据世界卫生组织发布的口腔黏膜炎分度标准[11]。0度:黏膜正常;Ⅰ度:黏膜红斑、疼痛,不影响进食;Ⅱ度:黏膜红斑明显,疼痛加重,散在溃疡,能进食半流质;Ⅲ度:黏膜溃疡及疼痛比Ⅱ度明显,只能进流质;Ⅳ度:疼痛剧烈,溃疡融合成大片,不能进食。(2)BAZ:计算公式为(BMI实测值-数据中位数)/数据标准差,BAZ<-2为消瘦,-2≤BAZ<2为正常,2≤BAZ<3为超重,≥3为肥胖[14]。
1.3资料收集 本科室医生记录患儿发生口腔黏膜炎的部位、程度,事先经过统一培训的不知情的第3方研究人员完成对患儿口腔黏膜炎的分度判断。由经过统一培训的研究人员收集患儿的病历资料,针对住院或居家的ALL患儿分别采用现场调查或电话随访的方式收集患儿的口腔卫生及进食情况资料。

2 结果
2.1ALL患儿的一般资料及CTOM发生情况 470例ALL患儿年龄4(3,7)岁,男289例,女181例,临床危险度分型低危(IR)252例,中危(SR)96例,高危(HR)122例。470例ALL患儿发生CTOM 212例,发生率为45.1%,其中Ⅰ度138例,Ⅱ度43例,Ⅲ度14例,Ⅳ度17例。
2.2ALL患儿发生CTOM的单因素分析 将建模组376例ALL患儿分为发生CTOM组和未发生CTOM组,单因素分析结果见表1。

表1 ALL患儿发生CTOM的危险因素单因素分析
2.3ALL患儿发生CTOM的多因素分析 多因素分析结果显示化疗周期≥5个疗程、携带HSV-1、感染白色念珠菌、此次化疗药物含MTX/DNR/Ara-C、临床危险度为HR、年龄≥6岁、此次化疗前每天进行预防性漱口的频率≥3次为影响因素,变量赋值结果见表2,分析结果见表3。

表2 多因素回归分析变量赋值表
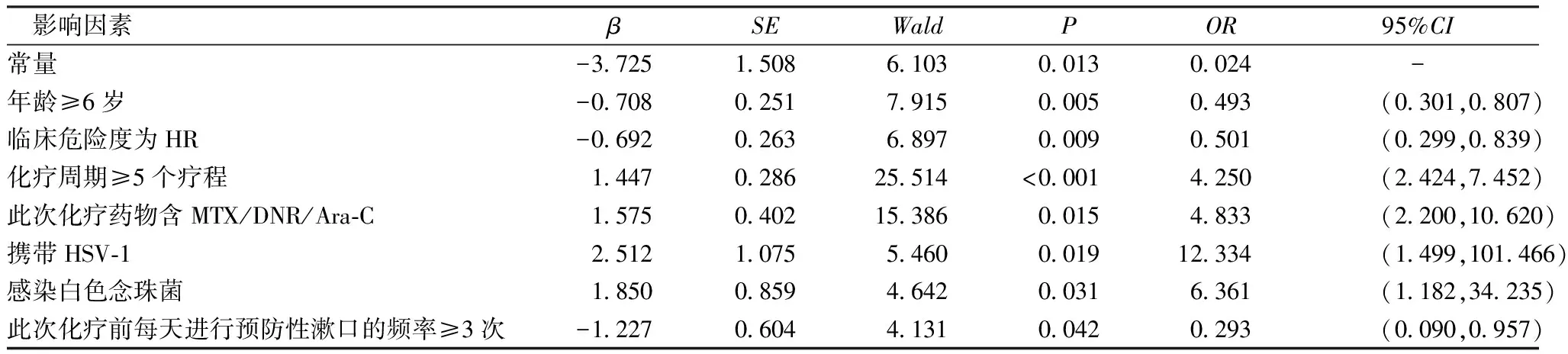
表3 ALL患儿发生CTOM的危险因素多因素logistic回归分析
2.4ALL患儿CTOM风险预测模型的构建与验证 基于logistic回归分析结果构建风险预测模型,可得logit(P)=-3.725+1.447×化疗周期(≥5个疗程)+2.512×携带HSV-1+1.850×感染白色念珠菌+1.575×此次化疗药物含MTX/DNR/Ara-C-0.682×临床危险度为HR-0.708×此次化疗前每天进行预防性漱口的频率(≥3次)-1.227×年龄(≥6岁),建模组的C统计量为0.769(95%CI:0.729~0.822),约登指数最大值为0.409,灵敏度59.9%,特异度81.0%,内外部验证的C统计量分别为0.772(95%CI:0.725~0.819)和0.865(95%CI:0.789~0.941),C统计量>0.7,模型区分度较好[15]。研究[16]表明,Brier值越小,模型的一致性越好,校准曲线内部验证Brier值0.194,外部验证0.150,拟合良好,模型具有良好的一致性。风险预测模型验证校准曲线图,见图1和图2。
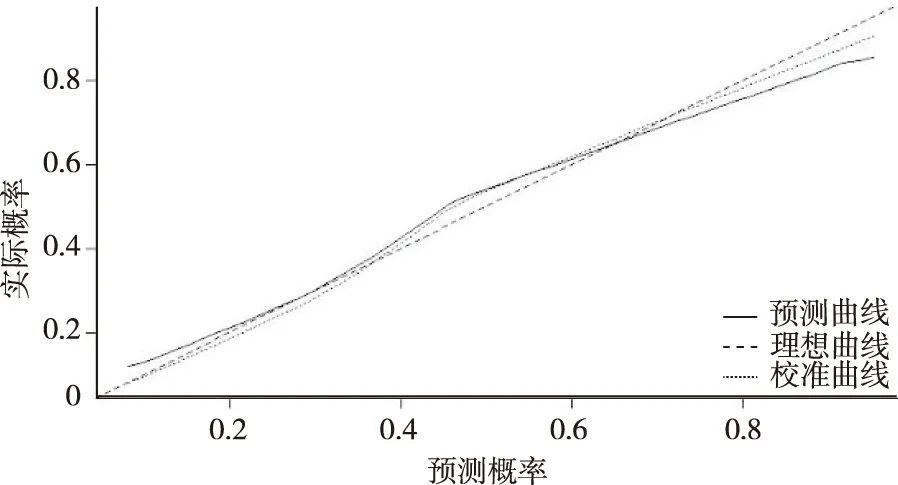
图1 风险预测模型内部验证校准曲线图

图2 风险预测模型外部验证校准曲线图
2.5ALL患儿CTOM风险预测模型的临床可用性评价 构建的ALL患儿CTOM风险预测模型外部验证DCA图,见图3。图3显示在0.00~0.85的阈值范围内不靠近两种极端情况线(全干预、全不干预),具有正的净获益,表明模型具有一定的临床可用性。

图3 风险预测模型外部验证DCA图
3 讨论
3.1ALL患儿CTOM的发生状况 本研究调查发现ALL患儿CTOM的发生率为45.1%,与Figliolia等[3](46%)和Devi等[17]的(48.7%)研究结果相近,高于Murshid等[18](23.3%)和Azher等[19](20%)研究结果,原因可能与Murshid等和Azher等研究仅纳入了处于诱导缓解期的ALL患儿,而本研究纳入了处于不同治疗阶段的ALL患儿有关。提示在化疗期ALL患儿CTOM发生率较高,应予以充分重视。
3.2ALL患儿发生CTOM的影响因素分析
3.2.1年龄≥6岁 本研究发现相比年龄<6岁的ALL患儿,年龄≥6岁的ALL患儿更不易发生CTOM,与Figliolia等[3]的研究结果一致。原因可能在于年龄越小的患儿口腔黏膜组织细胞有丝分裂率更高,使用细胞毒性化疗药物致使正常口腔黏膜组织细胞凋亡更多。提示应加强关注年龄<6岁的ALL患儿的口腔状况,及早评估,制定个性化口腔护理方案。
3.2.2临床危险度为HR 本研究发现,相比临床危险度为IR的患儿,HR的患儿化疗后更不易发生口腔黏膜炎,与以往研究[18]结果存在差异,原因可能在于尽管临床危险度为HR患儿使用的化疗药物剂量、浓度会高于IR的患儿,但是临床医护人员会加强对其的监测,化疗前水化用量也会加大,一定程度上避免了CTOM的发生。提示对于临床危险度为IR的ALL患儿应加强重视,化疗前制定血药浓度监测计划,加强口腔护理强度和频率。
3.2.3化疗周期≥5个疗程 本研究结果显示,相比化疗疗程1~2次的ALL患儿,化疗周期≥5个疗程的ALL患儿更易发生CTOM。可能与化疗疗程越长,患儿使用的化疗药物的种类越多,毒性作用更为突出有关[20]。除此之外,化疗疗程越长,ALL患儿发生骨髓抑制的可能性也会越大,也是原因之一[21]。提示对于化疗周期≥5个疗程的ALL患儿,应加强血药浓度监测,及时解救。同时,应密切关注患儿的血象情况,提升免疫力。
3.2.4化疗药物含MTX/DNR/Ara-C 本研究结果发现,化疗药物含MTX/DNR/Ara-C是ALL患儿发生CTOM的危险因素,以往研究[20]多关注ALL患儿使用MTX后发生口腔黏膜的毒性作用,本研究发现DNR和Ara-C同样也会导致ALL患儿发生CTOM。MTX和Ara-C同属于广谱类抗肿瘤药物,在杀灭肿瘤细胞的同时也会对正常组织细胞造成伤害,尤其对于增殖速度快的组织细胞伤害最大,口腔黏膜组织细胞增殖速度快,因此使用MTX和Ara-C化疗药物易导致口腔黏膜炎[20]。DNR使用时也会对正常口腔黏膜组织细胞造成损害,导致口腔黏膜炎的发生[22]。提示对于使用上述化疗药物的ALL患儿,在诊疗过程中应充分考虑其对口腔黏膜的损害作用,严格控制好用量和频率,充分水化,加强监测。
3.2.5携带HSV-1和感染白色念珠菌 本研究发现,携带HSV-1会引发ALL患儿发生CTOM,与以往研究[23-24]结果相同。HSV-1主要定殖于口腔,是口腔中最为常见的病毒,通常处于潜伏状态,而ALL患儿化疗后免疫力极为低下,容易激活HSV-1,引发口腔黏膜炎[23-24]。除此之外,化疗期间患儿进食、饮水减少,口腔环境干燥,分泌唾液量减少,加之使用广谱抗生素,口腔内环境被破坏,也是携带HSV-1引发ALL患儿发生CTOM的重要原因[17]。本研究发现感染白色念珠菌也是ALL患儿发生CTOM的危险因素,与以往的研究[23]结果一致。白色念珠菌为口腔内最为常见的定殖真菌,在机体免疫力低下时,易引发口腔黏膜炎[23]。提示临床医护人员在ALL患儿正式进行化疗前,应系统评估患儿的HSV-1和白色念珠菌感染情况,尽早采取干预措施,例如预防性使用抗菌、抗病毒药物[25-26]。
3.2.6化疗前预防性漱口频率≥3次 本研究发现,相比化疗前预防性漱口频率<1次的ALL患儿,化疗前预防性漱口频率≥3次的ALL患儿更不易发生CTOM。与Murshid等[18]和Devi等[17]的研究结果一致。口腔清洁情况不佳的患儿,食物残渣容易积留在牙齿缝隙中,对口腔微生物入侵产生负向的协同影响作用,化疗前预防性漱口可以帮助维持口腔良好的清洁度,预防口腔黏膜炎的发生[17]。提示临床医护人员和患儿照顾者应充分重视预防性漱口的重要性,督促患儿使用漱口水漱口,同时,注意应当让漱口水与口腔黏膜充分接触,漱口时间不宜过短。
3.3本研究构建的风险预测具有良好的预测效能 早期识别ALL患儿发生CTOM的高危人群并进行及早干预,对于降低CTOM发生风险、促进患儿化疗疗程的顺利进行、提升治疗效果具有重要意义。但目前,对于ALL患儿发生CTOM的评估多采用口腔黏膜炎分度标准,仅能判断发生CTOM的程度。本研究前期通过系统评价全面地获取ALL患儿发生CTOM的危险因素,并咨询相关专家,选取包含主客观指标、临床易获取、不会对患儿造成伤害的危险因素指标构建风险预测模型,能够真实反映ALL患儿发生CTOM的状况。结果显示,构建的模型具有良好的区分度、一致性以及一定的临床可用性,可以有效预测ALL患儿发生CTOM的风险概率。
综上所述,ALL患儿CTOM发生率较高,构建的风险预测模型具有良好的预测效能,可用于早期识别高危人群,医护人员应针对ALL患儿发生CTOM的影响因素进行早期评估,尽早采取针对性措施。本研究尚存在一定局限性:(1)本研究为回顾性分析,可能存在选择偏倚和信息偏倚。(2)因条件受限,本研究未纳入基因、细胞因子数据。(3)本研究仅回顾性收集广东省内2家三甲医院的病历资料。未来研究可尝试进行前瞻性的队列研究,发现更多可能的危险因素,纳入基因和细胞因子数据进行分析,收集多中心、大样本的数据进行分析,提高模型的预测效能。
