傅克烷基化法制备β-苯乙醇的工艺研究
2023-10-17赵松芳刘永新张奥文刘景辉胡国勤
赵松芳 , 刘永新 , 张奥文 , 刘景辉 , 胡国勤*
(1.三门峡奥科化工有限公司 , 河南 三门峡 472123 ; 2.郑州大学 化工学院 , 河南 郑州 450001)
β-苯乙醇作为一种芳香醇,常用作化妆品等调味剂。当其被配制成低浓度(体积浓度≤1%)时,可用作抗菌防腐剂。此外,其还可以作为医药、化工中间体或底物合成附加值更高的化合物[1-3]。
β-苯乙醇的制备方法主要包括化学合成法、物理提取法以及生物转化法。物理提取法得到的产品为天然产品,提取工艺绿色环保,但原料来源范围较窄,提取成本较高。生物转化法制备的β-苯乙醇也具有天然属性,环境污染小,但生产周期较长,生物合成活性逐渐丧失,产量低,远远不能满足市场需求,而化学合成法可以克服物理提取法和生物转化法的不足且易工业化。本文拟通过化学合成法制备β-苯乙醇。
化学合成法制备β-苯乙醇的工艺路线主要有两种:①以苯和环氧乙烷为原料,采用傅克反应法制备目标产物,该路线原料简单易得,反应条件和操作流程简单,产率较高,适合规模化生产。②以苯乙烯为原料,双氧水为氧化剂,乙腈为溶剂氧化,采用先氧化再加氢的方法制备目标产物,该路线流程复杂、副产物较多,成本高[4]。因此本文拟采用傅克反应法,以苯和环氧乙烷为原料制备β-苯乙醇。
1 实验部分
1.1 主要仪器与试剂
LC-20AD型液相色谱仪,岛津企业管理有限公司;600 MHz型核磁共振波谱仪,德国布鲁克公司;DFY-5/80 ℃型低温恒温反应浴,郑州宇祥仪器有限公司;Nicolet Is5型傅里叶红外光谱仪,美国赛默飞世尔科技有限公司。
苯,分析纯,郑州派尼化学试剂厂;环氧乙烷,98.5%,河南华文化工有限公司;三氯化铝,分析纯,天津市恒兴化学试剂制造有限公司;苯乙醇,99%,上海麦克林生化科技公司。
1.2 实验原理
苯和环氧乙烷在固体路易斯酸(三氯化铝)为催化剂的作用下发生傅克反应,反应原理见图1。

图1 反应原理
1.3 实验过程
将定量的苯(除水操作后)分成两部分,一部分苯和催化剂加入到低温循环反应浴的反应瓶中,控制温度,搅拌得到混悬液;另一部分苯和环氧乙烷经混合滴加,调控滴加速度,控制滴加温度,滴加结束之后继续搅拌反应,反应结束后反应液经水解、静置、萃取、旋蒸得粗品β-苯乙醇,常压蒸馏纯化即可得到纯品[5]。
1.4 分析方法
采用液相色谱外标法分析反应液含量。色谱柱:C18柱(Dikma DiamonsilC18,250 mm×4.6 mm,5 μm),流动相(V乙腈∶V水=45∶55)、柱温(30 ℃)、波长(254 nm)、进样量(3 μL)、流速(1.0 mL/min)。
1.4.1β-苯乙醇标准溶液的配制
在精密天平上称取0.613 0 g(精度为0.000 1 g)β-苯乙醇标品于25 mL容量瓶中,用乙腈定容,超声震荡均匀,配制成24.52000 g/L的标准溶液。
1.4.2标准曲线的绘制用移液枪准确量取0.50、1.0、2.0、3.0、4.0、5.0 mLβ-苯乙醇标准溶液,分别用乙腈定容至10 mL容量瓶中,摇匀,分别配制成1.226000、2.452000、4.904000、7.356000、9.808000、12.26000g/L的标准溶液。经有机滤膜(0.45 μm)过滤,注入液相色谱仪,测定β-苯乙醇的色谱峰面积。以β-苯乙醇标准溶液的浓度为横坐标,峰面积为纵坐标,绘制标准曲线如图2所示,其线性回归方程为:
Y=2.90×105X-35 129.945R2=0.999 3
结果表明,浓度在1.226000~12.26000 g/L的范围内线性关系良好。

图2 液相外标法标准曲线图
2 结果与讨论
2.1 单因素实验
苯的凝固点5.5 ℃,环氧乙烷的沸点10.5 ℃,本实验在滴加原料时温度控制在6~9 ℃。
2.1.1反应温度对反应收率的影响
实验条件:加料配比为n(苯)∶n(三氯化铝)∶n(环氧乙烷)=1.0∶0.2∶0.2,保持滴加混合液中m(苯)∶m(环氧乙烷)=4.5∶1,温度为6~9 ℃,反应时间为1 h,探究反应温度对反应收率的影响。结果如图3所示。
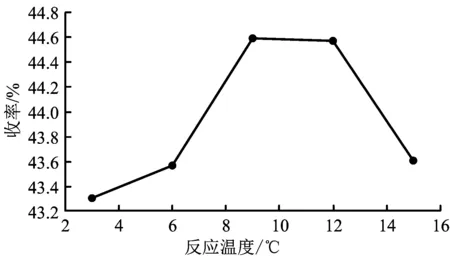
图3 反应温度对反应收率的影响
由图3可知,随着反应温度的升高,收率逐渐升高,且反应温度为6~9 ℃时,反应收率加速升高。主要原因可能是一方面反应温度升高,反应速率加快,另一方面当苯和环氧乙烷的混合液滴加到反应瓶中,环氧乙烷立刻和三氯化铝反应生成中间体1(ClCH2CH2OAlCl2),此中间体比较稳定,不易受温度影响,然后与苯反应生成中间体2(C6H5CH2CH2OAlCl2)。考虑到工厂进行规模化生产时,温度波动范围较大,故选择反应温度6~12 ℃。
2.1.2苯投料量对反应收率的影响
实验条件:保持滴加混合液中m(苯)∶m(环氧乙烷)=4.5∶1,滴加温度6~9 ℃,反应温度为6~12 ℃,反应时间为1 h不变,探究苯投料量对反应收率的影响,实验结果如表1所示。

表1 苯投料量对反应收率的影响
由表1可知,随着苯投料量的增加,收率先增加后减少。故苯的投料量不能无休止的增加,过量增加会造成苯实际参与反应的量较少,苯的循环量增多,增加能耗,增加成本,原子经济性降低。因此,选择n(苯)∶n(三氯化铝)∶n(环氧乙烷)=2.4∶0.2∶0.2。
2.1.3反应时间对反应收率的影响
实验条件:加料配比n(苯)∶n(三氯化铝)∶n(环氧乙烷)=2.4∶0.2∶0.2,保持混合液中m(苯)∶m(环氧乙烷)=4.5∶1,滴加温度6~9 ℃,反应温度6~12 ℃不变,探究反应时间对反应收率的影响。实验结果如图4所示。

图4 反应时间对反应收率的影响
由图4可知,随着反应时间的增加,其收率先增加后减小。傅克烷基化反应是可逆反应,随着时间的继续增加,其逆反应发生的机率可能增大。因此,最适宜的反应时间为80 min。
2.1.4催化剂投料量对反应收率的影响
实验条件:保持滴加混合液中m(苯)∶m(环氧乙烷)=4.5∶1,滴加温度为6~9 ℃,反应温度6~12 ℃,反应时间为80 min不变,探究催化剂投料量对反应收率的影响。催化剂投料量对反应收率的影响结果如表2所示。
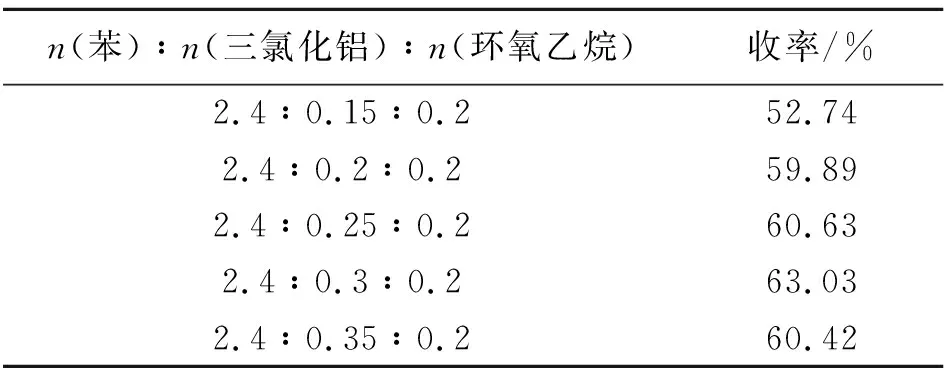
表2 催化剂投料量对反应收率的影响
由表2可知,随着催化剂投料量的增加,其收率先增加后降低。可能是因为三氯化铝不仅是该反应的催化剂,还作为反应原料和环氧乙烷发生反应生成中间体,增加反应原料的量有利于反应正向进行,其收率升高。但三氯化铝极易吸水,其加入量过大吸水也增多,一方面会降低三氯化铝的催化能力,引起体系生成副产物氯乙醇;另一方面还会导致环氧乙烷发生水解反应,损失部分环氧乙烷,由此造成了苯乙醇的收率下降。故选择n(苯)∶n(三氯化铝)∶n(环氧乙烷)=2.4∶0.3∶0.2。
2.1.5环氧乙烷投料量对反应收率的影响
实验条件:保持滴加混合液中m(苯)∶m(环氧乙烷)=4.5∶1,滴加温度为6~9 ℃,反应温度6~12 ℃,反应时间为80 min不变,探究环氧乙烷投料量对反应收率的影响。实验结果如表3所示。
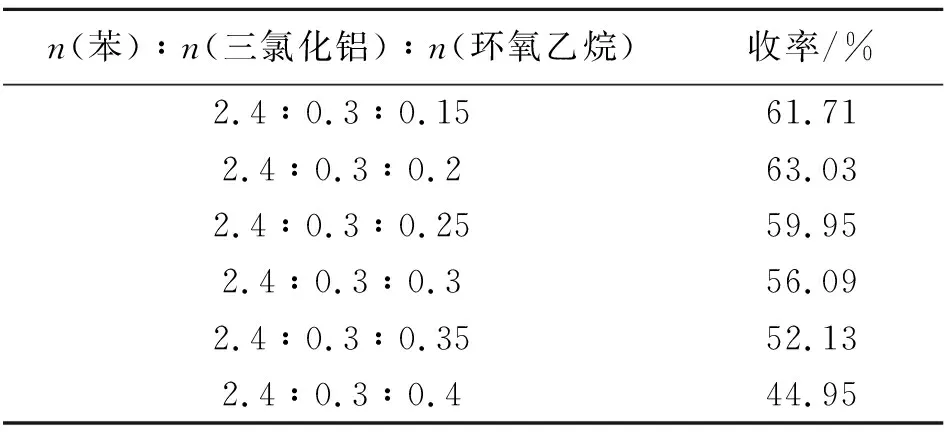
表3 环氧乙烷投料量对反应收率的影响
由表3可知,随着环氧乙烷投料量的增加,其收率先增加后减小。其原因可能是增加了其与催化剂的接触机率,且环氧乙烷是反应原料,增加对反应的正向进行有促进作用。但当环氧乙烷投料量过大时,其自身发生聚合反应的机率增大,与盐酸发生副反应生成氯乙醇的概率也增大,故收率下降。所以最佳投料比为n(苯)∶n(三氯化铝)∶n(环氧乙烷)=2.4∶0.3∶0.2。
2.1.6苯和环氧乙烷混合比例对反应收率的影响实验条件:加料配比n(苯)∶n(三氯化铝)∶n(环氧乙烷)=2.4∶0.3∶0.2,保持滴加温度为6~9 ℃,反应温度6~12 ℃,反应时间为80 min不变,探究滴加混合液中m(苯)∶m(环氧乙烷)对反应收率的影响。实验结果如图5所示。

图5 苯和环氧乙烷混合比例对反应收率的影响
由图5可知,随着苯和环氧乙烷质量混合比例的增加,其收率符合先增后减的趋势。降低体系中环氧乙烷浓度有利于降低环氧乙烷自聚合反应以及发生其他副反应的机率,从而提高β-苯乙醇的收率。环氧乙烷浓度过低会降低其与催化剂三氯化铝的接触机率,且添加过多的苯来稀释环氧乙烷,会延长环氧乙烷的苯溶液滴加时间,延长了中间体促进三氯化铝溶解的时间,导致三氯化铝部分溶解,收率反而下降。故m(苯)∶m(环氧乙烷)=12∶1。
2.2 正交试验
实验分别选取总苯量、三氯化铝用量、环氧乙烷用量、混合液中苯和环氧乙烷质量比四个因素,设计成四因素三水平表(见表4)。实验按照L9(34)正交表进行,其结果如表5所示。
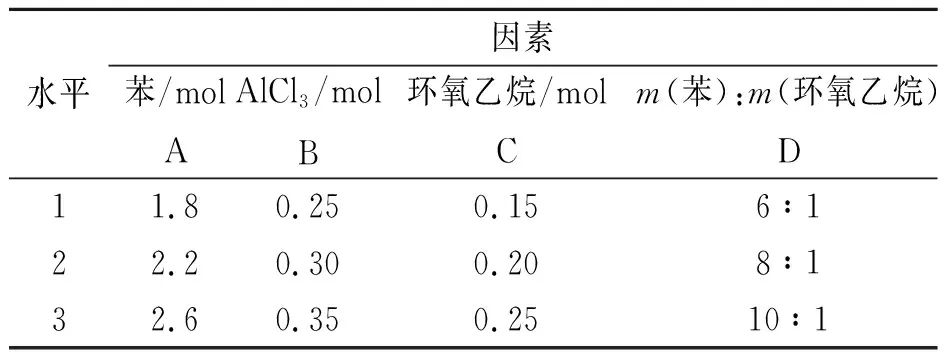
表4 正交试验因素水平表
由表5可知,对实验收率影响最大的是总苯量,其次是环氧乙烷用量,混合液中苯和环氧乙烷质量比及三氯化铝用量,即A >C >D >B。分析可得:最佳条件为A3B2C1D3。
因此,正交试验得到的最佳投料比为:n(苯)∶n(三氯化铝)∶n(环氧乙烷)=2.6∶0.3∶0.15,滴加混合液比例为m(苯)∶m(环氧乙烷)=10∶1。

表5 正交试验结果分析表
2.3 产物结构表征
2.3.1IR表征分析
β-苯乙醇标品和反应目标物的红外吸收光谱图如图6所示。

图6 标品和样品的红外吸收光谱图
由图6可知,其红外光谱图基本一致。1 600、892 cm-1处的吸收峰为苯环的骨架振动,1 455 cm-1处的吸收峰为(CH2—CH2)的C—H伸缩振动,3 326 cm-1处的吸收峰为—OH的伸缩振动,由此可大致确定生成了目标产物β-苯乙醇。
2.3.21H NMR表征分析
β-苯乙醇标准品的核磁共振氢谱图报告为1H NMR (CDCl3,600 MHz)δ:7.21(t,J=7.5 Hz,2H),7.13 (t,J=7.5 Hz,3H),3.73(t,J=6.7 Hz,2H),2.75(t,J=6.7 Hz,2H),1.79(s,1H)。
反应目标物的核磁共振氢谱图报告为1H NMR (CDCl3,600 MHz)δ:7.20(t,J=7.5 Hz,2H),7.12(t,J=7.5 Hz,3H),3.71(t,J=6.7 Hz,2H),2.74(t,J=6.7 Hz,2H),1.93(s, 1H)。
通过对比,证明此产物为目标产物β-苯乙醇。
3 结论
以苯和环氧乙烷为原料,氯化铝为催化剂制备β-苯乙醇。通过单因素和正交试验得到了最佳工艺条件:n(苯)∶n(三氯化铝)∶n(环氧乙烷)=2.4∶0.3∶0.2,保持加料方式不变(其中混合液中m(苯)∶m(环氧乙烷)=12∶1),滴加温度6~9 ℃,反应温度为6~12 ℃,反应时间为80 min。在此反应条件下,β-苯乙醇收率达68.35%。
