超高效液相色谱串联质谱法快速测定水产品中地西泮
2023-10-08孙娟沈媛杨静赵春晖吴仑陈翔贾晨李英方芳
孙娟,沈媛,杨静,赵春晖,吴仑,陈翔,贾晨,李英*,方芳*
(1.北京市农产品质量安全中心,北京 100029 2.北京市水产技术推广站,北京 100176)
地西泮(Diazepam,DXP),又称安定,属苯二氮卓类镇静剂,具有抗惊厥、镇定等作用。近年来,一些不法商贩在在水产捕捞和运输环节非法使用地西泮,导致地西泮在水产品中出现残留,人体如果长期摄入被地西泮污染的水产品,会导致中枢神经系统损伤。因此许多国家将镇静剂类药物划为水产动物捕捞和运输过程中的禁用类药物[1]。2022年3月农业农村部印发《2022年国家产地水产品兽药残留监控计划》和《2022年国家水生动物疫病监测计划》[2],启动新一轮全国范围的水产养殖用兽药及其他投入品监管和水生动物疫病风险防控工作,其中《2022年国家产地水产品兽药残留监控计划》共监测7种水产养殖禁(停)用药、2种常规用药、2种农药和地西泮[2]。地西泮作为2022年新增监测指标,标志着农业农村部对未经批准使用的水产养殖用兽药的监管进一步加强。地西泮属于镇静类药物,目前中国未批准作为水产养殖用兽药。依据《兽药管理条例》有关规定,水产养殖过程中使用该药物属于违规用药[3]。GB 31650—2019《食品安全国家标准 食品中兽药最大残留限量》中规定[4],地西泮不得在动物性食品中检出。2022年11月15日农业农村部渔业渔政管理局《关于发布<水产养殖用药明白纸2022年1、2号>宣传材料的通知》新增了地西泮等畜禽用兽药在中国均未经审查批准用于水产动物,在水产养殖过程中不得使用[5]。
农业农村部2023年1月关于监督抽查发现的15批次问题农产品情况的通告中显示,在江苏省扬州市养殖的1批次乌鳢(Channaargus)、安徽省安庆市养殖的3批次黄鳝(Monopterusalbus)中有地西泮药物检出[6]。北京市场监督管理局2023年第一季度最新数据显示,在北京市大兴、门头沟和昌平等地抽检样品中均有地西泮药物检出,检出值在1.35~7.58 μg/kg之间[7]。因此针对地西泮在全国检出率较高的问题,建立一种前处理简单、检出限低,适用于水产品中地西泮检测的方法意义重大。
目前水产品中地西泮测定方法在国内外已报道的主要有:酶联免疫法、高效液相色谱法(HPLC)[8-9]、气相色谱质谱法(GC-MS)[10-11]以及液相色谱串联质谱法[12-21]。其中,气相色谱串联质谱法需要衍生处理,前处理过程较复杂;液相色谱法相比液相色谱串联质谱法灵敏度较低,不能满足禁用药物检出限低的要求;超高效液相色谱串联质谱法(HPLC-MS/MS)具有灵敏度高、测定时间短、基质干扰小,定量限低等优势,在兽药残留分析中广泛应用。目前已有的检测标准[22]是唯一可用于水产品中地西泮的检测标准,但在实验室实际测定过程中发现,由于该方法利用外标法定量,存在明显的基质效应,导致实验回收率低、重现性差等不足。而KJ202105[23]《水产品中地西泮残留的快速检测胶体金免疫层析法》规定了水产品中地西泮胶体金免疫层析快速检测方法,适用于鱼、虾中地西泮的快速定性测定,适合做筛查使用,出现阳性样品仍需要仪器法准确定量核实。
本研究通过参考国内外文献,对样品的前处理方法以及仪器分析方法进行了改进和优化,并对本研究方法的有效性进行了评价,建立了一种应用超高效液相色谱串联质谱法(UPLC-MS/MS)测定水产品中地西泮的定量分析方法,该方法具有操作简单、高效快捷,可有效节省检测时间以及试剂耗材用量,为实验室进行批量样品快速筛查测定提供依据,也为今后完善地西泮残留检测标准提供技术支撑。
1 材料与方法
1.1 主要仪器与设备
配有电喷雾离子源ESI+的超高效液相色谱-串联四级杆质谱(型号为UPLC-XEVO TQ-XS),美国沃特世科技有限公司;台式高速冷冻离心机:Sorvall ST16R,美国赛默飞世尔科技有限公司;氮吹仪:N-EVAP 112,上海力创科学仪器有限公司;电子天平(感量0.000 1 g):ME204E,梅特勒-托利多仪器(上海)有限公司;涡旋混匀器,上海安谱实验科技有限公司;MILLI-Q Advangtage纯水机,法国 Merck Millipore公司。
1.2 材料与试剂
实验样品于2023年2月购于北京大红门京深海鲜批发市场,体重约2 kg,不少于3尾鱼,购买后取背部肌肉,试样量不少于400 g,将肌肉部分切成小块匀浆装入样品袋,密封后贴上样品标签于-18 ℃冰箱保存。
乙腈、乙酸乙酯、甲醇及甲酸(均为HPLC级),购于美国Thermo Fisher公司;地西泮(DXP)及内标物氘代地西泮(DXP-D5),购于国家标物中心,纯度均大于99%。HSS T3柱(2.1 mm×100 mm,1.8 μm),CORTECS UPLC(2.1 mm×100 mm,1.6 μm)和ACQUITY UPLC BEH C18柱(2.1 mm×50 mm,1.7 μm)3种不同型号色谱柱均购于美国沃特世科技有限公司。
1.3 仪器条件
色谱条件:色谱柱:ACQUITY BEH C18柱(50 mm×2.1 mm,1.7 μm),进样体积为5 μL,柱温为35 ℃,流速为0.3 mL/min,流动相为甲醇和0.1%甲酸水溶液。
质谱条件:离子源为电喷雾离子源(ESI),采用正离子扫描方式,多反应监测模式(MRM),离子源温度为110 ℃,毛细管电压为2.50 kV,溶剂气温度为450 ℃,去溶剂气流量为800 L/h。其他质谱参数详见表1。

表1 地西泮液相色谱串联质谱测定参数Tab.1 UPLC-MS/MS parameters for determining diazepam
1.4 样品前处理
称取5.00 g鱼糜试样(精确到0.01 g)于50 mL离心管中,加入0.2 mL氘代地西泮内标溶液,准确加入25.0 mL乙酸乙酯,恒温振荡器中涡旋10 min,4 000 r/min离心5 min,取5 mL乙酸乙酯于15 mL离心管中,50 ℃水浴氮吹至干,用20%甲醇水溶液溶解,定容至2 mL,涡旋2 min,加入3.5 mL正己烷,振荡2 min,弃上层正己烷层及中间杂质膜,过0.22 μm聚醚砜滤膜于2 mL样品瓶中,待测。
1.5 标准溶液的配制
地西泮标准储备液(100 mg/L)配制方法:准确称取10 mg地西泮标准品,用纯甲醇超声溶解,完全溶解后定容至100 mL棕色容量瓶中,配制成100 mg/L的标准储备液,-18 ℃储存,保存期为6个月。
氘代地西泮内标标准储备液(100 mg/L)配制方法:准确称取10 mg氘代地西泮标准品,用纯甲醇超声溶解,完全溶解后定容至100 mL棕色容量瓶中,配制成100 mg/L的内标储备液,-18 ℃储存,保存期为6个月。
氘代地西泮内标标准工作液(200 μg/L)配制方法:准确移取200 μL氘代地西泮内标储备液,用纯甲醇定容至100 mL棕色容量瓶中,配制成200 μg/L的内标工作液,-4 ℃储存,保存期为3个月。
地西泮标准工作溶液配制方法:用20%甲醇水溶液稀释地西泮标准储备液,加入内标溶液最终配制成0.01、0.05、0.10、0.50、1.00和2.00 μg/L的标准工作溶液,现用现配。
2 结果与分析
2.1 色谱柱优化
分别选取HSS T3柱(2.1 mm×100 mm,1.8 μm),CORTECS UPLC(2.1 mm×100 mm,1.6 μm)和ACQUITY UPLC BEH C18柱(2.1 mm×50 mm,1.7 μm)3种不同规格的色谱柱进行地西泮及其内标化合物的分离比较。结果(图1)表明,ACQUITY UPLC BEH C18柱(2.1 mm×50 mm,1.7 μm)作为地西泮化合物的分离色谱柱时,分离度和峰型较好,无分叉及拖尾现象,且能够在5.0 min内完成样品分离。因此,选择ACQUITY UPLC BEH C18柱(2.1 mm×50 mm,1.7 μm)作为分析色谱柱。
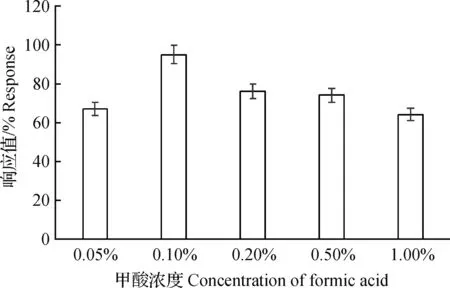
图1 不同甲酸浓度流动相对地西泮响应值的影响Fig.1 Effect of different concentration of formic acid on the response of diazepam
2.2 流动相种类和比例的选择
根据地西泮化合物含有苯环,极性较小的特征,选择以C18色谱柱作为色谱分析柱。分别考察了乙腈-水溶液、甲醇-水溶液作为流动相,发现使用以上两种流动相地西泮均能出峰。相比较甲醇-水溶液作为流动相,质谱响应信号较高,色谱峰形较对称。为了确定更优流动相种类条件,分别添加浓度为0.05%、0.10%、0.20%、0.50%及1.00%的甲酸,考察甲酸对地西泮响应的影响。结果表明:甲酸浓度为0.10%时,地西泮响应和峰型均较好(图1),因此采用甲醇-0.10%甲酸水溶液作为流动相。
在此流动相条件下,优化流动相比例,确定流动相梯度洗脱程序为0.0~1.0 min,95% A;1.0~3.0 min,95%~0% A;3.0~4.0 min,0%~95% A;4.0 min,95% A,平衡1 min(A为0.1%甲酸水溶液)得到地西泮及其内标的多反应监测(MRM)色谱图(图2)。
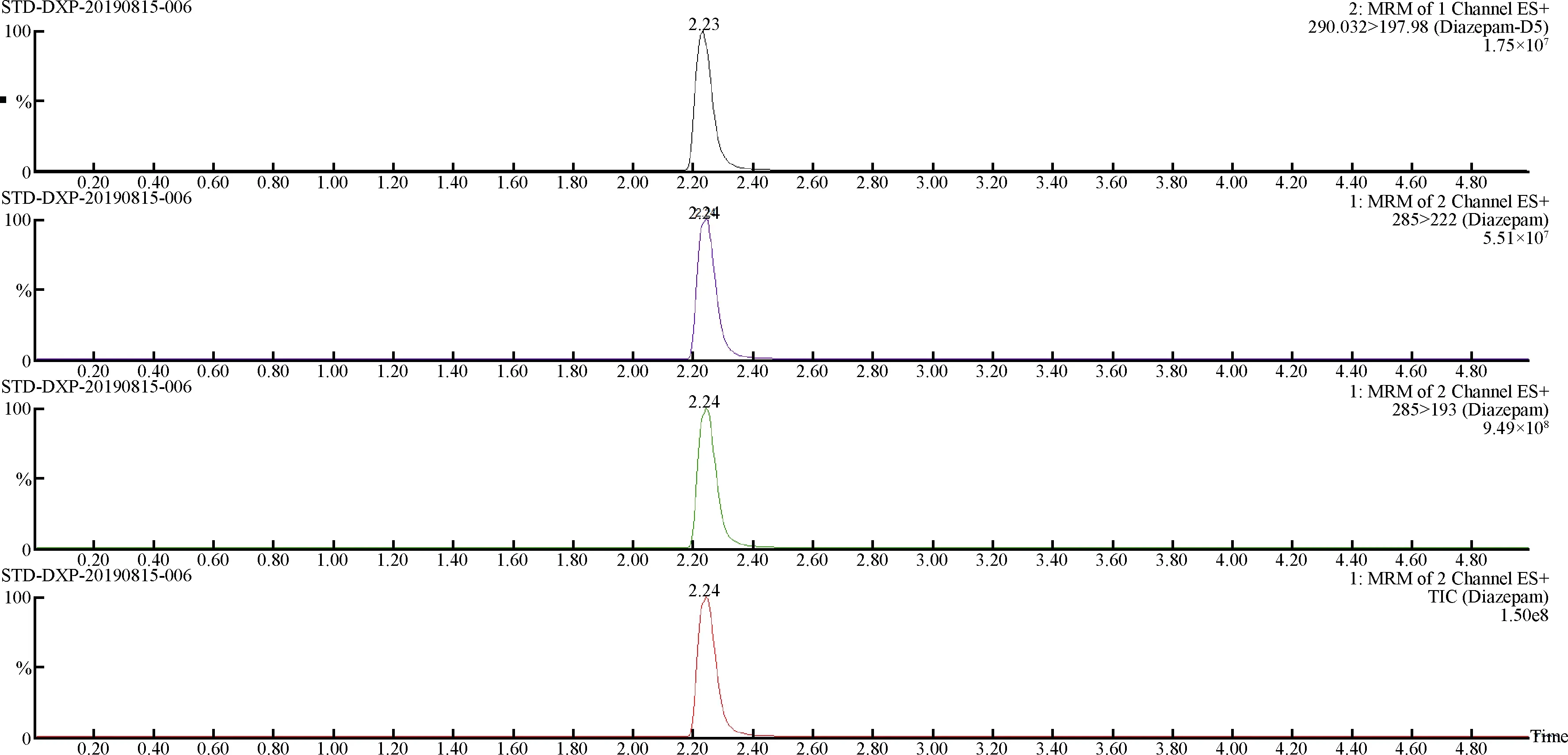
图2 地西泮及其内标标准溶液MRM色谱图(ESI+)Fig.2 MRM chromatograms of diazepam and inter standard in ESI+ model
2.3 提取条件的选择
根据前期查阅资料,地西泮极性较弱,易溶于甲醇、乙酸乙酯等有机溶剂,不易溶于水。本研究以鲤(Cyprinuscarpio)和狭鳕(Theragrachalcogramma)为例,比较了甲醇、乙腈、乙酸乙酯、1%甲酸乙腈、1%甲酸甲醇5种提取方式(图3),实验结果表明:直接加入1%(V/V)甲酸甲醇、1%(V/V)甲酸乙腈、甲醇、乙腈做提取剂后样品提取效率和加标回收率均没有乙酸乙酯高,因此,选择乙酸乙酯作为最终提取溶液。

图3 不同提取剂对地西泮回收率的影响Fig.3 Effect of different extraction solvent on the recovery rates of diazepam
2.4 方法学验证
2.4.1 线性范围
在最佳优化条件下,用初始流动相准确配制质量浓度分别为0.01~20.00 μg/L的标准溶液曲线系列,同时加入内标溶液,液相色谱串联质谱仪测定分析,以定量离子峰面积与氘代地西泮峰面积之比为纵坐标(y),待测化合物浓度与氘代地西泮浓度之比为横坐标(x),绘制标准工作曲线,得到线性工作范围及相关系数。结果表明,地西泮在正离子模式下线性关系良好,相关系数(r)均不低于0.995(图4)。
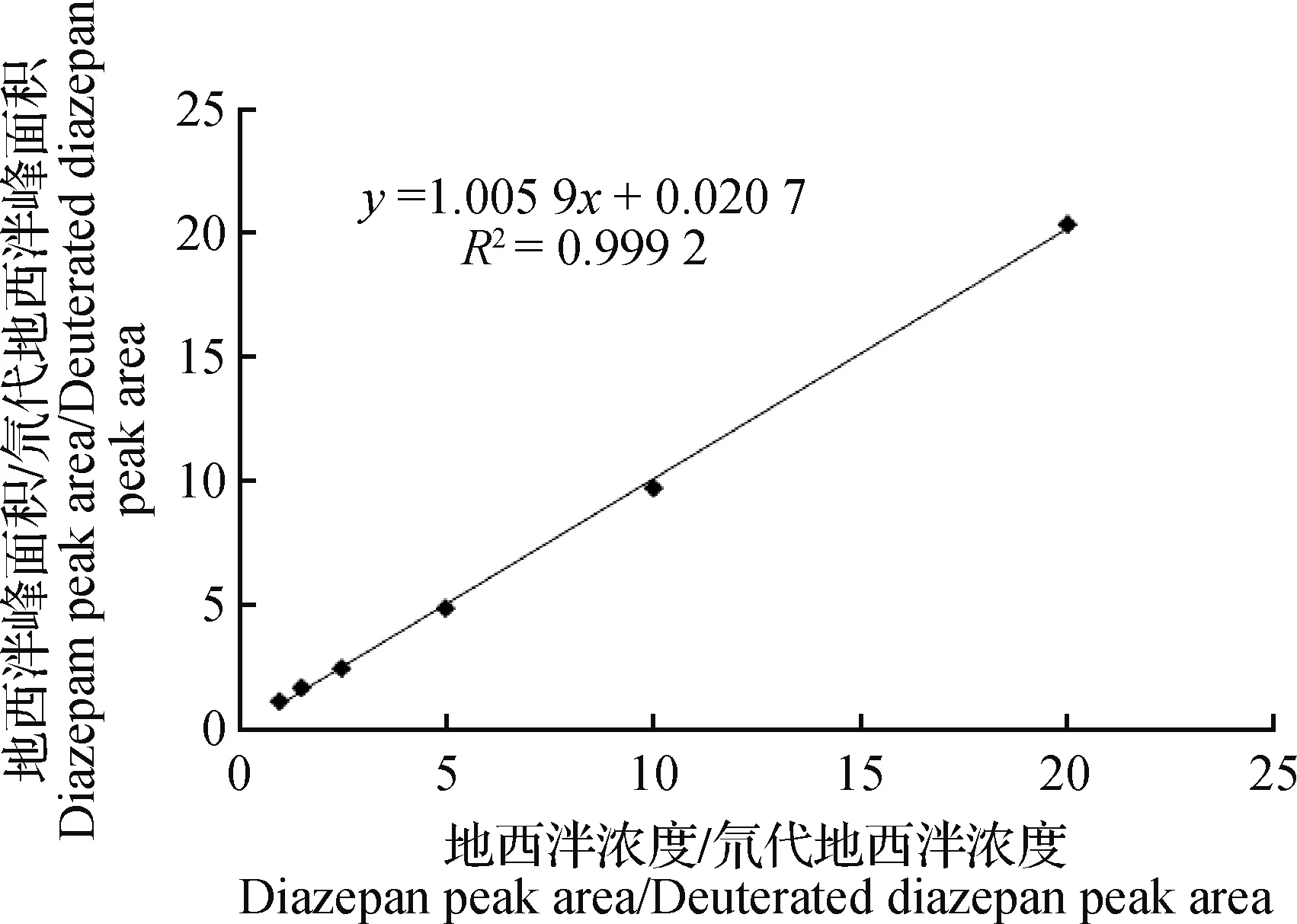
图4 地西泮标准工作曲线Fig.4 Standard working curve of diazepam
2.4.2 检出限和定量限
分别取空白狭鳕和鲤鱼糜样品作为基质,添加不同浓度的地西泮标准溶液,按照1.4样品前处理方法处理,分析测定后,以S/N=3作为最低检出限,以S/N=10作为最低定量限(表2)。结果表明,地西泮的最低检出限LOD在0.05~0.10 μg/kg,最低定量限LOQ在0.25~0.50 μg/kg之间,均低于中国、欧盟和日本等国家和地区规定的最大残留限量。
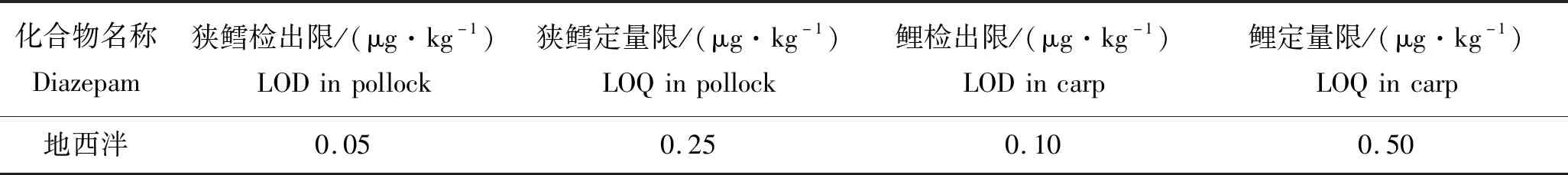
表2 地西泮检出限及定量限Tab.2 LODs and LOQs of diazepam
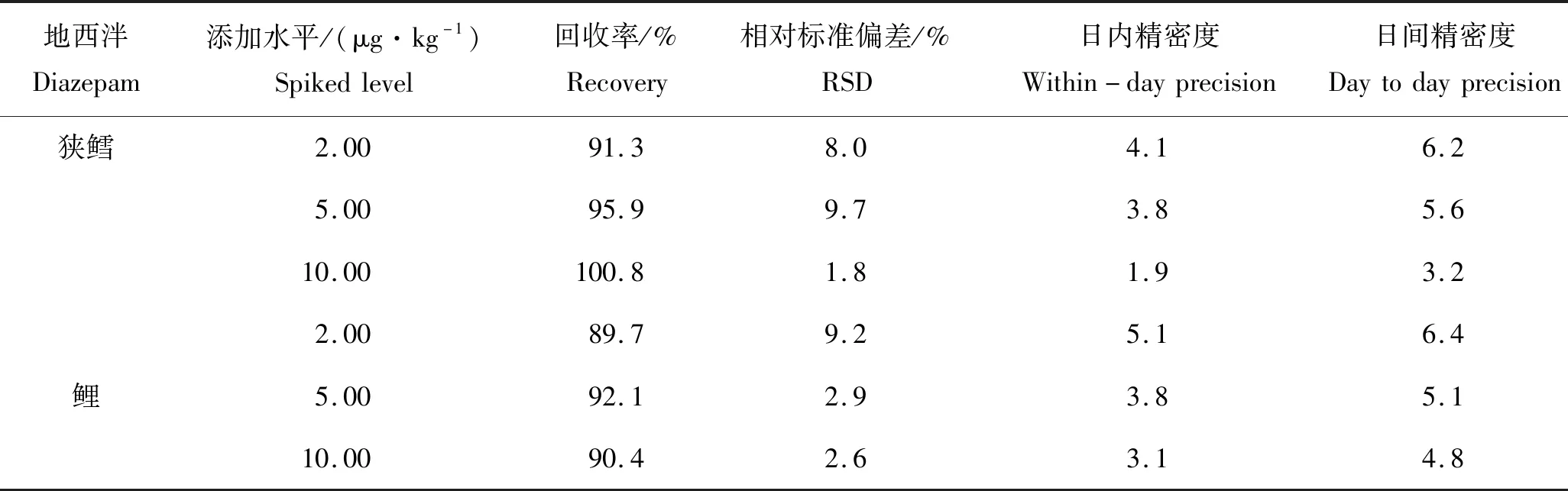
表3 地西泮不同添加水平回收率及精密度Tab.3 Recoveries and precisions of diazepam in different additive level
2.5 方法回收率与精密度
分别称取狭鳕和鲤鱼糜空白样品5.00 g,对地西泮进行低、中、高3个不同水平的添加,添加含量依次为2.0、5.0和10.0 μg/kg,不同添加水平进行6次平行测定,计算添加回收率以及方法日内精密度。按照同样的样品处理方法,连续测定6 d,计算方法的日间精密度。结果表明:地西泮药物平均回收率为89.70%~100.80%,相对标准偏差为1.80%~9.70%(表4)。

表4 本方法与国家已有标准方法对比结果Tab.4 Comparison results between the method used in the study and the national standard method
2.6 同标准方法比对
为了进一步验证该方法的可行性,采取了与标准方法的比对试验。目前可查到的国家标准方法只有SN/T 3235—2012《出口动物源食品中多类禁用药物残留量检测方法液相色谱-质谱/质谱法》[22],该标准方法适用于水产品中地西泮的筛查和测定,采用外标法定量,样品经过处理后上机会存在较强的基质效应,影响回收率,而内标法通过内标校正可以有效解决基质效应问题,通过随机抽取实际样品送到有资质的部级质检中心进行测定比对,结果表明(表5),该方法与国家标准方法的结果均在规定范围内,从而证明该方法的可靠性。
2.7 实际样品测定
应用所建立的分析方法,对190份样品进行测定,有8份样品检出,检出样品结果见表5。190份样品中,地西泮检出率为4.2%,其中最高检出浓度为34.1 μg/kg。而且在实际样品测定过程中发现,所有检出样品品种均为鲤。
本实验室从2019年至今每年对北京地区不同养殖场及市场进行样品抽取测定,从近几年检测结果发现有部分鲤样品有地西泮检出,而且2022年检出率较前几年要高。王守英等[24]研究发现上海市售水产品中有一定的地西泮残留隐患,其残留主要存在于鲫(Carssiusauratus)、草鱼(Ctenopharyngodonidella)等淡水鱼类中。在检出产品中,残留量绝大多数低于1 μg/kg。张璇等[25]对2020年8月采自上海市农贸市场和超市的 167 个水产品(包括鱼、虾、蟹、贝) 进行镇静剂残留筛查,结果表明除了草鱼以及鲫检出地西泮残留外,还包括淡水鲈(Lateolabraxjaponicus)。从目前北京地区抽样检测数据结果来看地西泮检出主要存在于鲤品种,因此,不同水产品品种之间地西泮药物代谢差异仍需进一步探讨。
目前地西泮检出原因仍待研究,分析可能原因有运输过程作为镇定剂使用、渔用饵料中作为诱食剂使用、水体污染或投入品添加等。杨光昕等[26]调查了渔用饵料中地西泮及其降解产物的残留状况,发现地西泮的检出率较高,残留量较大,最高可达82 214 μg/kg,其认为饵料中的地西泮极有可能是人为添加所致,且存在非法原药来源途径,使用来源不受监控增加了药物在水产品中污染残留风险,这可能是造成养殖环境污染、水产品中频繁检出地西泮的主要原因。下一步研究工作将通过对检出样品继续跟踪调查,对养殖鱼塘底泥、水体、品种、代谢物等进一步分析探究,争取找到地西泮检出来源。
3 结论
本研究建立了超高效液相色谱串联质谱法(UPLC/MS/MS)测定水产品中地西泮残留的分析方法,该方法提取步骤简单快速稳定,通过内标法定量有效消除了基质效应以及前处理过程损失的影响,有效提高了水产品中地西泮测定的回收率,方法具有较低的检出限和定量限,重复性好,可适用于水产品中地西泮药物残留的快速筛查和定量分析。
