双波长HPLC法同时测定上清丸中栀子苷及连翘酯苷A含量
2023-10-07肖琳婧秦学玲付兴情张赟华
肖琳婧 秦学玲 付兴情 金 蒙 龙 琴 张赟华
云南省食品药品监督检验研究院,云南 昆明 650106
上清丸来源于《丹溪心法》“朱丹溪方上清散加减”[1],但与现行处方一致的上清丸最先记载于《北京市中药成方选集》[2]。上清丸现标准收载于卫生部药品标准《中药成方制剂》第十册[3],标准编号为 WS3-B-1878-95,标准收载大蜜丸和水丸两种剂型,后增加水蜜丸的规格。上清丸由菊花、薄荷、川芎、白芷、荆芥、防风、桔梗、连翘、栀子、黄芩(酒炒)、黄柏(酒炒)及大黄(酒炒)十二味药材组成。主要有清热散风、解毒通便的功效。临床上常用于头晕耳鸣、目赤、鼻流黄涕、口舌生疮、牙龈肿痛,大便秘结[4]。方中主药大黄清热凉血、泻火通便,黄芩清上焦火,黄柏泻下焦火,栀子泻三焦火;辅以连翘、菊花、薄荷、荆芥、防风疏散风热,清利头目,川芎活血行气止痛,白芷祛风散寒,消肿止痛;佐以桔梗引药上行,宜肺散风,消肿利咽,以消上、中焦风热。文献[5-7]报道,采用HPLC方法对上清丸中的欧前胡素、黄芩苷、绿原酸、大黄中蒽醌类等成分进行含量测定,但对上清丸栀子中栀子苷及连翘中连翘酯苷A 含量测定未见报道。
上清丸为2022年全国中成药评价性抽验重点监管品种之一,本次专项抽验,共抽取上清丸样品103批次。抽样地域覆盖了全国26个省、自治区、直辖市,涉及14家生产企业,包括大蜜丸、水丸、水蜜丸3种剂型。为综合评价市售上清丸中栀子和连翘质量,本实验采用了HPLC双波长同时测定103批样品中栀子苷及连翘酯苷A 含量,以期对上清丸中栀子及连翘的质量进行评价。
1 仪器与材料
1.1 仪器 岛津LC-20A高效液相色谱仪;赛多利斯BS224S电子天平;赛多利斯SECURA225D电子天平。
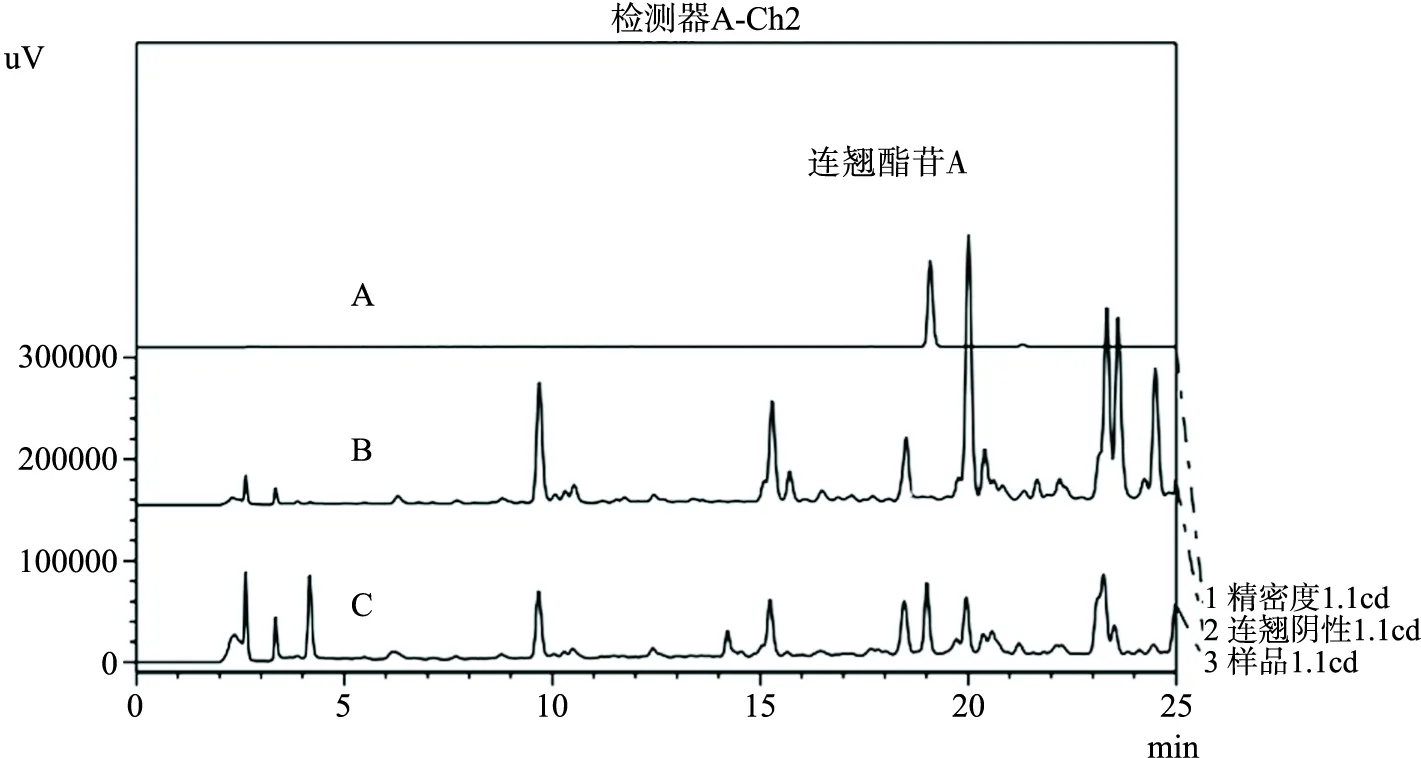
A.混合对照品溶液;B.缺连翘阴性供试品溶液;C.供试品溶液
1.2 材料 方法学考察用的样品:上清丸(水蜜丸,批号:A12003,广州白云山陈李济药厂有限公司生产),其余103批次上清丸样品来源于14家生产企业,由于国家专项抽验,涉及数据保密,生产企业由A~N代替,具体信息见表3。栀子苷(批号:110749-201919,含量以97.1%计)、连翘酯苷A(批号:111810-201707,含量以97.2%计),以上对照品均购于中国食品药品检定研究院,乙腈为色谱纯(默克公司),水为纯化水,甲醇、乙醇、磷酸等其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件 采用ZORBAX C18色谱柱(4.6 mm×250 mm,5 μm),以乙腈为流动相A,以0.1%磷酸为流动相B,梯度洗脱,流速为1 mL/min,柱温30 ℃,检测波长为238 nm(栀子苷)、330 nm(连翘酯苷A)。

表1 梯度洗脱表
2.2 对照品溶液的制备 分别取栀子苷、连翘酯苷A对照品适量,精密称定,加甲醇制成每1 mL含40 μg的混合对照溶液。
2.3 供试品溶液的制备 取本品重量差异项下大蜜丸,剪碎,取2 g,精密称定;或取水蜜丸或水丸,研细,取1 g,精密称定,置具塞三角锥形瓶中,精密加入70%乙醇20 mL,称定重量,加热回流30 min,放冷,再称定重量,用70%乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.4 阴性供试品溶液的制备 按处方比例,在实验室模拟工艺,分别配制缺连翘、栀子的两种细粉,分别取约1 g,同供试品溶液制备,即得两种阴性供试品溶液。
2.5 系统适应性与专属性试验 按“2.2、2.3、2.4”项下制备的对照品溶液、供试品溶液和阴性供试品,在上述试验条件下,采用紫外检测器检测,测定,记录色谱图。结果表明上述液相色谱条件下,供试品溶液色谱中呈现与对照品保留时间相同的色谱峰,栀子苷、连翘酯苷A,分离度大于1.5,阴性供试品在相应位置处未见色谱峰,表明其他药味不干扰2种待测成分的测定,方法专属性良好。
2.6 线性关系考察 ①精密称取栀子苷、连翘酯苷对照品10.41 mg、10.29 mg置于25 mL量瓶中,用甲醇溶解定容至刻度,摇匀,得对照品储备液(C=400 μg/mL);②精密吸取 5 mL、5 mL、5 mL、1 mL对照品储备液置于 10 mL、20 mL、25 mL、10 mL 量瓶中,加甲醇稀释定容至刻度,摇匀;③再取80 μg/ mL的对照品溶液5 mL置于20 mL量瓶、取20 μg/mL对照品溶液置于10 mL量瓶,加甲醇稀释定容至刻度,摇匀,即得系列线性溶液。取续滤液按“2.1”项下色谱条件分别进样,以峰面积为纵坐标,浓度(μg/mL)为横坐标,分别计算栀子苷的回归方程为Y=15581X+5599.3(r=1.0000)、连翘酯苷A的回归方程为Y=17230X-21735.4(r=0.9997),说明栀子苷在 404.32~2.02 μg/mL、连翘酯苷A在 403.96~2.02μg/mL的浓度范围内线性关系良好。
2.7 精密度试验 取混合对照品适量,按上述方法制备,连续6次测定,测得栀子苷、连翘酯苷A的峰面积RSD(n=6)分别为0.14%、0.10%,仪器的精密度良好。
2.8 稳定性试验 取同一供试品溶液,按“2.1”项下色谱条件分别进样,分别在0 h、4 h、8 h、12 h、20 h、24 h各进样一次,测定各组分的峰面积,栀子苷、连翘酯苷A峰面积RSD(n=6)分别为0.45%、1.20%,样品溶液在24 h内基本稳定。
2.9 重复性试验 取上清丸(批号:A12003),按上述方法制备6份供试品溶液,进样测定,测得栀子苷、连翘酯苷A 的含量RSD(n=6)分别为0.29%、0.45%,该方法的重复性良好。
2.10 加样回收试验 分别精密称6份样品(批号:A12003)0.5 g,采用加样回收试验方法,分别按下表精密加入2种对照品溶液,计算回收率和RSD。见表2。
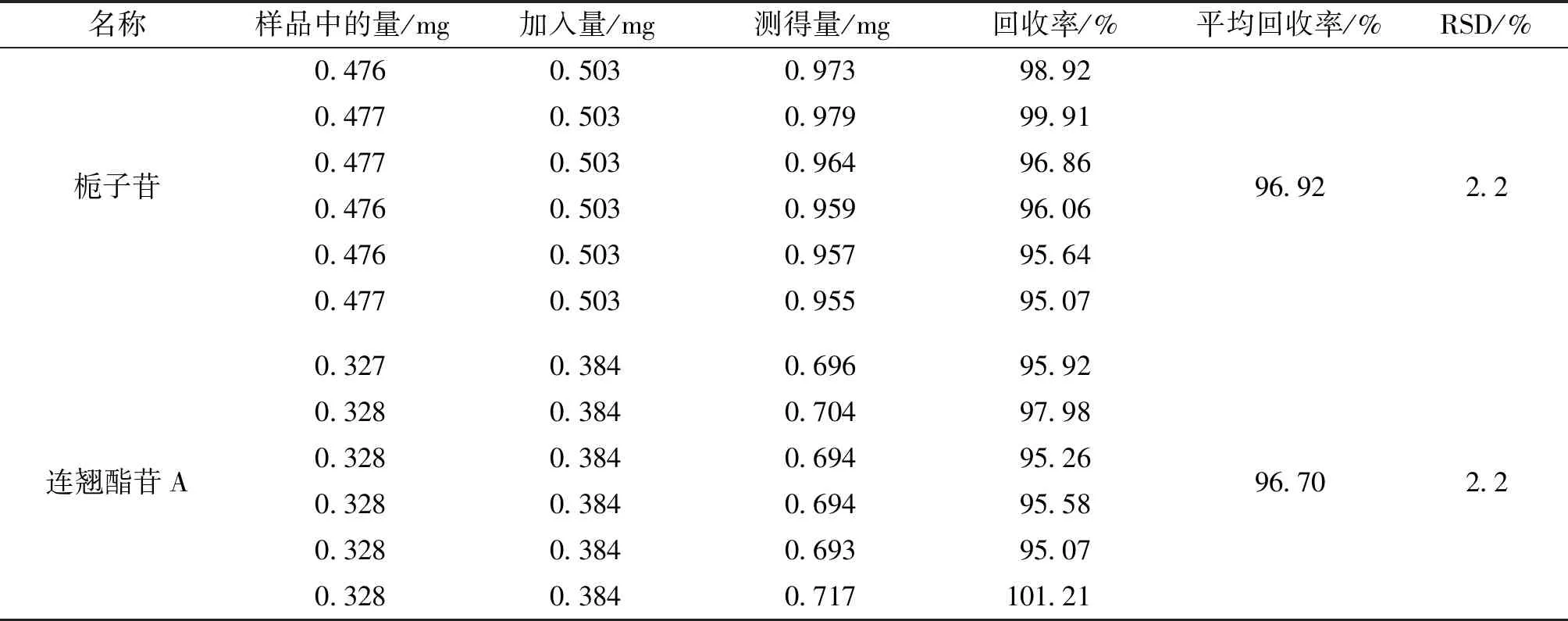
表2 加样回收率实验结果
2.11 含量测定结果 取上清丸103批,按照2.2.2项下方法制备供试品溶液,各精密吸取10 μL,注入HPLC中,采用外标法计算各成分的含量,结果见表3。各生产企业栀子苷含量统计图如图2所示,连翘酯苷A如图3所示。
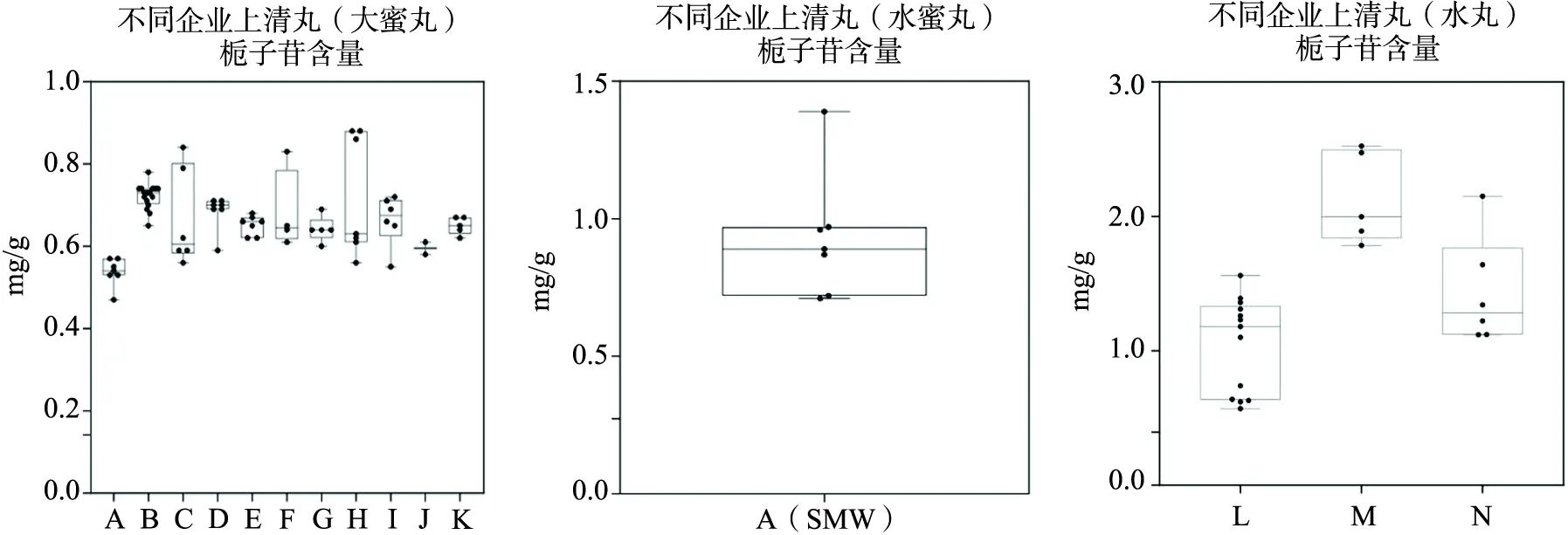
图2 不同生产企业上清丸栀子苷含量统计图
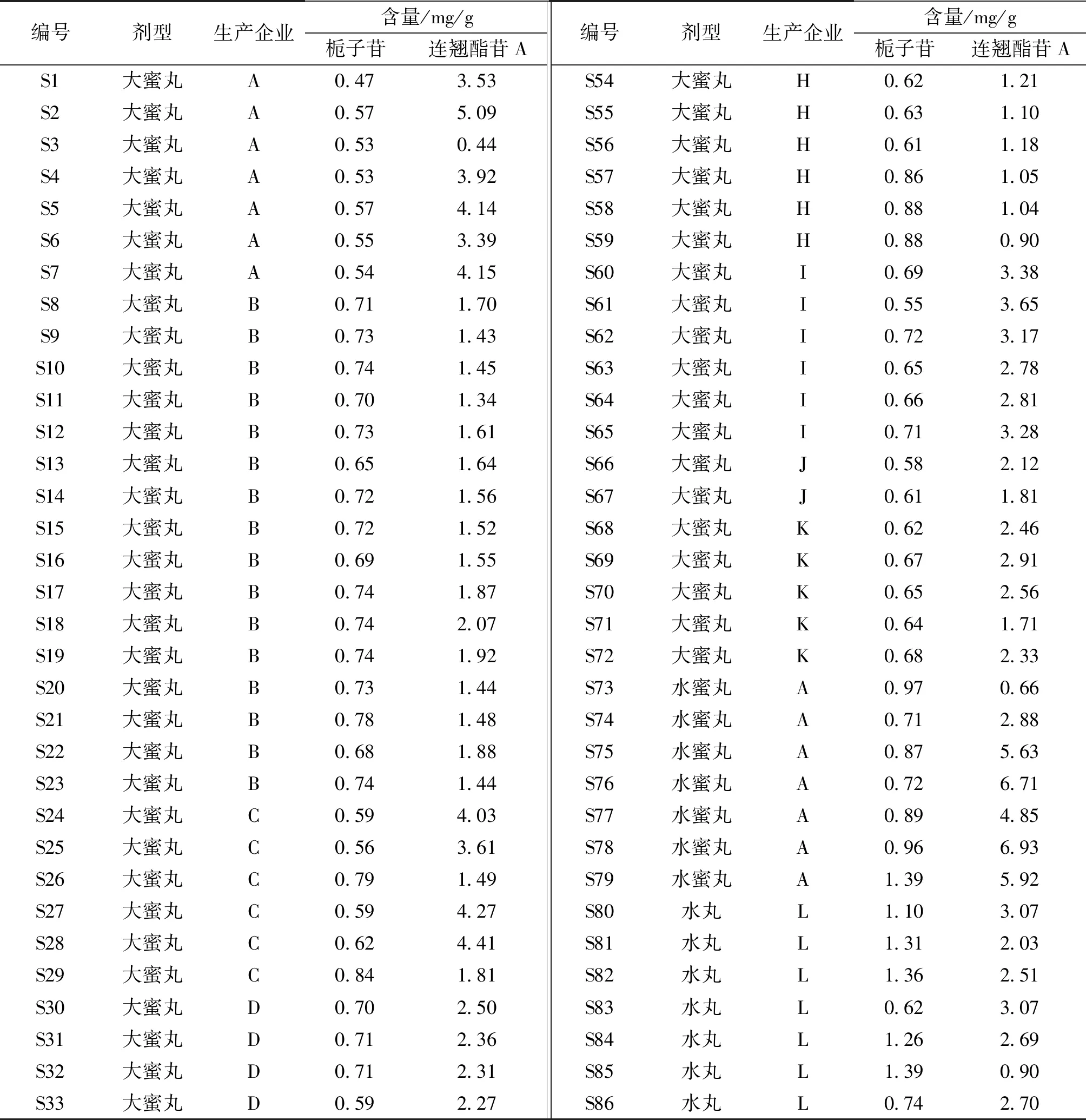
表3 103批次上清丸样品信息及栀子苷、连翘酯苷A含量测定结果
结果表明不同企业上清丸(大蜜丸)栀子苷的含量较集中且差异较小,但来自C、F、H生产的上清丸栀子苷不同批次间栀子苷含量差异较大。上清丸(水蜜丸)为A企业独家生产,6批次栀子苷的含量差异较大,说明该企业不同批次样品栀子药材质量存在差异。不同企业上清丸(水丸)栀子苷的含量差异大,L企业不同批次之间栀子苷的含量相差3倍。
结果表明不同企业上清丸连翘酯苷含量差异较大,参考《中国药典》2020年版连翘项下规定,青翘和老翘中连翘酯苷A限度相差14倍[8]。其中A企业上清丸(大蜜丸)中的连翘酯苷A的含量相差15倍,水蜜丸中连翘酯苷A的含量相差10倍,主要是青翘和老翘投料不固定,造成连翘酯苷A含量差异较大。结合调研情况,仅有B和M企业固定青翘投料。
3 讨论
3.1 供试品溶液制备方法选择 本研究比较了不同提取溶剂(90%甲醇、70%甲醇、70%乙醇、甲醇),不同提取方式(超声30 min、加热回流30 min),不同回流时间(30 min、45 min、60 min),最终确定最佳提取条件是70%乙醇加热回流提取30 min。此条件提取较完全,通过上述色谱条件,可以较好地测定上清丸栀子苷及连翘酯苷A含量。
3.2 检测波长的选择 本研究通过二极管阵列检测器检测,栀子苷在238 nm波长附近均最大吸收并参照《中国药典》2020年版一部栀子含量测定项下的规定[9],选择238 nm 为栀子苷检测波长。连翘中连翘酯苷A在330 nm波长附近有最大吸收,并参照《中国药典》2020年版一部连翘含量测定项下的规定[8],选择330 nm为连翘酯苷A检测波长。
3.3 流动相的选择 本实验在筛选流动相时,通过对乙腈-水、甲醇-水的运行,筛选出乙腈-水系统优于甲醇-水系统,但色谱峰出现了拖尾现象,进而以乙腈-0.1%磷酸水溶液为流动相,同时测定上清丸中栀子苷及连翘酯苷A 含量。结果发现,以乙腈-0.1%磷酸水溶液为流动相梯度洗脱时,供试品中栀子苷和连翘酯苷A可达到基线分离,峰型较好,并且干扰较少,出峰时间适中,故选取此条件为流动相。
3.4 样品分析 通过测定103批上清丸栀子苷,部分企业上清丸不同批次间栀子苷含量的存在较大差异,说明各批次间均一性较差。为了提高上清丸的一致性,相关企业应加强对投料栀子的质量控制,对栀子产地、采收时间做出相应的规定。
通过测定103批上清丸连翘酯苷A含量,部分企业上清丸中连翘酯苷A含量差异巨大,主要原因是上清丸中连翘投料不固定。为了保证上清丸质量的均一性,各生产企业应固定青翘或老翘投料。
本实验采用HPLC结合双波长同时测定栀子苷及连翘酯苷A含量。所建立的方法操作简单、结果准确,不同企业不同批次上清丸中栀子苷及连翘酯苷A的含量存在一定差异,可能与制剂生产所用原药材的产地、来源、采收季节以及原药材批间质量差异等因素有关,提示相关生产企业关注栀子及连翘原药材质量,并且在连翘投料过程固定青翘或老翘投料,不断提高和完善上清丸的质量控制标准,确保上清丸质量稳定和临床疗效一致。
