前列地尔治疗慢性肾脏病对患者血管钙化的影响观察
2023-09-28向成伦
向成伦
【摘要】 目的 探讨前列地尔治疗慢性肾脏病对患者血管钙化的影响。方法 选取2019年1月—2021年12月恩施市中心医院76例慢性肾脏病(CKD)患者,采用随机数字表法分为对照组(38例,接受常规饮食、血糖及血压控制治疗)与研究组(38例,接受常规治疗联合前列地尔),疗程均为1个月。比较2组治疗前后的血清肌酐(SCr)、血磷、血钙、尿白蛋白排泄率(UAER)、血钾水平,比较2组的临床疗效及药物不良反应。结果 治疗前2组的SCr、血磷、血钙、UAER、血钾水平差异无统计学意义(P>0.05);治疗后研究组的SCr、血磷、UAER、血钙、血钾水平低于对照组(P<0.05)。研究组的治疗总有效率高于对照组,差异有统计学意义(P<0.05)。2组不良反应发生率差异无统计学意义(P>0.05)。结论 前列地尔可有效改善CKD患者血钙与血磷水平,降低血管钙化风险,促进肾功能恢复。
【关键词】 慢性肾脏病;前列地尔;血管钙化;影响
中图分类号:R318.16;R692 文献标识码:A
文章编号:1672-1721(2023)14-0044-03
DOI:10.19435/j.1672-1721.2023.14.015
慢性肾脏病(chronic kidney disease,CKD)是临床常见肾病,目前,临床治疗CKD主要以肾功能保护为主要原则[1],通过血压、血脂及饮食控制等常规治疗能够有效逆转CKD患者肾功能损伤,改善生活质量并减少心血管并发症发生风险[2]。但CKD病程长且易反复,常规治疗虽然能稳定患者临床症状,但仍存在疗效不理想等局限性。血管钙化是CKD的常见并发症,会增加患者心血管疾病发生风险,影响预后[3]。前列地尔是一种具有血小板聚集抑制与血管扩张作用的前列腺素E1制剂,对于降低CKD患者尿蛋白含量、稳定肾小球血流动力学以及减小肾小球滤过膜孔径具有积极作用[4]。本研究旨在探讨前列地尔对CKD患者血管钙化的影响,报告如下。
1 资料与方法
1.1 一般资料 选取2019年1月—2021年12月恩施市中心医院76例CKD患者,采用随机数字表法分为对照组与研究组各38例,本研究经医学伦理委员会批准。对照组:男20例、女18例;年龄45~73岁,平均年龄(58.27±3.51)岁;体重指数19~26 kg/m2,平均(22.35±3.78)kg/m2;CKD病程4~11个月,平均(6.65±0.57)个月;临床分期:2期13例、3期25例;合并基础疾病:高血脂7例、高血压13例。研究组:男22例、女16例;年龄46~75岁,平均年龄(58.52±3.67)岁;体重指数18~28 kg/m2,平均(22.43±3.59)kg/m2;CKD病程5~10个月,平均(6.43±0.64)个月;临床分期:2期15例、3期23例;合并基础疾病:高血脂9例、高血压12例。2组患者一般资料比较差异不明显(P>0.05)。
纳入标准:(1)符合《慢性肾脏病筛查诊断及防治指南》[5]中CKD诊断标准:在排除其他可能导致肾功能损伤因素的前提下,患者连续3个月肾小球滤过率<60 mL/(min·1.73 m2);(2)臨床分期2~3期[5];(3)全程在该院接受检查与治疗;(4)年龄≥18岁;⑤患者自愿参与本研究。排除标准:(1)合并腹部器质性损伤;(2)合并其他原发性肾脏病变;(3)合并血液感染或自身免疫疾病;(4)合并精神疾病;(5)合并凝血功能异常。
1.2 方法 对照组患者接受常规治疗,严格控制作息与饮食,遵循清淡、营养均衡、少量多餐、低优质蛋白原则饮食,禁烟酒及高脂、高蛋白食物,每周保持合理运动,同时根据患者实际情况进行针对性的血脂、血压控制治疗,维持患者血压与血糖水平处于理想值(收缩压/舒张压<140/90 mm Hg、空腹血糖<7.0 mmol/L),疗程1个月。研究组在对照组基础上联合前列地尔进行治疗,给予前列地尔注射液(本溪恒康制药有限公司,规格2 mL/10 μg,国药准字H20093175),10 μg/次,与10 mL 0.9氯化钠注射液混合后进行静脉推注,1次/d,疗程1个月。
1.3 观察指标 (1)肾功能指标:治疗前后采集患者空腹静脉血,采用免疫比浊法检测血清肌酐(serum creatinine,SCr),并收集患者24 h尿液样本计算尿白蛋白排泄率(urinary albumin excretion rate,UAER)。(2)临床疗效评价:显效:治疗后尿频尿浊等症状完全消失,UAER较治疗前降低>20%、24 h尿蛋白降低>40%;有效:治疗后尿频尿浊等症状显著改善,UAER较治疗前降低10%~20%、24 h尿蛋白降低30%~40%;无效:未满足上述疗效评价标准[5],总有效率=(显效+有效)/总例数×100%。(3)血管钙化相关指标:治疗前后采集患者空腹静脉血,采用全自动生化分析仪检测血磷、血钙、血钾水平。(4)药物不良反应:统计2组治疗期间恶心呕吐、头晕头痛、静脉炎等发生情况。
1.4 统计学方法 采用SPSS 22.0统计学软件进行数据分析,计量资料行t检验,计数资料行χ2检验,P<0.05为差异有统计学意义。
2 结果
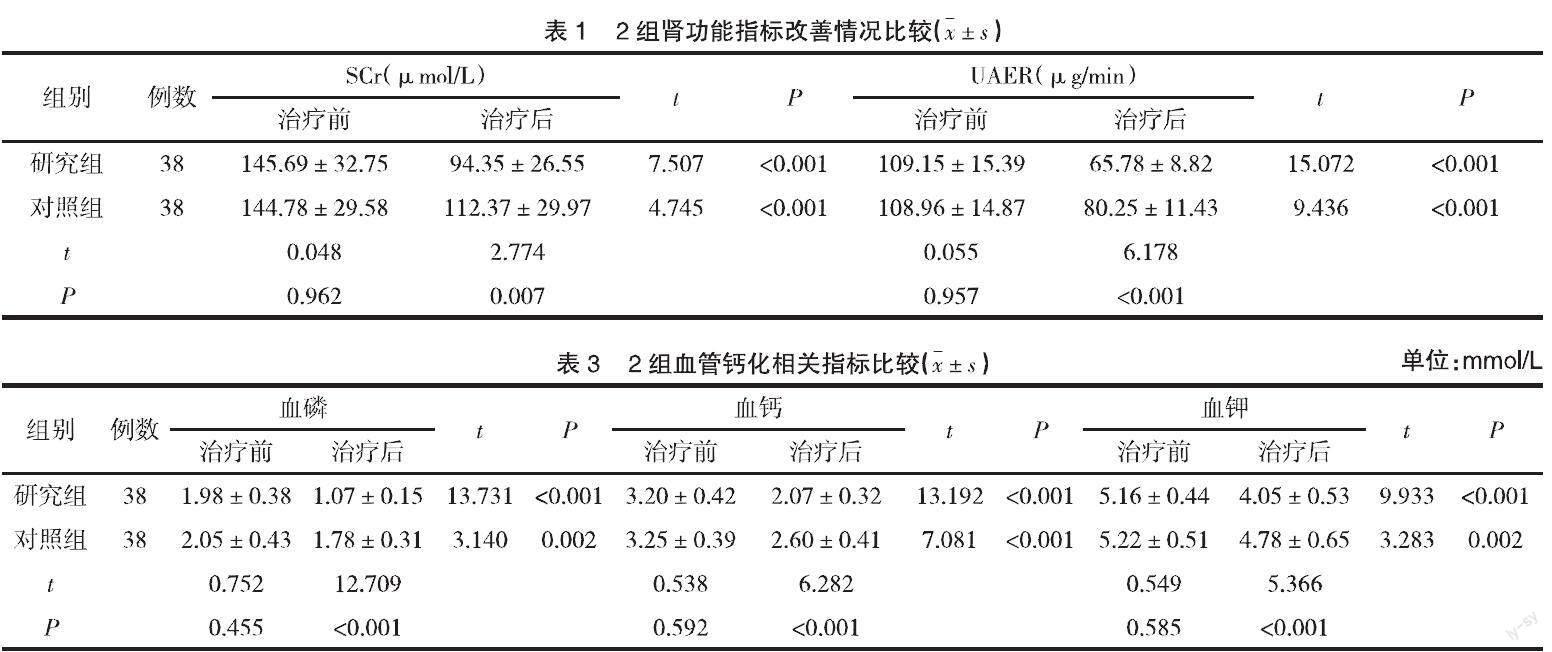
2.1 2组肾功能指标改善情况比较 治疗前2组的SCr、UAER水平差异无统计学意义(P>0.05);治疗后2组的SCr、UAER水平均低于治疗前,且研究组低于对照组,差异有统计学意义(P<0.05),见表1。
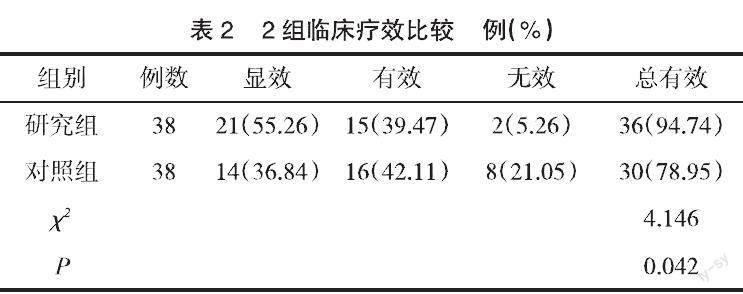
2.2 2组临床疗效比较 研究组治疗总有效率高于对照组,差异有统计学意义(P<0.05),见表2。
2.3 2组血管钙化相关指标比较 治疗前2组的血磷、血钙、血钾水平差异无统计学意义(P>0.05);治疗后2组的血磷、血钙、血钾水平均低于治疗前,且研究组低于对照组,差异有统计学意义(P<0.05),见表3。
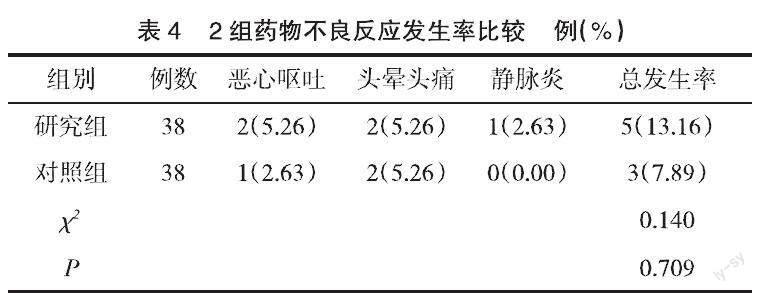
2.4 2组药物不良反应发生率比较 2组药物不良反应发生率比较,差异无统计学意义(P>0.05),见表4。
3 讨论
CKD可导致患者肾小球实质性改变和肾小球滤过率下降,若治疗不及时病情进展最终发展成为终末期肾脏病(end stage renal disease,ESRD),具有极强危害性。大量临床研究[6-7]表明,对早期CKD患者采取积极治疗能够有效延缓病情进展,预防ESRD的发生。因此如何在保证安全的前提下优化治疗结局、提高患者预后水平是临床医生考虑的重点问题。血糖、血压、血脂及饮食控制是临床治疗CKD的常规疗法,在纠正肾损伤、抑制病情进展、改善尿蛋白等方面具有积极意义。但常规疗法个体疗效差异较大且对于患者血管钙化的预防控制效果较弱,伴发血管钙化的风险较高,影响预后[8]。现代医学研究[9]证实,长期肾功能损伤引起的钙磷代谢紊乱可能导致CKD患者肺部及血管等组织的钙磷沉积,并最终导致血管钙化,增加心血管疾病发生风险。前列地尔能够改善人体局部微循环,提高肾脏及周围组织的血流量,保护肾功能。
目前,临床关于前列地尔对CKD患者血管钙化的保护效果尚不明确,故本研究探讨了前列地尔对CKD患者肾功能与血管钙化的保护作用。研究结果显示,治疗后研究组患者的UAER水平低于对照组(P<0.05),而UAER水平异常升高是CKD患者的主要临床表现,UAER水平与肾损伤程度呈正相关[10];该结果表明前列地尔治疗可有效保护CKD患者肾功能,促进肾功能的恢复,与张雪峰等[11]的研究基本对应。治疗后研究组患者的血磷与血钙水平低于对照组(P<0.05),表明前列地尔在抑制CKD患者血管钙磷沉积方面具有积极作用,可以降低血管钙化风险。研究组的治疗总有效率高于对照组(94.74% vs 78.95%),表明联合前列地尔治疗CKD的临床疗效优于常规治疗,与杨越[12]的研究基本对应。分析原因为前列地尔其具有抗血小板聚集、血管扩张、降低血黏度、改善微循环及溶栓等多种作用,可有效改善CKD患者肾脏血液循环,减轻局部血液循环障碍引起的神功功能损伤,进而降低了肾损伤风险,促进了患者肾功能的恢复;此外,由于前列地尔的血管扩张作用改善血液循环,从而降低了患者血管及肾脏组织的钙磷沉积风险,使得血磷与血钙水平降低,有效抑制了CKD患者血管钙化。2组药物不良反应率比较,研究组因加用前列地尔增加了1例静脉炎及1例恶心呕吐患者,但总体比较,2组药物不良反应发生率无明显差异(P>0.05),说明加用前列地尔治疗CKD,安全性较高。
综上所述,前列地尔治疗CKD的疗效确切,可有效改善患者血钙与血磷水平,降低血管钙化风险,同时还能促进肾功能的恢复,且安全性高,具有临床推广价值。
参考文献
[1] TRACZ J,HANDSCHUH L,LALOWSKI M,et al.Proteomic Profiling of Leukocytes Reveals Dysregulation of Adhesion and Integrin Proteins in Chronic Kidney Disease-Related Atherosclerosis[J].Journal of Proteome Research,2021,20(6):3053-3067.
[2] 张起铭,张妮娜.低蛋白米饮食在慢性肾脏病治疗中的应用研究[J].中国中西医结合肾病杂志,2020,21(2):158-159.
[3] 杨慧娟,陈卫东,潘艳.沙库巴曲缬沙坦在糖尿病并发慢性肾脏病和心血管疾病治疗中的研究进展[J].临床肾脏病雜志,2020,20(7):602-605.
[4] 刘冬玲,李莉,简新闻,等.前列地尔对肾功能不全患者造影剂肾病的预防作用研究[J].中国医药,2020,15(7):1067-1070.
[5] 上海慢性肾脏病早发现及规范化诊治与示范项目专家组,高翔,梅长林.慢性肾脏病筛查诊断及防治指南[J].中国实用内科杂志,2017,37(1):28-34.
[6] Clemens K K,AM Ouédraogo,Lam M,et al.Trends in basal insulin prescribing in older adults with chronic kidney disease in Ontario,Canada:A population-based analysis between 2010-2020[J].Diabetes,Obesity and Metabolism,2021,24(4):641-651.
[7] 马雷雷,王明哲,刘玉宁,等.肾炎防衰液延缓慢性肾脏病5期非透析患者透析时机的探索研究[J].中华中医药杂志,2020,35(4):2120-2123.
[8] NIKAGOLLA C,MEREDITH K T,DAWES L A,et al.Corrigendum to“Using water quality and isotope studies to inform research in chronic kidney disease of unknown aetiology endemic areas in Sri Lanka”[Sci.Total Environ.Volume 745(2020)/Article Number 140896][J].Science of The Total Environment,2021,757:144152-144163.
[9] 姚希,张凯旋.血清Apelin和补体C1q肿瘤坏死因子相关蛋白9与糖尿病肾病慢性肾脏病Ⅴ期患者血管钙化的关系[J].中华实用诊断与治疗杂志,2020,34(9):955-958.
[10] 王颖,朱铁虹,佟俊旺,等.糖尿病慢性肾脏疾病患者血清瘦素和血脂水平的变化及其临床意义的研究[J].中国糖尿病杂志,2015,23(8):711-713.
[11] 张雪峰,邱雨华,王轶萍,等.非布司他联合前列地尔对慢性肾脏病患者肾功能及血尿酸eGFR的影响[J].河北医学,2022,28(3):494-498.
[12] 杨越.慢性肾脏病予以肾康加前列地尔治疗的有效性研究[J].中国现代药物应用,2022,16(1):197-198.
(收稿日期:2023-02-13)
