血清葡萄糖参考方法的复现及一种避免校准品基质效应的赋值方法
2023-09-28林兵田园任瑞霞北京利德曼生化股份有限公司医学参考实验室北京100176
林兵,田园,任瑞霞(北京利德曼生化股份有限公司医学参考实验室,北京100176)
葡萄糖是一种六碳糖,在自然界中分布极为广泛,属醇醛类。人体血液中葡萄糖是生命活动的主要能量来源,它在人体内能直接参与新陈代谢过程。血液中葡萄糖含量的升高见于各型糖尿病[1]、妊娠期糖尿病[2]、糖尿病昏迷[3],降低见于胰岛瘤[4]、药物性低血糖[5]、酒精诱发的低血糖[6]、红细胞增多症等[7]。葡萄糖作为临床常规测量项目,目前检测方法主要有氧化酶法[8]、己糖激酶法[9]、葡萄糖脱氢酶法[10]等。其中己糖激酶法具有准确度高等优点,被美国临床化学协会标准委员会(AACC)于1980年提出作为候选参考方法。本研究以血清葡萄糖参考方法为比对方法,研究以不具备互换性的水溶液校准品作为工作校准品的赋值方法,通过采用常规测量方法与参考方法比对的方式验证工作校准品赋值方法的准确性。
1 材料与方法
1.1主要仪器与试剂 CARY100型紫外可见分光光度计购自美国Agilent公司,XSE205DU型分析天平、S220pH计均购自瑞士Mettler Toledo公司,移液器购自德国Eppendorf公司,离心机购自湖南湘仪实验室仪器开发公司,容量瓶购自日本ASONE公司。
Tris-Base、Tris-HCl、硫酸锌、氢氧化钡、5′三磷酸腺嘌呤(ATP)、氧化型β-烟酰胺腺嘌呤二核苷酸(NAD+)、醋酸镁、酚酞、乙醇、己糖激酶、6-磷酸葡萄糖脱氢酶均购自美国Sigma公司。有证参考物质SRM-917c和SRM-965b Level1~4均购自美国国家标准技术研究院(NIST)。2022年RELA样本由国际临床化学和检验医学联合会(IFCC)提供。葡萄糖水溶液工作校准品来源于北京利德曼公司。
1.2标准储备液与稀释液的配制方法 标准曲线稀释液:1 g/L安息香酸溶液;工作储备液:用SRM917c配制,浓度为55.5 mmol/L;工作标准液:分别移取0.0、2.5、5、10、15、20 mL储备液于50 mL容量瓶中,用1 g/L安息香酸溶液定容至刻度,配制成浓度为0.0、2.78、5.55、11.10、16.50、22.20 mmol/L标准工作液。
1.3蛋白质沉淀试剂配制与确认 酚酞指示剂:0.125 g酚酞溶解于25 mL乙醇中;饱和氢氧化钡溶液:80 g氢氧化钡溶解于1 000 mL无CO2水;硫酸锌溶液:22 g/L。0.11 mol/L氢氧化钡溶液:245 mL饱和氢氧化钡溶液用无CO2水稀释至1 000 mL,以酚酞为指示剂,用10 mL 0.11 mol/L氢氧化钡溶液滴定10 mL 22 g/L硫酸锌溶液确认溶液浓度是否正确,滴定允许误差为±0.1 mL。
1.4参考方法试剂配制 Tris-HCl原液:1.5%;Tris-Base原液:1.2%;Tris-Mg缓冲液:将1.1 g醋酸镁溶解于800 mL Tris-HCl原液和200 mL Tris-Base原液的混合液中;ATP原液:0.826 8 g ATP溶解于250 mL Tris-Mg缓冲液中;NAD+原液:0.995 2 g NAD+溶解于250 mL Tris-Mg缓冲液中;己糖激酶原液:1.25 KU己糖激酶溶解于250 mL Tris-Mg缓冲液中;6-磷酸葡萄糖脱氢酶原液:1.25 KU 6-磷酸葡萄糖脱氢酶溶解于250 mL Tris-Mg缓冲液中。
反应试剂:200 mL NAD+原液、200 mL ATP原液、800 U己糖激酶原液、800 U 6-磷酸葡萄糖脱氢酶原液,混合后以Tris-Mg缓冲液定容至1 000 mL。
1.5检测步骤 取0.5 mL血清或工作标准液加入5.0 mL 0.11 mol/L氢氧化钡溶液中,混匀5~10 s后加入5.0 mL 22 g/L硫酸锌溶液,剧烈震荡,充分混匀后以1 000×g离心10 min,取上清液0.5 mL加入2.5 mL反应试剂中,置于(25±1)℃水浴中反应10 min,然后将溶液加入比色皿中,在紫外可见分光光度计339 nm处读取溶液吸光度,计算葡萄糖浓度。
1.6精密度评价 取2022年RELA-A、RELA-B在多天内重复测定,计算2份样本的测定不精密度。
1.7正确度评价 测定有证参考物质SRM965b Level1-4,计算实测值与参考值之间的相对偏倚。
1.8校准品赋值与验证 以参考方法测定样本的浓度值为横坐标,任意校准品校准的常规方法测定样本信号值为纵坐标,绘制直线方程,将常规方法测量的工作校准品信号值代入直线方程中,计算其浓度。赋值后的工作校准品重新校准常规测量系统,采用与参考方法比对的方式验证赋值的有效性。
2 结果
2.1葡萄糖工作标准液的验证 根据1.2所述方法配制工作标准液,每天测试2次,测试4天,以理论浓度(X)为横坐标,测定吸光度均值(Y)为纵坐标建立曲线,直线方程为Y=0.049 63X+0.047 93,R2=1.000 0。
2.2精密度评价 4个工作日内,2份样本每天各测试4次,各16次测试结果的不精密度均小于1.5%,见表1。

表1 精密度验证结果
2.3正确度评价 测量有证参考物质SRM965 Level1-4各3次,偏差在±1.5%内,见表2。
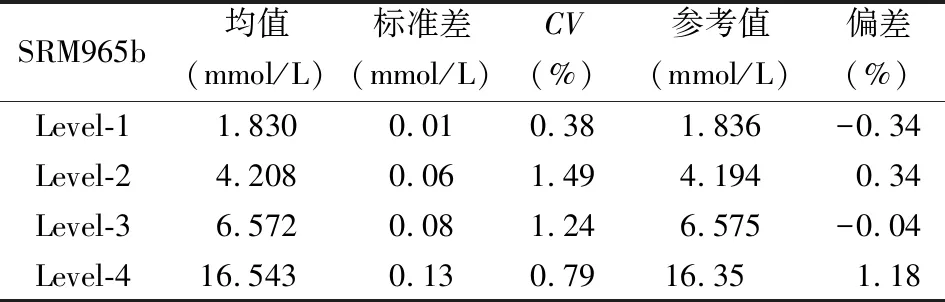
表2 正确度验证结果
2.4校准品赋值 参考方法和任意校准品校准的常规方法同时测定53例血清样本,以参考方法测定样本浓度值(X)与常规方法测定样本信号(Y)拟合直线方程,Y=500.74X-82.328,R2=0.999。同时将常规方法测定的工作校准品信号值代入方程中,计算浓度为9.92 mmol/L,不确定度为0.22 mmol/L(k=2)。
2.5校准品赋值验证 赋值后的工作校准品校准常规测量系统(Y)与参考方法(X)同时测试49例血清样本,直线方程为:Y=0.994 5X+0.023,R2=0.999 5,说明工作校准品赋值有效。
3 讨论
本研究复现了血清葡萄糖参考方法,评价了参考方法的2个主要性能:正确度、精密度。2022年RELA-A、RELA-B 2份样本的不精密度均小于1.5%,有证参考物质SRM965 Level1-4的偏倚均在±1.5%内,说明该方法具有良好的正确度与精密度。
检测系统是由仪器、校准品、试剂、操作程序等组成,而使用具有互换性与溯源性的校准品校准常规测量系统是实现检测结果一致化的前提。一般认为,校准品的互换性以混合血清最为理想[11],水溶液基质的校准品互换性则需要验证。使用参考方法直接赋值的混合血清作为测量系统的校准品,可实现溯源链的传递,提高测量系统检测结果的准确性及不同检测系统间检测结果的一致性[12-14],但血清来源困难,无法大量制备,且在低温储存的过程中,即使分析物保持稳定,血清基质的变化也可能会导致互换性发生改变,限制了混合血清的使用。
本研究中校准品的赋值方法与ISO 17511文件中描述的赋值方法不同,采用常规方法测得的信号值与参考方法测得的浓度值拟合曲线的方式对工作校准品进行赋值,避免了参考方法直接赋值校准品时由于校准品互换性差而导致结果不一致[15],同时可不再对工作校准品进行互换性验证即可实现使常规测量系统血清样本结果的量值溯源。减少了赋值过程,提高了常规方法测量结果的准确性。由于使用水基质校准品作为工作校准品,其制备简单,制作成本低,便于获得,稳定好,生物安全性高,有一定的应用价值。本研究的不足之处是未对多点校准对葡萄糖常规方法检测结果溯源性的影响进行探讨,因此后期需要继续实验研究。
