苯巴比妥钠对雌性BALB/c 小鼠的麻醉作用
2023-09-23郭凯凯王鹏辉
郭凯凯,冯 童,王鹏辉,高 畅
(1.海南医学院基础医学与生命科学学院,海南 海口 571199;2.海南医学院药学院, 海南 海口 571199)
小鼠是生物学和医学研究中最常见的哺乳动物之一,被广泛用于建立各种人类疾病模型。根据科学研究中动物伦理使用的3Rs(替换、减少和细化)原则,实验者应该采取措施以最大限度地减少实验动物的潜在压力和疼痛,促进动物的良好福利[1,2]。许多小鼠相关实验操作都需要使用麻醉,如采样、建模和外科研究。因此,有效的麻醉可以减轻小鼠的痛苦,帮助实验人员更好将其固定,确保实验的进行。可见,在小鼠及其他动物的手术操作中,适当的麻醉是成功完成实验的关键。
小鼠的全身麻醉有吸入麻醉和注射麻醉剂两种手段。异氟醚、七氟醚、氟烷或安氟醚吸入是麻醉小鼠的有效方法[3-5]。然而,吸入麻醉需要对实验动物进行精确监测,有较高的设备和技术要求,同时麻醉废气还可能会对实验者造成职业风险[6]。相比之下,注射麻醉只需要较少的辅助设备,易于实施,因此更常用于涉及小鼠模型的实验[7]。常见的注射麻醉剂包括巴比妥类药物、氯胺酮、依托咪酯、甲苯噻嗪、丙泊酚、替利他敏、阿法司琼、三溴乙醇、曲马多、美托咪定、咪达唑仑和布托啡诺[8-16]。在大多数国家和地区,麻醉剂是受管制的产品,其应用受到法律规范的严格限制[6,17]。
苯巴比妥钠(C12H11N2NaO3)是巴比妥类衍生物,在1904 年首次合成并于1912 年被引入临床癫痫治疗[18]。目前它仍是一种临床常用的镇静剂和催眠药,被世界卫生组织推荐用于低成本地治疗癫痫 持 续 状 态[19]。苯 巴 比 妥 钠 可 以 与γ-氨 基 丁 酸(GABA)受体结合,增加GABA 介导的氯通道开放的时间,使细胞膜超极化,增加动作电位阈值,从而抑制中枢神经系统活动[20]。苯巴比妥钠用于麻醉实验动物已有数十年的历史,早期的研究多通过翻正反射来评价麻醉诱导效果[21-23]。然而,翻正反射的单一指标并不能全面反应麻醉深度,因为实验动物在失去翻正反射后仍然可能处于清醒状态,并未达到实验手术要求。在实际操作中,还可能由于手术中的剧烈疼痛、强光刺激、温度改变、出血或操作时间延长等意外,导致实验动物从术中清醒。清醒的实验动物虽无法翻正,但实验人员往往难以有效识别其对疼痛的感知是否恢复,因此不能迅速、准确地完成照顾义务。这会带来潜在的伦理风险:实验动物感知痛苦的可能性,以及实验人员因此产生的心理负担[24]。因此,越来越多的研究者采用刺激指数的方法判断实验动物是否达到手术麻醉深度[25-27]。对于不同浓度/剂量的苯巴比妥钠诱导的小鼠麻醉能否达到实验手术深度标准,目前未见相关报道。为了更好地实现小鼠实验手术标准,为操作人员选择麻醉策略提供参考,本研究观察了不同浓度和剂量组合的苯巴比妥钠对雌性BALB/c 小鼠的麻醉效果,通过夹尾反射、前后肢退缩反射和眼睑反射等刺激指数观察了麻醉评分,并记录相关麻醉时间。
1 材料与方法
1.1 主要药品、试剂和仪器
注射用苯巴比妥钠购自上海新亚药业有限公司。氯化钠注射液(0.9%氯化钠)购自四川科伦药业股份有限公司。在注射药物前,使用氯化钠注射液将苯巴比妥钠粉末溶解并制成2%、5%和10%的浓度。小动物体温控制恒温系统(SS20-2)购自天津仪数科技有限公司。
1.2 实验动物
SPF 级雌性BALB/c 小鼠(18~20 g),8~12 周龄,购自北京维通利华实验动物技术有限公司,SCXK(京)2019-0009。小鼠饲养于符合优良实验室规范(GLP)的实验室中,控制室内温、湿度并进行12 h 光/暗循环,小鼠能够自由摄取食物和水。本课题实验操作遵循《实验动物饲养管理和使用指南》,并经过海南医学院伦理委员会批准。
1.3 实验方法
1.3.1 实验分组 将雌性BALB/c 小鼠随机分为15 组,每组6 只。每组小鼠接受一种浓度(2%、5%和10%)-剂量(75、100、125、150 和200 mg/kg)组合的麻醉方案。每只小鼠在腹膜注射苯巴比妥钠之前称重,每种浓度-剂量组合的注射体积如表1 所示。注射后,将小鼠置于38 °C 小动物体温控制恒温系统。

表1 不同浓度-剂量的苯巴比妥钠注射体积(每20 g 重小鼠)Tab 1 Injection volume of phenobarbital sodium at different concentrations and doses (every 20 g body weight mice)
1.3.2 小鼠麻醉刺激指数评分 根据Tsukamoto等[25]描述的方法,通过每只小鼠的夹尾反射、前后肢退缩反射和眼睑等刺激指数反射评估了麻醉深度。(1)夹尾反射(总分∶1):使用非创伤性镊子夹住小鼠的尾巴,如果尾巴不动,则得1 分。(2)前后肢退缩反射(总分∶2):使用非创伤性镊子分别轻轻拉动前肢和后肢,观察是否存在肌肉张力,如果有观察到退缩反应,则各得1 分。(3)眼睑反射(总分∶1),使用巴氏滴管吹出气流刺激小鼠的眼睛,如果小鼠不眨眼,则得1 分。在注射后5、10、20、30、60、90、120、150、180、210、240、270、300、330、360、390、420 和450 分钟对动物进行刺激。总分3 分或4 分被定义为达到手术麻醉深度。在评估过程中,同时记录发生呼吸困难和死亡的小鼠情况。
1.3.3 麻醉相关时间评估 在苯巴比妥钠注射完毕后,每只小鼠连续观察450 min,通过翻正反射(LORR)的出现和消失的时间来计算麻醉诱导时间和麻醉持续时间。将小鼠置于仰卧位并观察,若小鼠停止爬动且仰卧后30 s 内不能自行翻正,则视为LORR 消失。从麻醉剂注射到LORR 消失的时间为麻醉诱导时间;从LORR 消失到LORR 恢复之间的时间段为麻醉持续时间。
1.3.4 统计学处理 使用GraphPad Prism 软件进行统计分析。计数资料结果用率(%)表示,各组间数据比较采用χ2检验和Fisher 确切概率法。计量资料结果用平均值±标准偏差(±s)表示,各组间数据比较采用单因素方差分析(one-way ANOVA)。当在分析过程中进行多次比较时应用Bonferroni 校正。通过t检验进行差异显著性的检验。P<0.05为差异有统计学意义。
2 结果
2.1 安全性评价
各浓度-剂量苯巴比妥钠组小鼠呼吸困难率见表2。当苯巴比妥钠浓度为10%时,200 mg/kg 组小鼠出现呼吸困难比例显著高于75 mg/kg、100 mg/kg、125 mg/kg 和150 mg/kg 组小鼠(P<0.05)。其他浓度中各组间呼吸困难率均无显著性差异。

表2 各组小鼠的呼吸困难率(n=6,%)Tab 2 Dyspnea of female BALB/c mice in different groups(n=6,%)
各浓度-剂量苯巴比妥钠组小鼠死亡率见表3。同一浓度各用药组间死亡率均无显著性差异。此外,苯巴比妥钠的半数致死量 (LD50) 为10%~150 mg/kg 组合。
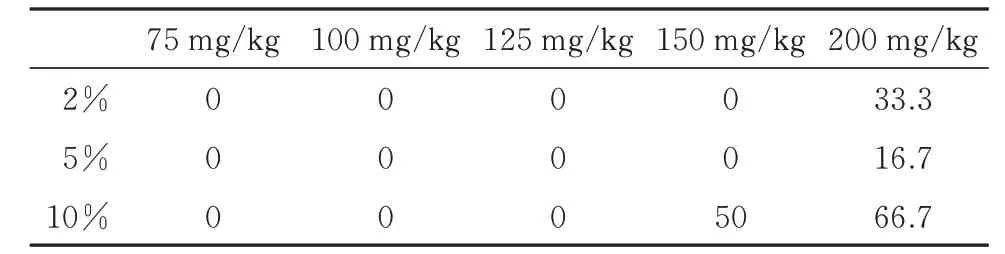
表3 各组小鼠的死亡率(n=6,%)Tab 3 Death of mice in different groups(n=6,%)
2.2 小鼠麻醉刺激指数评分
麻醉评分随着给药剂量的增加而增加。见图1。各浓度-剂量苯巴比妥钠组小鼠达到手术麻醉深度的小鼠百分率(达标率)见表4。当苯巴比妥钠浓度为2%时,200 mg/kg 组小鼠的达标率显著高于75 mg/kg 和100 mg/kg 组小鼠(P<0.05)。当苯巴比妥钠浓度为5%时,150 mg/kg 组小鼠的达标率显著高于75 mg/kg 和100 mg/kg 组小鼠(P<0.05);200mg/kg 组小鼠的达标率也显著高于75 mg/kg 和100 mg/kg 组小鼠(P<0.05)。当苯巴比妥钠浓度为10%时,各组间达标率均无显著性差异。

图1 苯巴比妥钠给药后的小鼠麻醉评分Fig 1 Anesthesia score of mice after administration of phenobarbital sodium
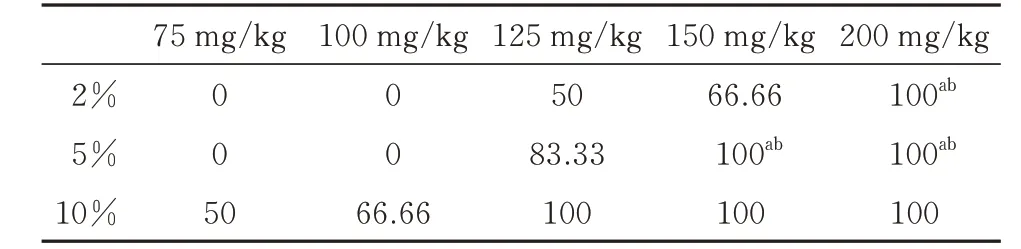
表4 各组小鼠达到手术麻醉水平的百分率(n=6,%)Tab 4 Mice reached surgical anesthesia in different groups(n=6,%)
2.3 LORR 情况
各浓度-剂量苯巴比妥钠组小鼠发生LORR 的百分率见表5。当苯巴比妥钠浓度为2% 时,150 mg/kg 组小鼠的LORR 百分率显著高于75 mg/kg和100 mg/kg 组小鼠(P<0.05);200 mg/kg 组小鼠的LORR 百分率也显著高于75 mg/kg 和100 mg/kg 组小鼠(P<0.05)。当苯巴比妥钠浓度为5%时,125 mg/kg、150 mg/kg、200 mg/kg 组小鼠的LORR百分率显著高于75 mg/kg 组小鼠(P<0.05)。当苯巴比妥钠浓度为10%时,各组间LORR 百分率均无显著性差异。见表5。
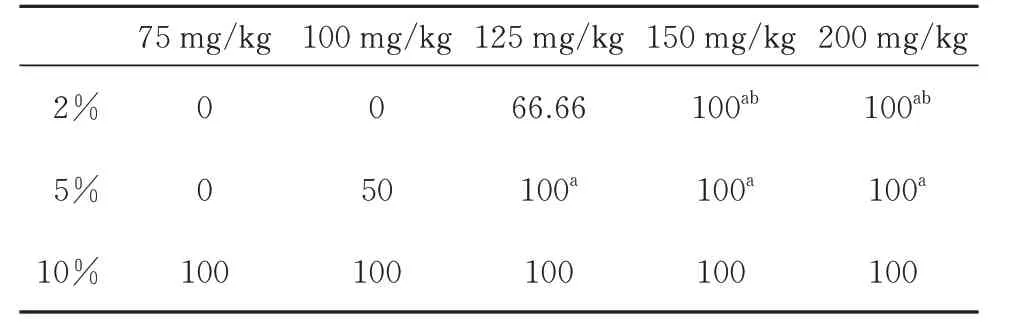
表5 各组小鼠的LORR 百分率(n=6,%)Tab 5 LORR of micein different groups(n=6,%)
2.4 麻醉诱导时间
各浓度-剂量苯巴比妥钠组的麻醉诱导时间见表6。其中,当苯巴比妥钠浓度为2%时,200 mg/kg组的麻醉诱导时间比125 mg/kg 组和150 mg/kg 组显著延长(P<0.05)。当苯巴比妥钠浓度为5%时,200 mg/kg 组的麻醉诱导速度显著快于100 mg/kg、125 mg/kg 和150 mg/kg 组(P<0.05)。当苯巴比妥钠 浓 度 为10% 时,125 mg/kg、150 mg/kg 和200 mg/kg 组的麻醉诱导速度显著快于75 mg/kg 和100 mg/kg 组(P<0.05)。
表6 各组小鼠的麻醉诱导时间(min,n=6,±s)Tab 6 Anesthetic induction time in different groups (min,n=6,±s)

表6 各组小鼠的麻醉诱导时间(min,n=6,±s)Tab 6 Anesthetic induction time in different groups (min,n=6,±s)
注:a 与相同浓度的75 mg/kg 组相比具有显著差异 (P<0.05) ;b 与相同浓度的100 mg/kg 组相比具有显著差异 (P<0.05); c 与相同浓度的125 mg/kg 组相比具有显著差异 (P<0.05); d与相同浓度的150 mg/kg 组相比具有显著差异 (P<0.05)。
F 75 mg/kg- -- -27.5±7.18 100 mg/kg- -43.00±19.70 33.83±5.71 125 mg/kg 43.00±15.06 35.50±7.92 10.50±1.05ab 150 mg/kg 39.17±8.86 34.83±5.27 10.67±2.66ab 200 mg/kg 14.00±4.24cd 14.67±3.01bcd 11.83±1.47ab 15.14 9.95 34.99 2%5%10%
2.5 麻醉持续时间
各浓度-剂量苯巴比妥钠组的麻醉持续时间见表7。当苯巴比妥钠浓度为2%时,75 mg/kg 和100 mg/kg 组显示出镇静作用,但没有麻醉效果;此外,200 mg/kg 组的麻醉持续时间显著长于100 mg/kg、125 mg/kg 和150 mg/kg 组(P<0.05)。当苯巴比妥钠浓度为5%时,75 mg/kg 组仅表现出镇静作用;125 mg/kg 组的麻醉持续时间明显长于75 mg/kg 组(P<0.05);150 mg/kg 组的麻醉持续时间明显长于75 mg/kg、100 mg/kg 组(P<0.05);200 mg/kg 组的麻醉持续时间显著长于75 mg/kg、100 mg/kg、125 mg/kg 和150 mg/kg 组(P<0.05)。在10%浓度的苯巴比妥钠下,125 mg/kg 组的麻醉持续时间明显长于75 mg/kg 和100 mg/kg 组(P<0.05)。
表7 各组小鼠的麻醉持续时间(min,n=6,±s)Tab 7 Anesthetic duration in different groups(min,n=6,±s)

表7 各组小鼠的麻醉持续时间(min,n=6,±s)Tab 7 Anesthetic duration in different groups(min,n=6,±s)
注:a 与相同浓度的75 mg/kg 组相比具有显著差异 (P<0.05) ;b 与相同浓度的100 mg/kg 组相比具有显著差异 (P<0.05); c 与相同浓度的125 mg/kg 组相比具有显著差异 (P<0.05); d与相同浓度的150 mg/kg 组相比具有显著差异 (P<0.05)。
75 mg/kg F 100 mg/kg 10.17±24.90 46.50±62.38 129.5±94.42 125 mg/kg 48.00±44.77 106.00±39.59a 401.00±120.00ab 150 mg/kg 68.33±37.98 131.70±36.75ab 340.00±121.00 200 mg/kg 331.80±162.30abcd 447.20±6.94abcd 311.80±155.60 18.55 135.50 5.63 2%5%10%0 0 159.7±109.1
3 讨论
3R 理论的提出者Russell 在1959 年的学术经典《人道的实验技术原理》(The Principles of Humane Experimental Technique)中就提出,麻醉是“人道技术中最伟大的进步”[28]。适当的麻醉是进行外科动物实验的重要组成部分,正确使用麻醉剂能在维护动物福利的同时,保证科学研究的完整性和准确性[29]。然而,目前没有针对实验动物的统一麻醉程序。注射麻醉操作简单,被广泛应用于小鼠的实验研究[7]。苯巴比妥钠是一种巴比妥类药物,具有较大的治疗指数[30,31]。然而,不同浓度、剂量的苯巴比妥钠诱导的小鼠麻醉是否能达到手术标准,未见相关报道。在本研究中观察不同浓度-剂量组合的苯巴比妥钠对雌性BALB/c 小鼠的麻醉安全性、评分、诱导及维持时间,寻找适合手术操作的苯巴比妥钠浓度-剂量组合策略。
苯巴比妥钠是一种广泛使用的镇静催眠药物。由于其有效性和耐受性好,长期被用于临床病人,尤其是新生儿的惊厥性癫痫的治疗[32]。研究表明,过量服用苯巴比妥钠会导致不良反应,包括神经毒性作用、呼吸抑制和低血压[33]。研究结果显示,苯巴比妥钠在高浓度和高剂量组合(2%/5%/10%~200 mg/kg,以及10%~150 mg/kg)下会导致小鼠死亡。苯巴比妥钠麻醉小鼠的LD50为10%~150 mg/kg 组合。研究结果表明,高浓度和高剂量是麻醉相关死亡的关键风险因素。同时,在本研究中观察到高浓度、剂量组的部分小鼠出现了呼吸困难。许多研究已经证明,苯巴比妥与GABA 受体的结合使氯离子通道保持开放,这会导致呼吸髓质神经元的膜电位超极化,从而导致呼吸频率下降[20,34]。推测GABA 受体活化导致的呼吸抑制可能是高剂量苯巴比妥钠导致小鼠死亡的主要原因。此外,在各组中没有观察到其他明显的副作用。推测5%~150 mg/kg 苯巴比妥钠或者10%~125 mg/kg 苯巴比妥钠可能是麻醉雌性BALB/c 小鼠的最大安全浓度和剂量组合。
在外科实验操作中,通过一定深度的麻醉让动物达到并保持无意识和镇痛状态对实验动物的福利至关重要[6]。翻正反射是麻醉评价的常见指标,但并不足以评价麻醉效果是否达到手术要求的深度。在本研究中通过夹尾反射、前后肢退缩反射和眼睑反射进行了测试,以评估小鼠的麻醉深度,以总分3 或4 的麻醉深度认定为符合手术要求。研究表明,苯巴比妥钠麻醉小鼠的半数有效量(AD50)分别在2%和125 mg/kg 以及10%和75 mg/kg,这意味着浓度和剂量都会影响麻醉效果。苯巴比妥钠引起的麻醉深度具有显著的剂量依赖性。当以2%的浓度给予200 mg/kg 苯巴比妥钠时,每只小鼠都能达到了手术麻醉深度(评分>3),但是麻醉持续时间长达5 h,远高于1~2 h 的实验性手术时间。因此,2%和200 mg/kg 苯巴比妥钠的组合可能不适用于外科手术。当苯巴比妥钠浓度为5%和10%时,125、150 和200 mg/kg 剂量能让80%以上的小鼠达到手术标准。由于5%~200 mg/kg、10%~125 mg/kg、10%~150 mg/kg 以及10%~200 mg/kg 剂量组的小鼠达到手术麻醉深度的比例较高,用于外科手术实验小鼠麻醉的苯巴比妥钠应在上述几个浓度-剂量组合中选择。
麻醉的诱导和持续时间是评估动物麻醉效果的基本指标。将苯巴比妥钠注射到小鼠腹腔后,小鼠的兴奋性会明显升高,并在一段时间后进入呼吸加速、步态不稳定和向前爬行的状态,直到出现LORR。有研究表明,100~135 mg/kg 的苯巴比妥钠是在小鼠中诱导催眠作用的剂量[35,36]。同样研究表明,低浓度和小剂量的苯巴比妥钠(≤2%~100 mg/kg 或≤5%~75 mg/kg)会对小鼠产生镇静和催眠作用。随着浓度和/或剂量的增加,苯巴比妥钠对诱导了小鼠进入麻醉状态,包括LORR 诱导,失去了夹尾反射、前后肢退缩反射和眼睑反射。因此,苯巴比妥的作用具有显著的剂量依赖性。另外,随着苯巴比妥钠浓度和/或剂量的增加,麻醉诱导时间逐渐缩短,麻醉持续时间明显延长。然而,发现在10% 苯巴比妥钠浓度组中,150 mg/kg 及200 mg/kg 组的平均麻醉持续时间并未长于125 mg/kg 组。推测动物死亡是高浓度剂量苯巴比妥钠组麻醉持续时间意外缩短的原因。因此,建议在小鼠手术麻醉中使用5% 和125 mg/kg 以及5% 和150 mg/kg 组合的苯巴比妥钠。
值得注意的是,当应用高浓度-剂量苯巴比妥钠时,小鼠的麻醉持续时间过长,一些死亡发生在给药后8~24 h 之间。尽管有恒温系统支持,尚不清楚体温过低是否是小鼠死亡的原因之一。此外,本研究有几个局限性。首先只研究了苯巴比妥钠对8-12 周龄雌性BALB/c 小鼠的麻醉作用。然而,麻醉 剂 的 效 果 受 到 品 系、性 别 和 年 龄 的 影 响[25,37,38]。这些因素需要充分考虑,才能在实践中达到更好的麻醉效果。其次没有评估苯巴比妥钠引起的生理指标的变化。需要进一步研究苯巴比妥钠麻醉期间体温、血氧饱和度、血压、心率和肌肉放松等生命体征的变化。此外推测部分苯巴比妥钠高剂量组的麻醉持续时间可能长于一般实验性手术所需时间。由于不同麻醉剂的联合使用已成为基础研究和 临 床 应 用 的 一 种 趋 势[6,39,40],苯 巴 比 妥 钠 和 其 他麻醉剂的联合作用还有待探索。
综上所述,本研究为苯巴比妥钠用于小鼠实验的安全性、麻醉评分、麻醉诱导和持续时间提供了基本信息。研究发现苯巴比妥钠单独使用可以为雌性BALB/c 小鼠的手术麻醉提供适当的深度和持续时间。麻醉方案对实验动物手术的成功至关重要,实验人员可以根据手术所需的麻醉时间选择适当的苯巴比妥钠浓度-剂量组合。本研究为麻醉药物的选择,保障小动物外科手术性实验的进行和实验动物福利的改善提供了基础。
作者贡献度说明:
高畅:设计实验、撰写论文;郭凯凯,冯童,王鹏辉:参与动物实验,记录数据,参与讨论。
本文作者声明不存在任何利益冲突。
