碱法提取普洱茶渣膳食纤维的工艺优化
2023-09-19孟圆夏婷程艳耿贝贝权冰艳宋睿喆于金浩王敏白晓丽
孟圆,夏婷*,程艳,耿贝贝,权冰艳,2,宋睿喆,于金浩,王敏,白晓丽
(1. 天津科技大学 生物工程学院省部共建食品营养与安全国家重点实验室,天津 300457;2. 天士力医药集团股份有限公司 创新中药关键技术国家重点实验室,天津 300410)
茶起源于我国,已有千年发展历史,并成为风靡世界的三大无酒精饮料之一[1-2]。近年来,我国茶产业发展迅速,种植面积不断扩大,产量急剧增长,2021 年茶园面积达326 亿m2,茶叶产量达306 万t[3]。普洱茶属于黑茶,是以云南大叶种晒青茶为原料,经发酵制成,具有独特品质特征。普洱茶中含有多种营养成分,膳食纤维含量9%~22%,蛋白质含量20%~30%,此外还含有茶褐素、茶多酚和茶多糖等活性成分[4]。据报道,约90%的茶叶在加工和消费后成为茶渣,这些茶渣通常被直接丢弃,会造成环境污染,此外,茶渣也通常作为燃料、肥料、生物吸附剂直接使用[5-6]。目前茶渣中营养物质的有效利用仍不足,因此,对普洱茶废弃物的高值化利用具有重要的科学意义。
膳食纤维是一种不被人体消化酶所消化,也不被小肠吸收的以多糖为主体的高分子物质的总称[7]。膳食纤维被称为人类第七大营养素,按照溶解性可分为水溶性膳食纤维和水不溶性膳食纤维。其中水不溶性膳食纤维具有良好的吸水性和膨胀性,能调节肠道功能,防止便秘,同时对心血管疾病、糖尿病、结肠癌等具有预防作用[8]。近年来多项研究显示化学法、物理法、酶法和发酵法是膳食纤维的主要提取方法[9]。其中化学法中的碱法是膳食纤维提取的常用方法。丁莎莎[10]采用质量分数为8%的NaOH 溶液提取油橄榄果渣膳食纤维,结果得到产率为52.39%的油橄榄果渣不溶性膳食纤维。Wang 等[11]发现采用5%的NaOH 提取得到的猕猴桃膳食纤维含量相较于酶法、酸法更高,并且提取后膳食纤维表现出更高的热稳定性。Karra 等[12]发现碱法提取的椰枣花膳食纤维含量为89.75%,比水提取的椰枣花膳食纤维含量高,并且蛋白质和脂质含量较水提法明显降低。因而,采用碱法能更有效地提高膳食纤维提取率,更好地去除植物中的蛋白质和脂质杂质。
本研究拟以普洱茶渣为原料,采用碱法提取普洱茶渣中的膳食纤维(tea dietary fiber,TDF),通过Box-Behnken 试验设计和响应面分析,获得最佳提取工艺条件。并对提取前后的普洱茶渣中TDF 的含量及组成进行分析,以期提高普洱茶渣的综合利用价值。
1 材料与方法
1.1 材料与试剂
茶渣:云南天士力帝泊洱生物茶集团有限公司;氢氧化钠:天津市致远化学试剂有限公司;盐酸:福晨(天津)化学试剂有限公司;95%乙醇:康科德科技有限公司;硫酸:国药集团化学试剂有限公司;十氢化萘、双氧水:天津市大茂化学试剂厂;无水亚硫酸钠:天津渤化化学试剂有限公司;丙酮:洛阳昊华化学试剂有限公司;十六烷基三甲基溴化铵:广东翁江化学试剂有限公司。以上试剂均为分析纯。
1.2 仪器与设备
火焰原子吸收光谱仪(GGX-100):北京海光仪器有限公司;紫外分光光度计(U-3900):日立株式会社;鼓风干燥箱(UF160):美墨尔特(上海)贸易有限公司;电热鼓风干燥箱(WGLL-125BE):天津市泰斯特仪器有限公司;快速水分测定仪(MA37-1CN):赛多利斯科学仪器(北京)有限公司;集热式恒温加热磁力搅拌器(DF-101S):邓州长城科工贸有限公司;马弗炉(SX2-2.5-10):天津市中环实验电炉有限公司;粗脂肪测定仪(SZF-06A):上海新嘉电子有限公司;数控超声波清洗器(KQ-500DB):昆山市超声仪器有限公司。
1.3 试验方法
1.3.1 茶膳食纤维碱法提取工艺
称取15 g 茶渣,按料液比1∶25(g/mL)加入1.40%的NaOH 溶液,搅拌至分散均匀,再进行超声辅助提取1 h,提取完毕后,水洗涤提取后的样品,直至滤液为中性,过滤,滤渣在105 ℃鼓风干燥箱中干燥,备用。
1.3.2 单因素试验
1)在固定碱解温度60 ℃、碱解时间1 h、料液比1∶10(g/mL)的条件下,考察碱液浓度(1%、2%、3%、4%、5%)对TDF 提取率的影响。
2)在固定碱液浓度2%、碱解时间1 h、料液比1∶10(g/mL)的条件下,考察碱解温度(60、70、80、90、100 ℃)对TDF 提取率的影响。
3)在固定碱液浓度2%、碱解温度60 ℃、料液比1∶10(g/mL)的条件下,考察碱解时间(1、2、3、4、5 h)对TDF 提取率的影响。
4)在固定碱液浓度2%、碱解温度60 ℃、碱解时间1 h 的条件下,考察料液比[1∶10、1∶20、1∶30、1∶40、1∶50(g/mL)]对TDF 提取率的影响。
1.3.3 响应面试验
基于单因素试验结果,根据Box-Behnken 中心组合试验设计原理,以碱液浓度(A)、碱解温度(B)、碱解时间(C)、料液比(D)为自变量,以TDF 提取率为响应值,采用四因素三水平的响应面分析方法求取优化的工艺参数,试验因素及水平如表1 所示。

表1 Box-Behnken 设计试验因素及水平Table 1 Factors and levels of Box-Behnken design
1.3.4 茶渣基本成分测定
1.3.4.1 总膳食纤维含量测定
参照GB 5009.88—2014《食品安全国家标准食品中膳食纤维的测定》测定总膳食纤维含量。
1.3.4.2 纤维素、半纤维素和木质素含量测定
参考Escarnot 等[13]的方法稍作修改,测定纤维素、半纤维素和木质素含量,具体操作方法如下。
中性洗涤纤维测定:准确称取1.00 g(M1)样品,添加100 mL 中性洗涤剂、数滴十氢化萘及0.5 g 无水亚硫酸钠,煮沸1 h,在已知质量的坩埚(M2)中用沸水和丙酮洗涤残渣。将残渣在105 ℃烘箱干燥过夜,冷却至室温后,称量恒重(M3)。
酸性洗涤纤维测定:准确称取1.00 g(M4)样品与酸性洗涤液(2%十六烷三甲基溴化铵)煮沸1 h,在已知质量的坩埚(M5)中用蒸馏水和丙酮清洗残渣,将清洗后的残渣放置在105 ℃烘箱中干燥过夜,冷却至室温后,称量恒重(M6)。
纤维素含量测定:向酸性洗涤过程中剩余的残渣中添加72%的硫酸进行消化3 h,消化完毕后用热蒸馏水清洗残渣,残渣再次在105 ℃烘箱干燥过夜,冷却至室温后,称量恒重(M7)。
木质素含量测定:将纤维素测定剩余的残渣置于马弗炉中550 ℃煅烧3 h 灰化,称量恒重(M8)。
中性洗涤纤维含量(Y1,%)按下列公式计算。
式中:M1为中性洗涤时试样的质量,g;M2为坩埚的质量,g;M3为坩埚和中性洗涤剩余残渣的质量,g。
酸性洗涤纤维含量(Y2,%)按下列公式计算。
式中:M4为酸性洗涤时试样的质量,g;M5为坩埚的质量,g;M6为坩埚和酸性洗涤后剩余残渣的质量,g。
纤维素含量(Y3,%)按下列公式计算。
式中:M7为经72%硫酸处理后的残渣的质量,g。
木质素含量(Y4,%)按下列公式计算。
式中:M8为经72%硫酸处理后的残渣灰化后的质量,g。
半纤维素含量(Y5,%)按下列公式计算。
1.3.4.3 果胶含量测定
参考Blumenkrantz 等[14]的方法测定果胶含量。
1.3.5 数据分析处理
所有试验均重复3 次,结果以平均值±标准差表示。采用SPSS 25.0 对试验数据进行ANOVA 方差分析和Tukey 显著性检验。P<0.05 表示组间的差异具有统计学意义。
2 结果与分析
2.1 茶膳食纤维提取单因素试验分析
2.1.1 碱液浓度对TDF 提取率的影响
碱液浓度对TDF 提取率的影响见图1。
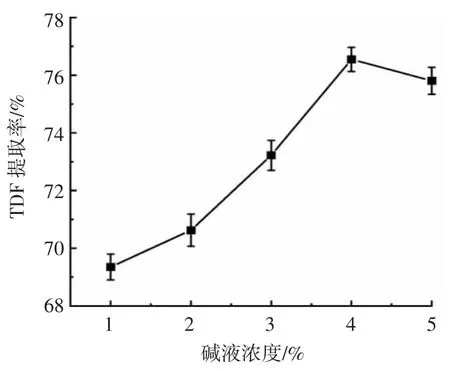
图1 碱液浓度对TDF 提取率的影响Fig.1 Effect of alkali concentration on the yield of TDF
如图1 所示,随着碱液浓度的提高,TDF 提取率呈现先上升后下降的趋势,当碱液浓度到达4%时TDF提取率达到最高,碱液浓度为5%时TDF 提取率下降。在TDF 提取工艺中,NaOH 主要发挥水解茶渣中蛋白质,皂化脂质和去除其他水溶性杂质的作用[15]。碱液浓度过高会使部分纤维水解[16],因此,这可能是碱液浓度为5%时TDF 提取率下降的原因。此外,碱液浓度过高会增加工业生产成本和对设备的腐蚀性[17]。因此,选择TDF 提取的碱液浓度为3%~5%,进行下一阶段的响应面优化试验。
2.1.2 碱解温度对TDF 提取率的影响
碱解温度对TDF 提取率的影响见图2。

图2 碱解温度对TDF 提取率的影响Fig.2 Effect of alkaline extraction temperature on the yield of TDF
如图2 所示,随碱解温度的升高,TDF 提取率呈现上升趋势,当温度升至90 ℃后,TDF 提取率趋于稳定,没有明显变化。可能是温度升高会促进原料中蛋白质的溶胀、降解和脱离[18]。李镕基等[19]发现随着碱浸温度的升高,蛋白质含量逐渐下降,当温度升至90 ℃时TDF 提取率达到最高。He 等[20]发现在高浓度碱液和高温下能更彻底地去除淡竹叶中的杂质,得到更高纯度的淡竹叶纤维。因此,综合经济成本、环境等因素考虑,选择碱解温度为80~100 ℃进行后续响应面优化试验。
2.1.3 碱解时间对TDF 提取率的影响
碱解时间对TDF 提取率的影响见图3。
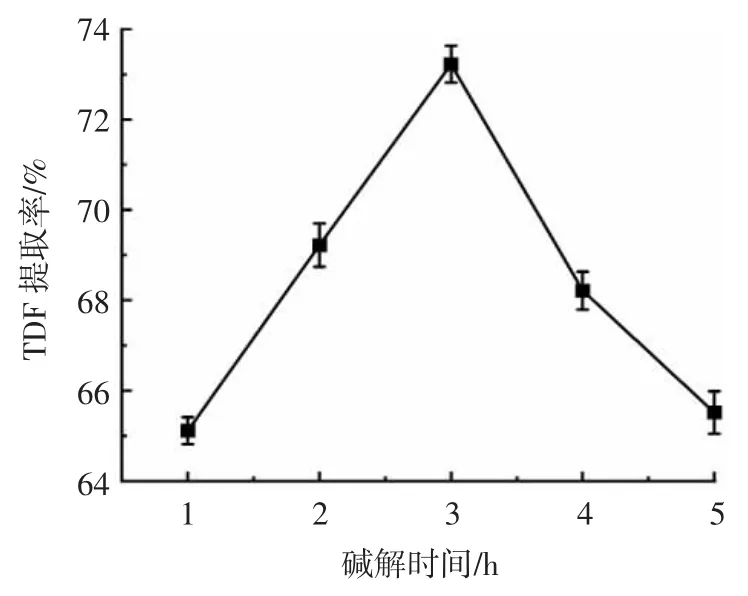
图3 碱解时间对TDF 提取率的影响Fig.3 Effect of alkaline extraction time on the yield of TDF
如图3 所示,随着碱解时间的延长,TDF 提取率逐渐上升,当碱解时间达到3 h 时,TDF 提取率达到最高,之后随着碱解时间的延长,TDF 提取率呈现下降趋势。碱解时间过长会导致部分纤维素和半纤维素发生水解[21],这是茶渣中TDF 提取率在3 h 后下降的原因。碱解时间延长能增加杂质的溶出率,也会降低膳食纤维含量百分比[22]。因此,选择碱解时间为2~4 h 进行后续响应面优化试验。
2.1.4 料液比对TDF 提取率的影响
料液比对TDF 提取率的影响见图4。
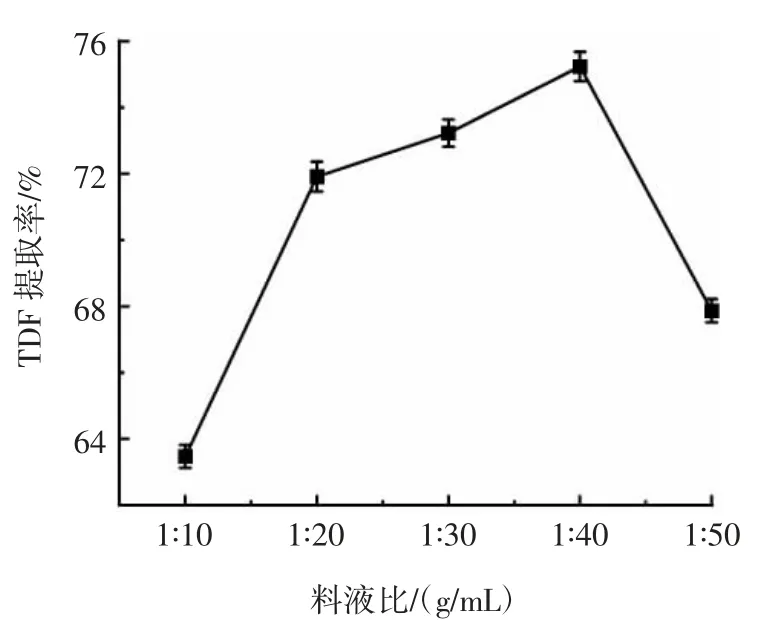
图4 料液比对TDF 提取率的影响Fig.4 Effect of solid-to-liquid ratio on the yield of TDF
如图4 所示,增加NaOH 溶液体积能提高TDF 提取率,当料液比为1∶40(g/mL)时,TDF 提取率达到最高,之后随NaOH 溶液体积增加,TDF 提取率出现下降趋势,NaOH 溶液体积增大,原料与提取溶剂的接触面积增大,进而增加杂质的溶出[23]。因此,选择料液比1∶20~1∶40(g/mL),进行下一阶段的响应面优化试验。
2.2 茶膳食纤维提取响应面优化分析
2.2.1 响应面试验结果
选择碱液浓度(A)、碱解温度(B)、碱解时间(C)及料液比(D)为考察对象,进行响应面优化试验,试验方案及结果如表2 所示。
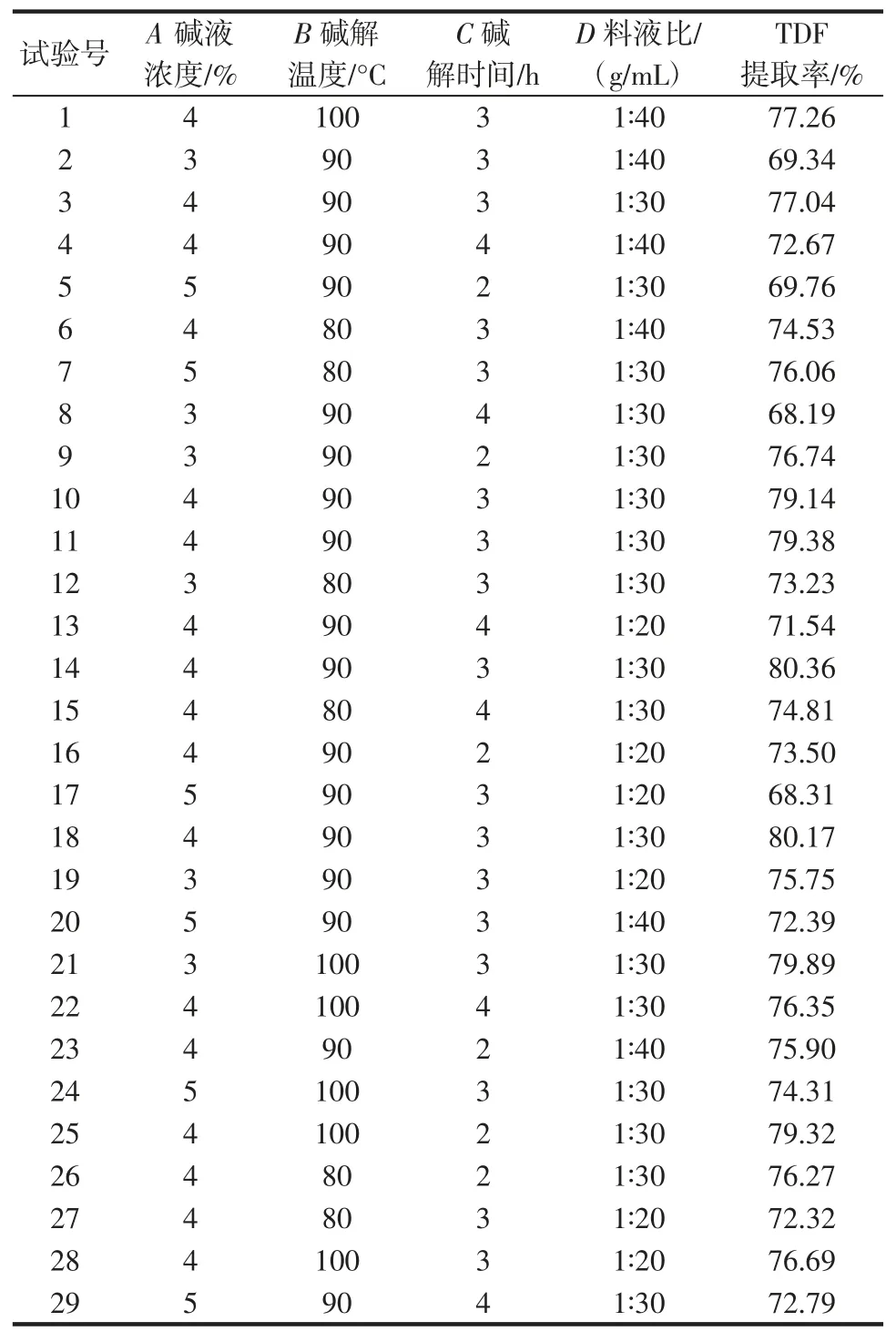
表2 响应面设计方案及结果Table 2 The response surface design and test results
2.2.2 响应面回归模型的建立及显著性检验
对响应面得到的试验结果进行多元拟合,得到碱液浓度(A)、碱解温度(B)、碱解时间(C)及料液比(D)4个因素与响应值TDF 提取率(Y)之间的二次多项回归方程:Y(TDF 提取率)=79.22-0.79A+1.38B-1.26C+0.33D-2.10AB +2.89AC +2.62AD -0.38BC -0.41BD -0.32CD -4.09A2+0.19B2-2.71C2-3.66D2。
方差分析结果见表3。
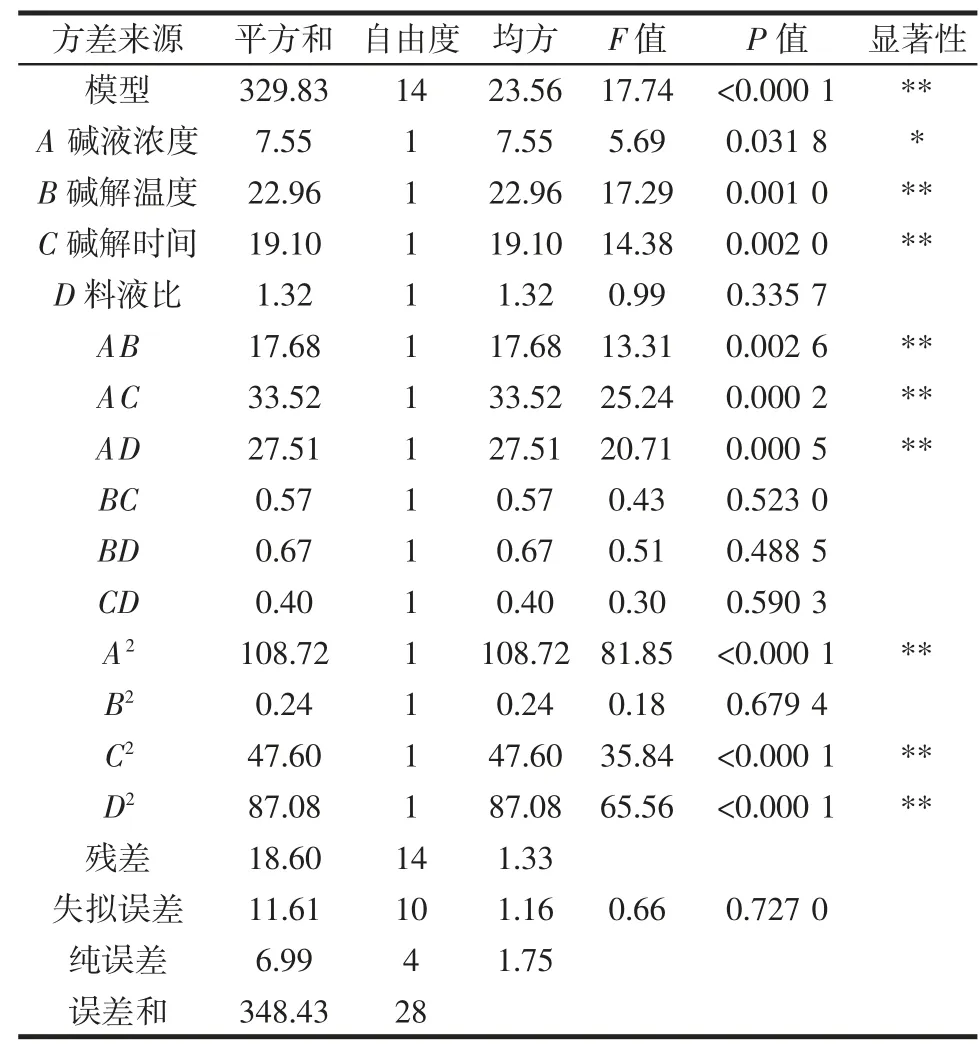
表3 方差分析结果Table 3 Analysis of variance
由表3 可知,该回归模型极显著(P<0.000 1),失拟项P=0.727 0>0.05。此外,模型的确定系数R2=0.946 6,R2Adj=0.893 3,结果表示本次拟合的模型能够解释89.33%的响应值变化。由表3 可知,影响TDF 提取率的4 个因素大小顺序为B>C>A>D,即碱解温度>碱解时间>碱液浓度>料液比。由该模型优化得到的最优工艺为碱液浓度3.35%、碱解温度100 ℃、碱解时间2.36 h、料液比1∶28(g/mL),在该条件下得到的TDF 提取率理论值为82.259%。
2.2.3 各因素相互作用对膳食纤维提取率的影响
为了更加直观地表示各因素交互作用与TDF 提取率之间的关系,通过Box-Behnken 试验设计,将4 个影响因素(碱液浓度、碱解温度、碱解时间及料液比)与TDF 提取率组成三维响应曲面。各因素交互作用对膳食纤维提取率的影响见图5。
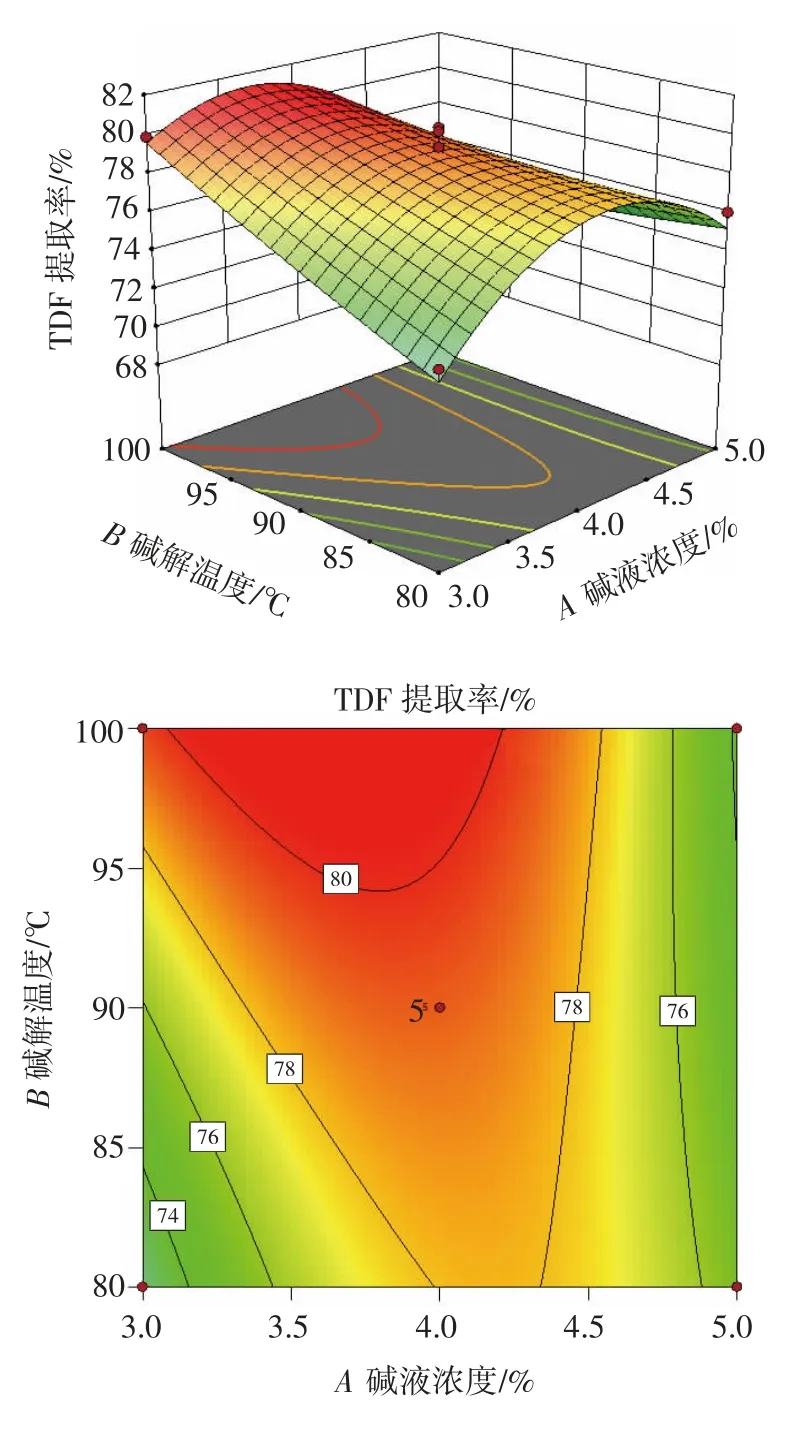
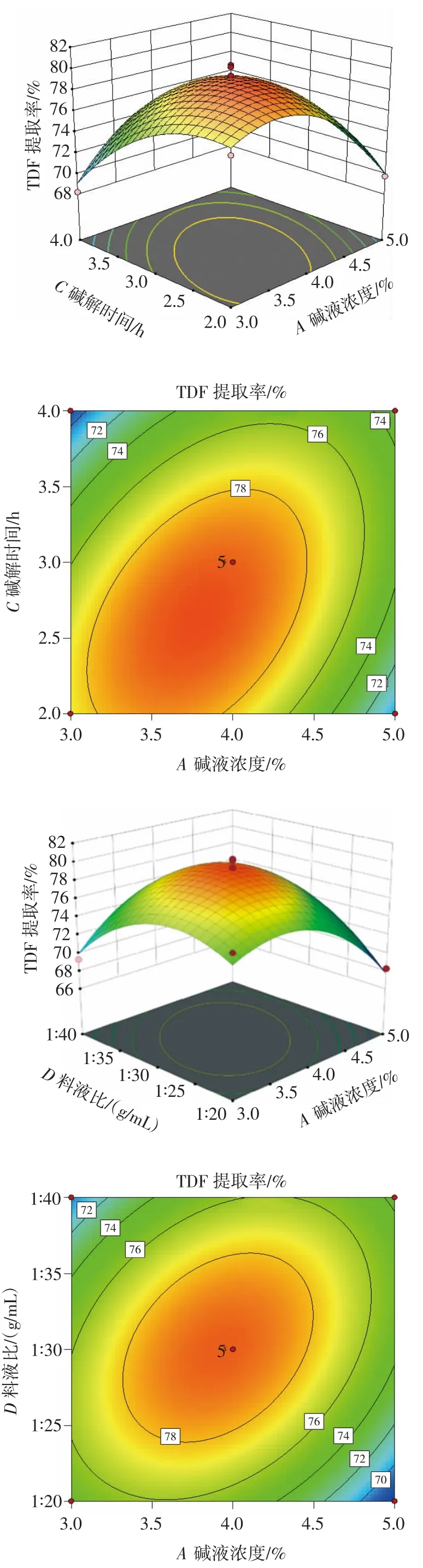
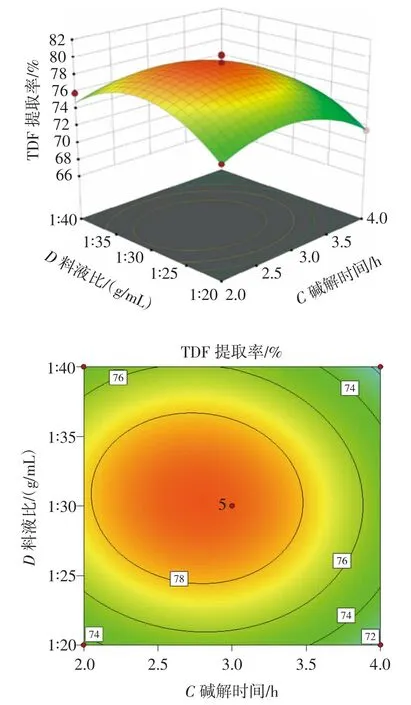
图5 各因素交互作用的响应面与等高线Fig.5 Response surface plot and contour plot of the effects of interactions between factors on the yield of dietary fiber from tea residue
由图5 可知,碱解温度较碱液浓度的曲面轴陡,说明碱解温度对TDF 提取率的影响更大,TDF 提取率随碱解温度的升高逐渐增大。碱液浓度和碱解温度两个因素的交互作用极显著。当碱液浓度一定时,TDF 提取率随碱解时间的延长先逐渐增大后减小,碱解时间一定时,TDF 提取率随着碱液浓度的增加先增大后减小,碱液浓度(A)和碱解时间(C)的等高线呈椭圆形,说明两者的交互作用对TDF 提取率的影响极显著。碱液浓度和料液比的交互作用影响极显著,碱液浓度比料液比曲面轴陡,说明碱液浓度对TDF 提取率的影响更大,与方差分析结果一致。碱解时间比料液比的曲面更陡,说明碱解时间对TDF 提取率的影响更大,二者的交互作用对TDF 提取率影响不显著。
综上所述,碱液浓度(A)和碱解温度(B)、碱液浓度(A)和碱解时间(C)以及碱液浓度(A)和料液比(D)的交互作用对TDF 提取率均有显著影响,并且交互作用大小顺序为AC>AD>AB。
2.2.4 工艺优化与验证试验
根据响应面分析法得到TDF 的理论最优提取条件为碱液浓度3.35%、碱解温度100 ℃、碱解时间2.36 h及料液比1∶28(g/mL),该条件下得到的TDF 提取率理论值为82.259%。在此工艺参数条件下进行验证,重复操作3 次,得到的TDF 膳食纤维含量为82.26%。试验结果表明,实际测得的结果与理论推测值高度一致。说明该回归模型可以较真实地反映各因素对响应值的影响,具有良好的预测效果。
2.3 茶膳食纤维成分分析
膳食纤维主要包括纤维素、半纤维素、木质素、果胶等。茶渣和TDF 中膳食纤维组成成分见图6。
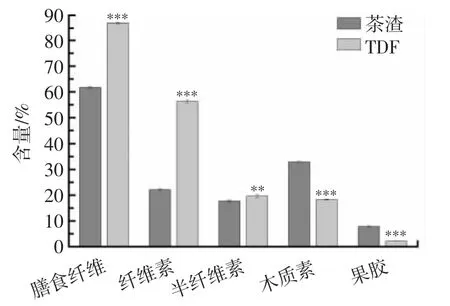
图6 茶渣和TDF 中膳食纤维组成成分Fig.6 Dietary fiber components in tea residue and tea dietary fiber
由图6 可知,提取前茶渣中膳食纤维含量为61.87%,其中的纤维素、半纤维素、木质素和果胶的含量分别为22.12%、17.72%、32.9%、7.81%。在最优工艺调节下,提取得到的TDF 中膳食纤维含量为82.26%,较茶渣中的含量极显著升高(P<0.001)。进一步分析TDF中膳食纤维的组成成分,研究发现TDF 的主要成分为以纤维素、半纤维素和木质素为代表的不溶性膳食纤维和以果胶为代表的可溶性膳食纤维,其含量分别为52.10%、14.20%、15.30 和5.00%,提取后纤维素含量极显著升高(P<0.001),半纤维素含量显著升高(P<0.01)。纤维素是一种天然高分子化合物,是构成植物细胞壁的重要组分,含有丰富的羟基,能与水分子结合,使纤维具有较好的水合能力,人体摄入纤维能增加粪便的含水量和体积,进而达到促进排便、改善便秘的效果[24]。半纤维素是一种由不同类型单糖组成的杂多糖,是构成植物细胞壁结构的第二大碳水化合物高聚物[25]。
3 结论
本研究采用碱法提取普洱茶渣膳食纤维,基于单因素试验,结合Box-Behnken 试验设计和响应面分析法,构建碱液浓度、碱解温度、碱解时间和料液比4 个因素对普洱茶渣膳食纤维提取率的回归模型。最终得到影响普洱茶渣膳食纤维提取率的主次因素依次为碱解温度>碱解时间>碱液浓度>料液比。根据模型及响应面分析,获得最佳提取工艺为碱液浓度3.35%、碱解温度100 ℃、碱解时间2.36 h 及料液比1∶28(g/mL)。在此条件下,提取得到的普洱茶渣膳食纤维得率最高,经验证得到的得率为82.260%,与理论推测值高度一致。提取得到的普洱茶渣膳食纤维得率较前明显提高了20.39%,该普洱茶渣膳食纤维主要为不溶性膳食纤维,其中纤维素和半纤维素含量分别为52.10%、14.20%,较提取前含量显著增高。普洱茶渣膳食纤维提取工艺的优化,为普洱茶渣的综合利用提供较好的理论依据和参考价值。
