微波消解-石墨炉原子吸收光谱法测定西兰花和茶叶中的微量铅
2023-09-06李姗姗户文涛师海雄王吉霞李卉袁新高桂莉杨全录
李姗姗,户文涛,师海雄,王吉霞,李卉,袁新,高桂莉,杨全录
(兰州文理学院 化工学院,甘肃 兰州 730000)
重金属污染在食品中的安全问题引起了研究人员的广泛关注.铅(Pb)是一种有毒的重金属,在我们日常生活中,食物、生活用品(化妆品、电池、学习工具等)以及装修材料、饮用水和天然水中往往含有一定量的铅,人类长期接触可能会导致其在体内的蓄积.而且铅是非生物降解物,具有生物毒性,它与人体内的蛋白质和酶发生作用,就会对人体产生危害,主要损害消化系统、呼吸系统以及中枢神经系统等.水果、蔬菜、饮用品(如茶叶、茉莉花、枸杞等)中重金属的富集主要是通过其根部或者大气摄入,人类在食用的时候,这些重金属通过食物链摄入人体,长时间会产生巨大的毒性.蔬菜作为生活中广泛食用的食物,快速准确地测定其中的重金属含量具有非常重要的意义[2].近几年,高分辨率连续光谱源石墨炉原子吸收光谱法作为一种微量金属的重要检测方法之一,对茶叶中25种微量金属进行了检测,其中,铅含量普遍在0.01~0.39 mg/kg[3].Zhong等人[4]通过电感耦合等离子体质谱法(ICP-MS)测定了茶叶中铅含量,研究表明,其含量普遍高于新鲜蔬菜中铅的含量.因此,茶叶中的铅含量检测备受重视.然而,由于ICP-MS设备成本投入高等不利因素,原子吸收光谱法成为了一种普遍的重金属检测方法[5-6].
石墨炉原子吸收光谱法(GFAAS)是用于样品元素分析的常用方法之一,由于只需要最少的样品预处理或根本不需要预处理,通常比其他方法更受欢迎,是一种灵敏度较高的分析方法[7-8].然而,在GFAAS中也存在环境干扰,因此,在测量样本中添加有效的基体改进剂可以消除背景干扰和解决难以量化的主要困难[9].目前对基体改进剂的研究报道较少,本研究针对多种基体改进剂对西兰花及茶叶测定的影响进行了探究,将西兰花、绿茶样品通过微波消解进行了预处理,测定过程中对基体改进剂的影响进行了比较,以磷酸二氢钾与磷酸二氢铵的混合物做为基体改进剂,在特定的仪器工作条件下,测定其中的铅含量,并分析实验的精密度、检出限、灵敏度以及加标回收率,以考察蔬菜和饮品中铅的含量.
1 实验部分
1.1 实验试剂及仪器
实验中所用的仪器如表1所示,试剂如表2所示.

表1 实验仪器

表2 实验试剂
标准储备液:1000 μg/mL铅标准溶液.
基体改进剂的配制:分别称取0.2 g磷酸二氢钾(KH2PO4)、磷酸二氢铵(NH4H2PO4)、酒石酸、抗坏血酸固体于4个50 mL烧杯中搅拌均匀后分别移入100 mL容量瓶中,用2% HNO3定容至刻度,即得2 g/L的目标基体改进剂[10].
西兰花样品(甘肃兰州)冲洗干净后,把该样品中的泥土、衰老暗黄的叶片以及变质部分剔除,用清水再次冲洗,然后反复进行若干次,直到干净为止,匀浆机刀盘和罐体也应使用清水清洗.采用四分法取样、匀浆机打碎西兰花样品,放置备用.将绿茶样品(甘肃陇南)用去离子水冲洗干净后,置于恒温干燥箱(65 ℃)烘干后备用.
1.2 实验方法
用分析天平称取6份质量为0.3003、0.3005、0.3009、0.3005、0.3007、0.3002 g的西兰花样品于微波消解罐中,分别加入6 mL 65%的HNO3,将消解罐装好,设定消解程序,启动程序消解样品45 min,消解详细情况如表3所示,消解结束后,等消解罐完全冷却,打开消解罐,把内杯取出放置在预处理炉上,在125~135 ℃条件下赶酸至1 mL左右,再加入5 mL去离子水驱赶硝酸,重复2~3遍,最终使其酸度控制在0.4%左右.然后把消解后的溶液转移至25 mL容量瓶中用2%的硝酸溶液定容至刻度,再加入单一基体改进剂和混合基体改进剂进行测定.其中,对照实验均未加基体改进剂、单一基体改进剂及混合基体改进剂.

表3 西兰花微波消解条件
同法,用分析天平称取0.3000、0.3005、0.3004、0.3007、0.3005、0.3004 g干燥的绿茶样品6份置于微波消解罐中,进行如上操作,由于材质原因,微波消解的时间略有不同,绿茶消解程序如表4所示.

表4 绿茶微波消解升温程序
西兰花、绿茶铅含量测定实验所用石墨炉原子吸收分光光度计最佳上机测试条件如表5所示:
1.3 标准工作曲线
配制25 μg/L的铅标准使用液,经石墨炉自动进样稀释,得到铅标准溶液浓度分别为5、10、15、20、25 μg/L,吸光度与浓度的测定值如表6所示.吸光度与浓度的标准工作曲线如图1所示:
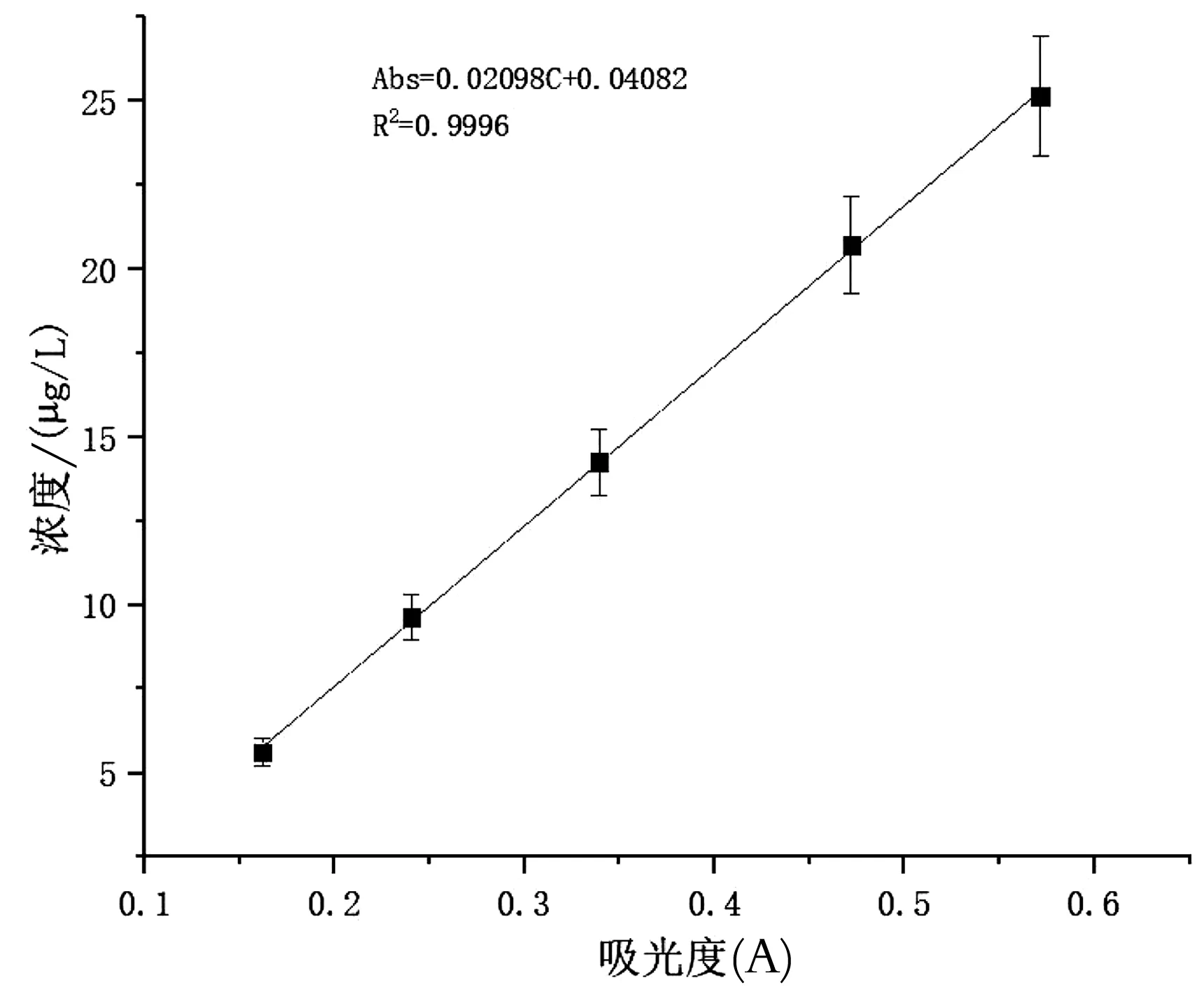
图1 标准工作曲线

表6 吸光度与浓度测定值
由实验可知,吸光度与浓度的线性回归方程为Abs=0.02098C+0.04082,R2=0.9996,回归拟合效果相对较好,仪器测量值相对稳定.由于该检测仪器的灵敏度可以用标准工作曲线的斜率表示[11],因此,灵敏度为S=0.02098.
1.4 基体改进剂的选择及仪器实验条件的确定
石墨炉原子吸收光谱法在使用过程中的干扰主要来源于基体,提高石墨炉原子吸收光谱法检测准确性的方法主要是通过使用基体改进剂消除基体产生的干扰.西兰花、绿茶前处理均与1.2处实验方案相同,只是在放入石墨炉时向试剂管1中注入2 g/L的KH2PO40.1 mL,试剂管2中注入0.05 mL 2 g/L的KH2PO4和2 g/L的NH4H2PO4,试剂管3中注入0.05 mL 2 g/L的磷酸二氢钾和2 g/L的酒石酸,试剂管4中注入0.05mL 2 g/L的KH2PO4和2 g/L的抗坏血酸[12],吸光度测定值如表7、表8所示,并计算其相对偏差.
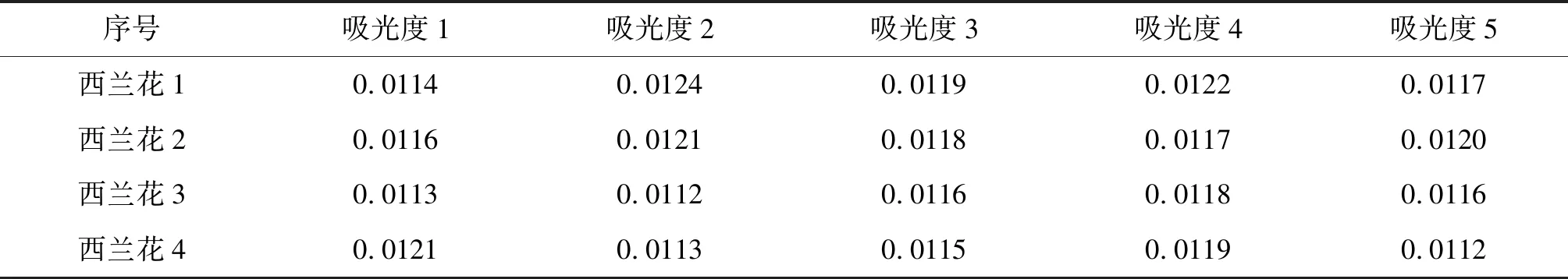
表7 西兰花吸光度测定值
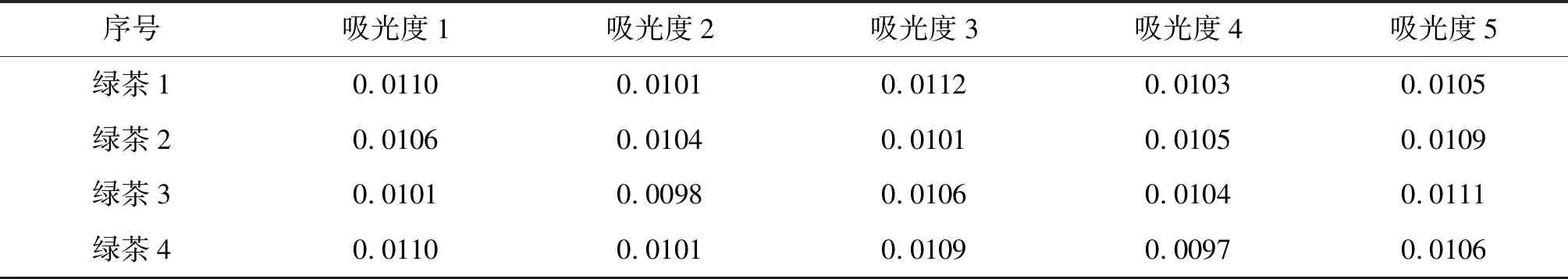
表8 绿茶吸光度测定值
标准偏差
(1)
相对标准偏差
(2)
经计算,西兰花待测样品中加入不同基体改进剂时,其相对标准偏差分别为2.97%、1.57%、1.91%、2.99%,由此可见,KH2PO4-NH4H2PO4为基体改进剂时,相对标准偏差稳定在1.57%,能有效消除环境所带来的影响,其相对标准偏差较其它基体改进剂要低.因此,测定西兰花时选用此基体改进剂较好.同样条件下进行分析,绿茶中加入基体改进剂时的相对标准偏差分别为3.92%、2.48%、4.26%、4.71%,KH2PO4-NH4H2PO4作为基体改进剂时,相对标准偏差为2.48%,较其它基体改进剂能更加有效地消除环境干扰.
通过分析比对本次实验所测定的蔬菜、绿茶中的铅含量所用石墨炉最佳测定参数如表9所示:

表9 石墨炉原子吸收分光光度计测定铅含量的最佳工作条件
1.5 样品含量的测定
采用自动进样系统,分别吸取20 μL试剂空白液和样品液(加入基体改进剂)注入石墨炉中[13],测其吸收值,并带入线性回归方程中,从而求得样品液中的铅含量结果如表10所示.
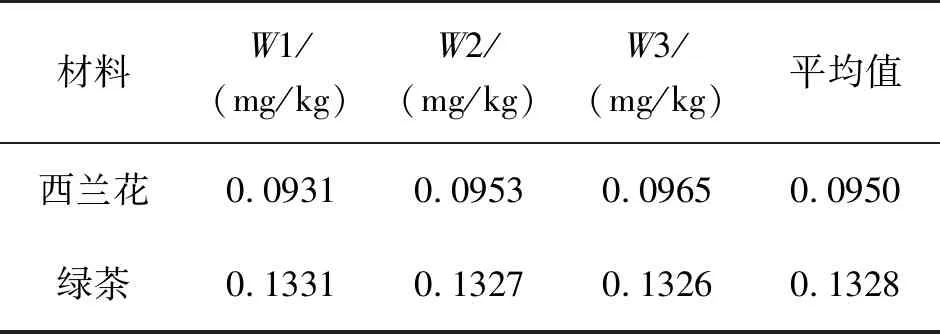
表10 铅含量的测定结果
按照式(3)计算西兰花、绿茶样品中的铅含量(基体改进剂降低环境干扰后的数值进行计算)[14]:
(3)
其中,W代表西兰花、绿茶中铅的质量分数,单位:mg/kg;ρ1代表铅的质量浓度,单位:μg/L;ρ2为代表空白液中铅的质量浓度,单位:μg/L;V代表消化液样品定容体积,单位:mL;m为样品质量,单位:g.
对西兰花、绿茶中铅含量测定结果取平均值,最终得出其含量分别为0.0950、0.1326 mg/kg,符合国家对新鲜蔬菜、茶叶中铅含量的最低限度[15].
1.6 测定方法的精密度、检出限分析
1.6.1 精密度分析
实际测定中大多采用相对标准偏差(RSD)反应测定值的精密度.因此,将加入基体改进剂的西兰花、绿茶待测样品注入石墨炉中连续测定吸光度、浓度,测定结果如表11、表12所示.
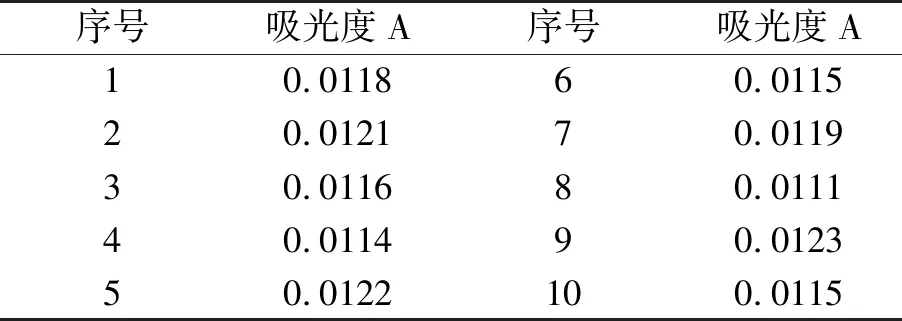
表11 西兰花精密度测定
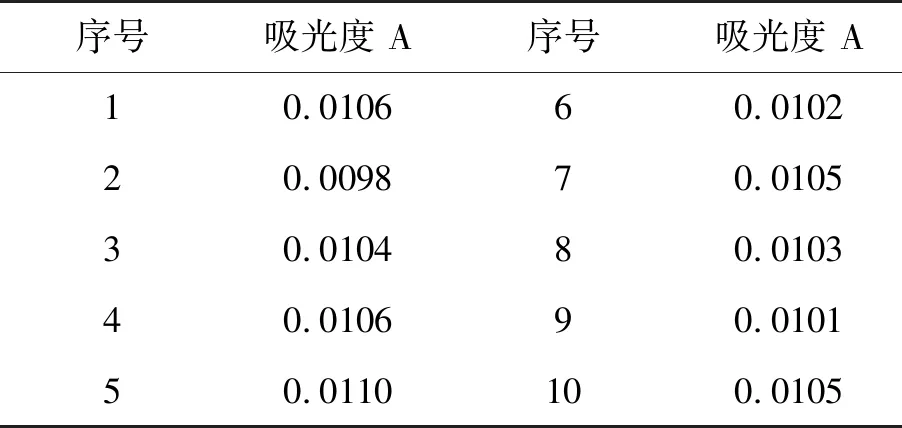
表12 绿茶精密度测定
(4)
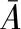
1.6.2 检出限
对空白试样反复测定吸光度、浓度,确定其线性检测限.结果如表13所示:
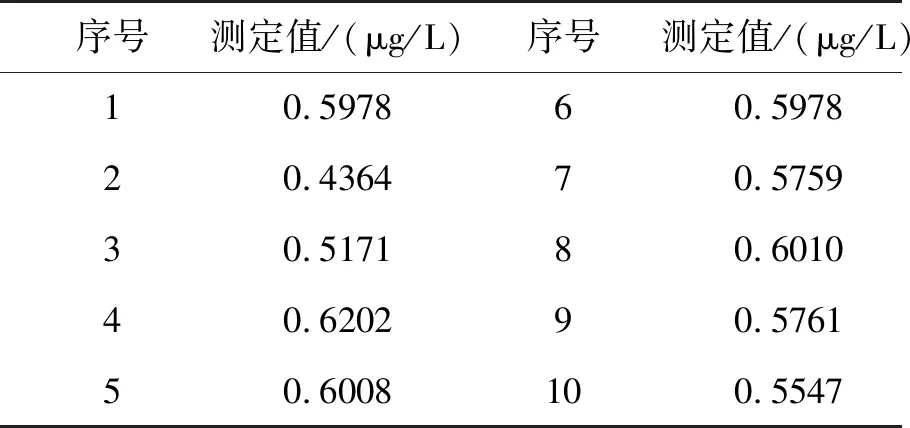
表13 检出限的测定
以3倍标准偏差(3S)作为该方法检出限的计算方法[16],结果为0.16 μg/L.
1.6.3 加标回收率
两种处理后的样品在加入基体改进剂的前提下,测定了物质中的铅含量,在待测试样中分别加入不同浓度的铅标液,运用石墨炉原子吸收光谱法再次测定铅含量,测定与计算结果如表14所示:
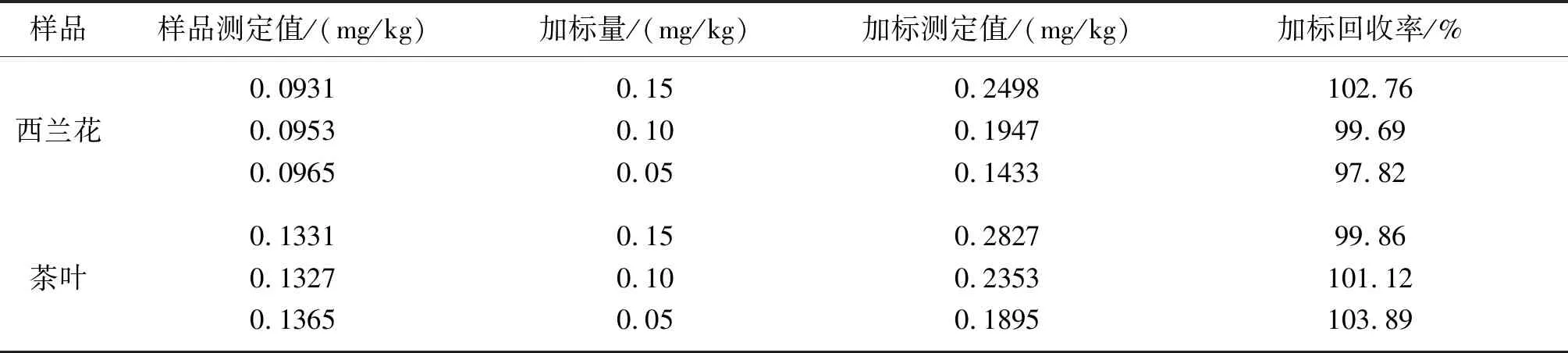
表14 加标回收率测定值
在三个不同浓度水平下,西兰花和绿茶的加标回收率分别在97.82%~102.76%、99.86%~103.89%之间,可见该方法的准确度良好.
2 结 论
该实验运用微波消解法对兰州本地西兰花及甘肃陇南茶叶样品进行处理,采用石墨炉原子吸收光谱法测定样品中的微量铅元素,测定结果符合国家标准要求的最低限度,具有一定的参考价值.在铅含量分析测定过程中,对石墨炉原子吸收光谱仪测定铅的最佳工作条件进行了探讨,通过对不同类型的基体改进剂进行分析,KH2PO4-NH4H2PO4作为基体改进剂时,在西兰花、绿茶试样中,相对标准偏差分别为1.57%、2.48%,较其它基体改进剂效果好,能有效消除环境干扰.该方法检出限低,灵敏度高,能有效测定该类物质中的铅含量.但是,由于该样品中铅含量大多来自农药化肥等,因此测定结果会由于地域及农药化肥的使用存在一定差异.
