细辛标准煮散剂的质量评价
2023-08-30王梦蓝张淑涵王安琪李西文
王梦蓝 张淑涵 郭 宁 徐 核 王安琪 李西文 孙 奕
(中国中医科学院中药研究所,北京,100700)
细辛为马兜铃科植物北细辛AsarumheterotropoidesFr.Schmidt var.mandshuricum(Maxim.)Kitag.、汉城细辛AsarumsieboldiiMiq.var.seoulenseNakai或华细辛AsarumsieboldiiMiq.的干燥根和根茎,在《神农本草经》中被初次记载,同时被列为上品,其味辛性温,归心、肺、肾经,具有行水通窍、温肺化饮、祛风散寒、止痛的功效,也可用于鼻塞鼻渊、风湿痹痛、风寒感冒、痰饮喘咳等症[1]。细辛根部的挥发油类成分主要包括甲基丁香酚和黄樟醚,其次为3,5-二甲氧基甲苯、肉豆蔻醚、β-蒎烯、α-蒎烯、优葛缕酮、α-细辛醚、榄香素等[2-7]。从其根及根茎的去挥发油部分则鉴定出2E,4E,8Z,10E-N-异丁基-2,4,8,10-十二碳四烯酰胺、细辛脂素、芝麻脂素、山柰酚-3-O-葡萄糖苷、5,7-二-O-β-D-吡喃葡萄糖基柚皮素、马兜铃酸Ⅰ(Aristolochic Acid Ⅰ,AAⅠ)等多种非挥发性成分[8-11]。临床研究表明,细辛具有解热、镇痛、抗炎、免疫抑制、调节血压、抗过敏、抗衰老等药理作用[12-13]。
“煮散”首次记载于唐代孙思邈的《备急千金要方》,而在更早的汉朝《伤寒杂病论》中已经出现关于剂型的描述。中药煮散是将药物制成细粉或粗粉,加入水或引药煎煮,去掉药渣留下汤汁,最终制成的汤剂。目前,仍沿用至今的煮散剂包括银翘散、玉屏风散等。在当代,随着中药饮片的需求量逐年上升,煮散剂可以发挥简、便、廉、验的优势,能够大量节约药源,因此有必要重新考量其应用价值[14]。目前研究较多的一是煮散剂的临床研究并观察其疗效,二是将煮散剂与中西医其他疗法结合来进行临床试验,三是探讨影响煮散有效成分浸出的相关因素等,四是对比研究煮散剂与传统饮片煎出率的差异以及产生差异的因素[15-17]。本实验对细辛的精准煮散剂进行了出膏率、有效成分转移率、指纹图谱等方面的研究;与药材饮片中有效成分的含量进行比较,并分析不同规格煮散之间的成分及其含量的差别,确定了药材煮散的最佳粉碎粒径,同时评价煮散与原饮片的质量均一性,建立煮散剂的质量评价系统。
1 仪器与试药
1.1 仪器 高效液相色谱仪(Waters公司,美国,型号:Waters 2695),超高效液相色谱仪(Waters公司,美国,型号:Acquity UPLC Class I),超高效液相系统(Waters公司,美国,型号:ACQUITY UPLC H-Class),高分辨质谱仪(Waters公司,美国,型号:Q-TOF),电子分析天平(北京赛多利斯科学仪器有限公司,型号:Sartorius-WWZA-124S),电子天平(上海精密科学仪器有限公司,型号:YP502N),超声波清洗器(昆山市超声仪器有限公司,型号:KQ-5200B),台式高速离心机(上海洪纪仪器设备有限公司,型号:D2012),高速万能粉碎机(天津市泰斯特仪器有限公司,型号:FW100),pH试纸(上海三爱思试剂有限公司精密试纸,批号:20056)。
1.2 试剂 细辛脂素对照品(北京索莱宝科技有限公司,批号:BBP03975,纯度≥98%),甲醇、乙腈均为色谱纯级别(Fisher,美国,批号:20191125),其他分析试剂均为分析纯级别,实验用水均为娃哈哈纯净水或屈臣氏饮用水。
1.3 分析样品 3批细辛饮片经中国中医科学院中药研究所李西文研究员鉴定,均由马兜铃科植物北细辛AsarumheterotropoidesF.Schmidt var.mandshuricum(Maxim.)Kitag.的干燥根及根茎炮制加工而成,药材标本存放于中国中医研究院中药研究所整合中药学中心。见表1。
表1 细辛产地及批次
2 方法与结果
2.1 溶液的制备
2.1.1 细辛饮片标准汤剂供试品溶液的制备 精密称取生产批号160960111的细辛20 g,加8倍量水,采用标准汤剂的方法进行煎煮。首先浸泡30 min,第1次加热回流30 min,用200目的筛网趁热过滤,再加入6倍量水,第2次加热回流30 min,趁热过滤,合并2次煎煮滤液,减压浓缩,使最终体积为100 mL,过0.22 μm微孔滤膜,即得。
2.1.2 不同规格煮散饮片水煎液供试品溶液的制备 取细辛饮片均匀粉碎后过筛,分别过5~10目,10~24目,24~65目筛,可得到3种不同规格的煮散饮片。称取上述煮散饮片各20 g,加8倍量水,采用标准汤剂方法进行煎煮。浸泡30 min,第1次加热回流30 min,用200目的筛网趁热过滤,接着加入6倍量水,第2次加热回流30 min,趁热过滤,合并2次煎煮滤液,减压浓缩,使最终体积为100 mL,过0.22 μm微孔滤膜即得。
2.1.3 细辛饮片供试品溶液的制备 本品粉末过3号筛后,精密称定约0.5 g,置于具塞锥形瓶中,精密加入15 mL甲醇,密塞称重,超声处理(功率500 W,频率40 kHz)45 min,待冷却后再次称重,用甲醇补足减失的重量后,过0.22 μm微孔滤膜,即得。
2.1.4 对照品溶液的制备 精密称定适量细辛脂素对照品,加入甲醇制成50 μg/mL的细辛脂素对照品溶液,4 ℃保存,即得。
2.2 细辛脂素含量测定
2.2.1 色谱条件 Thermo BDS Hypersil C18色谱柱(250 mm×4.6 mm,5 μm);0.2%乙酸水(A)-流动相乙腈(B),梯度洗脱(0~8 min,5%B;8~20 min,5%~20%B;20~40 min,20%~60%B;40~45 min,60%~95%B;45~50 min,95%B),流速为1.0 mg/mL,柱温设置为30 ℃,检测波长为280 nm,进样量为10 μL。
2.2.2 线性关系考察 取细辛脂素对照品溶液,分别稀释2、4、8、16、32倍,按2.2.1项色谱条件进行测定,横坐标(X)为对照品质量(μg),纵坐标(Y)为峰面积,绘制标准曲线,得到回归方程Y=1 282.8X+593 3,r=1,线性范围为50~500 ng。
2.2.3 精密度试验 取煮散剂供试品溶液(S1),按2.2.1项色谱条件连续测定6次,结果显示供试品溶液中细辛脂素峰面积相对标准偏差(Relative Standard Deviation,RSD)为0.1%,表明仪器精密度良好。
2.2.4 稳定性试验 取煮散剂供试品溶液(S1),分别在0、2、4、8、12、24 h时按照2.2.1项色谱条件进行分析,结果表明供试品中细辛脂素峰面积RSD为1.3%,表明标准煮散供试品溶液在24 h内稳定。
2.2.5 重复性 取相同批次的标准煮散剂样品(S1),按2.1.2项中的方法平行制备6份供试品溶液,分别按2.2.1项色谱条件进行检测分析,计算得出细辛脂素的平均质量分数分别为0.025,0.025,0.024,0.024,0.025,0.024 mg/mL,RSD为2.2%,表明该方法重复性良好。
2.2.6 加样回收率试验 精密吸取同一批次已知含量的供试品溶液适量(S1),按1∶1的比例添加细辛脂素对照品,平行制备6份后按2.2.1项色谱方法对细辛脂素进行分析,计算出细辛脂素的平均回收率为101.3%,RSD为2.1%,表明该实验方法准确可靠。
2.2.7 细辛样品中细辛脂素含量测定 依照2020年版《中华人民共和国药典》方法,制备不同批次细辛饮片样品溶液,精密吸取3批次供试品溶液各10 μL,并在2.2.1项下的色谱条件进样分析,测定细辛脂素的峰面积,通过外标法计算细辛脂素含量。见表2。
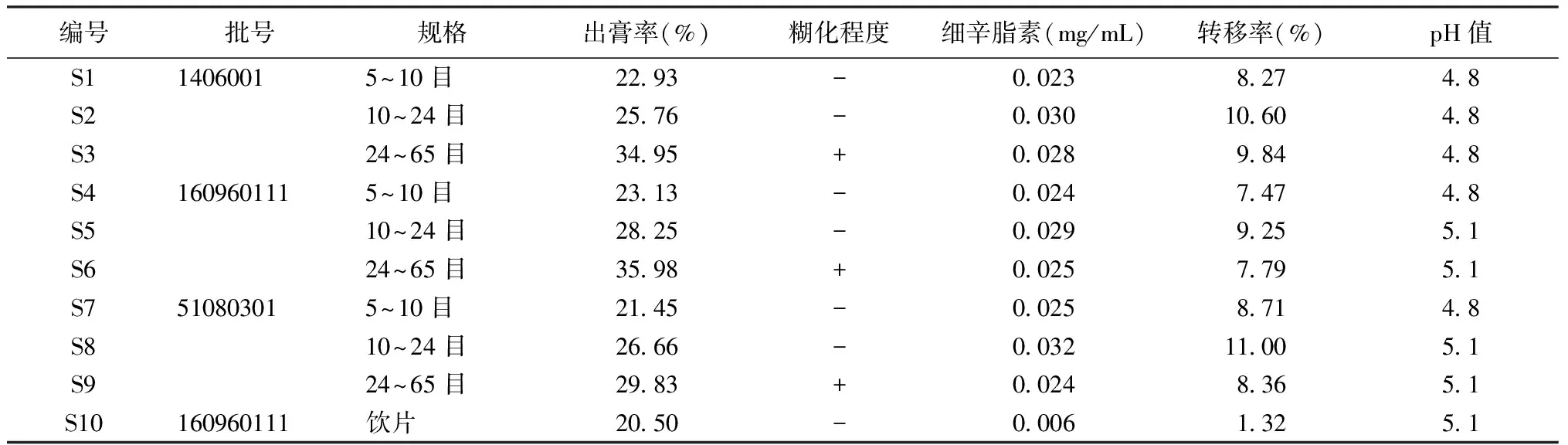
表2 细辛标准煮散剂的理化特征参数与细辛脂素参数
2.2.8 细辛饮片标准汤剂中细辛脂素含量测定 精密吸取2.1.1项下细辛饮片标准汤剂供试品溶液10 μL,并在2.2.1项色谱条件下进样分析,测定细辛脂素的峰面积,根据外标法计算细辛脂素含量。见表2。
2.2.9 细辛煮散饮片水煎液中细辛脂素量测定 精密吸取2.1.2项下各个批次不同规格的供试品溶液各10 μL,并在2.2.1项的色谱条件下进样分析,测定细辛脂素的峰面积,接着通过外标法计算细辛脂素含量。见表2。
2.3 细辛脂素转移率 根据以上实验测得的细辛脂素含量得结果,按照转移率的公式计算细辛脂素转移率,转移率=标准汤剂或煮散剂中细辛脂素含量/相应饮片中细辛脂素含量×100%,发现粉碎后的不同粒径煮散饮片水煎液细辛脂素的转移率均比原饮片有显著增加,其中以中等粒径细辛脂素转移率最高。见表2。
2.4 出膏率 精密量取2.1.1项下制得的细辛饮片标准汤剂和2.1.2项下制得不同规格煮散饮片水煎液25 mL,置于干燥的蒸发皿中,水浴加热蒸干,接着在105 ℃烘箱中干燥3 h,取出后放置干燥器中冷却30 min,称重,计算出膏率。见表2。
2.5 指纹图谱的建立 将3批细辛饮片标准煮散剂生成高效液相色谱指纹图谱,对照指纹图谱则由平均数生成。见图1~2。根据峰形、峰面积、保留时间等参数,最终选择出共有峰5个,以峰5作参照,来计算5个共有峰的相对保留时间、保留时间、相对峰面积以及峰面积。见表3。通过对比高效液相色谱色谱图信息可知,3批细辛标准煮散剂所生成的指纹图谱的相似度均大于90%。见表4。
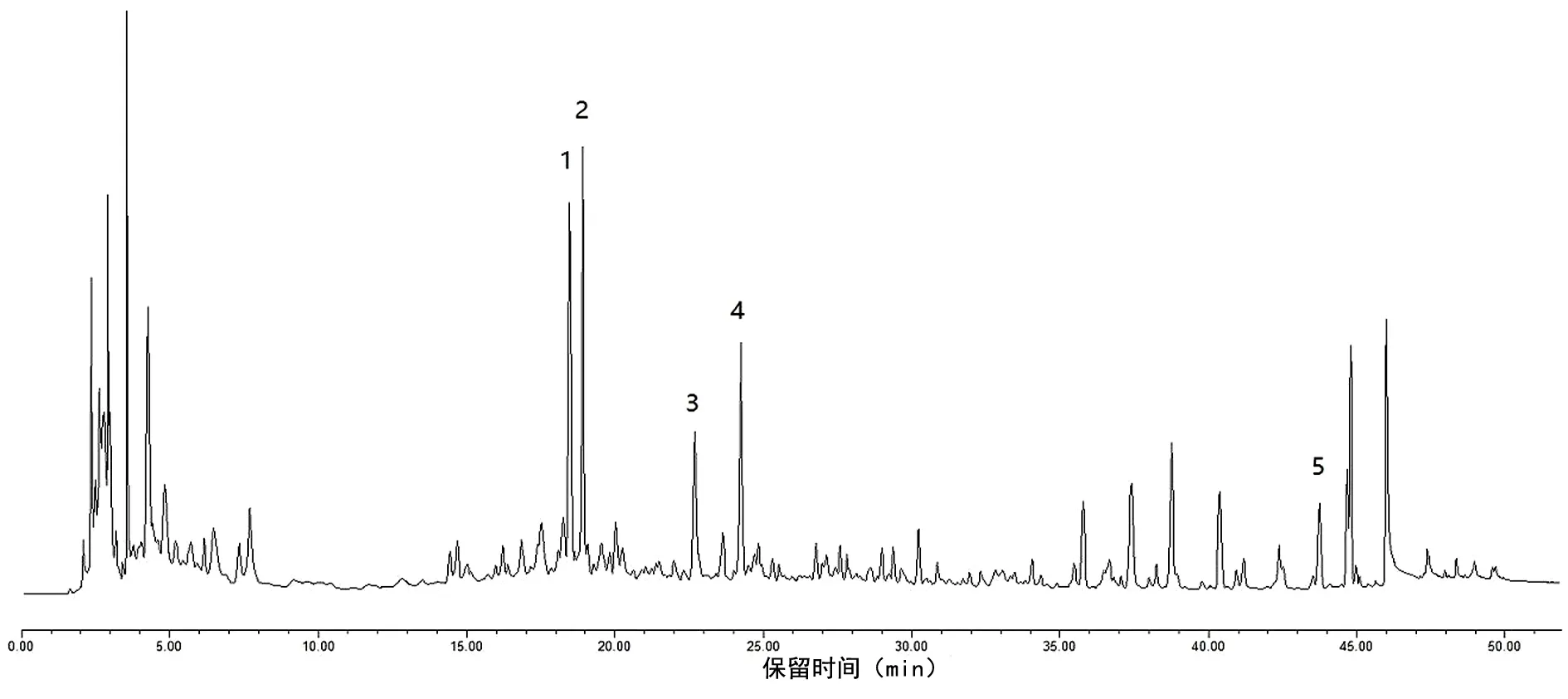
图1 细辛标准煮散剂的高压液相色谱图谱
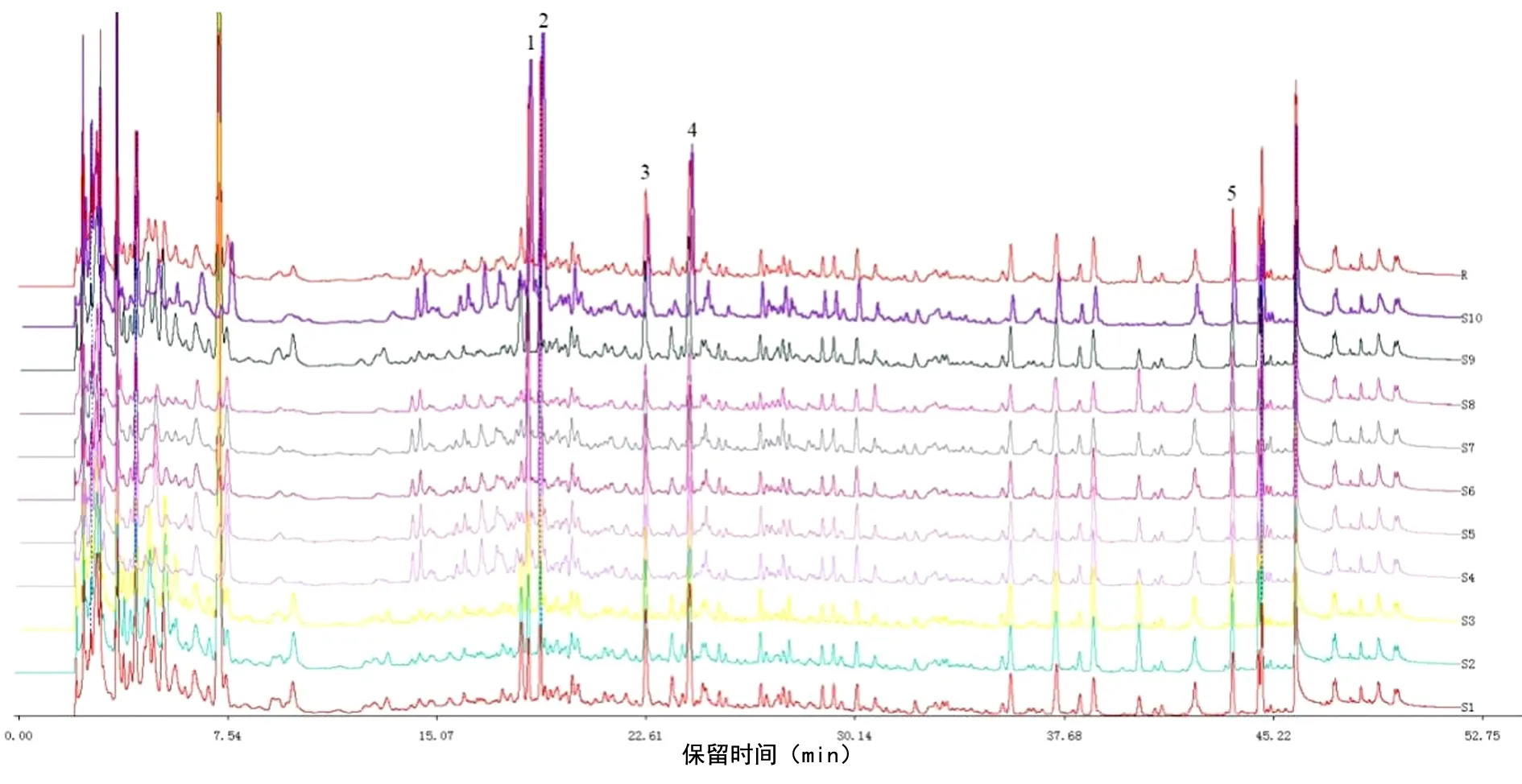
图2 细辛标准煮散剂的高效液相色谱指纹谱
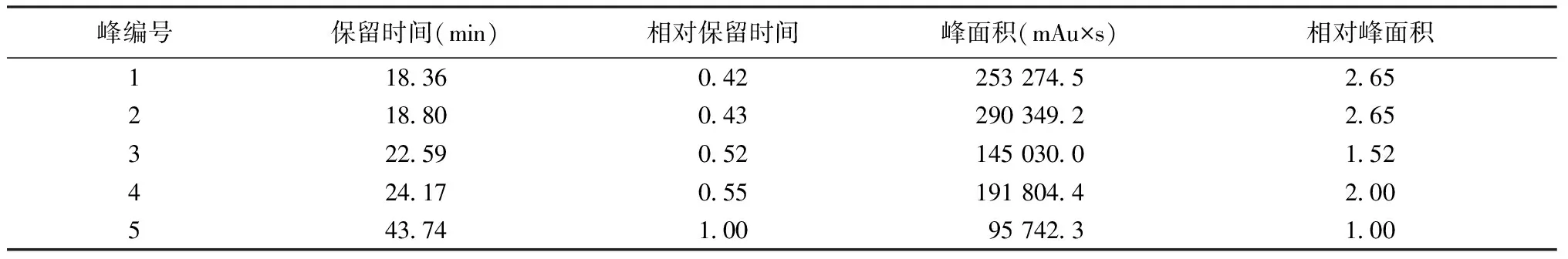
表3 细辛标准煮散剂的主要共有指纹峰指标参数
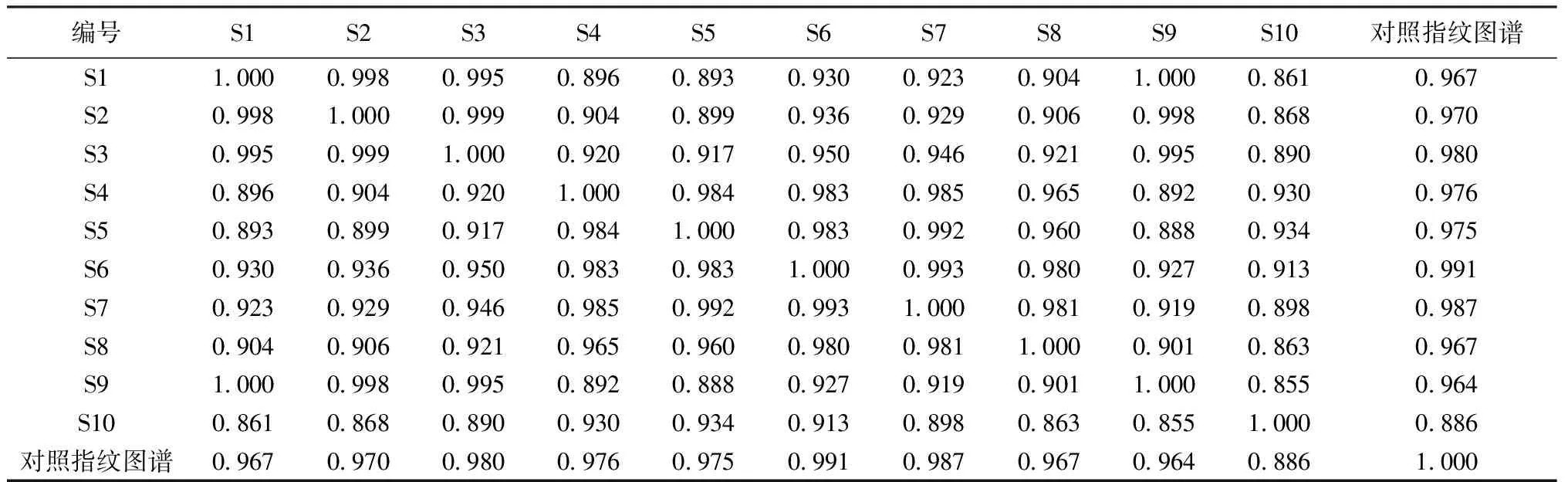
表4 细辛标准煮散剂的高效液相色谱指纹图谱的相似度
2.6 超高效液相色谱-串联质谱法(Ultra-performance Liquid Chromatography-tandem Mass Spectrometry,UPLC-MS/MS)成分指认
2.6.1 检测条件 色谱条件为Waters ACQUITY HSS T3 C18色谱柱(2.1 mm×100 mm,1.8 μm);流动相0.1%甲酸水溶液(A)-乙腈(B),梯度洗脱(0~2 min,5%B;2~17 min,5%~95%B;17~19 min,95%B;19~24 min,95%~5%B),流速0.3 mL/min,进样2 μL,柱温设置为40 ℃,检测波长为270 nm。
质谱条件为电喷雾电离(Electrospray Ionization,ESI),正离子模式全扫描;离子源工作参数为毛细管电压3.0 kV,锥孔电压30 V,锥孔反吹气流量(N2)50 L/h,脱溶剂气流量1 000 L/h,离子源温度120 ℃,脱溶剂气温度450 ℃,每0.2秒采集1次谱图,扫描范围m/z 50~1 000,采用UNIFITM 1.9.4质谱分析软件进行数据采集和分析。
2.6.2 色谱峰指认 精密吸取2 μL的细辛标准煮散供试品溶液注入超高效液相色谱-四极杆-飞行时间串联质谱法(Ultra Performance Liquid Chromatography Tandem Quadrupole Time of Flight Mass Spectrometry,UPLC-Q-TOF-MS)仪器,在正离子模式下测定,利用UNIFITM1.9.4质谱分析软件进行数据处理,对比分析相对分子质量、特征离子碎片,并结合MassFragmentTM确定化合物的分子式和相对分子质量等信息。最终鉴定出16个色谱峰。化合物及相关离子推断见表5,图3。
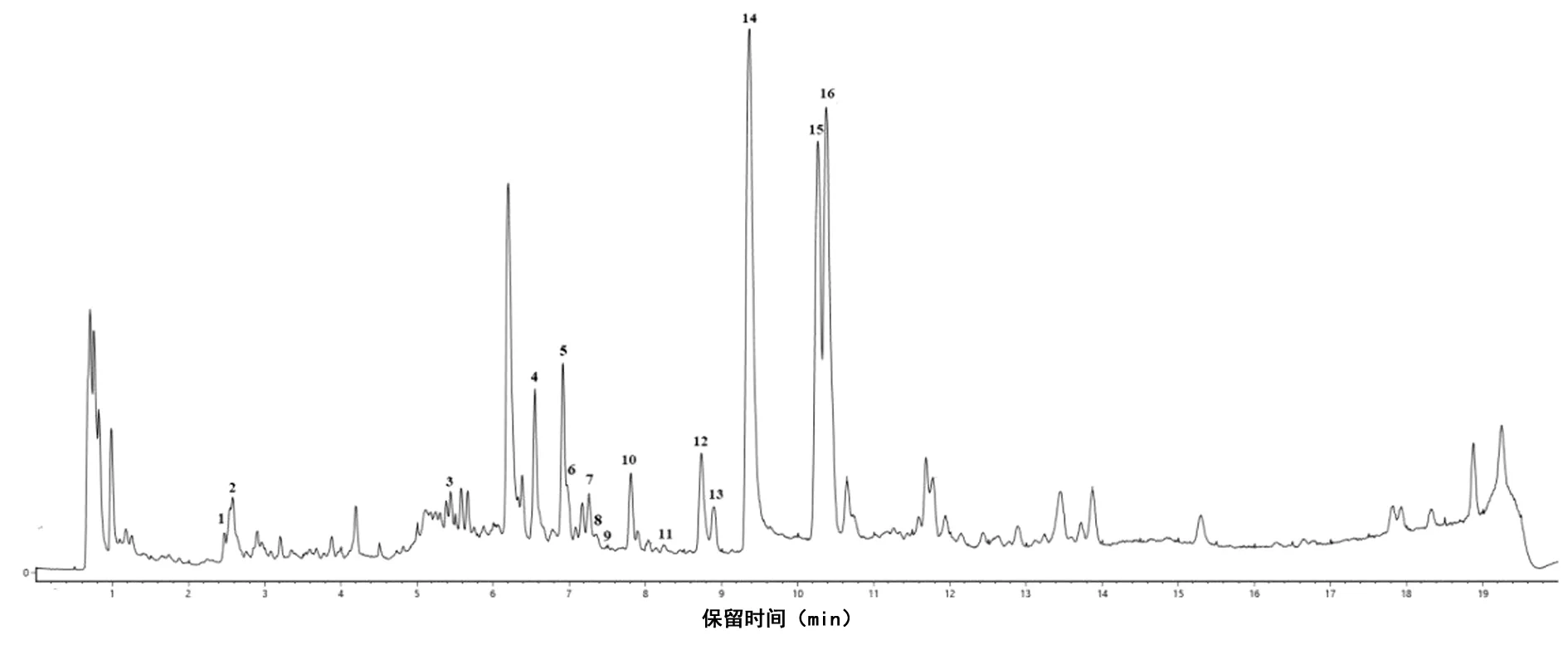
图3 细辛标准煮散剂UPLC-Q-TOF-MS分析的基峰离子(Base Peak Ion,BPI)色谱图
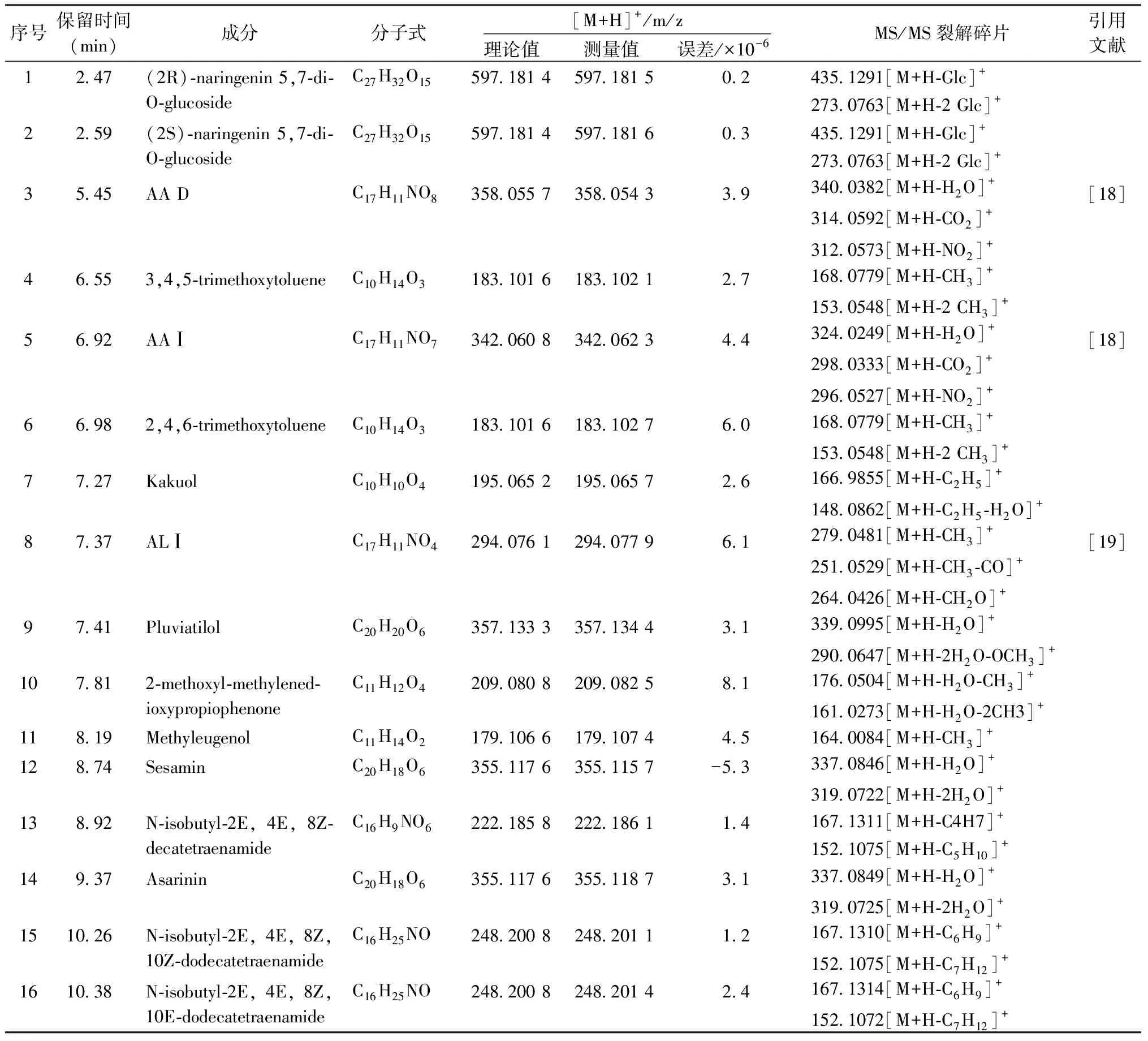
表5 正离子模式下细辛煮散剂溶液中的色谱峰鉴别
3 讨论
本实验选取了不同产地的细辛制成煮散剂,分别测定了出膏率和pH值。结果显示,粉碎成不同粒径的煮散饮片与原饮片pH值无明显差异,而出膏率则比原饮片有所增加;然而最小粒径容易出现轻微糊化现象,故选用中等细度的颗粒制备煮散剂最为合适。
中药生产中计算出膏率最重要的是要确保中药的提取程度够完全,并保证中药材能煮透,计算出膏率的基础上可以降低生产成本,使药品质量得到控制以实现良好的经济效益。并且出膏率和含量之间的关联密切;控制好药材的质量和工艺提取参数,有利于更好地保证产品的最终质量。
采用高压液相色谱法-二极管面阵(High-performance Liquid Chromatography-diode Array Detection,HPLC-DAD)色谱法进行分析,根据其高分辨数据以及分析结果,说明不同规格煮散剂与原饮片在主要成分上并没有明显差别,具有属性上的一致性;根据其相似度计算结果,不同规格煮散剂与原饮片批次之间相似度较好,说明粉碎后的煮散饮片与原药材饮片中的成分种类没有太大差别,是否粉碎及粉碎程度对其药物成分几乎没有影响。本实验制成了3个不同规格煮散剂,包括粗粒径(24~65目)、中粒径(10~24目)、细粒径(5~10目),通过查阅2020版《中华人民共和国药典》,借鉴其中方法,对有效成分细辛脂素的含量及转移率进行了测定,与饮片制得的标准汤剂比较,粉碎后不同粒径煮散饮片水煎液中细辛脂素的含量均明显增加,其中中等粒径(10~24目)细辛脂素含量及转移率均为最高,有效成分含量最高,且不易糊化。如果细辛药材制成10~24目粒径的颗粒再加工成煮散剂,则可以得到最高的药材提取率,从而更广泛地应用于生物医药行业。
细辛在炮制入药时,饮片中的有效成分之一细辛脂素的转移率不高,但制成煮散后,可使其出膏率和转移率有所提高。研究发现,不同规格的煮散剂之间的出膏率也存在差异,其中以中等颗粒的细辛脂素的转移率最高,且具有良好的均一性。采用UPLC-QTOF-MS进行检测,用UNIFITM1.9.4质谱分析软件分析,结合文献查阅,以及对照品质谱分析和保留时间等参数,最终鉴定出16个化合物,这对于细辛煮散剂的质量评价具有一定的研究意义。
4 小结
本实验按照制备中药饮片标准煮散剂的方法,建立细辛饮片标准煮散剂的质量标准,而煮散可以使得患者煎煮服药过程更简单、快捷;并且价格相对低廉,一定程度上减轻患者的经济负担;技术的改进可以大大提高效率,节约资源的同时能保护环境。传统汤剂由于长时间沸腾会导致挥发性有效成分的散失,煮散恰好避免这个问题。同时煮散可以减少药材使用、缩短煎煮时间、煎药出率高,有助于药效更好的发挥,方便携带以及服用。煮散虽好,但也存在一些缺点,比如无法清晰辨认原材料是何种药材,不易长久保存等问题。目前对于煮散剂的研究已比较深入且取得不小成就,但仍有缺陷需要系统地完善,这也将是煮散方向今后研究和讨论的热点。
利益冲突声明:无。
