基于治疗胃肠感染性腹泻的藿香正气系列制剂再评价研究
2023-08-25李玉婷杨放刘涛雷阳谭瑶琳
李玉婷?杨放?刘涛?雷阳?谭瑶琳
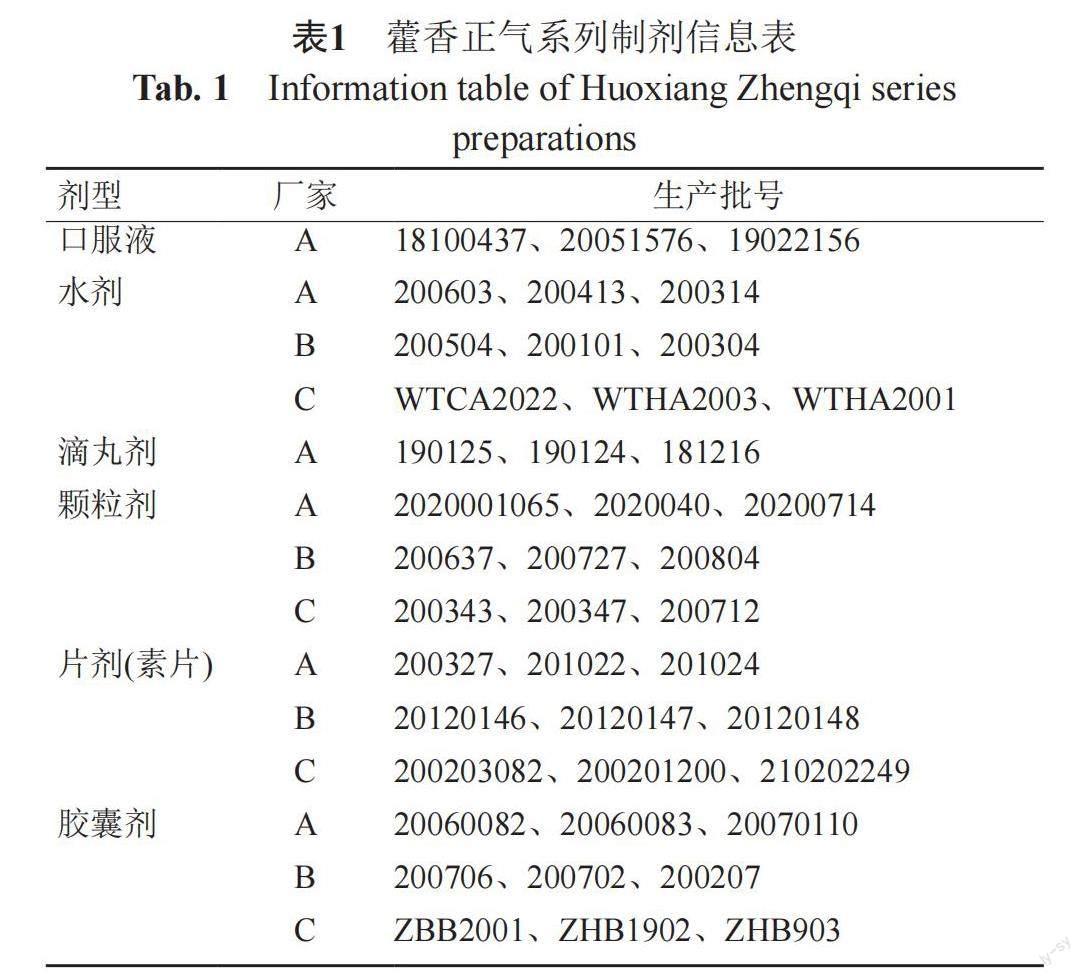
摘要:目的 对藿香正气系列制剂的内在质量差异进行评价,为其临床应用提供参考。方法 利用网络药理学、分子对接技术对藿香正气系列制剂针对胃肠感染性腹泻的活性成分进行筛选,以中度值较大的活性成分汉黄芩素以及藿香正气系列制剂中的指标性成分和厚朴酚、厚朴酚等3种活性成分为度量指标,采用HPLC法,在检测波长277 nm,体积流量1.0 mL/min,柱温30℃,进样量10 μL下,以乙腈:0.6%磷酸=45:55(V/V)为流动相进行检测,采用体外抑菌试验对评价结果进行验证。结果 相同生药量下,不同剂型的含量存在差异,本实验下藿香正气水对大肠埃希菌、金黄色葡萄球菌有抑制作用。结论 藿香正气系列制剂存在一定的内在质量差异,其说明书中标示功能主治完全一致的合理性有待进一步研究。
关键词:藿香正气系列制剂;网络药理学;分子对接;胃肠感染性腹泻
中图分类号:R961.1文献标志码:A
Reevaluation of Huoxiang Zhengqi series preparations for gastrointestinal infectious diarrhea
Li Yu -ting1, Yang Fang2, Liu Tao1, Lei Yang1, and Tan Yao-lin3
(1 College of Food and Bioengineering, Chengdu University, Chengdu 610106; 2 Sichuan Provincial Key Laboratory of New Drug Pilot Test, Chengdu Tianhe Integrated Traditional Chinese and Western Medicine Technology Conservation Co., Ltd., Chengdu 610106; 3 School of Pharmacy, Guangxi University of Traditional Chinese Medicine, Nanning 530200)
Abstract Objective The internal quality differences of Huoxiang Zhengqi series preparations were evaluated to provide a reference for clinical application. Methods The active components of Huoxiang Zhengqi series preparations for gastrointestinal infectious diarrhea were screened by network pharmacology and molecular docking technology. The active components of wogonin with moderate value, the index components of Huoxiang Zhengqi series preparations, magnolol, and honokiol were used as measurement indexes. HPLC method was used to detect the active components of Huoxiang Zhengqi series preparations under the conditions of the detection wavelength of 277 nm, the volume flow rate of 1.0 mL/min, column temperature of 30℃, and the injection volume of 10 μL. The mobile phase was acetonitrile : 0.6 % phosphoric acid = 45 : 55(V/V). The results were verified by in vitro antibacterial test. Results Under the same dosage, the content of different dosage forms was different. In this experiment, Huoxiang Zhengqi water had inhibitory effects on Escherichia coli and Staphylococcus aureus. Conclusion There are some internal quality differences in Huoxiang Zhengqi series preparations, and the phenomenon of completely consistent functional indications in the instructions needs further study.
Key words Huoxiang Zhengqi series preparations; Network pharmacology; Molecular docking; Gastrointestinal infectious diarrhea
胃腸感染性腹泻主要是由于胃肠道被病毒、细菌、真菌等病原体感染而导致,临床症状多表现为粪便异常、呕吐、腹痛等症状,目前多以具有抑菌、抗病毒作用的中成药进行治疗,其具有较好的疗效;部分细菌、病毒会引起机体出现炎症,因此还需要通过中成药相应的抗炎作用减轻炎症[1]。藿香正气处方中,以藿香化湿,以紫苏、白芷解表,以苍术、厚朴、大腹皮健脾燥湿,以茯苓、陈皮和胃清心,配伍后可使湿滞得消,胃肠调和[2-3]。实验研究表明藿香正气系列制剂在抗炎方面表现出了优异的药理活性,且对各种致病性真菌、细菌有抑制作用[4-6]。藿香正气系列制剂是由藿香正气散在现代制药技术上演变而来,主要包括胶囊剂、片剂、颗粒剂、水剂和口服液等近10种剂型,在临床上普遍应用于治疗肠胃型感冒、急性胃肠炎等疾病,具有改善胃肠功能、有效促进肠动力、保护肠胃屏障功能和镇静的作用,在《中国药典》2020版一部等相关标准中,其所标示的主治功能均为解表化湿,理气和中;主要用于外感风寒、内伤湿滞或夏伤暑湿所致感冒[7-13]。不同剂型的藿香正气制剂其处方虽然相同,但生产工艺参数甚至制备方法及工艺路线完全不同,如藿香正气水醇提的药材为苍术、陈皮、厚朴、白芷等4味,提取工艺为渗漉法。并以40%~50%的乙醇作为成药的溶媒,而藿香正气口服液仅将厚朴一味药材进行醇提,提取工艺为回流法,且以水为成药的溶媒,显然,两者由于制备工艺不同,其所含物质基础有异,因此临床上治疗效果可能有异,其标示的功能主治完全一致的合理性有待再评价。
由于中成药具有多成分、多靶点和多通路的特点,网络药理学与分子对接技术主要利用网络对中成药的多成分进行分析并通过多种途径对相关信号通路进行调节;同时组成多成分-多靶点-多途径网络。网络药理学以及分子对接技术主要利用分子生物学将中成药中的有效成分与靶点基因相联系,从而提高药物疗效,降低不良反应,还可用其进行老药新用的研究。因此本研究利用网络药理学筛选藿香正气系列制剂处方药材中针对胃肠感染性腹泻的抗炎、抑菌潜在活性成分,根据文献及网络药理学评价方法指南的要求[14]。本文利用分子对接技术对筛选出的活性成分进行再验证,筛选得到汉黄芩素,并根据文献报道将和厚朴酚及厚朴酚作为临床上治疗感染性腹泻的指标性成分,用以评价不同剂型的藿香正气制剂在治疗胃肠感染性腹泻方面的物质基础差异,再以大肠埃希菌和金黄色葡萄球菌为例,研究藿香正气系列制剂的体外抑菌活性,对筛选结果进行验证[15],以期为其临床使用提供参考。
1 仪器与试剂
PS-40型超声波清洗器(深圳得康清洗设备有限公司);DH系列电热恒温培养箱(西安禾普生物科技有限公司);BS-6KH 型电子天平(上海友声衡器公司);FA2004电子分析天平(上海良平仪器仪表有限公司);Ichrom5100高效液相色谱仪(大连依利特)。
厚朴酚对照品(批号:wkq1012107质量分数≥98%)、和厚朴酚对照品(批号:wkq21012507质量分数≥98%)、汉黄芩素对照品(批号:wkq20030204质量分数≥98%)等购买自四川省维克奇生物科技有限公司;藿香正气系列制剂收集情况见表1;甲醇(批号:2021012002)、磷酸(批号:201910001)、乙腈(批号 20210104)、氯化钠(批号:2015042401)、琼脂粉(批号:2020092701)等购自成都市科隆化学品有限公司;蛋白胨(批号:20180928)购自北京奥博星生物技术有限公司;牛肉膏(批号:20160303)购自北京双旋微生物培养基制品厂、水为蒸馏水。
2 方法
2.1 网络药理学、分子对接研究
2.1.1 药物有效活性成分及靶标筛选
本文通过TCMSP(http://lsp.nwu.edu.cn/tcmsp.php)数据库网站对藿香正气系列制剂的10味中药材进行检索,本文筛选满足口服生物利用度(oral bioavailability,OB)≥30%及类药性(drug-likeness,DL)≥0.18的中药成分;得到相应的靶标蛋白。借助 Uniprot(https://www.uniprot.org/)数据库查询相关靶标蛋白对应的基因名简称,利用GeneCards(http://www.genecards.org/)网络数据库对炎症(inflammatory)、抑菌(antibacterial)进行检索,得到疾病基因,利用Venny(http://bioinfogp.cnb.csic.es/tools/venny/)网络数据库,将药物靶标基因和疾病基因导入数据库中进行整合,得到相应交集基因及韦恩图。将整合后的交集基因导入STRING(http://string-db.org/cgi/input.pl)网络数据库中进行GO分析,设置物种选择为“Homo sapiens”(人类),并选择最低蛋白相互作用阈值为“highest confidence”(最高置信度)0.9,默认其余参数,得到PPI网络,再将交集基因导入DAVID(https://david.ncifcrf.gov/home.jsp)网络数据库中,选择“OFFICIAL GENE SYMBOL”和“Homo sapiens”,并清除所有默认选项进行KEGG富集分析。并用Prism软件进行GO分析柱状图的构建,利用Omishare(http://www.omicshare.com/tools/index.php/)网络数据库设定阈值P<0.05,选取前20个信号通路进行高级气泡可视化分析,得到KEGG分析高级气泡图。
将不重复的通路基因导入STRING(http://string-db.org/cgi/input.pl)网络数据库,选择网络复杂程度为0.900进行PPI网络构建,借助Cytoscape3.7.2软件将PPI数据中的成分-靶标文件和靶标-通路文件导入进行网络拓扑学分析,将得到的数据进行可视化分析,得到成分-靶標-通路网络,利用Microsoft Excel软件对网络拓扑数据进行处理以得到各个节点的中心度值(degree),以中心度值的中位数11为节点从大到小筛选关键核心基因,大于中位数两倍为关键节点,得出排名靠前的药物活性成分。
2.1.2 关键化合物-靶点分子对接
利用PDB数据库(https://www.rcsb.org/)下载关键基因的蛋白受体,运用Discovery Studio 2020软件移除蛋白受体中的配体和水分子;从PubChem(https://pubchem.ncbi.nlm.nih.gov/)数据库中下载网络药理学筛选出的有效活性成分的2D结构文件。利用Discovery Studio 2020软件将蛋白受体与2D结构结合,并显示蛋白受体与配体相连的氢键得到优化的2D结构,利用PyRx软件上传已经去掉水分子加上氢的蛋白文件,将其进行格式转化,再上传2D结构格式文件使其能量最小化后,进行对接;借助PyMOL软件导入2D结构选择显示蛋白受体与化合物配体间的氢键,修改绘制成3D对接图,最后利用Microsoft Office PowerPoint软件进行3D对接图的调整。
2.2 含量测定方法
2.2.1 含量测定色谱条件
色谱柱为Supersil C18柱(250 mm×4.6 mm,5 μm),以乙腈-0.6%磷酸水溶液(45:55)(V/V)为流动相,进样量10 μL,体积流量为1.0 mL/min,在277 nm检测波长下测定,柱温为30℃,理论塔板数以各定量成分峰计算均大于3000。
2.2.2 对照品溶液制备
称取汉黄芩素、和厚朴酚以及厚朴酚对照品适量,精密称定,用甲醇分别配制成汉黄芩素1.1558 μg/mL、和厚朴酚8.8 μg/mL、厚朴酚0.0111 mg/mL的对照品溶液,待用。
2.2.3 供试品溶液制备
(1)藿香正气口服液供试品溶液的制备:精密量取藿香正气口服液10 mL于25 mL容量瓶中,用甲醇定容至刻度,超声提取(30℃、300 W、50 Hz)30 min,放冷,滤过,取滤液用 0.45 μm 微孔滤膜滤过,取续滤液,即得。
(2)藿香正气水供试品溶液的制备:同“2.2.3(1)”。
(3)藿香正气滴丸供试品溶液的制备:将藿香正气滴丸研碎,取相同生药量细粉,精密称定,置于具塞锥形瓶中,精密量取25 mL分析甲醇,称定重量,超声提取(30℃、300 W、50 Hz)30 min,放冷,再称定重量,用分析甲醇补足减失的重量,摇匀;滤过,滤液用0.45 μm 微孔滤膜滤过,取续滤液,即得。
(4)藿香正气颗粒、藿香正气片剂供试品溶液的制备:将藿香正气颗粒、片剂研碎,取相同生药量细粉,同“2.2.3(3)”项下藿香正气滴丸供试品溶液制备方法自“置于具塞锥形瓶……”起,同法操作。
(5)藿香正气胶囊供试品溶液的制备:取相同生药量藿香正气胶囊内容物,同“2.2.3(3)”项下藿香正气滴丸供试品溶液制备方法自“置于具塞锥形瓶……”起,同法操作。
2.2.4 方法学考察
(1)系统适用性试验:精密移取“2.2.2”项下对照品溶液、藿香正气水供试品溶液各10 μL,按“2.2.1”项下色谱条件测定。含量测定结果表明,供试品溶液的出峰位置与对照品溶液的出峰位置的相对保留时间对应一致,分离度均大于1.5。
(2)系统方法学考察:本文含量测定方法已经方法学考察,仪器精密度试验、线性条件考察、样品稳定性试验、供试品重复性试验及加样回收试验均符合相关要求,限于篇幅,将另文发表。
2.2.5 样品测定
“2.2.3”项下制备的供试品溶液按照“2.2.1”项下的高效液相含量测定色譜条件进行测定。 相关高效液相含量测定色谱图,见图1~3。
2.3 抑菌药效实验
2.3.1 固体培养基制备及菌悬液制备
称取牛肉膏1.2 g,蛋白胨4 g,NaCl 2 g,琼脂粉8 g左右,加入400 mL纯化水,在电热套上边搅拌边加热,使其完全溶解,在121℃高压灭菌30 min后备用。在超净工作台无菌操作下,挑取适量大肠埃希菌、金黄色葡萄球菌于固体培养基中在37℃恒温培养箱中倒置培养24 h左右。待细菌培养好后,在超净工作台无菌条件下,挑取适量已培养好的大肠埃希菌、金黄色葡萄球菌于装有适量无菌水的试管中与麦氏比浊管对比制成1×106~107 CFU/mL的菌液,振荡摇匀后备用。
2.3.2 抑菌供试品溶液的制备
(1)藿香正气口服液、藿香正气水直接使用。
(2)藿香正气滴丸供试品溶液的制备:将藿香正气滴丸研碎,取相同生药量细粉,精密称定,分别置于具塞锥形瓶中,精密量取10 mL纯化水,超声提取(30℃、300 W、50 Hz)30 min,摇匀;滤过,取续滤液,即得。
(3)藿香正气颗粒、片剂供试品溶液的制备:将藿香正气颗粒、片剂分别研碎,取相同生药量细粉,同“2.3.2(2)”项下藿香正气滴丸供试品溶液制备方法自“分别置于具塞锥形瓶……”起,同法操作。
(4)藿香正气胶囊供试品溶液的制备:取相同生药量藿香正气胶囊内容物,同“2.2.3(3)”项下藿香正气滴丸供试品溶液制备方法自“分别置于具塞锥形瓶……”起,同法操作。
2.3.3 抑菌活性的测定
固体培养基高压灭菌后,在超净工作台无菌条件下进行倒平板操作,待固体培养基冷却凝固后,精密量取1 mL已制备好的大肠埃希菌、金黄色葡萄球菌菌液于培养基表面涂布均匀,将牛津杯按照顺序放置在固体培养基上,在牛津杯中加入80 μL的供试品溶液,采用0.0068 mg/mL阿莫西林溶液作阳性对照,45%乙醇作为藿香正气水的阴性对照、纯化水作其他制剂阴性对照,确定其抑菌效果。
3 结果与分析
3.1 网络药理学预测结果
3.1.1 药物有效活性成分及靶标筛选
通过TCMSP网络数据库检索组成藿香正气系列制剂的10味中药材,并设置口服生物利用度OB≥30%且类药性DL≥0.18筛选出6种中药材的有效活性化合物成分。继续借助Uniprot网络数据库检索得到130个靶标简称,合并相同靶标简称得到117个不同成分靶标。通过GeneCards(https://www.genecards.org/)网络数据库查询炎症(inflammatory)、抑菌(antibacterial)两个方面的疾病基因,并进行整合得到共539个疾病基因相关靶点。通过Venny网络数据库,将117个成分靶点与539个疾病基因靶点相整合得到藿香正气系列制剂对炎症、抑菌的潜在作用靶点39个,如图4所示。
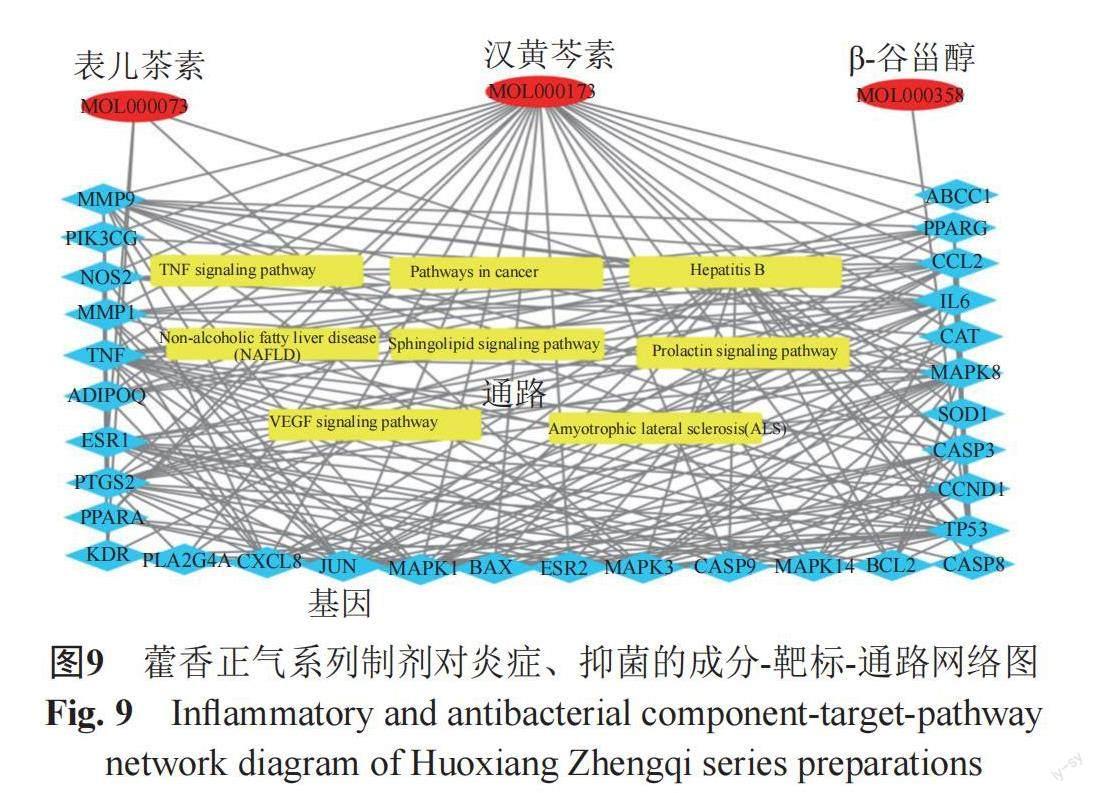
经KEGG分析得图5~7中显示富集的主要条目有细胞过程的阳性调节(positive regulation of cellular process),细胞对化学刺激的相应(cellular response to chemical stimulus);在细胞组成中作用的靶点主要在细胞质(cytoplasmic part),细胞器的管腔(intracellular organelle lumen)等区域。KEGG分析筛选得到203条信号通路,选择P值较小的前20个信号通路进行高级气泡可视化分析,得到KEGG分析高级气泡图,见图8。图中相关靶点主要富集在癌症通路(pathways in cancer)、乙型肝炎(hepatitis B)、肿瘤信号通路(TNF signaling pathway)等相关的信号通路上。
通过STRING网络数据库有效活性成分的基因与交集基因整合得到通路-基因的PPI网络。借助Cytoscape3.7.2软件对网络拓扑数据进行可视化分析,得到成分-靶标-通路网络如图9以及网络拓扑学参数。以网络拓扑学参数中心度值(degree)的中位数11为节点从大到小筛选关键核心基因,大于中位数为重要节点,大于中位数两倍为关键节点,得到Degree排名为汉黄芩素(MOL000173)为关键节点、表儿茶素(MOL000073)及β-谷甾醇(MOL000358)为重要节点。
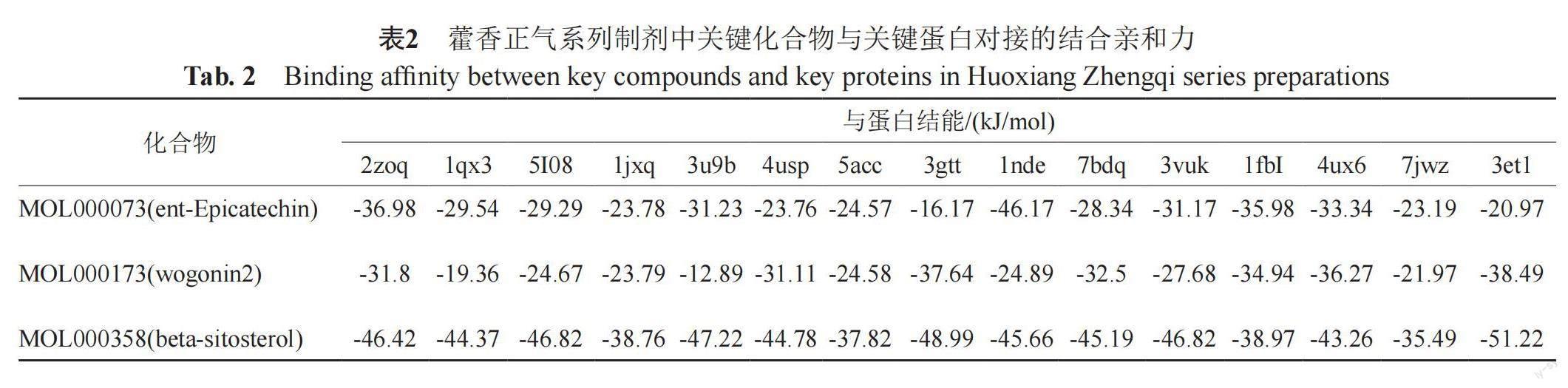
3.1.3 分子对接结果
当配体与受体结合的构象稳定时能量越低时,配体与受体自发结合的阻力越小,发生的作用可能性越大。分子对接3D结构图显示,将藿香正气系列制剂通过网络药理学筛选出的活性成分汉黄芩素(wogonin2)、表儿茶素(ent-Epicatechin)、β-谷甾醇(beta-sitosterol)与关键靶标基因进行分子对接,关键化合物与关键蛋白对接的结合亲和力均在数值-10以下,见表2;其中3D分子对接图,见图10。据图可知,藿香正气系列制剂针对胃肠感染性腹泻抑菌、抗炎的治疗效果最佳的有效活性成分为汉黄芩素。3.2 含量测定结果 根据筛选结果及相关文献,选择汉黄芩素、和厚朴酚及厚朴酚作为指标,对不同剂型的藿香正气制剂进行评价,并在相同生药量下,推测不同剂型的藿香正气制剂针对胃肠感染性腹泻的临床使用效果,在生药量相同的情况下不同剂型不同厂家不同批次间的含量测定结果,如表3及图11所示。结果表明,片剂、胶囊剂、滴丸与藿香正气口服液均呈极显著差异(P<0.01);水剂、颗粒剂与藿香正气口服液也有明显差异;相同厂家相同剂型不同批次间含量也存在差异。
3.3 藿香正气系列制剂对大肠埃希菌、金黄色葡萄球菌的抑菌作用
在大肠埃希菌、金黄色葡萄球菌的平板中加入供试品溶液、阴性对照品溶液及阳性对照品溶液,观察藿香正气系列制剂的抑菌作用,并测量其抑菌圈面积大小(每皿两个平行样品)。实验结果表明藿香正气水对大肠埃希菌、金黄色葡萄球菌均有抑制作用,其他制剂对大肠埃希菌、金黄色葡萄球菌均未见明显抑菌作用;不同廠家生产的藿香正气水对不同菌种的抑制作用不同,且相同厂家不同批次间的抑菌作用也存在差异,结果见表4及图12~17。
4 讨论
藿香正气系列制剂在临床上普遍应用于治疗肠胃型感冒、胃肠感染性腹泻、急性胃肠炎等消化系统的疾病以及呼吸内科、皮肤科、儿科疾病,在《新型冠状病毒肺炎诊疗方案(试行第四版)》至试行第八版均将藿香正气系列制剂作为新型冠状病毒医学观察临床表现为乏力伴有肠胃不适患者的推荐用药。本研究及相关文献表明,藿香正气系列制剂其物质基础、成分含量、制备工艺不同;且相关文献表明系列制剂的适应症有所不同[16-22];因此说明书中标治的主治功能完全一致的合理性还有待评价。
本研究主要利用了系统的网络药理学筛选出藿香正气系列制剂针对胃肠感染性腹泻对炎症、抑菌作用的活性成分,分析结果的靶点主要是汉黄芩素(MOL000173)、表儿茶素(MOL000073)、β-谷甾醇(MOL000358);然而利用分子对接技术对3种活性成分进行与关键靶标基因进行3D分子对接,结果表明仅有汉黄芩素对治疗胃肠感染性腹泻的抗炎、抑菌作用有效;相关标准将厚朴酚、和厚朴酚以及橙皮苷作为制剂的指标性成分,但由于汉黄芩素和橙皮苷均为黄酮类化合物,其化学结构相似,均具有抗炎抑菌等药理作用[23-24]。因此本文仅选用汉黄芩素、和厚朴酚及厚朴酚作为度量治疗感染性腹泻抗炎、抑菌的理论指标,并辅以抑菌作用实验对含量测定结果进行验证。
本文研究结果表明在基于网络药理学以及分子对接技术研究的基础上,不同藿香正气系列制剂具有不同的物质究基础;在指标性成分的测定基础上,不同剂型、不同厂家、不同批次的藿香正气系列制剂间3种活性成分存在差异。部分文献表明汉黄芩素因其本身所带有的酚羟基较多且在溶液中不稳定, 采用乙醇可使汉黄芩素充分溶出,和厚朴酚及厚朴酚在乙醇浓度为40%~60%之间时的厚朴总酚得率较大;而藿香正气水多味药材采用乙醇浸提,且以40%~50%的乙醇为溶媒[25];含量测定结果中也表明藿香正气水中3种成分度量指标较其他剂型数值更大,抑菌药效学实验结果表明在本实验条件下藿香正气系列制剂中只有藿香正气水对大肠埃希菌、金黄色葡萄球菌表现出明显抑制作用,其他制剂均未表现出明显抑菌作用,与含量测定结果有一定关联性。本研究于一定程度上揭示藿香正气系列制剂说明书上标示主治功能相同的现象可能不合理,研究结果为藿香正气系列制剂在临床上针对不同病症的用药选择提供参考。
参 考 文 献
叶青艳, 陈建杰, 周华, 等. 感染性腹泻的中医治疗进展[J]. 辽宁中医杂志, 2014, 41(12): 2730-2732.
付丽娜, 张启堂, 庞榕. 藿香正气四种制剂的药效学和毒理学研究[J]. 广东化工, 2014, 41(14): 35-37.
张慧, 李诗畅, 肖洪彬. 藿香正气类制剂的临床应用研究概况[J]. 湖南中医杂志, 2018, 34(3): 203-205.
钱星文, 何雁, 罗晓健, 等. 高效液相色谱法测定藿香正气制剂中橙皮苷的含量[J]. 江西中医学院学报, 2005, 17(3): 38-39.
王泽想, 卢丹, 张鹏, 等. 藿香正气方的化学成分与药理作用及质量标志物的预测分析[J]. 中国医药科学, 2019, 9(21): 28-34.
罗黎霞. 藿香正气水(液、丸)中脂溶性成分的测定及比较[J]. 中华中医药学刊, 2011, 29(12): 2789-2792.
张慧敏, 任虹, 何瑶, 等. 藿香正气制剂中厚朴不同提取工艺对胃肠活动的影响研究[J]. 中药与临床, 2014, 5(6): 30-32.
尚曙玉, 张启堂, 李曉光, 等. 藿香正气不同制剂对动物小肠运动的影响[J]. 中国医药导报, 2012, 9(6): 96-98.
黄庆芳, 龚梦鹃, 陈艳芬, 等. 藿香正气口服液对湿困脾胃证大鼠肠屏障功能的作用研究[J]. 中国中药杂志, 2020, 45(9): 2144-2150.
刘瑶, 卢素宏, 林华景. 藿香正气口服液对DSS诱导结肠炎小鼠肠黏膜屏障的保护作用及机制研究[J]. 中药新药与临床药理, 2021, 32(4): 473-478.
曹苗苗, 门鹏, 温剑, 等. 藿香正气口服制剂治疗胃肠功能紊乱的循证评价[J]. 中国医院用药评价与分析, 2021, 21(05): 600-602.
曹爽, 孙超越, 张楠, 等. 针药结合治疗腹泻型肠易激综合征70例[J]. 光明中医, 2011, 26(12): 2488-2489.
刘海燕. 藿香正气系列制剂在皮肤科的临床应用[J]. 世界最新医学信息文摘, 2016, 16(84): 164-165.
牛明, 张斯琴, 张博, 等. 《网络药理学评价方法指南》解读[J]. 中草药, 2021, 52(14): 4119-4129.
Wu B H, Wang G W, Xin L, et al. Network pharmacology-based therapeutic mechanism of Kuanxiong aerosol for angina pectoris[J]. J Ethnopharmacol, 2020, 261: 113079.
Gao D, Wu S N, Zhang C E, et al. Exploration in the mechanism of rhubarb for the treatment of hyperviscosity syndrome based on network pharmacology[J]. J Ethnopharmacol, 2020, 261: 113078.
邓燕君, 刘博文, 贺桢翔, 等. 基于网络药理学和分子对接法探索藿香正气口服液预防新型冠状病毒肺炎(COVID-19)活性化合物研究[J]. 中草药, 2020, 51(5): 1113-1122.
王金榜, 梁保丽, 孙树椿. 新型冠状病毒(COVID-19)感染性肺炎现代中医诊疗建议方案与探讨[J]. 世界中医药, 2020, 15(1): 35-46.
汪海英. 藿香正气丸(水、液等制剂)在消化系统疾病临床应用的药理研究[J]. 大家健康(学术版), 2014, 8(4): 243-244.
张洪坤. 中药藿香正气水抑菌药效物质及其质量控制研究[D]. 广东药学院, 2013.
钟林江, 杨俊莉, 奉梅, 等. 基于数据挖掘的金莲花系列制剂治疗上呼吸道感染的作用机制[J]. 成都大学学报(自然科学版), 2021, 40(1): 1-7.
胡一冰, 罗虹, 潘春晖, 等. 基于光谱法的六味地黄系列制剂质量再评价研究[J]. 成都大学学报(自然科学版), 2020, 39(4): 368-373.
方灵芝, 吴雪松, 张玥. 高效液相色谱-电雾式检测器法同时测定小儿解感片中7种黄酮类成分的含量[J]. 中国医院药学杂志, 2019, 39(23): 2402-2406.
李文娟, 潘馨, 陈晓兰, 等. 黄芩中汉黄芩素的提取制备[J]. 亚太传统医药, 2014, 10(9): 33-35.
徐洲, 李旭, 郭军伟, 等. 响应面优化超声辅助醇碱法提取厚朴总酚的工艺条件[J]. 四川农业大学学报, 2013, 31(1): 93-98.
