苯炔参与的N-桥环衍生物的合成*
2023-07-27王艳娇张佳佳张珂怡高艳蓉
王艳娇,张佳佳,张珂怡,高艳蓉
(咸阳市分子影像与药物合成重点实验室 陕西国际商贸学院 医药学院,陕西 咸阳 712046)
桥环化合物是指化合物中的任意两个环共用两个不直接相连的碳原子的环烃[1]。桥环化合物通常具有复杂的刚性结构、较大的角张力和环张力,因而显示出特殊的化学性质及广泛的生物活性,被广泛应用于药物化学、天然产物化学、合成化学、材料化学及生命科学等领域[2]。作为桥环化合物中具有代表性的一类,N-桥环衍生物广泛存在于天然产物结构中,如马钱子碱(Strychnine)[3]、莨菪碱(Hyoscyamine)[4]、可待因(Codeine)[5]、吗啡(Morphine)[6]、阿托品(Atropine)[7]、樟柳碱(Anisodine)等[8]。同时,N-桥环骨架还是许多重要生物活性分子的核心结构,在药物化学研究中扮演着重要的作用,如托品类生物碱Pervilleines 通过与P-糖蛋白介导的药物作用进而降低癌细胞的耐药性[9];可卡因可以作用于神经系统,对可卡因进行修饰研究可以用于开发局部麻醉剂等[10]。正是基于N-桥环衍生物在药物研究中的重要作用,近年来,N-桥环衍生物的合成研究得到了快速的发展,已经有多种合成方法被报道[11,12]。
为了合成一类结构新颖的N-桥环衍生物,本研究报道一种通过苯炔参与的构建N-桥环骨架的方法(图1)。首先,以4-溴-2-(溴甲基)苯甲醛(1)为原料,分别和两种胺(甲胺、苄胺)反应,得到两种二烯中间体(2a)和(2b),然后分别与苯炔前体化合物[5-(甲氧羰基)-2-(三甲基硅)苯基](苯基)碘P 三氟甲烷磺酸盐(3)反应得到N-桥环化合物(4a)和(4b),其中,化合物(4b)经过脱苄基得到7-溴-9,10-二氢-9,10-环亚胺蒽-2-甲酸甲酯(5),化合物(5)再发生N-乙酰化反应得到N-桥环化合物(6)。同时以(4a)的合成为模型,考察并确定苯炔参与的Diels-Alder 反应的最佳条件。该反应工艺具有简洁高效、收率较高等优点,为新型N-桥环骨架的构建提供了一种简便可行的方法。

图1 N-桥环衍生物(4a~6)的合成路线Fig.1 Synthetic route for N-bridged ring derivatives(4a~6)
1 实验部分
1.1 主要仪器与试剂
AV300 型核磁共振仪(DMSO-d6或CDCl3为溶剂,TMS 为内标,德国Bruker 公司);Ultima Global Spectrometer 型质谱仪(ESI 源,美国Waters 公司);XT4 型显微熔点测定仪(温度计未校正,北京科仪电光仪器厂);RE-52AA 型旋转蒸发仪(上海亚荣生化仪器厂);SHB-Ⅲ型循环水式多用真空泵(郑州长城工贸有限公司)。
4-溴-2-(溴甲基)苯甲醛(化合物1,纯度95%),按照文献方法合成[11];[5-(甲氧羰基)-2-(三甲基硅)苯基](苯基)碘P 三氟甲烷磺酸盐(化合物3,纯度97%),按照文献方法合成[12];甲胺盐酸盐(纯度99%)、苄胺盐酸盐(纯度99%)、四丁基氟化铵(TBAF)(1mol·L-1四氢呋喃溶液)(试剂纯)、N-溴代丁二酰亚胺(NBS)(纯度98%)、乙酰氯(AR)、三乙胺(纯度99%),阿达玛斯试剂有限公司;柱层析硅胶(300~400 目 青岛海洋化工厂);其它试剂均为市售分析纯。
1.2 实验方法
1.2.1 二烯中间体(2)的合成 将胺(甲胺或苄胺)(5.50mmol)加入乙醇(25mL)中,再加入3.03 g(10.0mmol)三乙胺和1.38g(5.0mmol)4-溴-2-(溴甲基)苯甲醛,反应体系室温搅拌2h,减压浓缩,得到5-溴-2-甲基-2H-异吲哚(2a)或2-苄基-5-溴-2H-异吲哚(2b),均为淡黄色油状液体,无需纯化,快速直接用于下一步反应(收率按照100%计算)(由于该化合物不稳定,可以短时间在N2保护下低温保存)。
1.2.2 N-桥环化合物(4)的合成
将(5.0mmol)二烯中间体(2)溶于二氯甲烷(20mL)中,在0℃下缓慢滴加1.4 g(2.5mmol)化合物(3)的二氯甲烷溶液(20mL),然后再缓慢滴加1mol·L-1的四丁基氟化铵(TBAF)的四氢呋喃溶液(5mL, 5.0mmol),加完后反应体系在0℃下继续搅拌30min。TLC 监测反应结束后,向反应体系中加入饱和NaCl 溶液(50mL),用二氯甲烷萃取(3×50mL)、无水Na2SO4干燥后减压旋干,粗品经硅胶柱层析分离纯化(v(石油醚)∶v(乙酸乙酯)=5∶1),得到化合物(4)。
(1)7-溴-11-甲基-9,10-二氢-9,10-环亚胺蒽-2-甲酸甲酯(4a) 黄色固体586mg,收率68.3%(以化合物1 计)。1H NMR(300MHz,DMSO-d6):δ 7.88(s,1H),7.68(d,J=7.5Hz,1H),7.55(s,1H),7.47(d,J =7.5Hz,1H),7.32 (d,J =7.5Hz,1H),7.20 (d,J =7.5Hz,1H),5.10(s,2H),3.80(s,3H),2.09(s,3H)。ESI-MS,m/z:344[M+H]+。
(2)7-溴-11-苄基-9,10-二氢-9,10-环亚胺蒽-2-甲酸甲酯(4b) 棕黄色固体760mg,收率72.5%(以化合物1 计)。1H NMR(300MHz,DMSO-d6):δ 7.88(s,1H),7.69(d,J= 7.5Hz,1H),7.54(s,1H),7.47(d,J=7.5Hz,1H),7.33-7.31(m,1H),7.23-7.18(m,1H),5.11(s,2H),3.81(s,3H),3.51(s,2H)。ESI-MS,m/z: 420[M+H]+。
1.2.3 7-溴-9,10-二氢-9,10-环亚胺蒽-2-甲酸甲酯(5)的合成 将(550mg,1.3mmol)化合物(4b)加入二氧六环(10mL)中,再加水(1mL)、NaHCO3(135mg,1.6mmol)、NBS(278mg,1.6mmol),反应室温搅拌20h,然后降温至0℃以下,将反应体系加入水合肼(5mL)的甲醇溶液(5mL)中,继续搅拌30min,TLC监测反应结束后,体系中加入乙酸乙酯(50mL),有机相经饱和NaCl 溶液(50mL)洗涤、无水Na2SO4干燥、减压浓缩,粗品经柱层析分离纯化(v(二氯甲烷):v(甲醇)=10∶1),得到247mg 棕色固体,收率57.8%(以化合物4b 计)。ESI-MS,m/z:330[M+H]+。
1.2.4 7-溴-11-乙酰基-9,10-二氢-9,10-环亚胺蒽-2-甲酸甲酯(6)的合成 将(200mg, 0.61mmol)化合物(5)加入二氯甲烷(10mL)中,再加入(123mg,1.22mmol) 三乙胺,搅拌均匀后加入(52mg,0.66mmol)乙酰氯,室温反应1h 后,TLC 监测反应结束后,减压浓缩,粗品经柱层析分离纯化(v(二氯甲烷):v(甲醇)=15:1),得到淡黄色固体195mg,收率86.4%(以化合物5 计)。1H NMR(300MHz, DMSO-d6):δ 7.98(s,1H),7.75-7.63(m,2H),7.57(d,J=7.5 Hz,1H),7.38(d,J=7.8Hz,1H),7.26-7.21(m,1H),6.49-6.40(m,1H),6.35(d,J=3.6Hz,1H),3.81(s,3H),1.95(s,3H)。ESI-MS,m/z:372[M+H]+。
2 结果与讨论
2.1 化合物(4)的合成
在合成N-桥环化合物(4)的过程中,苯炔前体化合物[5-(甲氧羰基)-2-(三甲基硅)苯基](苯基)碘P 三氟甲烷磺酸盐(3)首先在四丁基氟化铵(TBAF)作用下原位形成苯炔中间体,然后苯炔中间体与二烯体(2)发生Diels-Alder 反应得到N-桥环化合物(4),反应过程中,物料比、溶剂种类、反应温度及时间对产物(4)收率均有明显影响。以5-溴-2-甲基-2H-异吲哚(2a)与苯炔前体化合物(3)在TBAF 作用下反应合成7-溴-11-甲基-9,10-二氢-9,10-环亚胺蒽-2-甲酸甲酯(4a)的反应为模型,研究反应条件对N-桥环化合物(4)收率的影响,确定最佳反应条件。
2.1.1 物料比对化合物(4a)收率的影响 苯炔前体化合物[5-(甲氧羰基)-2-(三甲基硅)苯基](苯基)碘P 三氟甲烷磺酸盐(3)在四丁基氟化铵(TBAF)作用下,原位形成苯炔中间体,然后与二烯体5-溴-2-甲基-2H-异吲哚(2a)反应制备7-溴-11-甲基-9,10-二氢-9,10-环亚胺蒽-2-甲酸甲酯(4a),反应中的物料比,即摩尔比n(2a)∶n(TBAF)∶n(3)对产物收率具有重要的影响,考察结果见表1。

表1 物料比对产物(4a)收率的影响Tab.1 Effect of mole ratio on the yield of(4a)
考虑原料成本,为了尽可能使苯炔中间体反应完全,所以选择二烯体5-溴-2-甲基-2H-异吲哚(2a)和TBAF 选择丙酮过量。当物料摩尔比n(2a)∶n(TBAF)∶n(3)=2.0∶1.0∶1 时,收率仅为44.1%(序号1),增加TBAF 用量,当物料比为2.0∶2.0∶1 时,产物收率最高达到67.2%(序号3),继续增加TBAF 的用量,产物(4a)收率没有明显变化(序号4)。然后固定TBAF 的用量,考察(2a)的用量,发现降低(2a)的用量,产物(4a)收率明显降低(序号5,6),而增加(2a)的用量,当物料比为2.5∶2.0∶1 时,产物收率没有明显变化(序号7)。最终确定最佳物料比为n(2a)∶n(TBAF)∶n(3)=2.0∶2.0∶1。
2.1.2 反应溶剂对化合物(4a)收率的影响 当确定了物料比n(2a)∶n(TBAF)∶n(3)=2.0∶2.0∶1 时,考察4 种反应溶剂(四氢呋喃、甲苯、二氯甲烷、乙二醇二甲醚)对产物(4a)收率的影响,结果见表2。

表2 溶剂对产物(4a)收率的影响Tab.2 Effect of solvent on the yield of(4a)
由表2 可见,该反应在4 种溶剂中均可以进行,但在四氢呋喃和乙二醇二甲醚中收率较低,分别为26.3%和37.5%,而在二氯甲烷和甲苯中,收率较高,其中,在二氯甲烷中反应产物收率最高达到67.2%,因此,确定最佳反应溶剂为二氯甲烷。
2.1.3 反应温度及时间对化合物(4a)收率的影响当确定了物料比n(2a)∶n(TBAF)∶n(3)=2.0∶2.0∶1,反应溶剂为二氯甲烷后,考察反应温度和反应时间的影响,结果见表3。
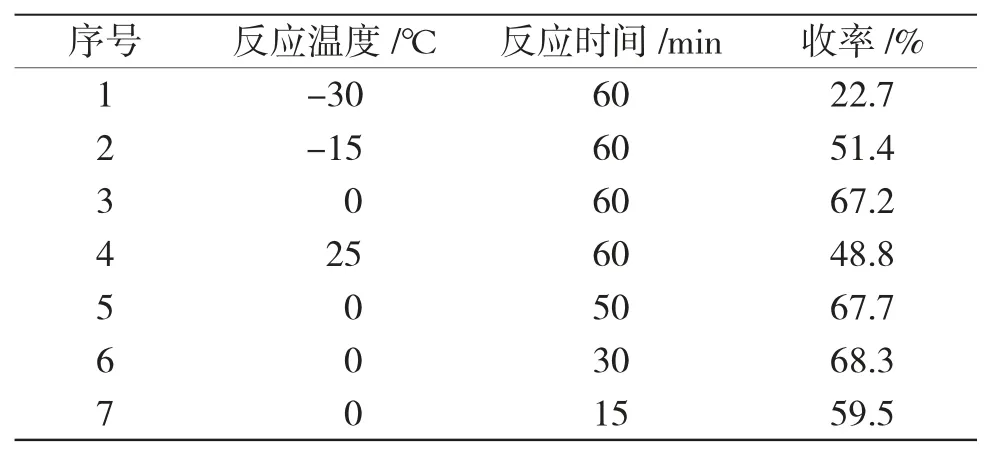
表3 反应温度及时间对化合物(4a)收率的影响Tab.3 Effect of reaction temperature and time on the yield of compound(4a)
苯炔是一种活泼的有机中间体,在常态下很难稳定存在,因此,需要控制较低的反应温度,避免副反应发生。首先,固定反应时间为60min,考察反应温度(-30℃、-15℃、0℃、25℃)发现,在-30℃下反应,产物(4a)收率仅为22.7%,温度升高到0℃,产物(4a)收率增加到67.2%,但是当温度升高到25℃时,产物(4a)收率反而降低至48.8%,主要原因是温度升高,苯炔反应活性增加,副产物增多。所以确定反应温度为0℃。然后在0℃下考察反应时间,缩短反应时间为30min 时,产物4a 收率最高达到68.3%,而继续缩短反应时间为15min,收率明显降低至59.5%。所以确定最佳反应温度为0℃,反应时间为30min。
3 结论
本研究以4-溴-2-(溴甲基)苯甲醛(1)为原料,分别和两种胺反应,得到两种二烯中间体(2a 和2b),然后,在四丁基氟化铵(TBAF)作用下发生Diels-Alder 反应,得到两种氧桥环化合物(4a 和4b)。其中,化合物4b 依次经历脱苄基反应和N-乙酰基化反应,分别得到两种氧桥环化合物(5)和(6)。并以4a 的合成为模型,考察并确定该Diels-Alder反应的适宜条件。该研究最大的特点是采用原位形成苯炔然后发生Diels-Alder 反应的策略来构建结构新颖的N-桥环衍生物,为N-桥环衍生物的合成提供了一种新的选择。
