一种多孔的有机小分子催化剂合成及性能表征*
2023-07-27唐贝
唐 贝
(河南应用技术职业学院,河南 郑州 450042)
受传统催化反应操作要求高等问题的影响,光催化合成技术成为现代科技发展的重点。但目前的光催化剂在可见光区域光捕获能力和光催化效果方面均无法达到理想的效果。对此,褚佳欢[1]制备了一种新型复合光催化剂,并对其性能进行分析。实验结果表明,该复合光催化剂在可见光照射180min 条件下,对RhB 的降解率达到了93%,表现出良好的降解性能。曹德路[2]则制备了一种新型BiOCl/BiOI 复合光催化剂,并对其性能进行研究。欧玉静、柴立涛、李宁[3-6]等人研究了纳米TiO2及其复合物作为光催化剂的可行性。实验结果表明,TiO2光催化剂具有能耗低、化学性能稳定,使用范围广等优点。以上学者的研究为光催化剂的发展提供了参考,但在光催化性能方面还有优化空间,基于此,本文制备了一种新型复合光催化剂,并对其光催化活性和机理进行了分析。
1 实验部分
1.1 材料与设备
无水乙醇(创世化工)、Cu(NO3)2·3H2O(旭祥化工)、乙酸(创通化学)、Bi(NO3)3·5H2O(克米克生物)、NaOH(辉腾化工)、Na2WO·42H2O(华翔科洁生物)、柠檬酸(坤丰化工)、HC(l汇源化工)、苯甲醇(金晟新材料)、正己烷(彦硕化工),以上均为分析纯。
101 型烘箱(宇烨干燥设备);HWCL-5 型磁力搅拌器(卓成仪器);XRD-7000 型X 射线衍射仪(赛力威仪器);F5000 型透射电镜(晟泽科技);UV-8000 型固体-紫外可见分光光度计(赛默飞仪器);BNX-S30 型超声波清洗机(布兰森设备);Fls920 型光致发光光谱仪(爱丁堡仪器)。
1.2 实验方法
1.2.1 CuBi2O4的制备
(1)在30mL 无水乙醇中加入1mmol 的Cu(NO3)2·3H2O,在5mL 乙酸中加入2mmol 的Bi(NO3)3·5H2O,充分搅拌混合均匀,得到Cu(NO3)2溶液和Bi(NO3)3溶液。
(2)将步骤(1)制备的Bi(NO3)3溶液逐滴滴入Cu(NO3)2醇溶液中,待其混合均匀后,用NaOH 将其pH 值调节至14。
(3)通过容积为100mL 的高压釜对混合溶液进行加热处理,加热温度和时间分别为120℃和90min。
(4)依次用去离子水和无水乙醇进行清洗,然后再烘干,烘干温度和时间分别为60℃和12h,得到CuBi2O4光催化剂,记为CBO 光催化剂。
1.2.2 WO3的制备
(1)依次将1g Na2WO4·2H2O 和0.6g 柠檬酸溶于60mL 去离子水中,用浓度为3mol·L-1的HCl 将混合物pH 值调节至1,充分搅拌反应60min。
(2)通过反应釜对混合物进行加热处理,加热温度和时间分别为120℃和12h,反应结束后取出产物自然冷却,依次用去离子水和无水乙醇进行洗涤。
(3)将产物置于电热鼓风干燥箱内烘干,烘干温度和时间分别为80℃和12h。以3℃·min-1的加热速率对干燥后产物进行煅烧处理,煅烧温度和时间分别为400℃和3h,将煅烧产物研磨,得到WO3光催化剂。
1.2.3 CBO/WO3的制备
(1)按照不同质量比混合CBO 和WO3,溶于60mL 甲醇中,在BNX-S30 型超声波清洗机的作用下进行超声处理,时间为4h。
(2)通过磁力搅拌器对超声产物进行搅拌处理,搅拌时间为12h,用无水乙醇将反应产物清洗3 次,然后在烘箱中进行干燥处理,干燥温度和时间分别为80℃和12h,研磨后得到X-CBO/WO3光催化剂(X 为CBO 质量百分比)。
1.2.4 苯甲醇转化实验
(1)以带有400~800nm 的500W 卤钨灯作为光源,设置光照强度为2.5×10-2W·cm-2。
(2)在圆底烧瓶中依次放入6mL 溶剂、一定量碱、光催化剂和反应物进行反应,反应温度和时间分别为30℃和12h。反应后,将沉淀物过滤出来,通过气相色谱法对1μL 残留溶液组分含量进行分析[7,8]。转化率和选择性表达式为[9,10]:
式中 A0:反应物初始峰面积;At:t 时刻反应物峰面积;A1t:t 时刻主产物峰面积;A2t:t 时刻所有副产物的峰面积。
1.3 性能测试
1.3.1 X 射线衍射(XRD)分析 通过X 射线衍射仪对光催化剂的特征峰进行分析。
1.3.2 透射电子显微镜(TEM)分析 通过透射电子显微镜对光催化剂的微观形貌进行分析。
1.3.3 紫外可见漫反射(UV-vis DRS) 通过固体-紫外可见分光光度计对光催化剂的光学吸收特性进行分析。
1.3.4 光致发光光谱 通过光致发光光谱仪对光催化剂的光生载流子复合情况进行分析。
2 结果与讨论
2.1 催化剂形貌及结构分析
2.1.1 XRD 分析 图1 为XRD 分析结果。

图1 光催化剂的XRD 图谱Fig.1 XRD spectrum of photocatalyst
由图1 可见,在CBO/WO3光催化剂中,同时存在CBO 特征峰和WO3特征峰,且随体系内CBO 质量百分比的增加,CBO 主峰强度也有一定增加,WO3的主峰强度有一定减小。以上变化说明成功制备出复合光催化剂X-CBO/WO3,且复合光催化剂XCBO/WO3中的所有峰均来自于CBO 和WO3,同时,峰值大小直接受物质的质量百分比影响。
2.1.2 TEM 分析 图2 为材料的微观形貌分析结果(以30%-CBO/WO3为代表)。

图2 微观形貌分析结果Fig.2 Micromorphology analysis results
由图2 可见,复合光催化剂的结构由CBO 的纳米柱和WO3的纳米片组成,这与2.1.1 结论相同,即成功制备出复合光催化剂。
2.2 光催化分析
2.2.1 UV-vis DRS 分析 图3 为可见光利用率分析结果。

图3 UV-vis DRS 分析结果Fig.3 UV-vis DRS analysis results
由图3 可见,制备的所有材料均具备明显可见光吸收作用,且复合光催化剂的可见光吸收强度明显高于WO3光催化剂,即WO3光催化剂的可见光利用率得到了明显提升。
2.2.2 PL 分析 图4 为PL 分析结果。

图4 光催化剂PL 图谱分析结果Fig.4 Analysis results of PL spectrum of photocatalyst
由图4 可见,在激发波长为325nm 的条件下,均在350~600nm 范围内出现较强的发射峰,其中CBO 光催化剂的发射峰强度明显低于WO3光催化剂。当CBO 光催化剂与WO3光催化剂复合形成异质结后,光催化剂的发射峰强度较WO3光催化剂有一定降低,且体系内存在的CBO 光催化剂质量百分比越高,发射峰强度越低。这是因为两种光催化剂形成异质结后,抑制了WO3光催化剂的电子-空穴重组,进而增强了光催化剂的光催化效率[11,12]。
2.3 苯甲醇的选择性氧化反应
2.3.1 光催化剂种类的影响 表1 为光催化剂种类优化结果。

表1 光催化剂优化结果(%)Tab.1 Effect of photocatalyst on reaction
由表1 可见,未添加光催化的反应组反应转化率明显低于添加了光催化剂的反应组,这说明在苯甲醇的选择性氧化反应过程中,光催化剂是不可或缺部分[13,14]。在有催化剂参与反应的组别中,复合光催化剂反应组的转化率明显高于单一光催化剂反应组的转化率,这说明复合光催化剂能明显提升反应的转化率。在4 组复合光催化剂反应中,30%-CBO/WO3的催化效果最好,此时反应转化率为38.5%,选择性超过99%。
2.3.2 光催化剂用量的影响 在2.3.1 节中,已经确定了30%-CBO/WO3复合光催化剂的催化效果最好,因此在本节中,使用该复合光催化剂继续进行实验。改变30%-CBO/WO3复合光催化剂用量,观察30%-CBO/WO3复合光催化剂用量对反应转化率的影响,结果见表2。
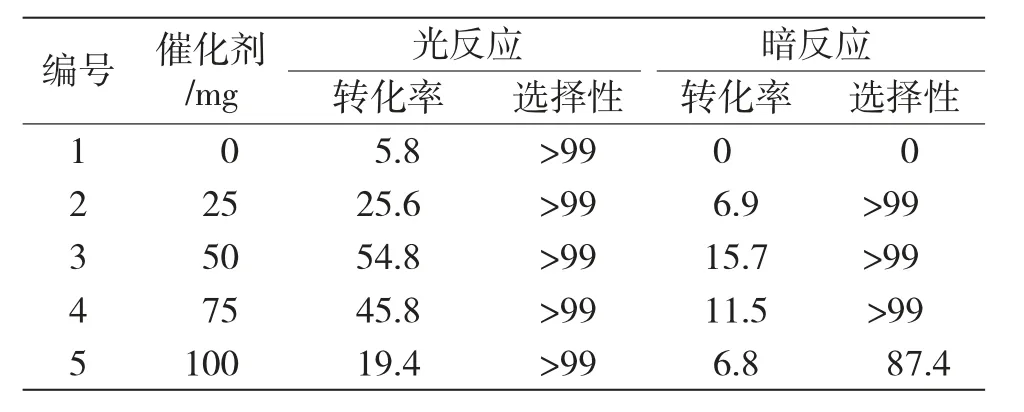
表2 光催化剂用量的影响(%)Tab.2 Effect of photocatalyst dosage
由表2 可见,当光催化剂用量为50mg 时,反应转化率达到最高为54.8%。这是因为,光催化剂用量较少时,提供的光催化活性位点也相对较少,无法很好的促进转化反应,使得反应转化率较低[15]。而光催化剂用量较多时,提供了较多的光催化活性位点,分散了转化材料,抑制了转化反应,使得反应转化率有一定降低。综上,选择适合的光催化剂用量为50mg。
2.3.3 溶剂对反应的影响 表3 为溶剂对反应的影响。

表3 溶剂对反应的影响(%)Tab.3 Effect of solvent on reaction
由表3 可见,以正己烷作为极性溶剂时,反应的转化率最高,达到了38.5%。这说明在反应过程中,正己烷不会对复合光催化剂的催化性能产生抑制,因此,选择适合的溶剂为正己烷。
2.3.4 碱种类及用量的影响 表4 为碱对反应转化率的影响。
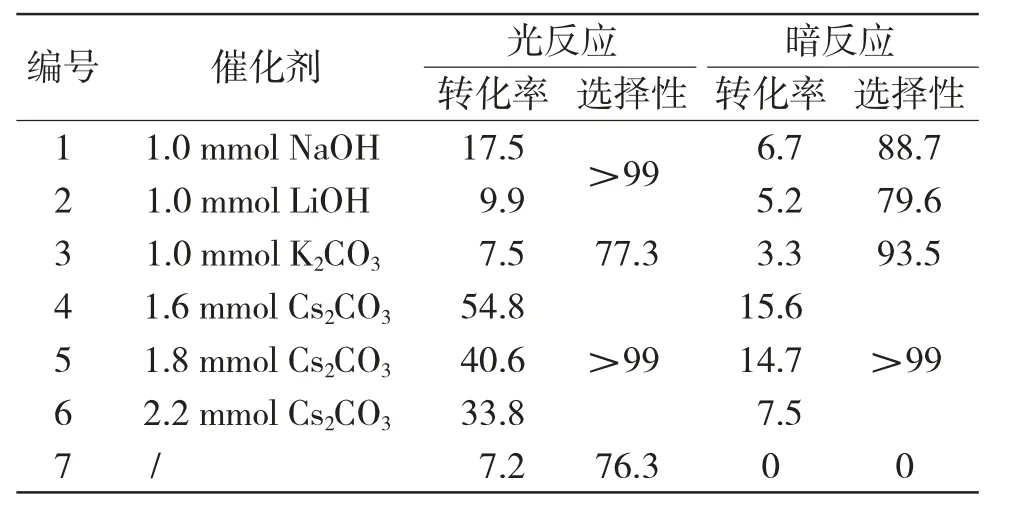
表4 碱对反应的影响(%)Tab.4 Effect of alkali on reaction
由表4 可见,未添加碱的反应组转化率和选择性明显低于其他组别,这就说明在转化反应的过程中,碱承担着较为重要的角色。而碱种类和碱用量不同,反应的转化率也不相同,这说明反应转化率同时受碱种类和用量的影响。其中,1.6mmol Cs2CO3的转化率最高,达到了54.8%。因此,在后续实验中,选择适合的碱种类及碱用量为1.6mmol Cs2CO3。
2.4 光催化剂循环测试
通过对CBO/WO3光催化剂重复进行多次实验,观察多次循环后,反应转化率的变化,结果见图5。

图5 重复性测试结果Fig.5 Repeatability test results
由图5 可见,第二次使用的光催化剂催化的反应转化率与一次使用光催化剂催化反应转化率基本一致。经过5 次循环以后,反应转化率虽然有一定下降,但仍维持在48%以上,表现出良好的循环效果。经过多次循环后,反应转化率降低的主要原因在于,在进行光催化剂循环实验的过程中,回收光催化剂时,存在CBO/WO3丢失或污染的情况,使得光催化剂催化反应转化率有一定降低。但总的来说,CBO/WO3光催化剂表现出较为稳定的催化性能,可以在苯甲醇选择性氧化反应中重复多次使用。
2.5 反应机理分析
为了探究复合光催化剂的催化机理,将活性基团·OH、·O2-、e-和h+对应的淬灭剂IPA、BQ、CCl4和EDTA 加入反应,观察加入淬灭剂后,反应转化率的变化,结果见图6。

图6 活性物种捕获试验Fig.6 Active species capture test
由图6 可见,加入几种淬灭剂后,苯甲醇的转化率均有不同程度的下降。说明在光催化反应过程中,所有活性物质均发挥了较为重要的作用。其中,加入淬灭剂EDTA 和BQ 时,反应转化率急速下降至4.5%和9.9%,CBO/WO3光催化剂反应转化率为54.8%,说明在催化反应进行的过程中,h+和·O2-发挥着至关重要的作用。以上变化表明,光催化剂在催化反应过程中是由4 种活性物质协同发挥作用,其中h+和·O2-的作用尤为关键。究其原因,是CBO 导带的光生电子进行转移,附着在WO3的价带上,对载流子重组概率有减小作用,在CBO 导带中的电子和WO3价带中的空穴作用下,使得O2形成·O2-、H2O 形成·OH,因此,复合催化剂可以提供更多的活性物种,能促进反应的进行,进而提升反应的效率。
3 结论
综上,本实验制备的CBO/WO3光催化剂表现出良好的综合性能,可以用于催化反应的进行,具体结论如下:
(1)光催化剂形貌及结构分析表明,XRD 图谱中,CBO/WO3光催化剂同时存在CBO 特征峰和WO3特征峰;透射电镜观察到,CBO/WO3的结构是由CBO 的纳米柱和WO3的纳米片组成,说明成功合成了CBO/WO3光催化剂。
(2)复合光催化剂的可见光吸收强度明显高于WO3光催化剂,PL 发射峰强度高于CBO 光催化剂,说明CBO/WO3的光催化作用明显优于单一光催化剂。
(3)通过苯甲醇的选择性氧化反应对光催化剂的活性进行表征,得到优化条件。
(4)经过多次循环后,苯甲醇转化率仍在48%作用,说明本实验制备的催化剂表现出良好的稳定性。
(5)通过添加淬灭剂的方式研究催化机理,结果表明,在光催化反应过程中,所有活性物质均发挥了较为重要的作用,其中h+和·O2-的作用尤为关键。进一步分析催化机理,CBO 与WO3形成CBO/WO3复合催化剂后,在CBO 导带中的电子和WO3价带中的空穴作用下,使得O2形成·O2-、H2O 形成·OH,复合催化剂可以提供更多的活性物种,促进反应的进行,进而提升反应的效率。
