分散液相微萃取-气相色谱-质谱法快速检测水体中17种芳香胺
2023-07-20杨超尹明明戴维徐颖
杨超,尹明明,戴维,徐颖
(江苏省南京环境监测中心,南京 210013)
芳香胺是一类含有—NH2、—NH或其它含氮基团的胺类化合物,其结构中通常含有一个或多个苯环,按照取代基的种类、数目和位置的不同形成多种异构体。这类化合物大多是高沸点的液体或低熔点的固体,在水中的溶解度小,易溶于有机溶剂,在空气中易氧化变色。芳香胺普遍具有特殊的气味,可通过呼吸道或消化道摄入人体,也能够被皮肤快速吸收[1],其生物毒性较大。环境中的芳香胺主要来源于橡胶、印染、制药、塑料、合成树脂等生产过程,苯胺是芳香胺类最有代表性的物质,而联苯胺及其衍生物则来源于各种染料及有机颜料,是染料工业的重要中间体[2‒3]。苯胺类和联苯胺类化合物污染对水源环境及人们的生产生活易造成严重影响,因此需要建立健全苯胺类和联苯胺类污染的监测技术。
目前对于水体中芳香胺检测的研究日益增多,主要分析方法有分光光度法[4‒5]、气相色谱法[6‒7]、液相色谱法[8‒9]、气相色谱-质谱法[10‒11]、液相色谱-质谱法[12‒13]、毛细管电泳法[14‒15]、电化学法[16]等。分析有机污染物常用的样品处理方式有固相萃取法、液液萃取法,但是这两种传统方法普遍存在操作繁琐、耗时、有机溶剂用量大的缺点。分散液相微萃取是Rezaee等人[17]在2006年提出的一种新型萃取技术,仅用极少的有机溶剂作为萃取剂,能够集样品萃取和富集过程于一体,省略了浓缩步骤,具有操作简便快速、富集效率高、萃取溶剂用量少和成本低等优点,在液体样品痕量污染物分析中具有较大的优势,逐渐应用于环境样本中芳香胺的富集与测定[18‒22],但这些方法均存在测定的芳香胺种类偏少[19‒20]、定量方式多选用外标法[21]、检出限偏高[22]等缺陷。
笔者通过优化分散液相微萃取过程中的各种影响因素,建立了以内标法定量的高通量检测方法,成功将其应用于水体中17种芳香胺类物质的测定,该方法操作简单、重现性好、检出限低,为今后水体中芳香胺的快速定性定量分析提供实验依据与技术支持。
1 实验部分
1.1 主要仪器与试剂
气相色谱-质谱仪:Agilent 7890A-7000B型,安捷伦科技(中国)有限公司。
电子天平:BSA822型,感量为0.01 g,赛多利斯科技仪器(中国)有限公司。
涡旋混匀仪:XW-80A型,海门市其林贝尔仪器制造有限公司。
离心机:TGL16M型,长沙湘智离心机仪器有限公司。
12种芳香胺类混合标准溶液:含有苯胺、2-甲基苯胺、3-甲基苯胺、4-甲基苯胺、2,4-二甲基苯胺、2,6-二甲基苯胺、2-甲氧基苯胺、3-氯胺、4-氯胺、3-硝基苯胺、4-硝基苯胺、3,3′-二氯联苯胺,各组分质量浓度均为10.000 g/L,溶剂为甲醇,批号为33347 TM (F0057292),北京曼哈格生物科技有限公司。
1-萘胺、2-萘胺、2-硝基苯胺、4-氨基联苯:纯度(质量分数)分别为98.8%、98.1%、98.5%、98.7%,德国Dr.Ehrenstorfer股份有限公司。
2-氯胺:纯度(质量分数)为98.3%,北京曼哈格生物科技有限公司。
苯胺-d5标准溶液:2.000 g/L,溶剂为二氯甲烷,北京曼哈格生物科技有限公司。
苊-d10 标准溶液:4.000 g/L,溶剂为二氯甲烷,美国Accu Standard公司。
4-氯胺-d2:纯度(质量分数)为98.6%,加拿大C/D/N ISOTopes公司。
4-甲基苯胺-d9、3-硝基苯胺-d4:纯度(质量分数)分别为98.5%、97.7%,德国Dr.Ehrenstorfer 股份有限公司。
三氯甲烷、四氯化碳、N,N-二甲基甲酰胺、甲基叔丁基醚、硫酸钠、亚硫酸钠、硫代硫酸钠:均为分析纯,国药集团化学试剂有限公司。
乙酸乙酯、二氯甲烷、甲醇、乙腈、丙酮、异丙醇:均为色谱纯,德国默克EMD Millipore公司。
高纯氦气:纯度(体积分数)为99.999%,句容康泰特种气体有限公司。
实验用水为Milli-Q纯水系统制得的超纯水。
1.2 溶液配制
3 种内标混合标准溶液:各组分质量浓度均为5.000 g/L,分别准确称取4-氯胺-d2、4-甲基苯胺-d9、3-硝基苯胺-d4 各5 mg 于1 mL 容量瓶中,用乙腈定容至标线,混匀。
5 种内标混合标准储备液:各组分质量浓度均为100 mg/L,分别移取3 种内标混合标准溶液20 μL、苯胺-d5 标准溶液50 μL 和苊-d10 标准溶液25 μL于1 mL容量瓶中,用乙腈定容至标线,混匀。
5 种内标混合标准使用液:各组分质量浓度均为2 mg/L,移取5种内标混合标准储备液20 μL至1 mL容量瓶中,用乙腈定容至标线,混匀。
5 种苯胺类混合标准溶液:各组分质量浓度均为5.000 g/L,分别准确称取1-萘胺、2-萘胺、2-氯胺、2-硝基苯胺、4-氨基联苯各5 mg 于1 mL 容量瓶中,用乙腈定容至标线,混匀。
17种芳香胺类混合标准储备液:各组分质量浓度均为100 mg/L,分别移取12种芳香胺类混合标准溶液10 μL 和5 种苯胺类混合标准溶液20 μL 至1 mL容量瓶中,用乙腈定容至标线,混匀。
17种芳香胺类混合标准使用液:各组分质量浓度均为1 mg/L,移取17种芳香胺类混合标准储备液10 μL至1 mL容量瓶中,用乙腈定容至标线,混匀。
17种芳香胺类系列混合标准工作溶液:分别准确移取17 种芳香胺类混合标准使用液5.0、10.0、50.0、100、200 µL,置于盛有适量三氯甲烷的1.0 mL容量瓶中,用三氯甲烷定容至标线,再分别向各容量瓶中加入5种内标混合标准使用液20.0 µL,配制成目标化合物质量浓度均分别为5.0、10.0、50.0、100、200 µg/L,内标物质量浓度均为40.0 µg/L 的系列混合标准工作溶液。
1.3 仪器工作条件
1.3.1 色谱仪
色谱柱:DB-35 MS 石英毛细管柱(30 m×0.25 mm,0.25 μm,美国安捷伦科技有限公司);进样口温度:250 ℃;进样方式:分流进样,分流比为5∶1;进样体积:1.0 μL;柱温:程序升温,初始温度为60 ℃,保持2 min,以5 ℃/min 升温至130 ℃,然后以30 ℃/min 升温至300 ℃,保持4 min;载气:高纯氦气;柱流量:1.0 mL/min。
1.3.2 质谱仪
离子源:电子轰击源(EI 源);离子源温度:300 ℃;离子化能量:70 eV;接口温度:300 ℃;四极杆温度:150 ℃;溶剂延迟时间:5 min;数据采集方式:SIM模式;17种芳香胺的质谱参数见表1。
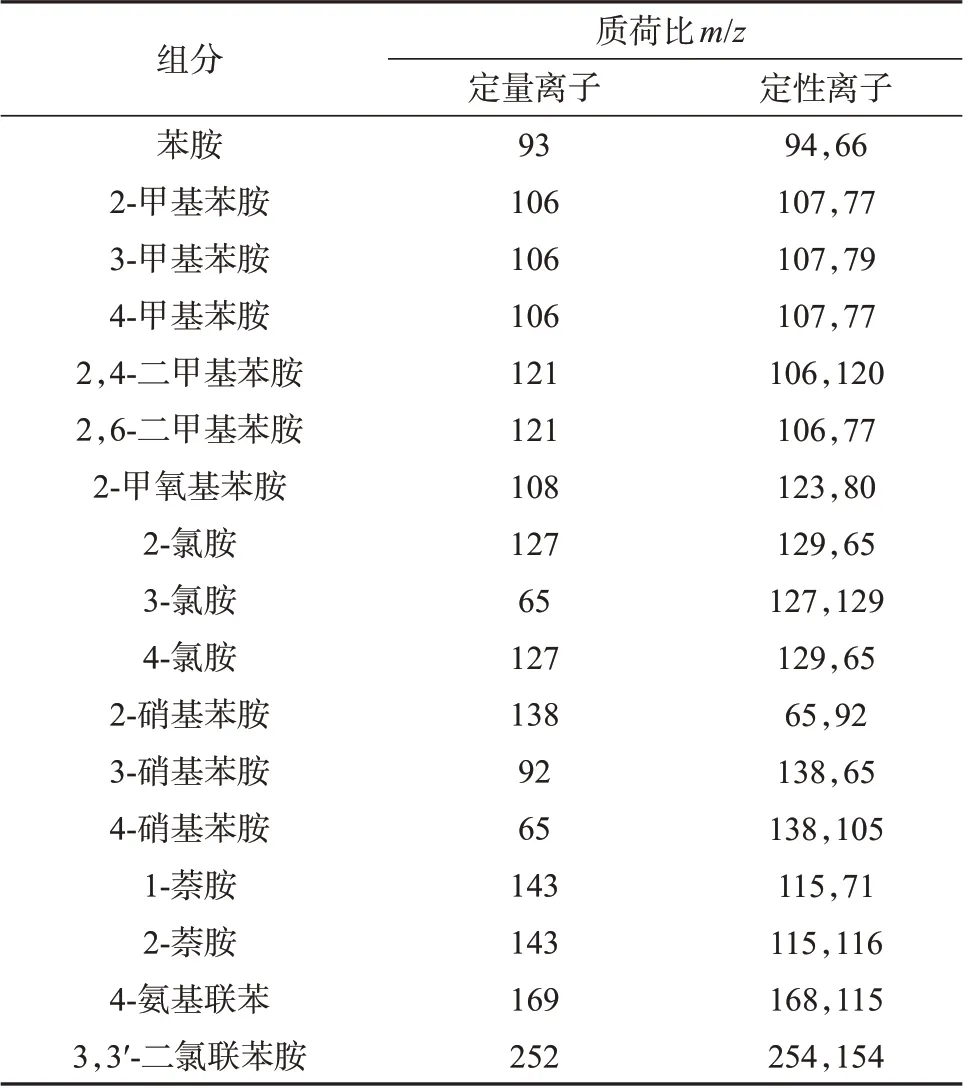
表1 17种芳香胺的质谱参数
1.4 样品处理
采集水样后,调节其pH 值约为11,移取10 mL水样于15 mL离心试管中,加入0.10 g亚硫酸钠,振摇使其完全溶解,用注射器分别将0.8 mL 乙腈和100 μL三氯甲烷迅速注入水样中形成乳浊样,涡旋混合60 s 后转移至离心机中,以4 000 r/min 转速离心5 min,然后用微量注射器伸入试管底部准确吸取50.0 μL 有机相,再加入5 种内标混合标准使用液1.0 μL,混匀后上机分析。
1.5 测定方法
按照1.3 仪器工作条件,测定17 种芳香胺类系列混合标准工作溶液,以目标物质量浓度与内标物质量浓度的比值为横坐标,以目标物与内标物定量离子响应值的比值为纵坐标绘制标准曲线,将待测溶液上机分析,计算目标物含量。
2 结果与讨论
2.1 色谱条件优化
选择常用的两种极性的石英毛细管色谱柱对17 种目标化合物进行分离。第一种为弱极性的HP−5MS 柱(30 m×0.25 mm,0.25 μm),固定相为5%苯基-甲基聚硅氧烷;第二种为中等极性的DB-35MS 柱(30 m×0.25 mm,0.25 μm),固定相为35%苯基-甲基聚硅氧烷。实验发现,HP−5MS柱对同分异构体的分离效果较差,尤其是2-甲基苯胺和4-甲基苯胺、2,4-二甲基苯胺和2,6-二甲基苯胺这两对异构体,无法实现基线分离,并且其余组分的色谱峰存在拖尾现象,影响定量分析的准确性;而DB-35MS柱则可以将17种目标组分分离,并且色谱峰形更加对称和尖锐,因此选用中等极性的DB-35MS 色谱柱。17 种芳香胺类和5 种内标混合标准溶液、空白地表水样品及加标地表水样品总离子流图如图1所示。

图1 17种芳香胺类和5种内标混合标准溶液、空白地表水样品及加标地表水样品的总离子流图
2.2 分散液相微萃取条件优化
2.2.1 萃取剂种类及用量
萃取剂是影响萃取效率及回收率的重要因素,由于苯胺类和联苯胺类化合物属于半挥发性极性物质,因此萃取剂应在中等极性的有机溶剂中选择。实验考察了二氯甲烷、三氯甲烷、四氯化碳、甲基叔丁基醚和乙酸乙酯5种溶剂对17种芳香胺类的萃取效果,结果表明:三氯甲烷、四氯化碳作为萃取剂离心后有机相的量较大,在水中损失较少;二氯甲烷因密度比三氯甲烷小,经萃取、离心后有机相的量较小,损失较大并且不方便移取,操作误差大;乙酸乙酯与甲基叔丁基醚因为密度较水小,所以有机相在上层,同时由于有机相体积小,导致离心后上层有机相移取难度大。对比三氯甲烷和四氯化碳的萃取效率,使用三氯甲烷作为萃取剂,苯胺类回收率普遍较高,故选择三氯甲烷为萃取剂。
分别以30、50、100、150、200 μL 三氯甲烷为萃取剂,考察目标化合物的萃取效率。结果表明,当萃取剂用量为30 μL 时,离心后试管底部几乎没有有机相,无法移取;当萃取剂用量由50 µL 增加到100µL 时,17 种芳香胺类回收率有所增大;当继续增加萃取剂用量时,17 种芳香胺类回收率无明显变化。萃取剂的体积与富集倍数成反比,体积越少可以获得更高的富集倍数和更低的检出限,故选择萃取剂三氯甲烷用量为100 µL。
2.2.2 分散剂种类及用量
分散剂的作用是提高萃取剂与目标物的接触面积,形成较好的乳浊液体系,从而提高萃取效率。分别选取甲醇、乙腈、丙酮、N,N-二甲基甲酰胺、异丙醇作为分散剂进行试验,结果显示,采用乙腈作为分散剂能够与三氯甲烷形成良好的乳浊液,萃取效果最好,故选择乙腈为分散剂。
固定萃取剂体积为100 µL,分别以0.2、0.4、0.8、1.0、2.0 mL 乙腈为分散剂,考察目标化合物的萃取效率,结果表明,随着分散剂乙腈用量的增大,各目标物的萃取效率逐渐增大,当乙腈用量为0.8 mL时,萃取效率达到最大。继续增大乙腈用量时,萃取效率反而有所下降,原因是当乙腈用量较少时,三氯甲烷未能在水中分散成细小液滴,导致与水接触不完全,提取效率偏低;乙腈用量过大反而增加三氯甲烷在水中的损失,使得萃取剂体积变小,萃取效率下降,因此选择0.8 mL乙腈作为分散剂。
2.2.3 还原剂种类及用量
苯胺类和联苯胺类容易氧化,尤其是3,3′-二氯联苯胺和萘胺受氧化作用较明显,因此在萃取体系中加入还原剂来抑制氧化作用。分别选取硫代硫酸钠、硫酸钠、亚硫酸钠作为还原剂,比较目标化合物的回收率。结果表明,3 种还原剂中亚硫酸钠对3,3′-二氯联苯胺和萘胺均有较好的抑制氧化效果,能够显著提高萃取率,故选择亚硫酸钠为还原剂。
分别以0.00、0.05、0.10、0.30、0.50 g亚硫酸钠为还原剂,比较目标物的回收率,结果表明,当亚硫酸钠用量逐渐增大时,17种芳香胺类萃取效率总体趋势为先增大后减小,在亚硫酸钠加入质量为0.10 g时,目标物回收率达到峰值,继续增加亚硫酸钠用量,回收率轻微下降。考虑到亚硫酸钠的溶解度受温度影响较大,固体加入越多溶解越困难,所以最终确定亚硫酸钠加入质量为0.10 g。
2.2.4 溶液pH值
芳香胺由于结构中的氮原子存在孤对电子,因此易与酸反应生成稳定的胺盐,水溶性增强,用有机溶剂萃取时萃取效率较低。合适的pH 条件能够使苯胺类物质以分子形态转移至有机相中,提高萃取效率。实验考查pH值分别为2、4、7、9、11条件下对目标化合物的回收率,结果表明,当溶液呈酸性(pH值小于7)时,大部分目标化合物回收率低于10%,证明了酸性条件下无法有效提取绝大部分目标化合物;当溶液呈弱碱性时,除了3,3′-二氯联苯胺外,其余组分回收率均在70%以上,当溶液pH值为11时,目标化合物整体回收率达到90%以上,表明目标化合物在碱性条件下萃取效率高,因此萃取时需将水样pH值调至11。
2.2.5 萃取时间
萃取时间是指将萃取剂/分散剂体系注入到样品溶液中至离心的时间。萃取溶剂体系进入样品溶液中后,采用涡旋方式可使萃取剂快速在水相中形成大量微小液滴,以增大比表面积,从而使目标物快速迁移至萃取溶剂中。分别设定涡旋振荡时间为30、60、90、120、150 s,考察17种芳香胺的回收率,结果表明,当涡旋振荡时间超过60 s后,萃取效率不再有明显增大趋势,因此涡旋振荡60 s 后即可直接进行离心。
2.2.6 内标物选择
本实验目标化合物种类较多,如果实验过程中使用的同位素内标物种类过多,会增加操作难度,同时成本也较高,对环境危害较大。考虑到目标组分与同位素内标物最大程度的一一对应,采用有代表性的5种同位素内标定量,具体定量内标见表2。

表2 目标化合物与定量内标
2.3 线性方程与检出限
按1.3仪器工作条件对17种芳香胺系列混合标准溶液进行测定,以目标物质量浓度与内标物质量浓度的比值为横坐标,以目标物与内标物定量离子响应值的比值为纵坐标,以最小二乘法绘制标准曲线,计算线性方程和相关系数。采用空白低浓度加标的方式计算方法检出限,分别对0.12、0.20 μg/L的加标样品进行萃取,对萃取液平行测定7次,计算标准偏差,按照HJ 168—2020[23]计算各组分的方法检出限,以4 倍检出限作为定量限。17 种芳香胺质量浓度范围、线性方程、相关系数、检出限及定量限结果见表3。

表3 17种芳香胺质量浓度范围、线性方程、相关系数与检出限
2.4 准确度及精密度试验
对实际水样分别添加低、中、高三个浓度水平的17种芳香胺混合标准溶液,按照实验方法进行测定,每个添加水平平行测定6次,结果见表4。由表4可知,3个添加水平下17种芳香胺的加标回收率为77.2%~114%,测定结果的相对标准偏差为2.6%~16.5%,表明该方法在不同添加水平下均有良好的重复性和回收率,方法的精密度和准确度能够满足测试要求。

表4 加标回收与精密度试验结果(n=6)
2.5 方法比对
目前对水中苯胺类物质检测的标准方法主要有HJ 822—2017《水质 苯胺类化合物的测定 气相色谱-质谱法》和HJ 1048—2019《水质 17种苯胺类化合物的测定 液相色谱-三重四极杆质谱法》,由于实验采用的是气相色谱-质谱联用法,将该方法与HJ 822—2017标准方法进行方法比对,验证该方法与标准方法有无显著性差异。按照两种样品处理方式分别对地表水、地下水、生活污水、工业废水进行检测,分别在4种类型水体中添加17种芳香胺混合标准溶液,加标质量浓度均为20 μg/L,采用t检验比较方法的差异性[24]。对样品质量浓度增加量进行统计,并计算配对差值均值、标准差Sd和t值,结果见表5和表6。
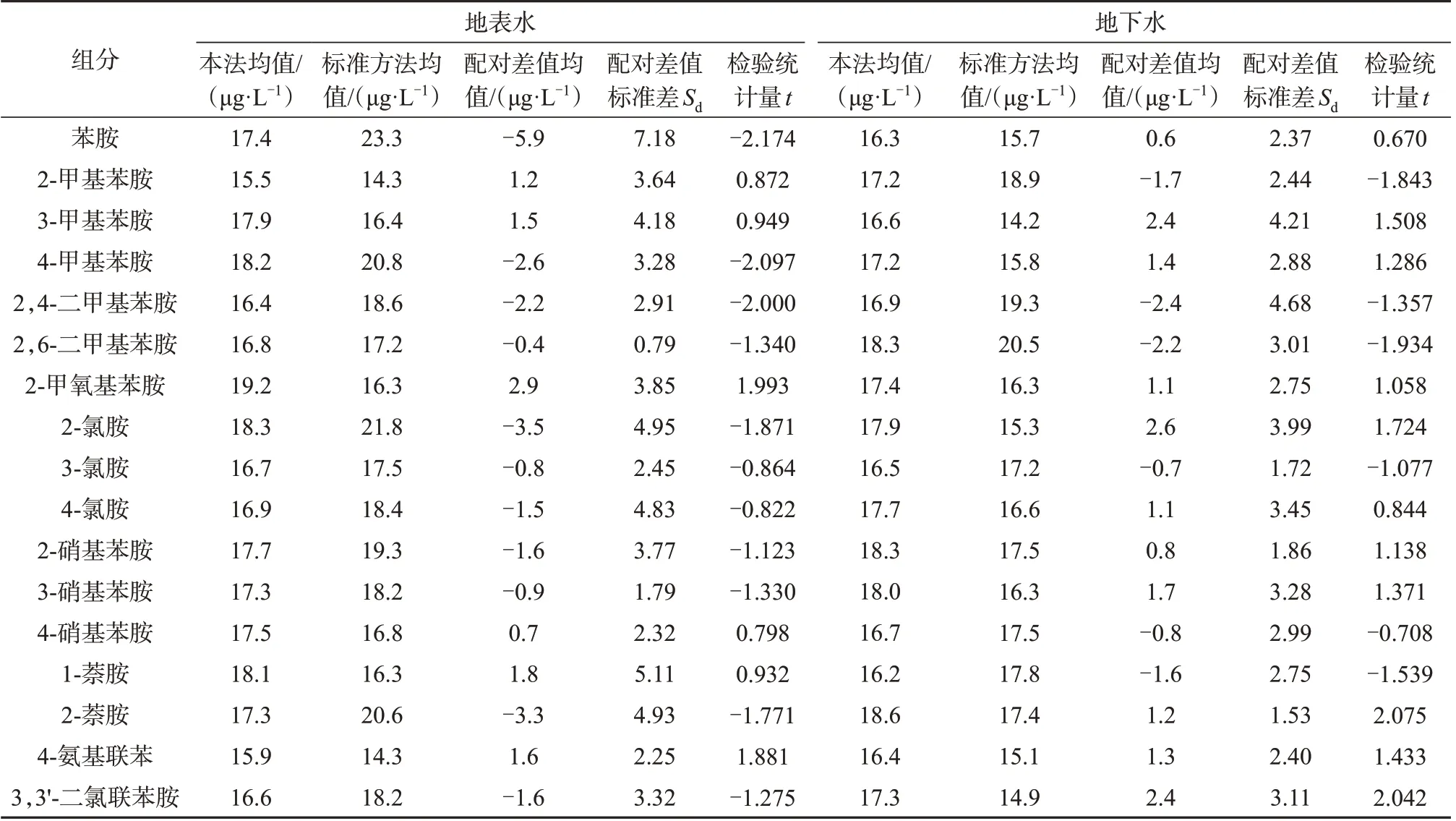
表5 地表水和地下水中17种芳香胺测定方法比对结果(n=8)

表6 生活污水和工业废水中17种芳香胺测定方法比对结果(n=8)
根据表5 和表6 汇总的结果,所有类型水体中17 种组分计算得到的t绝对值均小于2.365,即双侧检验P>0.05,因此对于检测地表水、地下水、生活污水、废水4种类型水体中的17种芳香胺,两种方法无显著性差异。
3 结语
建立了分散液相微萃取-气相色谱-串联质谱法检测水体中17种芳香胺类物质的分析方法,采用三氯甲烷作为萃取剂、乙腈作为分散剂,在碱性条件下快速提取水中的芳香胺,对分散液相微萃取过程中影响因素进行优化,得到较为满意的检出限、正确度、精密度,并将该方法与标准方法进行比较,采用t检验验证,两种方法没有显著性差异。该方法相比于标准方法,具有耗时短,试剂用量少,灵敏度高,回收率高等优点,适用于水体中芳香胺的快速检测。
