右美托咪定联合罗哌卡因实施“领结征”髂筋膜阻滞对髋部骨折患者围术期的镇痛效果
2023-06-13单国法夏焱志郭明仁
单国法,夏焱志,郭明仁
髋部骨折引起的围术期疼痛,包括外伤致疼、炎症疼、手术切口疼等,由急性延续为长期慢性,伴随整个康复期,对个人和经济造成了巨大的负担。疼痛可以分为伤害性疼痛、神经性疼痛,疼痛的生物-心理-社会模型将身体症状表现为生物、心理和社会因素之间动态交互作用的结果。虽然疼痛会导致心理困扰和睡眠问题,但许多医务人员并没有意识到这些作用是相互的[1]。髋部骨折术后疼痛严重降低患者的生活质量,极大地挑战“舒适化医疗”理念及“快速康复”医疗共识,给社会和家庭造成负担。围术期最理想的疼痛管理模式常采用多模式管理方法减少阿片类药物的使用,减少不良作用,利于术后康复、提高患者住院满意度,目前超声引导下的神经阻滞是多模式镇痛的重要组成部分[2]。在一项对2 000 多名患者的Meta 分析中,在臂丛阻滞中加入右美托咪定可延长神经阻滞持续时间,改善镇痛效果,同时吗啡消耗量显著减少[3]。罗哌卡因是一种长效酰胺类局麻药,广泛应用于临床局部麻醉或神经阻滞。本研究旨在探讨右美托咪定联合罗哌卡因实施“领结征”髂筋膜间隙阻滞对髋部骨折患者围术期疼痛的临床应用效果。
1 资料与方法
1.1 一般资料选取阜宁县人民医院骨科2020年7 月至2021 年6 月单纯髋部骨折老年患者60例,年龄≥70 岁,美国麻醉医师分级(ASA)Ⅰ~Ⅱ级。排除标准:(1)神志不清;(2)术前存在认知障碍/神经精神类疾病;(3)慢性疼痛病史;(4)进行急诊手术;(5)严重心律失常;(6)复合性损伤;(7)酒精滥用;(8)长期服用镇静镇痛药物者或对研究药物过敏;(9)拒绝参与。采用数字表法随机进行分组,其中Q 组实施“领结征”髂筋膜阻滞,阻滞药物为罗哌卡因;QY 组实施“领结征”髂筋膜阻滞,阻滞药物为罗哌卡因+右美托咪定;G 组实施超声引导下股外侧皮神经阻滞,阻滞药物为罗哌卡因,每组各20 例。
根据预实验,Q 组、QY 组和G 组间差异较大,因此规定3 组间差异达到较大效应量大小为差异具有临床意义,取α=0.05,power=0.90,f=0.50,利用G*Power 软件计算得到的样本量为每组18 例,考虑到10% 的脱落率,每组在基线时需至少纳入20 例,共计60 例。
Q 组、QY 组和G 组患者在性别、年龄、体重、ASA 分级等一般资料比较差异均无统计学意义(P>0.05)。见表1。通过阜宁县人民医院伦理委员会批准(2020 伦研批第011 号),并征求患者及家属同意。
表1 Q 组、QY 组和G 组患者一般资料比较[例,± s,每组n=20]

表1 Q 组、QY 组和G 组患者一般资料比较[例,± s,每组n=20]
注:ASA 为美国麻醉医师协会
组别Q 组QY 组G 组ASA 分级(Ⅰ/Ⅱ)10/10 9/11 11/9性别(男/女)11/9 13/7 8/12年龄(岁)74.70 ± 3.97 75.40 ± 3.55 76.90 ± 3.76体重(kg)65.65 ± 6.44 65.55 ± 7.36 68.40 ± 8.22
1.2 治疗方法术前常规禁食8~12 h、禁饮4 h,于麻醉开始前40 min 进入手术室。入室后常规开放静脉通路,连接监护仪监测心电图(ECG)、血氧饱和度(SpO2)和无创血压(NIBP)。然后分别给Q 组、QY 组和G 组患者实施超声引导下神经阻滞。
Q 组患者实施“领结征”髂筋膜间隙阻滞,穿刺针到达目标位置后注射0.375% 罗哌卡因20 ml。QY 组患者同样实施“领结征”髂筋膜阻滞,穿刺针到达目标位置后注射0.375% 罗哌卡因+右美托咪定0.5 μg/kg 混合液20 ml。G 组患者实施超声引导下股外侧皮神经阻滞,穿刺针到达目标位置后注射0.375%罗哌卡因20 ml。
麻醉诱导:静脉注射咪达唑仑0.05 mg/kg、依托咪酯0.3 mg/kg、顺阿曲库铵0.15 mg/kg、芬太尼0.003 mg/kg,充分给氧去氮以后,经口插入ID 7.0#气管导管后行机械通气。设置呼吸参数:潮气量(VT)8 ml/kg,呼吸频率(RR)10~12 次/min,吸呼比(I∶E)1∶1.5,维 持 呼 末 二 氧 化 碳(PetCO2)30~40 mmHg(1 mmHg=0.133 kPa)。麻醉维持:丙泊酚4~12 mg/(kg·h)、瑞芬太尼0.25~0.75 μg/(kg·min)持续静脉泵入,芬太尼、顺式阿曲库铵按需静脉注射,七氟醚1%~2%持续吸入。所有患者按照“4-2-1”法则及手术和失血情况,使用钠钾镁钙葡萄糖注射液及6% 羟乙基淀粉进行容量管理,失血量超过血容量20% 时输血。维持心率和血压在基础值20% 以内波动,必要时使用阿托品、麻黄碱或去氧肾上腺素等血管活性药物。患者术后均使用静脉自控镇痛(PCIA)方式进行镇痛管理。镇痛药配方:舒芬太尼2 μg/kg+阿扎司琼20 mg,用0.9%氯化钠注射液稀释至100 ml。手术结束即开始连接镇痛泵,无负荷量,自动输注速率为2 ml/h,单次按压剂量为2 ml,锁定时间15 min。
1.3 观察指标分别记录Q 组、QY 组和G 组患者阻滞前、诱导前、术后1、6、12、24 h 的静态及动态疼痛视觉模拟量表(VAS)评分,术中镇痛药物及镇痛泵使用情况及不良反应,如头晕恶心、穿刺位置血肿、药物中毒等。
1.4 统计学处理运用SPSS 22.0 统计软件对数据进行分析,计量资料以±s表示,组内比较采取重复测量方差分析,组间比较用t检验;计数资料以频数和百分比(%)表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 Q 组、QY 组和G 组患者不同时间点VAS 评分的比较QY 组与Q 组和G 组患者在静息和运动时间点阻滞前、术后24 h 时VAS 评分比较,差异无统计学意义(P>0.05),但QY 组患者静息和运动时间点诱导前、术后1、6、12 h 时VAS 评分与Q 组、G 组患者比较,差异有统计学意义(P<0.05)。见表2。
表2 Q 组、QY 组和G 组患者不同时间点VAS 疼痛评分的比较(分,± s,每组n=20)
注:与Q 组、G 组比较aP<0.05。VAS 为视觉模拟量表
组别Q 组QY 组G 组术后24 h 4.50 ± 0.61 4.95 ± 0.22 4.35 ± 0.67 4.85 ± 0.37 4.65 ± 0.49 5.10 ± 0.45时间点静息运动静息运动静息运动阻滞前6.15 ± 1.04 7.90 ± 0.85 6.35 ± 0.88 7.75 ± 0.85 6.30 ± 1.03 7.95 ± 0.76诱导前3.20 ± 0.89 5.90 ± 0.85 2.70 ± 0.47a 4.65 ± 0.81a 4.40 ± 0.50 6.00 ± 0.73术后1 h 4.15 ± 0.59 6.15 ± 0.75 2.85 ± 0.59a 4.95 ± 0.69a 4.30 ± 0.73 6.30 ± 0.92术后6 h 5.05 ± 0.76 6.30 ± 0.57 3.70 ± 0.57a 5.10 ± 0.72a 5.10 ± 0.45 6.40 ± 0.94术后12 h 5.10 ± 0.72 6.55 ± 0.76 3.85 ± 0.67a 5.35 ± 0.59a 5.25 ± 0.64 6.80 ± 1.15
2.2 Q组、QY 组和G 组患者术中镇痛药用量情况的比较QY 组患者术中芬太尼、瑞芬太尼使用量低于Q 组、G 组,差异有统计学意义(P<0.05)。见表3。
表3 Q 组、QY 组和G 组患者术中镇痛药用量的比较(mg,± s,每组n=20)
注:与Q 组、G 组比较aP<0.05
组别Q 组QY 组G 组瑞芬太尼0.78 ± 0.03 0.64 ± 0.04a 0.96 ± 0.04芬太尼0.42 ± 0.02 0.36 ± 0.02a 0.54 ± 0.05
2.3 Q组、QY 组和G 组患者术后不同时间点镇痛泵使用情况的比较 Q 组、QY 组和G 组患者在术后1 h 内,镇痛泵按压次数比较,差异无统计学意义(P>0.05),但QY 组患者,在术后6、12、24 h 时镇痛泵按压次数与Q 组、G 组患者比较,差异有统计学意义(P<0.05)。见表4。
表4 Q 组、QY 组和G 组患者术后不同时间点镇痛泵有效按压次数比较(次,± s,每组n=20)
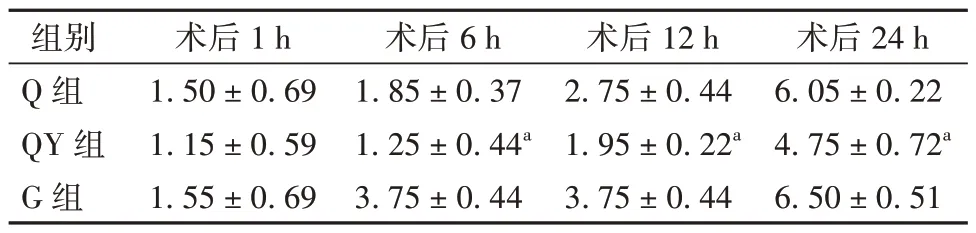
表4 Q 组、QY 组和G 组患者术后不同时间点镇痛泵有效按压次数比较(次,± s,每组n=20)
注:与Q 组、G 组比较aP<0.05
组别Q 组QY 组G 组术后24 h 6.05 ± 0.22 4.75 ± 0.72a 6.50 ± 0.51术后1 h 1.50 ± 0.69 1.15 ± 0.59 1.55 ± 0.69术后6 h 1.85 ± 0.37 1.25 ± 0.44a 3.75 ± 0.44术后12 h 2.75 ± 0.44 1.95 ± 0.22a 3.75 ± 0.44
2.4 Q 组、QY 组和G 组患者不良反应比较Q组、QY 组和G 组患者无一例出现呼吸抑制、局麻药中毒、穿刺部位出血血肿等情况,Q 组、QY 组和G组患者的总不良反应发生率方面,QY 组较Q 组、G组低,差异有统计学意义(P<0.05)。见表5。

表5 Q 组、QY 组和G 组患者术后不良反应比较[例(%),每组n=20]
3 讨论
髋部手术区域涉及神经支配较为复杂,包括臀上皮神经、肋下神经(T12 前支)的外侧皮支、髂腹下神经的外侧皮支支配切口的上段皮区;股外侧皮神经的后支支配切口中下段皮区;臀下神经支配臀大肌;臀上神经支配阔筋膜张肌、臀中肌;股神经支配髋关节囊前侧及前外侧;闭孔神经支配髋关节囊前内侧;坐骨神经支配髋关节囊的后内侧;臀上神经支配髋关节囊的后外侧。由此可见,髋部区域主要受股神经、股外侧皮神经、闭孔神经支配,而这3 支神经均通过髂筋膜间隙[4]。
本研究发现,在各项对比中,Q 组都比G 组要略低,进一步也表明髋部骨折的术后疼痛,“领结征”髂筋膜间隙比股外侧皮神经更能有效阻滞髋部骨折手术疼痛。同时还发现QY 组患者术中芬太尼、瑞芬太尼使用量低于Q 组、G 组。QY 组患者在诱导前、术后1、6、12 h 的VAS 评分以及在术后6、12、24 h 的镇痛按压次数与Q 组、G 组比较均差异有统计学意义。QY 组局麻药配伍了0.5 μg/kg 的右美托咪定,右美托咪定为美托咪定的右旋异构体,可刺激中枢神经系统α2-受体最密集的区域——脑干蓝斑(负责调解觉醒与睡眠),引发并维持自然非动眼睡眠状态,产生镇静、催眠作用[5]。研究提示,右美托咪定可抑制Na+通道α 亚单位Nav1.5,使细胞超级化[6];而Nav1.5 作为门控钠离子通道,通过调节细胞内外钠离子的转运,产生电位差,调控神经系统疼痛信号的转导[7]。临床研究又提示,使用该药能降低toll 样受体4 和核因子κB的表达及活化[8]。toll 样受体4 和核因子κB 能够介导炎症细胞合成分泌大量肿瘤坏死因子(TNF)-α、白细胞介素(IL)-6 及IL-1β,导致全身炎症且局部炎症疼痛[9]。此外,右旋美托咪定抑制氧自由基对机体的损伤作用,可以通过p38 蛋白激酶/细胞外调节蛋白激酶信号通路,增加Bcl-2 水平,降低Bax 和caspase-3 水平,增加细胞存活率,减少细胞凋亡[10]。p38 蛋白激酶/细胞外调节蛋白激酶信号通路能够通过影响疼痛因子,如神经激肽-1 和强啡肽,对疼痛产生作用[11]。推论右美托咪定可作用于外周及中枢神经系统细胞膜的Na+通道受体、toll 样受体4等,进一步抑制细胞内核因子κB、p38 蛋白激酶/细胞外调节蛋白激酶等通路作用,抑制炎症因子、疼痛因子的合成与分泌,对疼痛产生作用。另外有研究表明,右美托咪定有导致血管收缩,延迟并延长局部麻醉的效果[12]。同样也正是由于QY 组的镇痛效果较好,头晕嗜睡、恶心呕吐的总体不良反应发生率也远低于Q 组、G 组。课题研究中与局麻药配伍的右美托咪定量并不多,镇静量未达到嗜睡的程度,而课题组未能统计减慢心率的情况,是本研究的局限处,将在以后的研究中改正。本研究中其他2 组术后镇痛不如QY 组完善,增加了镇痛泵按压次数,阿片类药物使用量相对大,造成总不良反应多于QY 组。综上所述,罗哌卡因配伍0.5 μg/kg 右美托咪定实施“领结征”骼筋膜阻滞用于髋部骨折患者术后的镇痛效果较好,具有有效镇痛且安全的优点,因此可以推广。
