气相色谱法测定注射用盐酸头孢吡肟中异亚丙基丙酮
2023-06-11王婷婷李佩彭洁洪建文
王婷婷?李佩?彭洁?洪建文
摘要:目的 建立注射用盐酸头孢吡肟中基因毒性杂质异亚丙基丙酮的含量测定方法。方法 气相色谱法,采用DB-WAX毛细管柱(30 m×0.53 mm,1.0 μm),程序升温,起始柱温45℃,维持5 min,10℃/min的速率升温至180℃;进样口温度200℃,检测器(FID)温度250℃,氮气流量为5 mL/min;顶空法进样,顶空温度80℃,平衡时间20 min。结果 异亚丙基丙酮与难分离物质二甲基甲酰胺可良好分离;在浓度0.41~8.2 μg/mL范围内,线性良好,回归方程y=0.2457x-0.0066,相关系数r=0.9998;平均回收率为99.1%;检测限0.5 ppm,定量限1.5 ppm。结论 该方法专属性及耐用性良好,准确度及灵敏度高,可用于注射用盐酸头孢吡肟中异亚丙基丙酮杂质的含量测定。
关键词:头孢吡肟;异亚丙基丙酮;基因毒性杂质;含量;GC;异丙叉丙酮
中图分类号:R978.1, R917 文献标志码:A
Abstract Objective To establish a method for the determination of the content of the genotoxic impurity mesityl oxide in cefepime hydrochloride for injection. Methods Gas Chromatography was used, with a DB-WAX capillary column (30 m × 0.53 mm, 1.0 μm) and temperature programmed. The initial column temperature was 45℃, maintained for 5 min, and the temperature rose to 180℃ at the rate of 10℃/min; the inlet temperature was 200℃, the detector (FID) temperature was 250℃, and the flow rate of nitrogen was 5 mL/min. The head space temperature was 80℃ and the equilibrium time was 20 min. Results Mesityl oxid could be well separated from dimethylformamide, which was difficult to separate; The linear range was 0.41~8.2 μg/mL(y=0.2457x-0.0066, r=0.9998). The average recovery rate was 99.1%. The limit of detection was 0.5 ppm and the limit of quantitation was 1.5 ppm. Conclusion The method has good specificity, durability, accuracy, and sensitivity, and can be used for the determination of content of mesityl oxid in cefepime hydrochloride for injection.
Key words Cefepime; Mesityl oxid; Genotoxic impurity; Conetent; GC; Isopropylidene acetone
盐酸头孢吡肟为我国仿制成功的首个第四代头孢菌素,具有广谱高效的抗菌活性和对细菌β-内酰胺酶的高度稳定性,被用于防治多种细菌感染性疾病[1]。注射用盐酸头孢吡肟为盐酸头孢吡肟与一定比例的精氨酸的混粉制剂[2]。丙酮作为盐酸头孢吡肟中合成中的重要溶剂[3],在一定条件下可缩合形成异亚丙基丙酮,又称4-甲基-3戊烯-2酮(图1)[4]。异亚丙基丙酮为不饱和酮结构,含有遗传毒性致癌警示结构[5-6],并对咽喉、眼、皮肤等具有刺激作用[7]。国外药典在西司他丁钠和替考拉宁标准中已对异亚丙基丙酮的含量予以控制[8-9]。
在2020年的国家药品抽检探索性研究工作中,本课题组采用气相色谱-质谱(GC-MS)联用方法,发现国产注射用盐酸头孢吡肟(涉及国内5家原料生产企业)及1批自购参比制剂(百时美施贵宝,Bristol-Myers Squibb)中,普遍含有一定量的异亚丙基丙酮杂质,为该品种的共性风险[10]。本文建立了注射用盐酸头孢吡肟中异亚丙基丙酮杂质的GC定量方法。该方法不仅可为监管部门及生产企业对该品种开展上市后的质量再评价等提供检测手段,同时也为盐酸头孢吡肟原料中相应杂质的监管提供了数据支持。
1 儀器与试药
仪器:Thermo trace 1300气相色谱仪;Agilent 6890气相色谱仪;SHIMADZU GCMS-TQ8050 气相色谱/质谱联用仪;Sartorius CP225D电子天平。
试药:异亚丙基丙酮对照品(GC级,Aladdin,E1927178,含量≥98%);N,N二甲基甲酰胺(分析纯,广州市化学试剂厂,20151101-2);注射用盐酸头孢吡肟样品(来源:2020年国家药品抽检);超纯水。
2 实验方法
2.1 GC-MS方法参数
气相色谱条件:Agilent DB-5MS毛细管柱,30 m×
0.25 mm,1.0 ?m;顶空温度80℃,平衡时间20 min;
起始柱温45℃,维持5 min,以10℃/min的速率升温至180℃,维持5 min。
质谱条件:电子轰击电离(EI);采集方式Q3scan;离子源温度230℃;接口温度250℃;扫描范围:30~500 m/z;扫描速度:5000;溶剂延迟时间1 min。
2.2 GC定量方法参数
采用聚乙二醇为固定液的毛细管柱为色谱柱(DB-wax,30 m×0.53 mm,1.0 μm);起始柱温为45℃,维持5 min,再以10℃/min的速率升温至180℃;载气为N2,流速为5 mL/min;进样口温度为200℃;检测器温度为250℃;顶空平衡温度为80℃,平衡时间为20 min。
2.3 溶液的配制
2.3.1 GC-MS
供试品溶液:取1瓶供试品内容物(约相当于头孢吡肟1.0 g),置顶空瓶中,加水2.5 mL使溶解,密封。
对照品溶液:精密量取异亚丙基丙酮对照品约16 mg,置100 mL量瓶中,加水稀释至刻度,摇匀。精密量取1 mL,置20 mL量瓶中,加水稀释至刻度,精密量取2.5 mL,置顶空瓶中,密封(8 ?g/mL)。
2.3.2 GC
系统适用性溶液:取异亚丙基丙酮约16 mg,置200 mL量瓶中,加水稀释至刻度。取二甲基甲酰胺约70 mg,置100 mL量瓶中,加水稀释至刻度。分别精密量取上述溶液1 mL,置同一20 mL量瓶中,加水稀释至刻度,摇匀,精密量取5 mL置顶空瓶中,密封。
供试品溶液:取本品约0.38 g,精密称定,置顶空瓶中,精密加水5 mL使溶解,密封,摇匀。
对照品溶液:精密称取异亚丙基丙酮约16 mg,置200 mL量瓶中,加水稀释至刻度。精密量取此溶液1 mL,置20 mL量瓶中,加水稀释至刻度,摇匀,精密量取5 mL,置顶空瓶中,密封。
3 试验结果
3.1 GC-MS分析
取“2.3.1”项下待测溶液,照“2.1”项下条件,进样,结果显示,注射用盐酸头孢吡肟供试品溶液TIC图中,保留时间约9.726 min处未知色谱峰m/z为98.10,与异亚丙基丙酮对照品保留时间一致,质谱信息图一致,参考离子峰强度比一致,见图2~3。同时,该组分在岛津已知组分质谱数据库中相似度检索识别结果为异亚丙基丙酮(分子量98,CAS号141-79-7),匹配度97。
3.2 GC分析方法的建立
3.2.1 专属性
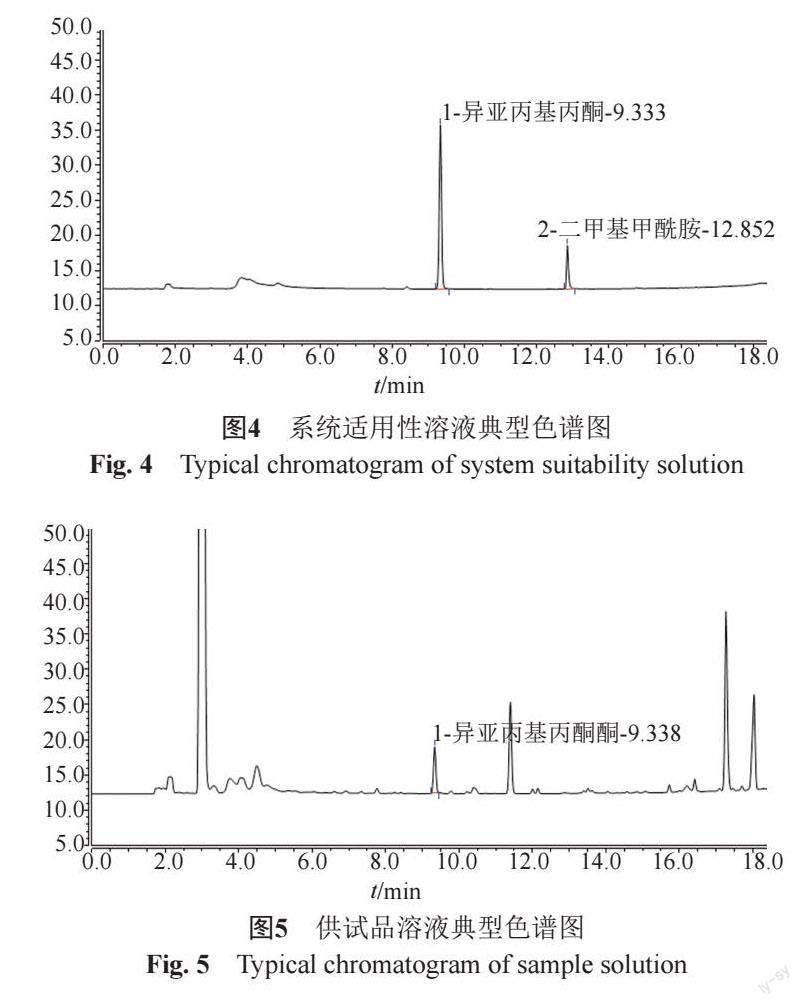
异亚丙基丙酮沸点约为133℃,与二甲基甲酰胺沸点(153℃)较为接近,且国内部分产品中含有微量残留的二甲基甲酰胺,本次研究采用二甲基甲酰胺作为难分离物质,考察方法专属性。取“2.3.2”项下系统适用性溶液、供试品溶液及空白溶液,选择3类不同极性色谱柱,同法测定,结果显示,采用“2.2”項下方法,在聚乙二醇填料的色谱柱中,系统适用性溶液中异亚丙基丙酮与二甲基甲酰胺可实现良好分离;供试品溶液中异亚丙基丙酮与其相邻杂质峰均能有效分离;空白溶剂无干扰;方法专属性良好,见图4~5。
3.2.2 线性
精密称取异亚丙基丙酮对照品适量,制成系列浓度溶液,按照“2.2”项下方法,顶空进样,以浓度(?g/mL)为横坐标,峰面积为纵坐标,绘制标准曲线,结果显示,在0.41~8.2 ?g/mL浓度范围内(约相当于供试品中头孢吡肟0.001%~0.02%浓度水平),线性良好,线性方程y=0.2457x-0.0066,相关系数r=0.9998。
3.2.3 准确度
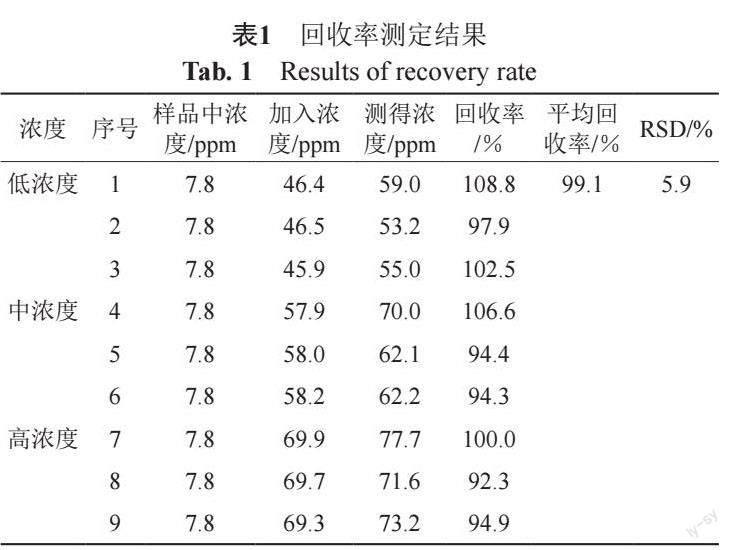
采用加样回收法,取已知浓度的同一批供试品9份,各约0.38 g(约相当于头孢吡肟0.2 g),精密称定,置顶空瓶中,分别加入异亚丙基丙酮对照品溶液(3.2、4和4.8 ?g/mL)5 mL溶解(约相当于供试品头孢吡肟0.008%、0.01%及0.012%浓度水平),配制回收率测定溶液,照“2.2”项下色谱条件测定,结果表明,方法准确度高,见表1。
异亚丙基丙酮在盐酸头孢吡肟中为微量残留,为进一步提高检测方法灵敏度,本次研究尝试提高供试品溶液浓度(2.5 mg/mL),结果显示,由于供试品中含有较高比例精氨酸辅料,其与对照品处于不同基质中,供试品浓度提高后,基质效应明显[11],低浓度水平回收率低于80%,不能满足ChP2020通则9101分析方法验证指导原则中回收率限度要求。采用“2.3.2”项下溶液制备方法,既能达到较高灵敏度,又可显著降低基质干扰,在高中低浓度范围,平均回收率达到99.1%,方法准确度较高,同时较标准加入法操作更为简单快捷。
3.2.4 重复性
选取同批次样品6份,重复测定,异亚丙基丙酮含量测定结果均为0.001%(以头孢吡计),方法重复性良好。
3.2.5 耐用性
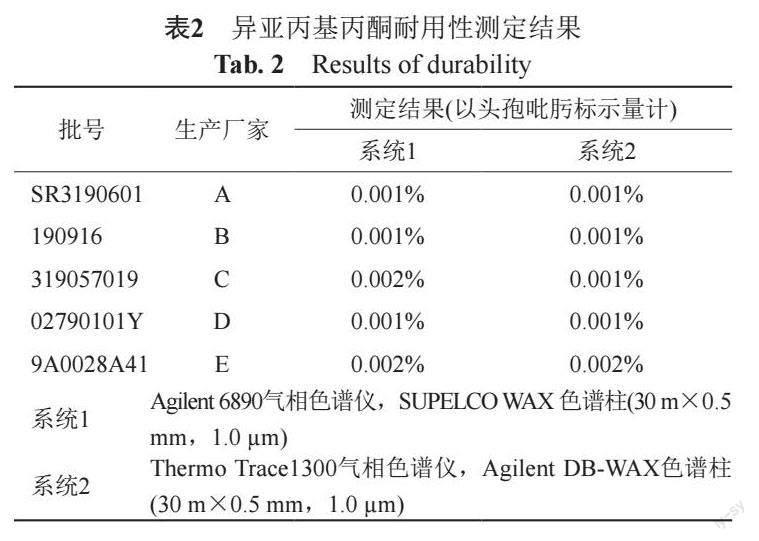
选取5批样品,采用不同色谱柱,不同气相色谱仪,于不同时间测定,结果基本一致,方法耐用性良好,见表2。
3.2.6 检测限与定量限
取异亚丙基丙酮对照品溶液逐级稀释,以3倍信噪比为检测限,10倍信噪比为定量限,该方法最低检测浓度0.02 ?g/mL,检测限0.00005%(以头孢吡肟计,约0.5 ppm),定量浓度0.06 ?g/mL,定量限0.0002%(以头孢吡肟计,约1.5 ppm)。
3.3 样品测定
选取48批次2020年国家药品抽检样品(涉及国内5家原料生产企业)及1批次参比制剂,照“2.2”项下条件测定,以头孢吡肟标示量计,除参比制剂异亚丙基丙酮含量测定结果为0.011%
(110 ppm),其余国产制剂中异亚丙基丙酮含量均在0.001%~0.003%(10~30 ppm)之间。
4 讨论
异亚丙基丙酮的常规合成途径为:在碱性条件下丙酮缩合成二丙酮醇,二丙酮醇在磷酸条件下缩水制得[4]。推测其在头孢吡肟中的可能引入途径为①工业丙酮引入;②丙酮在回收再利用处理过程中缩合产生;③吡肟合成工艺中产生。本次研究结果显示,新鲜工业丙酮中异亚丙基丙酮的含量约为4 ppm,其在生产中被回收利用后,异亚丙基丙酮的含量略微增至约7 ppm,而丙酮在盐酸头孢吡肟中总体残留量不超过0.5%;因而推测盐酸头孢吡肟中的该杂质不可能全部由丙酮引入,而可能在头孢吡肟合成过程中产生。生产工艺研究显示,盐酸头孢中间体合成中同时使用了丙酮和三乙胺等碱性化合物,而盐酸头孢吡肟本身酸性较强(pH值1.6~2.1),且丙酮作为最后一步的结晶溶媒,具备丙酮在碱性条件下缩合产生二丙酮醇,再遇酸性头孢吡肟缩水产生异亚丙基丙酮的可能。
国外药典在替考拉宁和西司他丁钠标准中已将异亚丙基丙酮作为特定杂质控制,其限度值分别为0.2%及0.4%,而注射用替考拉丁及注射用亚胺培南西司他丁钠制剂最大日剂量分别为800 mg及4 g,参考其控制限度及日剂量进行推算,注射用盐酸头孢吡肟中异亚丙基丙酮限度分别约为0.03%(267 ppm)及0.3%(2667 ppm),目前该品种中异亚丙基丙酮引入的质量风险总体可控。
参 考 文 献
雷军, 王浴生. 头孢吡肟[J]. 国外医药抗生素分册, 1996, (5): 354-358.
国家药典委员会. 《中国药典》(2015年版二部)[S]. 中国医药科技出版社, 2015: 916-917.
彭东明, 王晓红, 刘艳飞, 等. 盐酸头孢吡肟的合成[J]. 中南大学学报(自然科学版), 2015, 46(7): 2405-2411.
戚蘊石. 丙酮化学的发展现状[J]. 石油化工, 1986, (7): 439-445.
马磊, 马玉楠, 陈震, 等. 遗传毒性杂质的警示结构[J]. 中国新药杂志, 2014, 23(18): 2106-2111.
胡红梅, 胡彬彬, 李芳, 等. 气相色谱法同时测定工作场所中异亚丙基丙酮和苯系物[J]. 中国卫生检验杂志, 2012, 22(9): 2063-2065.
IPCS, International Chemical Safety Card on Mesityl oxide[DB/OL].(2006-11-01)[2022-10-27]https://www.inchem.org/documents/icsc/icsc/eics0814.htm.
The United States Pharmacopeial Convention. The United States Pharmacopeia[S/OL].(2018-5-2)[2022-10-27].https://online.uspnf.com.
EDQM.The European Pharmacopoeia[S/OL].(2022-4)[2022-10-27]https://pheur.edqm.eu.
王婷婷, 肖慧, 李佩, 等. 国产注射用盐酸头孢吡肟质量评价[J]. 中国抗生素杂志, 2022, 47(2): 128-133.
陈丹丹, 张涛, 任丽萍. 基质效应在气相色谱法测定农药残留中的影响[C]. 农药与环境安全国际会议论文集, 2005: 257-265.
