硫酸(55%)的H2S硫化降砷研究
2023-06-11刘海弟马小乐李伟曼陈运法罗永春
刘海弟, 蔡 兵,马小乐,李伟曼,陈运法*,罗永春
(1.中国科学院过程工程研究所 多相复杂系统国家重点实验室, 北京 100190;2.昆明理工大学 环境科学与工程学院, 云南 昆明 650500;3.云南锡业股份有限公司 铜业分公司, 云南 蒙自 661000;4.浙江华友钴业股份有限公司, 浙江 嘉兴 314500)
随着我国有色冶炼产能的不断扩大和有色矿产资源的日益紧张,有色冶炼行业不得不面对砷含量越来越高的矿石原料。因此,能否应对高砷原料成为决定有色冶炼企业长久发展和未来竞争力的重要因素,其中以铜冶炼行业最为典型。
铜熔炼过程中大量砷元素以气态白砷的形式进入高温烟气中。常见的工业操作先使用余热锅炉将烟气降温至350~400 ℃,然后通过电除尘去除大部分颗粒物,再进行湿式洗涤降温和电除雾处理,最终将烟气中的As、F和Cl的浓度降低至工艺许可的范围,然后烟气送往后续工段进行制酸,而烟气中的As2O3、HF和HCl大都通过洗涤进入污酸当中。对于污酸的处理已经有大量有色冶炼行业的技术人员进行了深入研究和充分优化,目前最常见的方法是通过硫化、石膏中和、石灰铁盐的三个步骤来完成治理,然而该过程大量产生的硫化渣、石膏渣和中和渣使有色冶炼企业面临巨大的环保压力和固(危)废治理成本。因此,如果能在确保烟气中白砷去除的前提下避免污酸的产生,将极大降低烟气治理工艺的固废产生量。云锡铜业和中国恩菲就该技术方案进行了深入思考和长期探索,提出了浓酸沉砷的烟气处理新工艺:该工艺中首先使用高温深度除尘技术捕集高温烟气(350~400 ℃)中的颗粒物,去除其中绝大部分碱(土)金属元素和过渡金属元素,再使用55%的硫酸对烟气进行降温、洗涤和脱砷,该浓度的硫酸中白砷的溶解度仅有5 g/L左右,烟气中的白砷被捕集后将自发沉淀出来,可以过滤去除,避免了原来硫化沉砷过程中大量的硫化剂消耗,硫酸从烟气中吸收的HF和HCl通过加热吹脱去除,最终通过少量H2S对硫酸中残余的白砷(以亚砷酸形态存在)进行沉淀脱砷,使净化后的硫酸可用于后序制酸系统的配酸而实现资源化,这样从根本上避免了石膏中和工艺产生大量石膏渣的问题,同时也避免了污酸的产生。
然而,55%的硫酸中残余的亚砷酸能否使用H2S来沉淀降砷是决定上述工艺能否成功的关键,众所周知:55%的硫酸中硫酸物质的量浓度高达8.12 mol/L,H2S的解离反应将被大大抑制,因此如此高浓度的硫酸中H2S和亚砷酸的反应机理需要从理论和实验两个角度加以研究和探讨。本研究从文献数据挖掘的角度分析了55%的硫酸中亚砷酸和H2S的反应可能性,同时通过实验方法研究了55%的硫酸中亚砷酸和H2S的反应可行性,研究发现两者可进行沉淀反应,反应产物为无定型的砷硫化合物沉淀,经硫化降砷后的硫酸的砷浓度降低至0.81ppm,这比理论计算得到的结果低近两个数量级,其原因可能在于部分As(III)被大大过量的H2S还原为 As(II),这使砷和硫之间的沉淀反应被显著促进。
1 实验验材料与方法
1.1 实验材料和实验方法
分析纯硫酸(H2SO498%)和硫化钠(Na2S·9H2O)购自北京化学试剂公司,含白砷(As2O3)的硫酸样品来自企业现场,硫酸浓度50 g/L(4.8wt%),含砷量≈2.5 g/L(2 481.43ppm),命名为现场酸样。通过向现场酸样中缓慢加入98%浓硫酸的方法配制硫酸浓度为55%的含砷硫酸,命名为硫化前酸样,取100 mL硫化前酸样进行H2S硫化,实验装置如图1所示。H2S气体来自Na2S和硫酸(30%)的反应,所生成的H2S气体通过砂芯鼓泡的方式与硫化前酸样相接触,同时使用磁力搅拌器对体系进行剧烈搅拌,反应温度为室温25 ℃,实验尾气经过CuSO4溶液和NaOH吸收净化后排放,硫化反应持续30 min至体系颜色不再变化后通过10 000 r/min高速离心将生成的亮黄色沉淀和硫酸分离,所分离出的硫酸命名为硫化后酸样,通过电感耦合等离子体(ICP)的方法检测现场酸样和硫化后酸样中的Na、Ca、Cu、Pb、Zn、As离子含量(数据见下文),而亮黄色沉淀经洗涤后通过X射线衍射的方法(XRD)研究其晶型,扫描电子显微(SEM)来分析其颗粒形貌,通过能谱扫描(EDX)确定其元素组成,通过透射电子显微镜(TEM)分析颗粒形貌的同时采用电子衍射的方法分析颗粒的结晶形态,采用X射线光电子能谱(XPS)研究As和S元素的价态和结合方式。实验中使用的去离子水为电阻18 MΩ的二次去离子水。
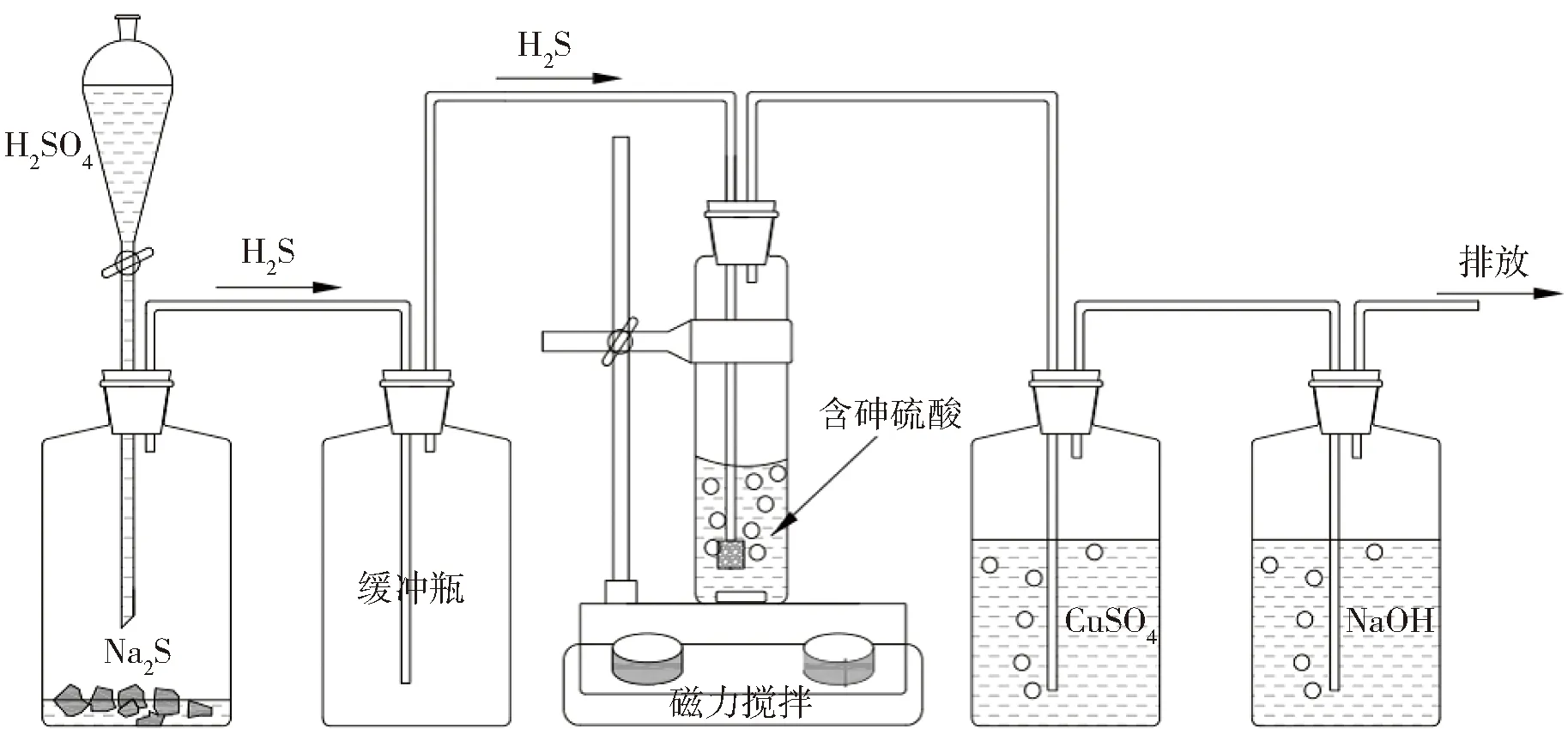
图1 硫化实验装置
1.2 测试方法
采用Philips PANanalytical X’ Pert Pro型X射线衍射分析仪(XRD,荷兰Philip公司)分析硫化所产生黄色沉淀的晶型(测试条件:CuKα,Ni滤波,管电压为40 kV,电流为30 mA,λ=0.154 18 nm,2θ范围5°~90°,步长0.02°),采用电感耦合等离子体方法(ICP,型号Vista-MPX,美国Varin公司)分析样品中的过渡金属离子含量。采用SU8020型扫描电子显微镜(日本HITACHI公司)在15 kV条件下分析硫化后沉淀的颗粒形貌,并在20 kV加速电压下进行EDX能谱扫描,使用JEM-2100F型高分辨场发射透射电子显微镜(日本电子JOEL公司)对样品的颗粒形貌和高分辨晶格条纹进行分析,采用X射线光电子能谱方法(XPS,型号Thermo Fisher ESCALAB XI+,美国Thermo Fisher Scientific公司)对样品的元素价态和结合方式进行分析。
2 实验结果与讨论
2.1 采用H2S硫化硫酸(55wt%)可行性的理论分析
经研究相关文献可知,溶解于硫酸当中的砷元素主要以砷酸和亚砷酸的形式存在,硫酸中白砷沉淀析出的过程其实是在硫酸的脱水作用下亚砷酸分子脱水聚合而生成白砷的过程,而H2S与该体系发生反应的过程其实就是H2S与其中亚砷酸分子的反应过程。
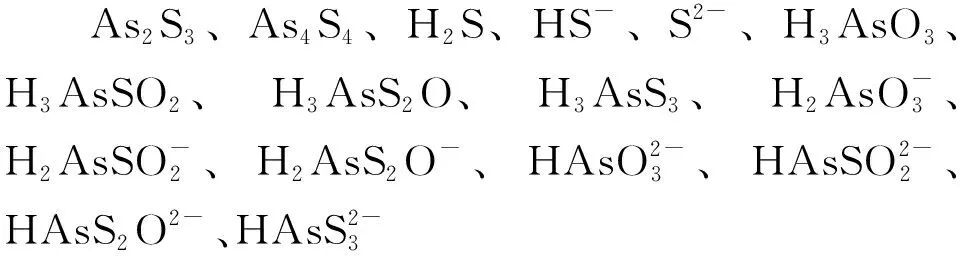
蒋国民[3]通过研究H2S对污酸梯级硫化的过程提出了污酸中总硫浓度[S]T、pH和总砷浓度[As]T的理论计算关系式,该计算公式在推导过程中巧妙的纳入了H2S和亚砷酸的两级解离常数、回避了两者产生的多种离子形态难以逐一计算的困难,所获得的计算公式如下[3]:
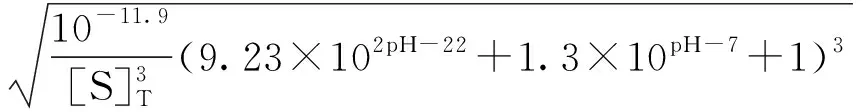
将酸溶液中As物种和S物种均看为来自As2S3的解离,因此总砷物种[As]T和总硫物种[S]T存在2∶3的定量关系,即3[As]T=2[S]T,故上式可以求解,对于55wt%的硫酸,查询硫酸基础物性[4]可知其物质的量浓度为8.11 mol/L,密度为1.445 g/mL,其氢离子浓度为8.12 mol/L,其pH为-0.91,代入上式可得其中[As]T为0.003 27 mol/L,换算为质量含量为75×0.003 27/1 445=169.7×10-6=169.7 ppm。
2.2 采用H2S硫化含砷硫酸的实验结果
2.2.1 H2S硫化前后硫酸的外观比较
未经硫化的55%含砷硫酸为澄清透明的酸液,当H2S气体通入时,酸液立刻变浑浊,并逐渐产生黄色沉淀,当实验结束时,有大量黄色固体因为气体鼓泡的作用而飘浮在酸液上部,如图2所示,虽然较纯的As2S3为柠檬黄色,但由于实验中使用的酸样由现场炼铜烟气经稀酸洗涤而得,其中溶有一定量的SO2,所以在H2S硫化过程中很可能发生S4+和S2-的归中反应而产生黄色的单质硫,因此体系中产生大量黄色沉淀的实验现象并不能简单推断为 As2S3的形成。

图2 硫化实验前后含砷硫酸的照片
2.2.2 H2S硫化前后含砷硫酸的离子浓度对比
H2S硫化前后的硫酸中Na、Ca、As、Cu、Pb、Zn的离子浓度分别如表1所示。
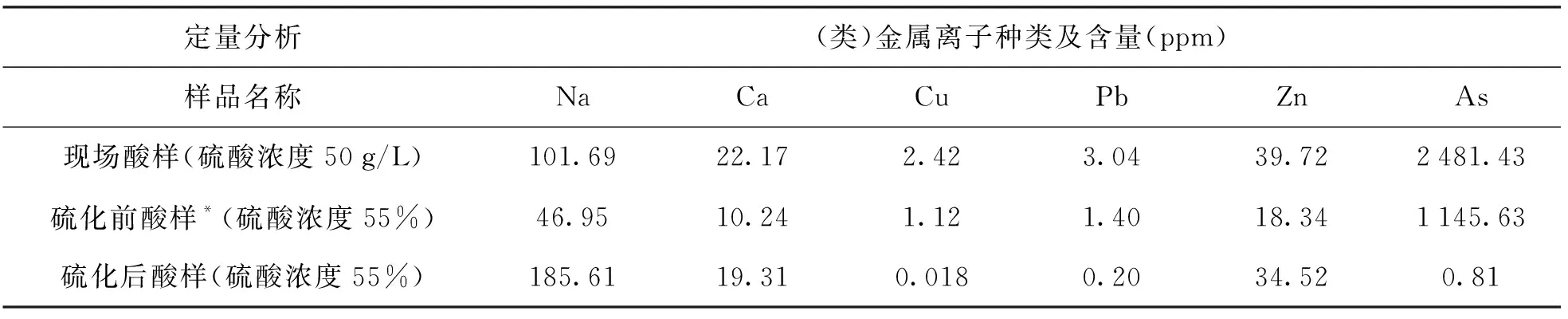
表1 硫化前后含砷硫酸中的(类)金属离子浓度表
由表1可知现场酸样中As离子浓度为 2 481.43 ppm,同时Na、Ca离子浓度也较高,这很可能来自烟气中含有Na+、Ca2+的粉尘和工艺水引入的盐分。就三种过渡金属Cu、Pb、Zn而言,现场酸样中Zn2+浓度最高(39.72 ppm),这可能与现场操作工况有关,另一个原因是Zn2+挥发性较强,易于随烟气排出。经过H2S硫化之后的酸样中As、Cu、Pb几种离子浓度发生了明显降低,As离子浓度从 1 145.63 ppm 降低至0.81 ppm,下降了99.93%,Cu2+和Pb2+浓度分别从1.12 ppm和1.40 ppm降低至0.018 ppm和0.20 ppm,可见即使在55%的硫酸浓度下,H2S硫化依然可以有效降低As、Cu的离子浓度,而Pb离子浓度的下降则很可能因为发生了硫酸铅的沉淀反应,同时可知,硫化后样品中Na、Ca、Zn的离子浓度反而有所上升,其原因可能是Na+和Ca2+无法通过形成不溶性硫化物的方法而被硫化脱除;此外实验中使用多孔砂芯对H2S气体进行鼓泡分散,浸泡在55%硫酸样品中的砂芯很可能会释放Na、Ca和Zn离子,这使硫化后酸样中Na、Ca、Zn离子浓度反而上升。根据文献可知:Zn2+和H2S的反应存在非常复杂的机理[5],高酸度下Zn2+是无法通过H2S硫化的方法加以沉降的[6]。
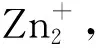
2.2.3 硫化实验所产生黄色沉淀的SEM/EDX分析
对硫化过程产生的黄色沉淀进行SEM分析所得的照片如图3所示,可知该沉淀物为粒径50 nm左右的微细颗粒,形状为类球状,其粒径微细,离心和过滤都具有一定难度。为了分析该固体颗粒的成分,对其进行了EDX能谱扫描,扫描区域照片如图4a所示,而针对As、S、O三个元素的扫描照片分别如图4b、图4c、图4d所示。

图3 硫化反应产生黄色沉淀的SEM照片

图4 硫化反应产生黄色沉淀的SEM-EDX能谱分析结果
由上述结果可知,As和S元素完全均匀分布于所有颗粒各个部分,而氧元素分布则非常稀疏,因此可以断定样品中As2O3的含量很低,从能谱扫描所得的As、S元素质量比为1.85∶1,略高于纯As2S3的1.56∶1的元素质量比,这有两个可能:(1)黄色沉淀中含有少量As4S4;(2)样品中含有少量As2O3。由于样品被贴在导电胶上进行测试,因此导电胶中的氧元素对能谱分析结果有巨大干扰,同时由于EDX分析得到的元素比例随机性很大,因此尚不能定论样品中As和S两种元素的化学结合方式和存在状态,只能断定样品为以As和S为主要成分的某种化合物。
2.2.4 硫化实验所产生黄色沉淀的TEM分析
采用TEM方法分析了硫化产生的黄色沉淀的形貌(如图5所示),与SEM分析结果类似,沉淀为类球形颗粒无规粘结堆积而成的网状结构,粒度仅20~50 nm左右,颗粒经高倍数放大后观察不到任何晶格条纹,视野下颗粒均为无定型的晶体结构,由于TEM分析的颗粒数量有限,因此有必要对样品进行XRD分析以进一步研究其结晶形态。

图5 硫化反应产生黄色沉淀的TEM分析结果
2.2.5 硫化实验所产生黄色沉淀的XRD分析
采用XRD方法分析硫化实验产生黄色沉淀的结果如图6所示,可知样品晶型确实为无定型,没有任何显著的衍射峰存在,仅在15~20°、25~35°、50~60°存在峰包,这分别和As2S3(Orpiment)、As4S4(Realgar)、S单质(Brimstone)的特征峰比较接近,可以粗略推断样品很可能含有无定型的As2S3、As4S4甚至单质S。但样品中As和S的化合方式、价态仍无法定论,需要进行进一步的研究。
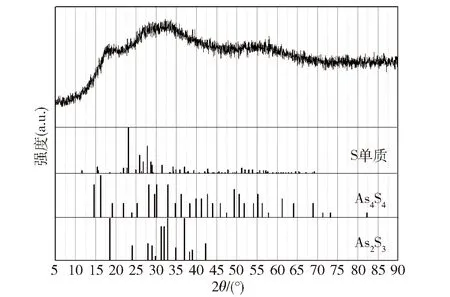
图6 硫化反应产生黄色沉淀的XRD分析结果
2.2.6 硫化实验所产生黄色沉淀的XPS分析
硫化实验产生的黄色沉淀经XPS分析后的As 3d5/2谱图如图7所示,样品As 3d5/2的峰位在43.2 eV,根据文献[7]报道的结合能数据:As2S3中As元素的结合能处在43.5 eV、As4S4中As元素的结合能在43.1 eV,因此可以推断:样品中同时存在分别以 As2S3和As4S4两种形态与S相结合的As元素。同时可以看到:样品As 3d5/2的结合能谱图在44.5 eV位置处略有隆起,这很可能是样品存在少量与氧结合的As(III),这说明黄色沉淀中存在少量无定型As2O3[7],这很可能来自硫化前酸样中溶解的亚砷酸,这部分亚砷酸在加入浓硫酸调节酸度为55%的过程中发生了缩合沉淀,以无定型白砷的形态存在于体系中,经H2S硫化后与新生成的无定型As2S3和As4S4一起形成了黄色沉淀。As 3d5/2的XPS分析结果说明样品中确实存在As4S4物种,说明体系中发生了As(III)到As(II)的还原反应,由于XPS谱图分峰存在一定不确定性,没有通过以上结果推测As(III)和As(II)的化学态定量分析。
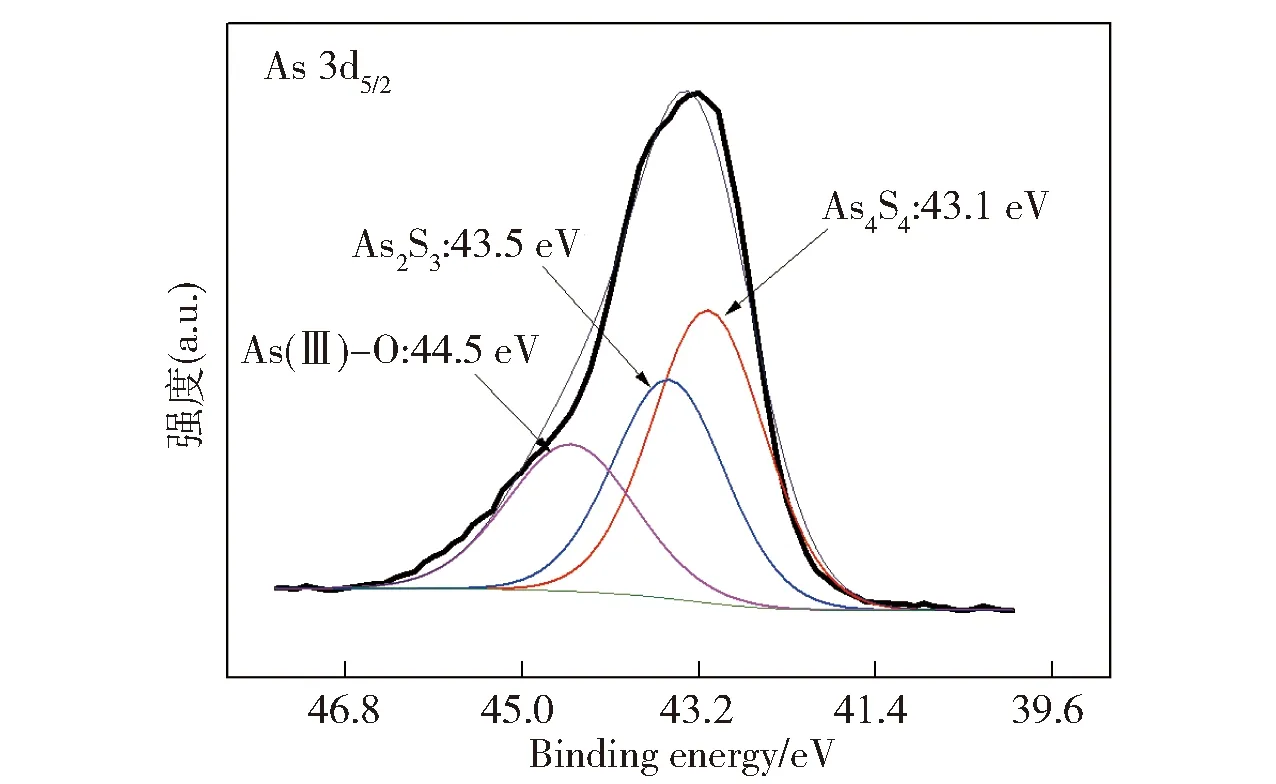
图7 硫化反应产生黄色沉淀的As 3d5/2XPS谱图
硫化实验产生的黄色沉淀经XPS分析后的S 2p1/2-3/2谱图如图8所示,其谱图中S的结合方式可以归属为As2S3和As4S4两种方式[8-9],两种方式中2p1/2和2p3/2的结合能间距均为1.18 eV、2p1/2和2p3/2的峰面积为1∶2。从分析结果可知,存在以 As4S4方式结合的S元素,这再次证明很可能有部分As(III)发生了还原而产生As(II)。
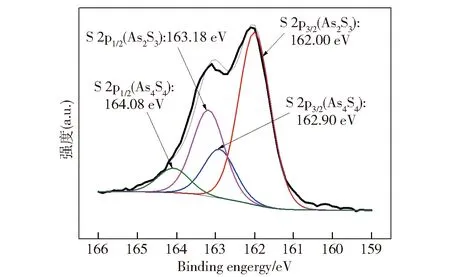
图8 硫化反应产生黄色沉淀的S 2p1/2-3/2 XPS谱图
3 结语
从理论分析和实验验证两个角度研究了55%硫酸中亚砷酸与H2S硫化沉淀的过程,根据文献提出的理论公式计算,两者之间的硫化反应可以将砷浓度降低至170 ppm左右,然而从实验角度得到的结果表明:55%的硫酸浓度下H2S硫化降砷后体系的砷浓度可降低至0.81 ppm,两者相差近两个数量级,采用SEM、TEM、XRD和XPS等方法分析了硫化后产生的黄色沉淀的颗粒形貌、晶型和元素价态,发现沉淀为As和S的无定型化合物,其中As的价态有+2价和+3价,推断样品为无定型As2S3、As4S4的混合物。之所以文献中理论计算所得到的硫化后砷浓度远高于实验中测得的硫化后砷浓度,其原因很可能在于该理论计算没有考虑As(Ⅲ)与过量H2S沉淀的同时发生还原生成As(Ⅱ)的情况,而As4S4的稳定性很可能远高于As2S3,这显著促进了体系中的As元素的沉淀脱除。研究发现:H2S硫化降砷可以成功去除55%硫酸中的As、Cu等元素,但对于Na、Ca、Zn等元素则无能为力,因此为了55%硫酸可以配酸回用,必须事先高效去除烟气中含Na、Ca、Zn等元素的粉尘,所以对烟气进行高温深度除尘操作是必不可少的。经过H2S硫化后的55%硫酸可以在干吸工序中代替工艺补水而进入成品酸中,按照烟气中SO2与SO3之间19∶1的比例计算(常见工况下SO2/SO3比例高于该值),生成1吨55%的含砷硫酸(源自SO3)后,制酸工序将把6.824吨SO2合成为硫酸产品,两者将合并为11.89吨92.5%的硫酸,该55%含砷硫酸导致产品硫酸的As浓度提高仅为0.068 ppm。按照净化后烟气SO2浓度10%、As2O3含量2 mg/m3计算,制酸所得92.5%硫酸的As含量为3.2 ppm,因此55%含砷硫酸回用导致的成品酸砷含量增加完全可以忽略不计,浓酸沉砷工艺有望避免污酸的大量产生并显著提高有色金属火法冶炼工艺的环境友好性。
