抗富亮氨酸胶质瘤失活1蛋白抗体相关脑炎的临床特点分析
2023-06-11朱朝阳韩静瑜王赵伟谢建平
朱朝阳 韩静瑜 王赵伟 谢建平*
自身免疫性脑炎(Autoimmune encephalitis,AE)泛指一大类由自身免疫反应介导的脑炎[1]。抗富亮氨酸胶质瘤失活1 蛋白(leucine-rich glioma-inactivated protein 1,LGI1)抗体脑炎是自身免疫性脑炎的主要类型之一,抗LGI1 抗体脑炎的早期精准诊断与积极的免疫调控治疗能获得相对较好的临床预后。本文回顾性分析5 例抗LGI1 抗体相关脑炎的临床特点,为该病的诊断和治疗提供参考。
1 临床资料
1.1 一般资料 2018 年6 月至2021 年6 月本院拟诊为自身免疫性脑炎81 例,其中5 例符合2017 年《中国自身免疫学脑炎诊治专家共识》中抗LGI1 抗体脑炎的诊断标准。5 例患者,男女比为2 ∶3,发病年龄29~74 岁,中位年龄43 岁,3例急性起病,2 例亚急性起病。所有患者均出现记忆力减退,其中2 例有前驱感冒发热病史;3 例癫痫发作,2 例面-臂肌张力障碍,1 例精神行为异常,见表1。5 例患者仅1 例脑脊液常规检查异常,表现为低颅内压:60 mmH2O;2 例血清和脑脊液LGI1 抗体均阳性,2 例单独血清抗体阳性,1 例单独脑脊液抗体阳性;2 例低钠血症,其中病例2 抗甲状腺过氧化物酶抗体及抗甲状腺球蛋白抗体异常,病例3 小细胞低色素贫血;病例4 抗核抗体、抗SS-A 抗体及抗SS-B 抗体阳性;所有患者肿瘤标志物均未发现异常,见表2。2 例脑电图检查可见局灶性慢波;5 例患者头颅MRI 均异常,病灶主要累及颞叶内侧及海马。所有患者胸部CT 检查均未发现异常。4 例患者治疗后复查头颅MRI 异常信号均有不同程度改善,病例2 出院后因病情缓解未复查。

表1 5例抗LGI1抗体脑炎患者临床特点
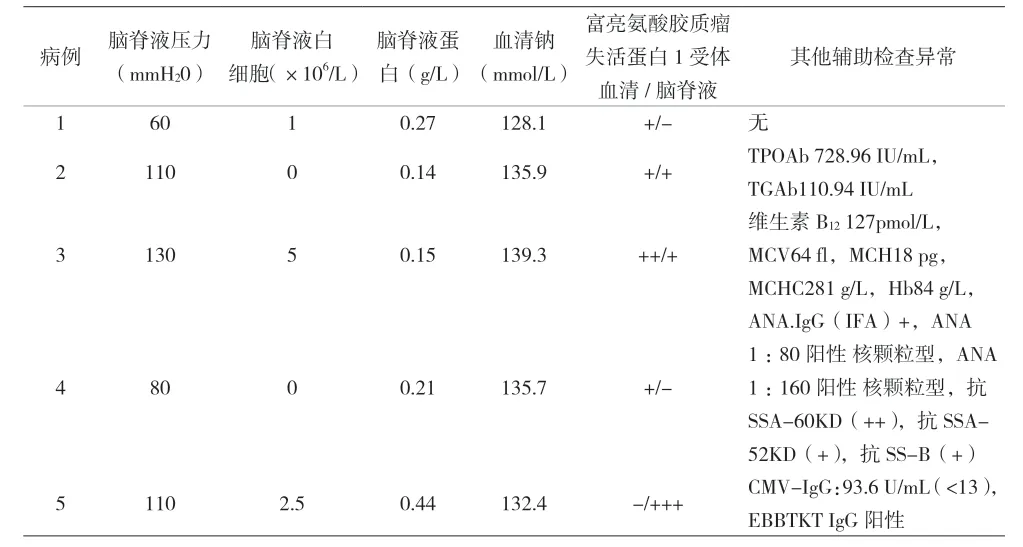
表2 5例富亮氨酸胶质瘤失活蛋白1受体脑炎患者实验室检查
1.2 治疗及转归 治疗包括免疫治疗和对症支持治疗。所有患者均接受免疫治疗,予500~1,000 mg 甲泼尼龙琥珀酸钠冲击3~5 d,每3 d 递减,病情好转后出院继续口服治疗4~11 个月,视病情变化调整剂量直至停药。其他症状癫痫、低钠血症、精神行为异常、认知功能障碍、干燥综合征、贫血予对症支持治疗,采用奥卡西平、丙戊酸钠、左乙拉西坦、吡拉西坦等抗癫痫;低钠血症为避免出现脑桥髓鞘溶解予口服补钠为主;病例4 予喹硫平、利培酮改善精神症状;经治疗后所有患者改良Rankin 评分(mRS)下降。出院后随访8~32个月,1 例遗留记忆力减退,1 例出现睡眠障碍、味觉异常,无死亡病例,见表3。
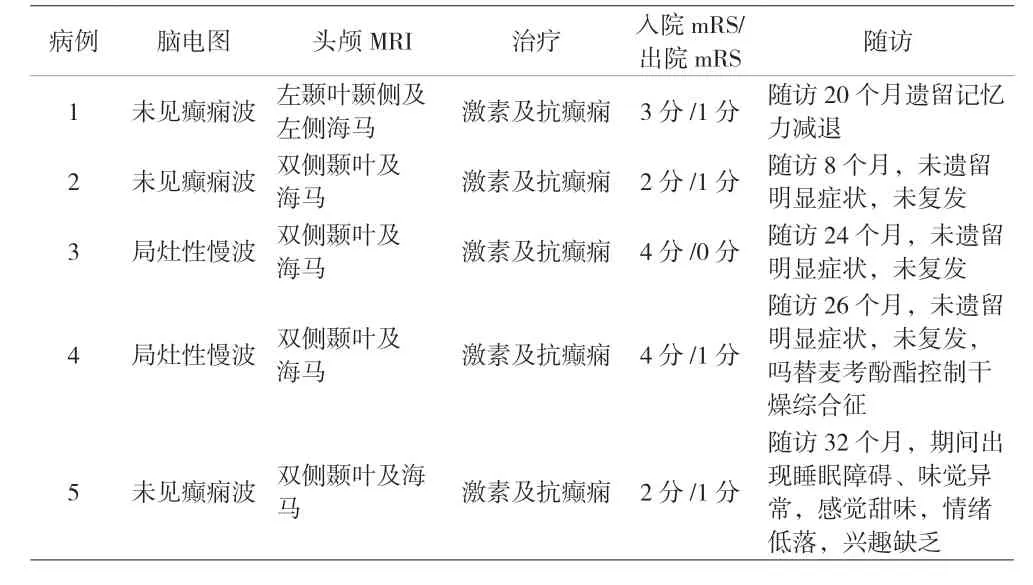
表3 5例富亮氨酸胶质瘤失活蛋白1受体脑炎患者辅助检查、治疗及转归
2 讨论
抗LGI1 抗体脑炎于2010 年首次发现,发病率为每年0.83/100 万[2],仅次于抗N-甲基-D 天冬氨酸受体(N-methyl-D-aspartate receptor,NMDAR)脑炎。抗LGI1 抗体脑炎好发于>60 岁人群,男女比例约为2 ∶1。本组仅1 例年龄>60岁,且女性患者多于男性,可能与近几年临床医师对该疾病认识增加以及本研究样本量偏小有关。抗LGI1 抗体脑炎临床特点包括认知功能障碍、癫痫发作和精神行为异常等边缘系统症状,较少伴发肿瘤[1]。本组5 例患者症状结果与文献基本相符。
约80%~90%患者病程中出现癫痫发作[2-3],癫痫发作主要包括FBDS、局灶性发作及全面强直阵挛发作。FBDS 是该病的特征性表现之一,发生在34%~47%的患者中[3-4],表现为短暂的(<3 s)、频繁的(10~100 次)上肢肌张力障碍发作,通常伴有同侧面部收缩和下肢收缩,常在认知功能下降前几周出现。因此FBDS 可以作为临床诊断抗LGI1 抗体脑炎的早期提示指标。关于FBDS 是癫痫发作还是肌张力障碍发作,目前仍有争议。CHEN 等[5]通过观察18 例抗LGI1 抗体脑炎患者后发现大多数在发生FBDS 后出现癫痫发作,推测其本质上是癫痫发作。本研究3 例患者伴有癫痫发作,其中病例3 和病例5 还伴有FBDS,早期仅用抗癫痫治疗后效果欠佳,在免疫治疗后继续抗癫痫治疗FBDS 症状改善明显。
认知功能障碍是该病的另一典型症状,约42%的患者以首发症状出现,97%患者可出现记忆力减退[3]。研究认为LGI1抗体脑炎患者认知功能障碍碍可能与海马CA2/3和CA4/DG 区域萎缩损害相关[6],早期免疫治疗可避免其症状加重。虽然大多数抗LGI1 脑炎患者对免疫治疗敏感,部分患者仍会遗留记忆功能障碍,且接受免疫治疗较晚的患者记忆障碍明显更差。本组5 例患者均有不同程度的记忆力下降,免疫治疗后预后均良好。因此,对于怀疑抗LGI1 抗体脑炎的患者,应尽早识别并给予相应的免疫治疗。顽固性低钠血症也是该病的常见临床表现之一,具体机制尚不清楚。一般认为是由于抗LGI 抗体表达于下丘脑和肾小管,引起抗利尿激素过度释放,进而导致低钠血症。本组2 例低钠血症,在免疫治疗后,随着病情改善,低钠血症也逐渐被纠正。此外,病例1腰椎穿刺的脑脊液压力仅为60 mmH2O,考虑与患者老龄,进食较少有关。
除了上述症状,病例4 出现口唇、眼部、皮肤干燥及唾液减少等表现,且抗核抗体、抗SSA 及抗SSB 抗体均阳性,提示结缔组织疾病。但由于患者治疗期间出现被害妄想,相应病理检查及化验较为困难,无法明确是否合并干燥综合征。研究发现,抗LGI1 脑炎患者比抗NMDAR 脑炎患者更易出现自身免疫性合并症。人类白细胞抗原(human leukocyte antigen,HLA)II 型等位基因已被证实与抗LGI1 抗体脑炎高度相关[4],其中DRB1*03 ∶01 或DQB1*02 ∶01 等位基因和扩展的DRB1*03 ∶01-DQB1*02 ∶01 单倍型是抗LGI1 脑炎的强易感性位点[7]。可以推测DRB1*03 ∶01 和DQB1*02 ∶01 可能是抗LGI1 抗体脑炎与干燥综合征共同含有的遗传性危险因素。在抗LGI1 抗体脑炎患者中,可能是由于易感基因造成自身免疫性疾病并发,然而两种疾病的关系有待进一步研究。
影像学检查对诊断抗LGI1 抗体脑炎十分关键,头颅MRI典型的异常表现是T2 Flair 序列上出现单侧或双侧颞叶内侧(杏仁体与海马)信号增高[2]。疾病初期,MRI 影像可为正常,随着病情进展可逐渐出现异常信号。既往报道在随访过程中,患者常出现海马萎缩,而认知功能缺陷往往伴随着明显的海马萎缩[8]。本研究病例1 随访中遗留记忆力减退,出院22 个月再次行头颅MRI 发现双侧海马萎缩,考虑与疾病本身和患者老龄相关。
关于抗LGI1 抗体脑炎的治疗,大多数仍是回顾性或者观察性研究。该病治疗主要为免疫治疗和抗癫痫治疗。一线免疫治疗主要为大剂量糖皮质激素冲击,基于疾病的严重程度联合应用丙种球蛋白或血浆置换。相关研究表明,双重血浆置换治疗抗NMDAR 抗体脑炎安全有效[9],但是对于抗LGI1抗体脑炎患者,其疗效仍需大样本随机对照研究证实。二线免疫治疗包括利妥昔单抗、吗替麦考酚酯、环磷酰胺、硫唑嘌呤等免疫抑制剂,一般用于一线免疫治疗效果不佳的患者。抗癫痫治疗主要为了在免疫治疗生效之前发挥抗癫痫作用。既往研究[10]认为单纯应用抗癫痫药物效果并不理想,但免疫治疗有利控制癫痫,尤其是早期接受免疫治疗的患者。对于患者是否有必要长期应用抗癫痫治疗,仍需更多的前瞻性研究。
综上所述,抗LGI1 抗体脑炎是一种可治疗且预后相对较好的自身免疫性疾病,临床较为罕见。当遇到出现认知功能障碍、癫痫发作、精神行为异常、FBDS 和低钠血症的患者,且头颅MRI T2 Flair 像出现单侧或双侧颞叶内侧信号增高,尽早完善抗体检测和应用免疫治疗。此外,当患者合可疑风湿性或免疫系统疾病症状时,建议尽早完善相关检查明确疾病,并给予相应治疗。
