三白草地上部分化学成分研究
2023-06-08陈建伟李金枝蔡红蝶罗益远陈宏降
葛 雯,陈建伟,李 祥,李金枝,蔡红蝶,陶 倩,罗益远,陈宏降*
1. 浙江药科职业大学,浙江 宁波 315500
2. 南京中医药大学药学院,江苏 南京 210046
三白草是三白草科植物三白草Saururus chinensis(Lour.) Baill.的干燥地上部分,具有利尿消肿、清热解毒的功效,临床主要用于治疗尿路感染、尿结石、肾炎水肿、白带过多、支气管炎等症,外敷治疗痈疮肿毒和皮肤湿疹等。三白草植物资源十分丰富,我国南方各地均有分布,同时在韩国、日本等也作为民间常用药物,用于治疗水肿、黄疸、淋病等[1]。研究表明其主要含有木脂素、黄酮、生物碱、萜类等多种化学成分,其中木脂素类为三白草的主要活性成分,迄今已从三白草中分离鉴定出100 多个木脂素类化合物,具有抗炎、保肝、抗病毒、抗肿瘤等多种药理活性[3-7]。为进一步丰富三白草的化学成分研究资料,本课题组在前期对三白草化学成分研究基础上[8-9],对三白草地上部分的化学成分进一步研究,从三白草地上部分的超临界CO2萃取物中分离得到15 个化合物,分别鉴定为2,3-二甲基-1,4-二(3,4,5-三甲氧基苯基)-1,4-丁二酮[2,3-dimethyl-1,4-bis(3,4,5-trimethoxyphenyl)butane-1,4-dione,1]、asperphenamate(2)、rel-(7S,8S,7′R,8′R)-3,3′,4,4′,5,5′- 六 甲 氧 基-7-O-7′,8.8′- 木 脂 素[rel-(7S,8S,7′R,8′R)-3,3′,4,4′,5,5′-hexamethoxy-7-O-7′,8.8′-lignan,3]、常春藤皂苷元(hederagenin,4)、schisandlignans C(5)、樟叶素(polysyphorin,6)、4-羟基-5-甲基己烷-5-内酯(4-hydroxy-5-methylhexan-5-olide,7)、异黑麦草内酯(isololiolide,8)、perseal B(9)、myrisfragransin(10)、heteroplexisolide E(11)、curcasinlignan C(12)、去氢催吐萝芙木醇(dehydrovomifoliol,13)、黑麦草内酯(loliolide,14)和三白草二萜E(sauruditerpene E,15)。化合物除3、6、13 外均为首次从该植物中分离得到,其中化合物15 为1 个新化合物,化合物为新的天然产物。
1 仪器与材料
Bruker AV-400 和Bruker AV-300 型核磁共振仪(TMS 为内标,瑞士布鲁克公司);Autopol IV 型自动旋光仪(美国Rudolph 公司);UV-2550 型紫外/可见分光光度计(日本岛津公司);FTIR-84005 型红外光谱仪(日本岛津公司);美国Waters UPLC AcquityTM系统、Xevo G2-XS Q TOF 质谱仪(美国Waters 公司);LC-20AP 制备型高效液相色谱仪(日本岛津公司);Dr Flash S 型快速中压制备系统(苏州利穗科技有限公司);HA220-40-11 型超临界CO2萃取仪(江苏南通华安超临界萃取有限公司);CO2气体(南京天泽气体有限责任公司);反相C18硅胶(60~80 μm,德国Merck 公司);MCI GEL CHP-20P(75~150 μm,三菱化学株式会社);薄层色谱和柱色谱硅胶(青岛海洋化工有限公司);制备液相用甲醇(色谱纯,江苏汉邦科技有限公司);其它试剂均为国产分析纯。
三白草药材(产地湖北,批号20140822)购自亳州药材公司,经南京中医药大学陈建伟教授鉴定为三白草科植物三白草S.chinensis(Lour.) Baill.的干燥地上部分,标本(ZH2014003)存放于南京中医药大学药学院中药化学实验室。
2 提取与分离
三白草地上部分粗粉8 kg,超临界CO2萃取,萃取压力30 MPa,萃取温度50 ℃,萃取时间2 h,95%乙醇为夹带剂,加入量为药材量的1 倍[9],减压浓缩后得萃取物(约140 g),将萃取物经硅胶柱色谱分离(湿法装柱,干法上样),先后通过石油醚-醋酸乙酯(50∶1~0∶100)、醋酸乙酯-甲醇(50∶1~0∶100)梯度洗脱得到10 个组分(Fr. 1~10)。Fr. 3 经MCI GEL CHP20P 色谱除色素(95%甲醇洗脱)后,再经ODS 中压制备,甲醇-水(30∶70→100∶0)梯度洗脱,得到14 个组份(Fr. 3-1~3-14)。Fr. 3-4 经反相HPLC 制备,甲醇-水(86∶14)洗脱得到化合物4(18 mg)。Fr. 3-6 经反相HPLC制备,甲醇-水(82∶18)洗脱得到化合物2(12 mg)。Fr. 3-9 经反相HPLC 制备,甲醇-水(78∶22)洗脱得到化合物8(16 mg)。Fr. 3-10 经反相HPLC 制备,甲醇-水(76∶24)洗脱得到化合物5(24 mg)。Fr.3-12 经反相HPLC 制备,甲醇-水(70∶30)洗脱得到化合物9(15 mg)。Fr. 4 经MCI GEL CHP20P 色谱除色素(95%甲醇洗脱)后,ODS 中压制备甲醇-水(20∶80→100∶0)梯度洗脱,得到13 个组份(Fr.4-1~4-13)。Fr. 4-3 经反相HPLC 制备,甲醇-水(75∶25)洗脱得到化合物3(20 mg)。Fr. 4-4 经反相HPLC 制备,甲醇-水(73∶27)洗脱得到化合物1(14 mg)。Fr. 4-6 经反相HPLC 制备,甲醇-水(70∶30)洗脱得到化合物6(16 mg)。Fr. 4-8 经反相HPLC制备,甲醇-水(70∶30)洗脱得到化合物10(15 mg)。Fr. 4-11 经反相HPLC 制备,甲醇-水(65∶35)洗脱得到化合物15(7 mg)。Fr. 5 经MCI GEL CHP20P色谱除色素(95%甲醇洗脱)后,ODS 中压制备甲醇-水(10∶90→100∶0)梯度洗脱,得到17 个组份(Fr. 5-1~5-17)。Fr. 5-2 经反相HPLC 制备,甲醇-水(22∶78)洗脱得到化合物13(8 mg)。Fr. 5-4经反相HPLC 制备,甲醇-水(35∶65)洗脱得到化合物7(10 mg)。Fr. 5-7 经反相HPLC 制备,甲醇-水(50∶50)洗脱得到化合物12(10 mg)。Fr. 7 经ODS 中压制备甲醇-水(10∶90→100∶0)梯度洗脱,得到9 个组份(Fr. 7-1~7-9)。Fr. 7-6 经反相HPLC 制备,甲醇-水(70∶30)洗脱得到化合物11(90 mg)。Fr. 8 经ODS 中压制备甲醇-水(10∶90→100∶0)梯度洗脱,得到11 个组份(Fr. 8-1~8-11)。Fr. 8-3 经反相HPLC 制备,甲醇-水(22∶68)洗脱得到化合物14(10 mg)。
3 结构鉴定
3.1 新化合物结构鉴定
1H-NMR (400 MHz, CDCl3) 谱显示了26 个氢信号,其中包括4 个烯质子信号[δ5.98 (1H, t,J= 7.6 Hz, H-10), 5.91 (1H, s, H-2), 5.49 (1H, t,J= 7.9 Hz,H-5), 5.06 (1H, m, H-14)] 和4 个甲基氢信号[δ2.15(3H, s, H-20), 1.65 (3H, s, H-16), 1.56 (3H, s, H-17),1.22 (3H, s, H-19)]。13C-NMR (100 MHz, CDCl3) 结合HMBC 谱共解析出20 个碳信号,其中包括1 个羧基信号δ172.4 (C-18),1 个羰基信号δ169.7(C-1),8 个烯碳信号[δ154.7 (C-3), 152.1 (C-4), 144.2(C-10), 132.3 (C-15), 131.3 (C-11), 123.4 (C-14),116.3 (C-2), 108.8 (C-5)],5 个亚甲基碳信号[δ41.3(C-8), 38.7 (C-6), 34.5 (C-12), 27.7 (C-13) 和24.6(C-9)],4 个甲基碳信号[δ26.8 (C-19), 25.6 (C-16),17.7 (C-17) 和11.8 (C-20)],以及1 个季碳信号δ73.1 (C-7)。
HMBC 谱中H-17 与C-14/C-17 的相关和H-16与C-14/C-17 的相关可推测出2-甲基戊-2-烯基的结构片段,H-10 与C-11/C-12/C-18 相关和H-12 与C-10/C-11/C-18 相关信号可推导出2-甲基-2-丙烯酸结构,结合1H-1H COSY 谱中H-13 与H-12/H-14 相关,H-9 与H-8/H-10 相关,可以推导出结构片段I:2-甲基戊-2-烯基→C-13→2-甲基-2-丙烯酸→C-9→C-8。同理,HMBC 谱中H-2 与C-1/C-3/C-4/C-20 的相关和H-20 与C-2/C-3/C-4 的相关结合相关碳的化学位移值,可推测出 4-methyl-5-methylenefuran-2(5H)-one 结构,结合1H-1H COSY谱中H-5 与H-6 相关,HMBC 中H-5 与C-3/C-4 相关,H-6 与C-4 相关,可以得到结构片段II:4-methyl-5-methylenefuran-2(5H)-one→C-5→C-6 。最后,根据HMBC 谱中H-5 与C-7 相关,H-6 与C-7/C-8/C-19 相关,H-8 与C-6/C-7/C-19 相关,H-9与C-7 相关,表明结构片段I、II 和C-19 通过C-7相连。将相连得到的结构片段与化合物15 的分子式C20H28O5进行对比,发现片段中少了1 个氢和1个氧,且C-7 的化学位移值(δ73.1)与饱和碳链上的季碳相比明显向低场区移动,与不饱和季碳相比向高场区移动,因此推测C-7 位还与羟基相连。同时HR-ESI-MS 出现m/z223 的碎片离子峰也进一步证实-OH 连在7 号位(图1)。

图1 化合物15 的ESI-MS/MS 的碎片离子Fig. 1 Diagnostic ESI-MS/MS fragment ions (m/z) of compound 15
NOESY谱中,H-10与H-12有明显的相关信号,提示C-10→C-11 的双键为顺式构型(Z)[10],结构见图2(本实验尚未对7 位手性碳的绝对构型进行确认,将在后续的研究中进行确认)。经过SciFinder Scholar 网络检索,未发现相关报道,表明化合物15 为新化合物,命名为三白草二萜E(sauruditerpene E),其13C-NMR、1H-NMR 信号归属见表1。

图2 化合物15 的结构和主要相关信号Fig. 2 Chemical structure and key correlations of compound 15
3.2 已知化合物结构鉴定
化合物1:白色无定形粉末,mp 103~104 ℃。HR-ESI-MSm/z: 445.182 1 [M-H]-(计算值为445.185 6,分子式为C24H29O8),结合1H-NMR、13C-NMR 确定分子式为C24H30O8。1H-NMR (400 MHz, CDCl3)δ: 7.33 (4H, s, H-2, 2′, 6, 6′), 4.01 (2H,m, H-8, 8′), 3.98 (12H, s, 3, 3′, 5, 5′-OCH3), 3.96 (6H,s, 4, 4′-OCH3), 1.17 (6H, d,J= 6.3 Hz, H-9, 9′);13C-NMR (100 MHz, CDCl3)δ: 202.6 (C-7, 7′), 153.2(C-4, 4′), 143.0 (C-3, 3′, 5, 5′), 132.0 (C-1, 1′), 105.9(C-2, 2′, 6, 6′), 61.0 (4, 4′-OCH3), 56.4 (3, 3′, 5,5′-OCH3), 43.2 (C-8, 8′), 17.8 (C-9, 9′)。
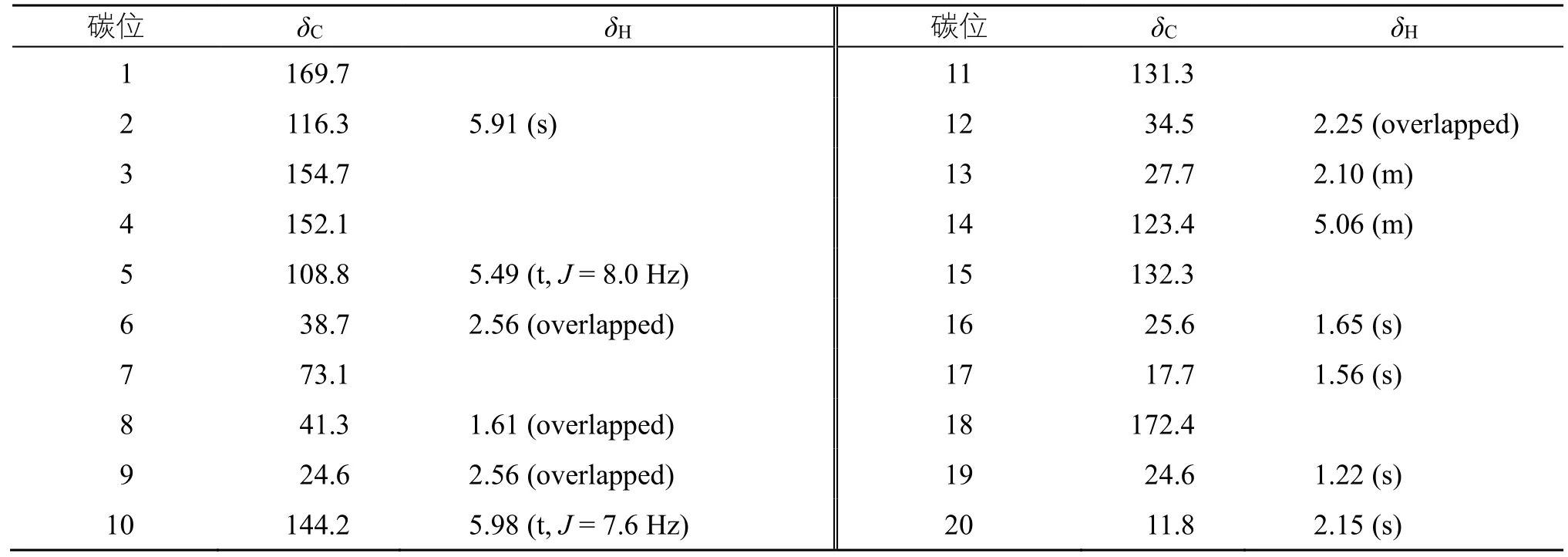
表1 化合物15 的NMR 数据 (400/100 MHz, CDCl3)Table 1 NMR Spectroscopic data of compound 15 (400/100 MHz, CDCl3)
1H-NMR 中δ7.33 (4H, s, H-2, 2′, 6, 6′), 3.98(12H, s, 3, 3′, 5, 5′-OCH3), 3.96 (6H, s, 4, 4′-OCH3),表明结构中可能存在2 个3,4,5-三甲氧基苯基部分,HMBC 谱中3,3′,5,5′-OCH3(δH3.98, 12H, s) 和4,4′-OCH3(δH3.96, 6H, s) 分别与143.0 (C-3, 3′, 5, 5′)和153.2 (C-4, 4′),远程相关,进一步证明甲氧基分别取代在3,3′,4,4′,5,5′位;1H-NMR 谱中剩下2 组质子信号δ4.01 (2H, m, H-8, 8′) 和1.17 (6H, d,J= 6.3 Hz, H-9, 9′) 表明结构中含有CH3-CH-部分且与不饱和基团相连,HMBC谱中H-9/9′ (δH1.17, d,J= 6.3 Hz), H-2, 2′, 6, 6′ (δH7.33, s) 分别与C-7/7′ (δC202.6) 相关,表明3,4,5-三甲氧基苯基和CH3-CH-部分通过7, 7′位羰基连接(图3)。经Sci Finder 数据系统检索,以上化合物结构与文献报道对照基本一致[11],故鉴定化合物1 为2,3-二甲基-1,4-二(3,4,5-三甲氧基苯基)-1,4-丁二酮。
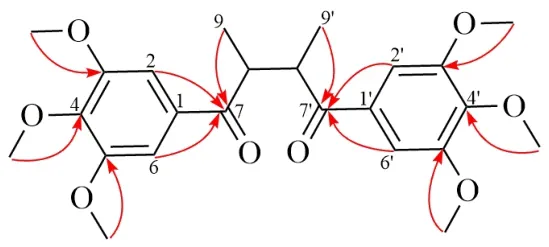
图3 化合物1 的结构和主要HMBC (→) 相关信号Fig. 3 Chemical structrue and key HMBC (→) correlations of compound 1
化合物 2:白色粉末,mp 210~212 ℃。HR-ESI-MSm/z: 505.212 2 [M-H]-,结合1H-NMR、13C-NMR 确定分子式为C32H30N2O4。1H-NMR (400 MHz, DMSO-d6)δ: 8.86 (1H, d,J= 8.0 Hz, -NH),8.31 (1H, d,J= 8.0 Hz, -NH), 7.16~7.78 (20H, m,Ar-H), 4.68 (1H, m, H-2), 4.45 (1H, m, H-2′), 4.18(2H, m, H-1′), 3.09~3.17 (2H, m, H-3), 2.86 (2H, m,H-3′);13C-NMR (100 MHz, DMSO-d6)δ: 171.5 (C-1),166.7 (C=O), 166.2 (C=O), 54.4 (C-2), 35.9 (C-3),65.5 (C-1′), 49.9 (C-2′), 36.3 (C-3′), 4 个苯环上的24个碳信号(138.3, 137.8, 134.5, 133.6, 131.5×2,131.2×2, 129.1×2, 129.0×2, 128.3×2, 128.2×2,127.4×2, 127.2×2, 126.5×2, 126.2×2)。以上波谱数据与文献报道对照基本一致[12-13],故鉴定化合物2 为asperphenamate。
化合物3:淡黄色油状液体。1H-NMR (400 MHz,DMSO-d6)δ: 0.99 (6H, d,J= 4.0 Hz, H-9, 9′), 2.24(2H, m H-8, 8′), 3.66 (6H, s, 4, 4′-OCH3), 3.78 (12H,s, 3, 3′, 5, 5′-OCH3), 4.53 (2H, d,J= 6.4 Hz, H-7, 7′),6.68 (4H, s, H-2, 2′, 6, 6′);13C-NMR (100 MHz,DMSO-d6)δ: 153.0 (C-5, 5′), 138.1 (C-1, 1′, 4, 4′),103.5 (C-2, 2′, 6, 6′), 86.6 (C-7, 7′), 60.2 (4, 4′-OCH3),55.9 (3, 3′, 5, 5′-OCH3), 44.1 (C-8, 8′), 12.9 (C-9, 9′)。以上波谱数据与文献报道对照基本一致[14],故鉴定化合物3 为rel-(7S,8S,7′R,8′R)-3,3′,4,4′,5,5′-六甲氧基-7-O-7′,8.8′-木脂素。
化合物4:白色粉末,mp 331~332 ℃。1H-NMR(400 MHz, DMSO-d6)δ: 5.19 (1H, t,J= 3.6 Hz,H-12), 3.40 (1H, overlapped, H-3), 3.31 (1H, d,J=10.2 Hz, H-23b), 2.73 (1H, dd,J= 16.4, 4.2 Hz,H-18), 1.09 (3H, s, H-27), 0.85 (9H, s, H-25, 29, 30),0.71 (3H, s, H-26), 0.52 (3H, s, H-26);13C-NMR (100 MHz, DMSO-d6)δ: 178.5 (C-28), 144.2 (C-13), 122.0(C-12), 70.9 (C-3), 64.4 (C-23), 47.0 (C-9), 42.6(C-14), 41.3 (C-4), 47.6 (C-5), 45.1 (C-19), 44.9(C-17), 40.4 (C-18), 39.2 (C-8), 37.2 (C-1), 36.6(C-10), 33.6 (C-21), 33.0 (C-22, 29), 32.5 (C-7), 30.3(C-20), 27.7 (C-15), 26.4 (C-2), 25.6 (C-27), 23.2(C-30), 22.8 (C-11, 16), 18.0 (C-6), 16.9 (C-26), 15.4(C-25), 12.5 (C-24)。以上波谱数据与文献报道对照基本一致[15],故鉴定化合物4 为常春藤皂苷元。
化合物5:淡黄色油状液体。1H-NMR (400 MHz,CDCl3)δ: 7.71 (1H, dd,J= 8.4 Hz, 1.6 Hz, H-6), 7.54(1H, d,J= 1.6 Hz, H-2), 6.88~6.96 (3H, m, H-2′, 5′,6′), 6.82 (1H, d,J= 8.4 Hz, H-5), 6.15 (1H, d,J= 7.6 Hz, H-7′), 3.94 (3H, s, 4-OCH3), 3.91 (3H, s, 4′-OCH3),3.87 (3H, s, 3′-OCH3), 3.84 (3H, s, 3-OCH3), 3.21(1H, m, H-8′), 2.05 (3H, s, H-9), 1.26 (3H, d,J= 6.8 Hz, H-9′);13C-NMR (100 MHz, CDCl3)δ: 165.3(C-7), 153.2 (C-3′), 148.8 (C-3), 148.7 (C-4′), 131.5(C-1′), 123.5 (C-6′), 122.5 (C-1), 119.0 (C-6), 112.1(C-2′), 110.2 (C-2), 110.0 (C-5), 76.3 (C-7′), 56.0 (3,4-OCH3), 55.9 (3′-OCH3), 55.8 (4′-OCH3), 52.9(C-8′), 29.7 (C-9), 12.85 (C-9′), 12.8 (C-4), 11.0(C-5′)。以上波谱数据与文献报道对照基本一致[16],故鉴定化合物5 为schisandlignans C。
化合物6:白色无定形粉末。1H-NMR (400 MHz,CDCl3)δ: 6.66~6.50 (4H, m, H-2, 6, 2′, 6′), 6.36 (1H,m, H-7′), 6.20 (1H, dt,J= 9.1, 6.5 Hz, H-8′), 5.32(1H, s, -OH), 4.62 (1H, dd,J= 8.3, 5.2 Hz, H-7), 4.00(1H, m, H-8), 3.91 (6H, s, 3′, 5′-OCH3), 3.87 (6H, s, 3,5-OCH3), 3.84 (3H, s, 4′-OCH3), 1.93 (3H, ddd,J=7.8, 6.9, 1.5 Hz, H-9′), 1.25 (3H, t,J= 6.0 Hz, H-9);13C-NMR (100 MHz, CDCl3)δ: 153.1 (C-3, 5), 152.8(C-3′, 5′), 137.6 (C-4), 136.4 (C-4′), 135.7 (C-1),133.9 (C-1′), 130.7 (C-7′), 125.7 (C-8′), 106.0 (C-2),104.3 (C-6), 102.9 (C-2′, 6′), 86.5 (C-8), 79.4 (C-7),60.8 (-OCH3), 56.1 (3, 5-OCH3), 56.0 (3′, 5′-OCH3),18.4 (C-9′), 17.7 (C-9)。以上波谱数据与文献报道对照基本一致[17],故鉴定化合物6 为樟叶素。
化合物7:无色油状液体。1H-NMR (400 MHz,DMSO-d6)δ: 4.63 (1H, brs, -OH), 4.25 (1H, t,J= 7.3 Hz, H-4), 2.45 (2H, m, H-2a, b), 2.09 (2H, dt,J= 9.2,7.4 Hz, H-3a, b), 1.13 (3H, s, H-6), 1.07 (3H, s, H-7);13C-NMR (100 MHz, DMSO-d6)δ: 177.8 (C-1), 86.2(C-5), 70.2 (C-4), 28.9 (C-2), 26.0 (C-3), 25.8 (C-6),22.1 (C-7)。以上波谱数据与文献报道对照基本一致[18],故鉴定化合物7 为4-羟基-5-甲基己烷-5-内酯。
化合物8:无色油状液体。1H-NMR (400 MHz,CDCl3)δ: 5.69 (1H, s, H-7), 4.11 (1H, m, H-3), 2.52(1H, ddd,J= 12.1, 3.9, 2.2 Hz, H-4a), 2.03 (1H, ddd,J= 12.8, 4.2, 2.2 Hz, H-2a), 1.57 (3H, s, H-11), 1.49(1H, t,J= 11.7 Hz, H-4b), 1.33 (1H, t,J= 11.7 Hz,H-2b), 1.32 (3H, s, H-10), 1.25 (3H, s, H-9);13C-NMR(100 MHz, CDCl3)δ: 181.4 (C-6), 171.9 (C-8), 113.0(C-7), 86.9 (C-5), 64.8 (C-3), 49.7 (C-2), 47.8 (C-4),35.1 (C-1), 29.9 (C-10), 25.5 (C-9), 25.0 (C-11)。以上波谱数据与文献报道对照基本一致[19],故鉴定化合物8 为异黑麦草内酯。
化合物9:白色无定形粉末。1H-NMR (400 MHz,CDCl3)δ: 9.87 (1H, s, -CHO), 7.45 (2H, d,J= 6.9 Hz,H-2′, 6′), 7.07 (1H, d,J= 8.7 Hz, H-5′), 6.96 (1H, d,J= 0.9 Hz, H-2), 6.90 (2H, t,J= 3.2 Hz, H-5, 6) , 4.73(1H, d,J= 7.8 Hz, H-7), 4.43 (1H, dt,J= 12.5, 6.3 Hz, H-8), 3.96 (3H, s, 3′-OCH3), 3.90 (3H, s,3-OCH3), 1.23 (3H, d,J= 6.2 Hz, H-9);13C-NMR(100 MHz, CDCl3)δ: 190.9 (-CHO), 153.2 (C-4′),150.8 (C-3′), 146.7 (C-3), 145.8(C-4), 131.5 (C-1′),130.9 (C-1), 126.4 (C-2′), 120.6 (C-6), 115.1 (C-5′),114.3 (C-5), 110.0 (C-6′), 109.4 (C-2), 81.9 (C-8),77.9 (C-7), 56.0 (3, 3′-OCH3), 16.4 (C-9)。以上波谱数据与文献报道对照基本一致[20],故鉴定化合物9 为perseal B。
化合物10:白色无定形粉末。1H-NMR (400 MHz, CDCl3)δ: 6.79 (1H, d,J= 8.1 Hz, H-3′), 6.69(1H, s, H-2), 6.61 (1H, d,J= 1.7 Hz, H-6′), 6.58 (1H,dd,J= 8.1, 1.8 Hz, H-2′), 6.54 (1H, s, H-5), 6.13 (1H,s, H-7), 5.32 (1H, s, -OH), 3.81 (3H, s, 3′-OCH3), 3.79(3H, s, 3-OCH3), 3.67 (1H, d,J= 3.0 Hz, H-7′), 2.37(1H, ddd,J= 10.3, 7.0, 3.5 Hz, H-8′), 1.80 (3H, brs,9′-CH3), 1.10 (3H, d,J= 7.1 Hz, 9-CH3);13C-NMR(100 MHz, CDCl3)δ: 146.2 (C-3), 145.1 (C-4), 144.1(C-3′), 143.8 (C-4′), 138.9 (C-1′), 137.8 (C-8), 127.8(C-6), 126.9 (C-1), 121.1 (C-7), 120.4 (C-6′), 111.7(C-5′), 114.0 (C-2), 112.1 (C-5), 110.1 (C-2′), 56.0(3′-OCH3), 55.8 (3-OCH3), 51.0 (C-7′), 42.2 (C-8′),22.2 (C-9), 18.8 (C-9′)。以上波谱数据与文献报道对照基本一致[21],故鉴定化合物10 为myrisfragransin。
化合物11:淡黄色液体。1H-NMR (400 MHz,CDCl3)δ: 6.55 (1H, m,J= 7.5, 2.8 Hz, H-6), 5.21(2H, m, H-5, 11), 3.15 (1H, m, H-4a), 2.63 (2H, t,J=7.1 Hz, H-8), 2.53 (1H, ddd,J= 6.0, 4.4, 2.9 Hz,H-4b), 2.37 (2H, m, H-7), 2.13 (3H, s, H-10), 1.75(3H, s, H-14), 1.73 (3H, s, H-13);13C-NMR (100 MHz, CDCl3)δ: 206.8 (C-9), 170.9 (C-2), 139.6(C-12), 138.0 (C-6), 127.8 (C-3), 123.6 (C-11), 74.5(C-5), 41.4 (C-8), 32.4 (C-4), 30.0 (C-10), 25.7(C-13), 24.0 (C-7), 18.4 (C-14)。以上波谱数据与文献报道对照基本一致[22],故鉴定化合物 11 为heteroplexisolide E。
化合物12:淡黄色液体。1H-NMR (400 MHz,CDCl3)δ: 9.84 (1H, s, -CHO), 7.37 (2H, d,J= 11.3 Hz, H-2′, 4), 6.93 (3H, dd,J=13.3, 6.2 Hz, H-2, 6, 6′),5.30 (1H, s, -OH), 5.26 (1H, d,J= 9.3 Hz, H-7), 3.95(3H, s, 3′-OCH3), 3.89 (3H, s, 3-OCH3), 3.57 (1H, dd,J= 8.7, 7.1 Hz, H-8), 1.45 (3H, d,J= 6.8 Hz, H-9);13C-NMR (100 MHz, CDCl3)δ: 190.8 (C-7′), 153.3(C-4′), 146.7 (C-3), 146.2 (C-5), 144.9 (C-3′), 133.7(C-5′), 131.4 (C-1), 131.0 (C-1′), 120.2 (C-6′), 120.1(C-2), 111.8 (C-2′), 114.4 (C-4), 109.0 (C-6), 95.0(C-7), 56.1 (3, 3′-OCH3), 44.8 (C-8), 17.8 (C-9)。以上波谱数据与文献报道对照基本一致[23],故鉴定化合物12 为curcasinlignan C。
化合物13:淡黄色油状物。1H-NMR (400 MHz,CDCl3)δ: 6.83 (1H, d,J= 15.7 Hz, H-7), 6.45 (1H, d,J= 15.7 Hz, H-8), 5.92 (1H, s, H-4), 2.46 (1H, d,J=17.2 Hz, H-2a), 2.30 (3H, s, H-10), 2.24 (1H, d,J=17.0 Hz, H-2b), 1.87 (3H, d,J= 1.1 Hz, H-11), 1.07(3H, s, H-12), 0.99 (3H, s, H-13);13C-NMR (100 MHz, CDCl3)δ: 198.2 (C-3), 197.9 (C-9), 161.8(C-5), 145.9 (C-7), 130.4 (C-8), 127.4 (C-4), 79.1(C-6), 49.5 (C-2), 41.6 (C-1), 28.2 (C-10), 24.4(C-12), 23.0 (C-13), 18.9 (C-11)。以上波谱数据与文献报道对照基本一致[24],故鉴定化合物13 为去氢催吐萝芙木醇。
化合物14:淡黄色液体。1H-NMR (400 MHz,DMSO-d6)δ: 5.79 (1H, s, H-7), 5.01 (1H, s, -OH),4.08 (1H, m, H-3), 2.30 (1H, dd,J= 13.3, 2.5 Hz,H-4a), 1.87 (1H, dd,J= 14.1, 2.5 Hz, H-2a), 1.67 (3H,s, H-11), 1.63 (1H, dd,J= 13.4, 3.9 Hz, H-4b), 1.42(1H, dd,J= 14.2, 3.7 Hz, H-2b), 1.38 (3H, s, H-9),1.20 (3H, s, H-10);13C-NMR (100 MHz, DMSO-d6)δ: 183.5 (C-6), 171.5 (C-8), 112.6 (C-7), 87.0 (C-5),65.3 (C-3), 47.1 (C-2), 45.7 (C-4), 36.1 (C-1), 30.9(C-10), 27.3 (C-11), 26.7 (C-9)。以上波谱数据与文献报道对照基本一致[19],故鉴定化合物14 为黑麦草内酯。
4 讨论
本实验对三白草地上部分超临界CO2萃取物的化学成分进行研究,从中分离鉴定出15 个化合物,除化合物3、6、13 外均为首次从该植物中分离得到,其中化合物15 为新化合物,化合物1 为新的天然产物。Asperphenamate 又名3-苯基-2-苯甲酰氨基丙酸-3′-苯基-2′-苯甲酰氨基丙酯,是具有多个酰胺键的天然产物,且对人乳腺导管癌T47D 细胞、人乳腺癌MDA-MB231细胞、人早幼粒白血病HL60细胞、人宫颈癌Hela 细胞和人胃癌SGC-7901 细胞等多种肿瘤细胞具有显著的抑制活性,半数抑制浓度(median inhibition concentration,IC50)分别为8.2、11.9、67.2、25.7、25.8 μmol/L[25];常春藤皂苷元能抑制前列腺癌DU145 细胞、人乳腺癌MCF-7细胞和肺癌A549 细胞等多种肿瘤细胞的增殖、迁移和侵袭[26],同时具有抗炎、抗抑郁[26-27]等多方面生物活性。本研究丰富了三白草的化学成分,后续将选择适宜的药理模型对上述化合物进行药效评价,以期阐明三白草药效物质基础,从而为三白草的产品开发提供理论依据。
利益冲突所有作者均声明不存在利益冲突
