手性萜类香料化合物制备的研究进展
2023-05-30毛悦汪薇白卫东王靖宇李湘銮姜浩赵文红
毛悦 汪薇 白卫东 王靖宇 李湘銮 姜浩 赵文红
摘要:手性萜类香料化合物具有柠檬、柏油、留兰香等香气,广泛应用于食品、日用品行业中。由于手性萜类香料对映体具有不同的香气特征,加上消费者对高品质天然香料的青睐,手性萜类香料化合物的生物制备法备受关注。文章介绍了柠檬烯、乙酸香茅酯、α-松油醇、香芹酮等萜类香料化合物的制备方法,分析了手性萜类香料生物法制备中面临的问题,旨在为更经济高效的生物法转化手性萜类香料提供借鉴。
关键词:手性;萜类香料化合物;制备方法
中图分类号:TS202.3 文献标志码:A 文章编号:1000-9973(2023)05-0208-06
Abstract: Chiral terpene spice compounds have lemon, pitch, spearmint and other spice, and are widely used in the food and daily necessity industries. Due to the different aroma characteristics of chiral terpene spice enantiomers and the preference of consumers for high-quality natural spices, the biological preparation method of chiral terpene spice compounds has attracted much attention. In this paper, the preparation methods of chiral terpene spice compounds such as cinene, citronellyl acetate, α-terpineol, carvone are introduced, and the problems faced in the preparation of chiral terpene spice by biological method are analyzed, aiming to provide references for the more economical and efficient conversion of chiral terpene spice by biological method.
Key words: chiral; terpene spice compounds; preparation methods
收稿日期:2022-12-05
基金項目:广东省重点研发项目(2022B020205003);广东省岭南特色食品科学与技术重点实验室(2021B1212040013);广州市科技计划项目(202103000062)
作者简介:毛悦(1999-),女,硕士研究生,研究方向:食品化学。
*通信作者:汪薇(1981-),女,副教授,博士,研究方向:生物催化与转化、天然香料。
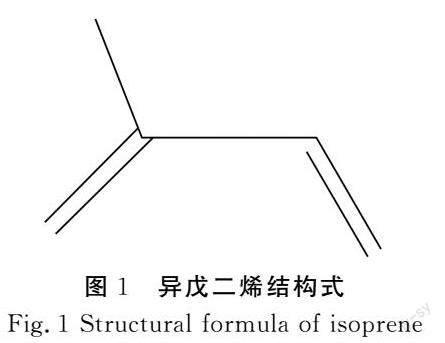
萜类化合物是指具有(C5H8)n通式(见图1)及其含氧和不同饱和程度的衍生物,可以看作是异戊二烯或异戊烷以各种方式连结而成的一类天然化合物[1]。萜类化合物广泛存在于自然界中,目前已知从天然产物中提取得到的萜类化合物大约有60 000种[2]。萜类按异戊二烯单元数目可分为单萜、倍半萜、二萜等[3]。萜类化合物具有较强的挥发性和香气,故在香料生产、农业、药物和生物燃料中广泛应用。研究结果表明,萜类是薄荷醇、芍药苷、青蒿素、榄香烯、紫杉醇等药用植物的活性成分,具有抗菌、抗炎、抗癌活性、抗HIV病毒等生物活性[4]。自然界中萜类化合物多种多样,但可利用的仅有一小部分,萜类天然产物的生物合成与合成生物学受到国内外广泛关注。
手性现象在香料中普遍存在,手性香料不同的对映异构体会表现出不同的香气。手性萜类香料对映体表现出不同的香气特征,如(R)-柠檬烯具有新鲜的柑橘香,而(S)-柠檬烯则具有柠檬的香气;(R)-香芹酮具有香芹籽味,(S)-香芹酮具有甜的留兰香味;(R)-香茅醇具有香茅气息,而(S)-香茅醇则散发五叶草气息;(R)-圆柚酮具有弱的木香,(S)-圆柚酮具有强的葡萄香味等[5]。
香精在食品、日用品、化妆品、烟草行业应用广泛,是化工行业常用的添加剂[6]。迷迭香精油中含有许多萜类化合物,如樟脑、桉叶油醇、L-α-松油醇、芳樟醇等。迷迭香精油可以用作香氛香薰或食品香料[7]。有研究表明,迷迭香精油的脂溶性提取液可明显抑制食用植物油中过氧化物的生成,表现出抗氧化性能[8]。
香料化合物又分为天然香料和合成香料[9]。经过对植物残渣的深入分析,对天然香料化合物的获取有了一定的了解。为了得到品质优良的香精香料,选择的提取方法十分重要,传统方法有水蒸气蒸馏法和索氏提取法[10]。水蒸气蒸馏法又分为很多种,新兴研究是通过使用离子液体辅助水蒸气对香精香料进行提取[11]。崔丽佼等[12]使用离子液体辅助水蒸汽法从柠檬中提取柠檬精油,为柠檬精油的综合开发利用提供了参考。同时,随着人工合成香料方法研究的深入,生物催化法成为一种兴起的合成香精香料方法。
手性萜类香料化合物的制备方法主要有天然提取法、化学法和生物法。植物提取法获得的产物原料匮乏、产量低、周期长、成本高,不能满足生产需求。化学合成法虽提高了产量,但对环境不友好,反应条件复杂,香气不够自然[8],使用生物合成法则可避免以上问题,具有广阔的应用前景。本文对具有代表性的手性萜类香料化合物合成方法的研究进展进行了综述。
1 柠檬烯
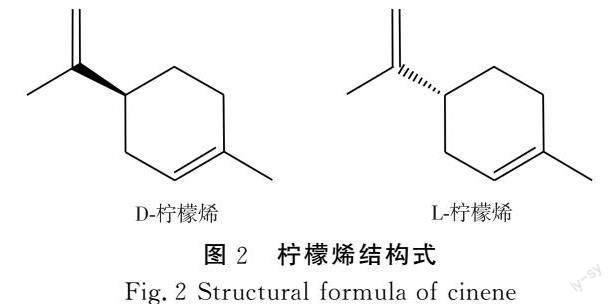
柠檬烯,又名苧烯[13],是一种单环单萜类化合物,分子式为C10H16。柠檬烯在自然界中有3种存在形式:D-柠檬烯、L-柠檬烯和DL-柠檬烯,见图2。
自然界中柠檬烯主要以D-柠檬烯的形式存在[14]。L-柠檬烯主要存在于薄荷等植物精油中,其味道与松节油相似。D-柠檬烯广泛存在于柑橘类果实中,如橘子、橙子、柚子的果皮中。DL-柠檬烯存在于云南松油等精油中,是一种重要的功能性单萜,主要具有抗菌活性[15]、抗癌活性[16]、抗炎症[17]、抗氧化[18]等功能。柠檬烯在食品、医药、日用品等行业中广泛应用,还可作为生物燃料使用[19]。
柠檬烯大部分是从柑橘类的果皮中分离提取出来的。目前使用的主要提取方法有超临界CO2萃取法、有机溶剂萃取法、蒸馏法、超声波辅助萃取法等[20]。有机溶剂浸提法主要是选择正己烷、乙醚、石油醚等有机溶剂进行浸提。但由于使用有机溶剂会污染环境,并且此法获得的柠檬烯用途有限,因此更多实际生产会使用蒸馏法。减压蒸馏与水蒸汽蒸馏相比,减压蒸馏压强小,使柠檬烯的沸点降低,避免了柠檬烯发生氧化等副反应,且效率较水蒸汽蒸馏高[21]。分子蒸馏是在高真空环境下,利用柠檬烯分子与其他分子的分子自由程度不同,从而将柠檬烯分离出来[22]。此法效率高、蒸馏时间短、无污染,但经济成本较高。超临界CO2萃取法提取的柠檬烯不会引入新的杂质,也避免了柠檬烯发生副反应[23],但是经济成本高,并未在工业化大规模生产中使用。从植物中提取柠檬烯,原料产量会受到气候的影响,从而影响柠檬烯产量,无法持续供应。马云建[24]建立了香料前体化合物(柠檬烯)的绿色天然低共熔溶剂(NADES)高效稳态化提取技术,效率达到了传统的萃取溶剂(如乙酸乙酯和正己烷)的80%以上。
一些研究者利用工程菌合成柠檬烯。Cao等[25]向Po1f菌株中插入NDPS1基因(橙花基焦磷酸合酶编码基因),将NDPS1基因和dLS基因过表达,最终得到能够生产D-柠檬烯的解脂耶氏酵母工程菌,这是首次使用解脂耶氏酵母异源生产柠檬烯的研究,该研究为后续的深入研究奠定了基础。吴计划[26]向大肠杆菌BW25113的基因组中插入了T7 RNA聚合酶的基因,以得到工程大肠杆菌BW25113(DE3)菌株,并对合成途径进行了优化,以葡萄糖为原料,发酵合成了柠檬烯。但该方法是位于质粒上的柠檬烯合成模块,在工业发酵的过程中会提高经济成本,故仍需进一步优化以降低成本。
2 乙酸香茅酯
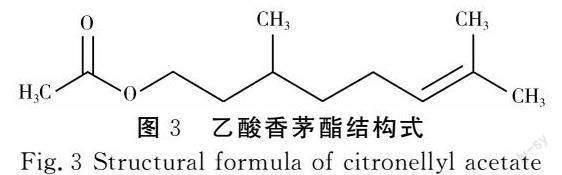
乙酸香茅酯是一种短链萜烯脂肪酸酯类化合物,分子式为C12H22O2,见图3。
乙酸香茅酯存在于玫瑰精油和香茅精油中[27],具有柠檬香气,广泛应用于日用品、医药等行业[28]。
少部分乙酸香茅酯从天然植物油中提取。通过普通蒸馏的方法将乙酸香茅酯从香茅油、玫瑰油等植物精油中分离出来。但由于原料稀缺,蒸餾成本较高,不适合大规模生产,因此天然提取法存在一定的局限性。
江云兵等[29]以NaHSO4·SiO2为催化剂催化香茅醇与乙酸酐生成乙酸香茅酯。这项研究突破了传统化学合成法的局限,充分发挥了微波辐射技术的优点。
天然提取法和化学合成法都有自身的局限性,而随着乙酸香茅酯需求的增长,研究者转向使用生物技术方法进行生产。为了突破酶只能在单一的水溶液介质中反应的局限,研究者对不同的反应介质进行了研究[30]。Macedo等[31]研究了非水相体系中根霉菌Rhizopus sp.脂肪酶的催化反应,底物香茅醇分别与乙酸乙酯、乙酸丁酯反应,合成乙酸香茅酯该反应的转化率分别为58%和48%。Xiong等[32]以乙酸乙烯酯为溶剂,使用荧光假单胞菌Pseudomonas fluorescens脂肪酶催化香茅醇合成乙酸香茅酯,研究发现乙酸香茅酯的转化率可达到96%。王楠等[33]研究了在醇酸混合反应体系中华根霉菌丝Rhizopus chinensis结合脂肪酶酯化香茅醇合成乙酸香茅酯,转化率可达94%,获得的产物香气纯正。
张蒙等[34]使用固定化荧光假单胞菌Pseudomonas fluorescens脂肪酶,催化香茅醇和乙酸乙烯酯合成乙酸香茅酯,研究发现转化率可达96%。此研究发现固定化酶具有高效催化作用,见表1。
3 α-松油醇
α-松油醇,又名α-萜品醇,它是一种单萜类化合物,分子式为C10H18O,见图4。
(S)-α-松油醇具有针叶树香、柏油味;(R)-α-松油醇具有浓郁的花香、丁香花香气[35]。在香水、化妆品及日用品行业中常用作香料。α-松油醇可作为食品防腐剂,也可作为食用香精调配柠檬、橙、桃子等水果香气 [36];因其具有抗菌和抗氧化特性,在医药行业中可用作抗真菌剂和消毒剂[37]。
α-松油醇可从油樟油中提取出来,油樟植株的根、茎、叶、果实均可提炼精油,但物质含量较低,且需要克服油樟生长周期的问题[38]。在实际生产中主要通过化学合成松油醇后精制得到。
工业合成松油醇主要使用一步法和二步法,通过H2SO4、H3PO4等无机酸催化松节油水合生成松油醇。一步法[39],即松节油在酸催化下水合为松油醇;二步法[40],即松节油在酸催化下先水合生成萜二醇,再由稀酸催化生产松油醇。其中,一步法虽操作简单,但所得松油醇香气质量差,与天然提取的松油醇有差异。二步法所得松油醇纯度高,但工艺流程繁琐,成本高昂。裴文使用手性催化剂催化 1-苯磺酰基-3-丁烯-2-酮与异戊二烯合成 (R)-α-松油醇(见图5),其光学纯度可达92%。
研究发现,真菌和细菌能在有氧条件下将柠檬烯进行生物转化为α-松油醇。Tai等[41]利用青霉菌Penicillium sp.将柠檬烯转化生成α-松油醇; Rottava等[42]利用黑曲霉Aspergillus niger使柠檬烯转化生成α-松油醇;Bicas等[43]利用双相体系(有机相为葵花油)提高鞘脂菌Sphingobium sp.转化柠檬烯生成α-松油醇的产量,产量为130 g/L。廉长盛等[44]使用栖稻假单胞菌 Pseudomonas oryzihabitans将柠檬烯转化为α-松油醇,转化率提高了10.6倍。黄金凤等[45]分离出油樟叶片的内生细菌T3-M-39,从中筛选出α-松油醇高产菌株,并对其进行紫外诱导选育,发现诱导后的菌株产α-松油醇能力提高了34.85%,见表2。
4 香芹酮
香芹酮,又名葛缕酮,是一种单环单萜类化合物,分子式为C10H16O,见图6。
L-香芹酮具有留兰香气味,D-香芹酮为葛缕子香,存在于香芹籽油中,广泛应用于日用品、食品行业[46];另外香芹酮可作为合成砌块来合成复杂的天然产品[47],这些化合物也可用于制备透皮吸收促进剂和其他产品。
从留兰香油中提取出香芹酮常用天然提取法。黃庭刚[48]通过普通间歇精馏法对留兰香油进行精制,香芹酮的含量提高了84.73%。陈连官[49]使用减压蒸馏法将香芹酮的沸点由230 ℃下降到99.6 ℃,降低了经济成本,且所得的香芹酮符合国家质量标准。罗运华等[50]使用超临界CO2萃取法提取香芹酮,所得产物含量为97%。
由于日用品工业的发展,对香芹酮的需求量日益增加,从留兰香油中提取的香芹酮已不能满足市场需求。早期,Linder等[51]首先报道了将柠檬烯经环氧化和水解后得到二醇,再氧化为酮醇,最后脱水成香芹酮。其获得率较低,仅有9.1%。谢海英等[52]先将环氧柠檬酸异构得到香芹醇,再氧化生成香芹酮。此法经济环保,无污水生成,原料易得,反应时间短、选择性好。马晨等[53]将柠檬烯与亚硝基氯反应生成柠檬烯的亚硝基氯化物,再经脱氢得到L-酮肟,再水解为香芹酮。姜志洁等[54]在室温条件下,利用有机电化学合成法催化柠檬烯以制备香芹酮,此法使用的电子代替催化剂符合绿色化学的要求。Li等[55]使用芦苇叶制作介孔二氧化硅,催化柠檬烯发生烯丙基转化生成香芹酮。因此,使用生物法合成香芹酮成为新的研究方向。
一些研究者利用真菌合成香芹酮。Molina等[56]发现从果实中筛选分离出的Aspergillus sp.能够将柠檬烯氧化成香芹酮。Bier等[57]从火炬松中分离得到的Phomopsis sp.可将柠檬烯转化香芹酮。Trytek等[58]还使用葡萄糖氧化酶和辣根过氧化酶氧化柠檬烯,从而得到香芹酮。
5 圆柚酮
圆柚酮((+)-nootkatone),又称(+)-诺卡酮,其分子式为C15H22O,见图7,是一种双环倍半萜酮,最早在阿拉斯加黄雪松的木质成分中分离得到,并存在于柑橘类果实果皮、香根草油中[59]。圆柚酮在低浓度时具有柚子、柑橘、橙子的香气,并带有甜橙、木香香调,味苦,其气味阈值较低,仅为1 μg/L[60]。作为香精香料可以广泛应用于食品、化妆品、日用品及烟草行业,具有极高的市场价值。同时研究者发现,圆柚酮具有抗炎[61]、抑制脂多糖活化[62]等活性,且有抗蚁虫活性[63]。天然产物中圆柚酮含量较低,且存在较多立体异构体,难以分离,故由天然产物中获得的圆柚酮价格非常昂贵。
樊猛等[64]使用同时蒸馏萃取制备圆柚酮,连续蒸馏时的精油提取率较分段蒸馏的精油提取率之和低,并发现延长蒸馏时间有利于柚皮中圆柚酮含量的提高。但使用蒸馏法获得的天然圆柚酮得率较低,无法满足工业需求,因此除了物理法之外,还可使用化学合成法进行制备。
最初,Palmerín-Carreo等[65]使用叔丁基铬酸盐将(+)-瓦伦西亚橘烯转化为(+)-圆柚酮。其他方法则是使用重铬酸钾和醋酸作为催化剂催化反应发生。另外,Salvador等[66]使用二氧化硅负载金属催化剂催化叔丁基过氧化氢,以氧化(+)-瓦伦西亚橘烯的烯丙基。
许多研究者对酶法和微生物法生产圆柚酮都进行了一定的研究,例如细菌、真菌、植物、细胞提取物、酶等。Drawert等[67]对柑橘组织培养物中芳香化合物进行了鉴定,发现其中有微量的圆柚酮。Río等[68]则对不同品种的柑橘愈伤组织培养物进行测定,其中均有瓦伦西亚橘烯和圆柚酮。
研究者利用细菌合成圆柚酮。Sowden等[69]以D-(+)-樟脑为底物,用恶臭假单胞菌Pseudomonas putida的细胞色素P450酶(P450cam)合成(+)-圆柚酮。野生型的P450cam不能氧化瓦伦西亚橘烯,可能是因为该酶的活性位点无法容纳更大的瓦伦西亚橘烯,因此他们研究了Y96、F87、V247、L244处的突变组合对瓦伦西亚橘烯与P450cam结合和氧化的影响,研究发现,F87V/Y967F/L244A的三重突变体可以得到圆柚酮的最大产量。同时,Sowden等发现使用重组巨大芽孢杆菌P450BM-3也可以获得圆柚酮,并且P450BM-3突变体的活性较P450cam更高。
另一些研究者利用真菌合成圆柚酮。最初,Willershausen 等发现,黄孢原毛平革菌Phanerochaete chrysosporium的过氧化氢酶能催化瓦伦西亚橘烯转化为圆柚酮, Kaspera等[70]用子囊菌球毛壳菌可将(+)-瓦伦西亚橘烯转化为(+)-圆柚酮,产率为8 mg/L。Mai等[71]描述了使用蛋白核小球藻Chlorella pyrenoidosa、杨树溃疡病菌 Botryosphaeria dothidea、可可球二孢菌Botryodiplodia theobromae,将(+)-瓦伦西亚橘烯转化为(+)-圆柚酮的生物转化方式。Raatz等[72]使用紫孢侧耳Pleurotus sapidus的担子菌脂氧合酶可将(+)-瓦伦西亚橘烯氧化为(+)-圆柚酮。
6 总结与展望
目前制备手性萜类香料化合物的方法主要有天然提取法、化学法和生物法。生物法制备的手性萜类香料化合物属于天然香料,深受消费者青睐,市场前景广阔。但是由于在生物催化或合成体系中,手性萜类香料化合物对微生物细胞会产生毒性作用,从而产生底物抑制和产物抑制作用,导致产率不理想,反应效率不高,限制了其工业化生产的进程。针对这个问题,不少研究者对菌种进行了改造,对反应体系进行了改进,但是还有很大的进步空间。未来可深入研究其代谢途径及其调控途径,运用离子液体、低共熔溶剂等绿色溶剂,开发新型生物反应器,加深对生物法制备手性萜类香料化合物的认识和研究,这对天然香料的高效生物制备具有重要意义。
参考文献:
[1]刘楠.徐闻普哥滨珊瑚共附生真菌的活性及其代谢产物的研究[D].湛江:广东海洋大学,2014.
[2]TAOFIQ O, MARTINS A, BARREIRO M F, et al. Anti-inflammatory potential of mushroom extracts and isolated metabolites[J].Trends in Food Science & Technology,2016,50:193-210.
[3]BAUNACH M, FRANKE J, HERTWECK C. Cheminform abstract: terpenoid biosynthesis off the beaten track: unconventional cyclases and their impact on biomimetic synthesis[J].Angewandte Chemie,2015,46(18):18288.
[4]李兆坤,王鳳寰,陈彬,等.大型真菌萜类化合物活性研究进展[J].天然产物研究与开发,2017,29(2):357-369.
[5]樊超,谢建华,周其林.手性香料的不对称催化合成研究进展[J].应用技术学报,2018,18(3):189-219.
[6]张媛媛,李涛.微生物法生产香料化合物的研究[J].中国调味品,2018,43(6):180-182.
[7]王有娣,姚小丽,肖青林,等.迷迭香精油和马郁兰精油化学成分及抗氧化活性研究[J].中国调味品,2021,46(1):135-141.
[8]王莹,曾祥辉,邓慧,等.迷迭香脂溶性抗氧化剂活性及抑制食用植物油脂氧化作用研究[J].中国调味品,2022,47(8):80-84.
[7]庄以彬,吴凤礼,殷华,等.芳香族香料化合物生物合成研究进展[J].生物工程学报,2021,37(6):1998-2009.
[8]张璐璐,范刚,何进,等.柠檬烯微生物转化及其相关酶的研究进展[J].食品工业科技,2019,40(12):317-325,330.
[10]蔡庭秀,乔杨波,吴森.“小油料”精油抑菌活性研究及其在食品保藏中的应用[J].中国调味品,2021,46(8):197-200.
[11]胡静,徐若夷,邓维钧.食用精油提取技术研究及应用进展[J].中国调味品,2022,47(9):209-213,220.
[12]崔丽佼,于有伟,张小敏,等.离子液体辅助水蒸气蒸馏法提取柠檬精油的研究[J].中国调味品,2021,46(3):150-153.
[13]NEJDET G. Protective effect of D-limonene derived from orange peel essential oil against Yersinia ruckeri in rainbow trout[J].Aquaculture Reports,2020,18:100417.
[14]JOKI S, MOLNAR M, CIKO A M, et al. Separation of selected bioactive compounds from orange peel using the sequence of supercritical CO2 extraction and ultrasound solvent extraction: optimization of limonene and hesperidin content[J].Separation Science and Technology,2020,55(15):2799-2811.
[15]JAVAD S, SEYEDEH H, MAJID S, et al. Phytochemical compositions and biological activities of essential oil from Xanthium strumarium L.[J].Molecules,2015,20(4):7034-7047.
[16]MANN A P, VERMA A, SETHI G, et al. Overexpression of tissue transglutaminase leads to constitutive activation of nuclear factor-kappaB in cancer cells: delineation of a novel pathway[J].Cancer Research,2006,66(17):8788-8795.
[17]冯堃,秦昭,王文蜀,等.5种柚皮精油成分及油脂抗氧化和抑菌活性[J].食品科技,2018,43(11):255-261.
[18]张芳,姜媛媛,杨洋,等.柚提取物含量测定及其抗氧化、抑菌活性研究[J].食品工业科技,2015,36(3):65-69,73.
[19]JONGEDIJK E, CANKAR K, RANZIJN J, et al. Capturing of the monoterpene olefin limonene produced in Saccharomyces cerevisiae[J].Yeast,2015,32(1):159-171.
[20]丁洁,沙芮,王爱霞,等.柑橘皮挥发油提取及HPLC测定柑橘皮挥发油中的柠檬烯含量[J].湖北农业科学,2017,56(17):3326-3330.
[21]赵优萍,张沙沙,张婷,等.不同提取方法对牡丹籽油品质与抗氧化性的影响[J].食品工业科技,2019,40(1):11-16,22.
[22]王芳,岳朝敏,ANDREEA D,等.结合 GC-MS 的分子蒸馏富集柚皮精油抗氧化成分的研究[J].中国粮油学报,2018,33(7):65-71.
[23]DEL VALLE M, CALDERON J, NUNEZ D, et al. Pressure drop may negatively impact supercritical CO2 extraction of citrus peel essential oils in an industrial-size extraction vessel[J].Journal of Supercritical Fluids,2019,144:108-121.
[24]马云建.酶级联催化柠檬烯环氧化与脂肪酸脱羧的研究[D].广州:华南理工大学,2019:50-68.
[25]CAO X, LYU Y B, CHEN J, et al. Metabolic engineering of oleaginous yeast Yarrowia lipolytica for limonene overproduction[J].Biotechnology for Biofuels,2016,9(1):214.
[26]吳计划.工程大肠杆菌合成柠檬烯[D].天津:天津大学,2019.
[27]DHAKE K P, DESHMUKH K M, PATIL Y P, et al. Improved activity and stability of Rhizopus oryzae lipase via immobilization for citronellol ester synthesis in supercritical carbon dioxide[J].Journal of Biotechnology,2011,156(1):46-51.
[28]MELO L, PASTOREASTORE G M, MACEDO G A.Optimized synthesis of citronelly flavour esters using free and immboilized lipase from Phizopus sp.[J].Process Biochemistay,2005,40(10):3181-3185.
[29]江云兵,熊兴泉.乙酸香茅酯的绿色合成与结构表征[J].华侨大学学报(自然科学版),2014,35(1):47-51.
[30]单天宇,王栋,徐岩,等.华根霉菌丝体结合脂肪酶催化酯合成动力学拆分2-辛醇[J].催化学报,2008(4):403-408.
[31]MACEDO G A, LOZANO M, PASTORE G M. Enzymatic synthesis of short chain citronellyl esters by a new lipase from Rhizopus sp.[J].Electronic Journal of Biotechnology,2003,6(1):3-4.
[32]XIONG J, HUANG Y J. Lipase-catalyzed transesterification synthesis of geranyl acetate in organic solvents and its kinetics[J].Food Science and Technology Research,2014,20(2):207-216.
[33]王楠,王栋,徐岩,等.华根霉脂肪酶催化合成乙酸香茅酯的研究[J].食品工业科技,2010,31(2):307-310.
[34]张蒙,丛方地,任德忠,等.静置的固定化荧光假单胞菌脂肪酶(PFL)生物反应器中催化合成乙酸香茅酯[J].生物加工过程,2020,18(5):572-576.
[35]BHATIA S P, MCGINTY D, FOXENBERG R J, et al. Fragrance material review on terpineol[J].Food & Chemical Toxicology,2008,46(11):275-279.
[36]JUNIOR M, SILVA T, FRANCHI G C, et al. Antioxidant potential of aroma compounds obtained by limonene biotransformation of orange essential oil[J].Food Chemistry,2009,116(1):8-12.
[37]RA J M, SIK J W, TANG H C. Health promoting properties of natural flavor substances[J].Food Science & Biotechnology,2006,15(3):329-338.
[38]尹礼国,凌跃,杜永华,等.宜宾油樟营养器官精油主成分分析[J].江苏农业科学,2014(11):348-350,355.
[39]曹松,安兰芝,卢祥,等.D型大孔磺酸树脂催化松节油水合一步合成松油醇[J].离子交换与吸附,2015,31(5):455-463.
[40]邹志平,孟中磊,刘六军,等.二步法松油醇生产工艺的问题与改进[J].广西林业科学,2020,49(3):458-461.
[41]TAI Y N, XU M, REN J N, et al. Optimisation of α-terpineol production by limonene biotransformation using Penicillium digitatum DSM 62840[J].Journal of the Science of Food and Agriculture,2016,96:954-961.
[42]ROTTAVA I, TONIAZZO G, CORTINA P F, et al. Screening of microorganisms for bioconversion of (-) β-pinene and R-(+)-limonene to α-terpineol[J].LWT-Food Science and Technology,2010,43:1128-1131.
[43]BICAS J L, FONTANILLE P, PASTORE G M, et al.A bioprocess for the production of high concentrations of R-(+)-α-terpineol from R-(+)-limonene[J].Process Biochemistry,2010,45:481-486.
[44]廉長盛,付冬梅,张俊鹏,等.酒花内生菌Pseudomonas oryzihabitans F0-1转化柠檬烯生成α-萜品醇的研究[J].保鲜与加工,2021,21(12):38-45.
[45]黄金凤,王鑫,梁玉娟,等.油樟内生细菌分离及α-松油醇高产菌株的筛选与诱变[J].食品与发酵工业,2020,46(1):75-81.
[46]何坚,孙宝国.香料化学与工艺学[M].北京:化学工业出版社,1995:77-78.
[47]秦斌,郭继阳,张瑞,等.香芹醇与二氢香芹醇的立体多向性生物催化合成[C]//第十二届中国酶工程学术研讨会论文摘要集,2019:126.
[48]黄庭刚.留兰香油的精制及其香芹酮含量的测定[J].河南化工,1995(11):20-21.
[49]陈连官.留兰香精镏精油的加工工艺与设备[J].香料香精化妆品,1987(3):60-61.
[50]罗运华,刘以红.超临界CO2从留兰香油中萃取香芹酮[J].精细化工,2004(2):119-120,128.
[51]LINDER S M, GREENSPAN F P. Reactions of limonene monoxide. The synthesis of carvone[J].Journal of Organic Chemistry,2002,22(8):243-251.
[52]谢海英,徐丽红,应登宇,等.一种香芹酮的合成方法:中国,201010232407.9[P].2010-11-24.
[53]马晨,刘兴利,赵志刚,等.香芹酮香料合成方法的改进[J].西南民族大学学报(自然科学版),2003(3):308-309,340.
[54]姜志洁,来争争,许清清,等.电化学催化制备香芹酮[J].山东化工,2022,51(3):22-24.
[55]LI J J, LI Z Q, ZI G L, et al. Synthesis, characterizations and catalytic allylic oxidation of limonene to carvone of cobalt doped mesoporous silica templated by reed leaves[J].Catalysis Communications,2015,59:233-237.
[56]MOLINA G, PINHEIRO D M, PIMENTEL M R, et al. Monoterpene bioconversion for the production of aroma compounds by fungi isolated from Brazilian fruits[J].Food Science and Biotechnology,2013,22:999-1006.
[57]BIER M, MEDEIROS A, SOCCOL C R. Biotransformation of limonene by an endophytic fungus using synthetic and orange residue-based media[J].Fungal Biology,2016,121(2):137-144.
[58]TRYTEK M, FIEDUREK J, SKOWRONEK M. Biotransformation of (R)-(+)-limonene by the psychrotrophic fungus Mortierella minutissima in H2O2-oxygenated culture[J].Food Technology and Biotechnology,2009,47:131-136.
[59]ERDTMAN H, HIROSE Y. The chemistry of the natural order cupressales: the structure of nootkatone[J].Acta Chemica Scandinavica,1962,16:1311-1314.
[60]FRAATZ M A, RIEMER S J L, STOBER R, et al. A novel oxygenase from Pleurotus sapidus transforms valencene to nootkatone[J].Journal of Molecular Catalysis B: Enzymatic,2009,61(3):202-207.
[61]YAMAGUCHI T. Antibacterial properties of nootkatone against gram-positive bacteria[J].Natural Product Communications,2019,14(6):1-5.
[62]DANTAS L B R, SILVA A L M, JUNIOR C P S, et al. Nootkatone inhibits acute and chronic inflammatory responses in mice[J].Molecules,2020,25(9):2181.
[63]BEHLE R W, FLOR-WEILER L B, ANUJA B, et al. A formulation to encapsulate nootkatone for tick control[J].Journal of Medical Entomology,2011,48(6):1120-1127.
[64]樊猛,謝建春,孙宝国.同时蒸馏萃取制备富含圆柚酮的柚皮油研究[J].食品科学,2006(12):490-492.
[65]PALMERN-CARREO D M, RUTIAGA-QUIONES O M, VERDE-CALVO J R, et al. Biconversion of (+)-nootkatone by Botryodiplodia theobromae using a membrane aerated biofilm reactor[J].Revista Mexicana de Ingeniería Química,2014,13(3):757-764.
[66]SALVADOR J, CLARK J H. The allylic oxidation of unsaturated steroids by tert-butyl hydroperoxide using homogeneous and heterogeneous cobalt acetate[J].Chemical Communications,2001(1):33-34.
[67]DRAWERT F, BERGER R G, GODELMANN R. Regioselective biotransformation of valencene in cell suspension cultures of Citrus sp.[J].Plant Cell Reports,1984,3(1):37-40.
[68]RO A D, ORTUO A, PUIG D G, et al. Accumulation of the sesquiterpenes nootkatone and valencene by callus cultures of Citrus paradisi, Citrus limonia and Citrus aurantium[J].Plant Cell Reports,1991,10(8):410-413.
[69]SOWDEN R J, YASMIN S, REES N H, et al. Biotransformation of the sesquiterpene (+)-valencene by cytochrome P450cam and P450BM-3[J].Organic & Biomolecular Chemistry,2005,3(1):57.
[70]KASPERA R, KRINGS U, NANZAD T, et al. Bioconversion of (+)-valencene in submerged cultures of the ascomycete Chaetomium globosum[J].Applied Microbiology and Biotechnology,2005,67(4):477-483.
[71]MAI F, HASHIMOTO T, NOMA Y, et al. Highly efficient production of nootkatone, the grapefruit aroma from valencene, by biotransformation[J].Chemical & Pharmaceutical Bulletin,2010,37(17):17185.
[72]RAATZ M A, RIEMER S, STBER R, et al. A novel oxygenase from Pleurotus sapidus transforms valencene to nootkatone[J].Journal of Molecular Catalysis B:Enzymatic,2009,61(3-4):202-207.
