肝细胞癌射频消融术后病灶残留的影响因素
2023-05-30唐建红张凯王丽华陈明高
唐建红 张凯 王丽华 陈明高

[摘要] 目的 分析单发肝细胞癌最大径≤3.0cm患者射频消融术后病灶残留的影响因素。方法 选取2013年1月至2022年6月金华市人民医院收治的肝细胞癌最大径≤3.0cm的患者239例,所有患者均行射频消融术治疗,按照术后病灶是否完全消融分为完全消融组(n=219)与病灶残留组(n=20),采用单因素分析比较两组临床资料的差异,进一步采用二元Logistic回归模型分析术后病灶残留的影响因素。结果 两组的病灶位于肝段间、肝细胞分化程度、肝纤维化程度、Child-Pugh分级以及甲胎蛋白水平方面比较,差异有统计学意义(P<0.05)。二元Logistic回归模型分析结果发现,病灶位于肝段间、肝细胞分化程度、肝纤维化程度以及甲胎蛋白水平≥200μg/L是术后病灶残留的独立影响因素(P<0.05)。结论 分析单发肝细胞癌最大径≤3.0cm患者射频消融术后病灶残留的影响因素,有助于临床医生术前早期制定治疗方案,提高治疗效果。
[关键词] 肝细胞癌;射频消融;残留病灶;影响因素
[中图分类号] R322.4+7 [文献标识码] A [DOI] 10.3969/j.issn.1673-9701.2023.02.012
[Abstract] Objective To analyze the influencing factors of residual lesions after radiofrequency ablation in patients with single hepatocellular carcinoma whose maximum diameter is ≤3.0cm. Methods A total of 239 patients with hepatocellular carcinoma with a maximum diameter of ≤3.0cm admitted to the People's Hospital of Jinhua from January 2013 to June 2022 were selected. All patients underwent radiofrequency ablation. According to whether the lesions were completely ablated after surgery, they were divided into the complete ablation group (n=219) and the residual lesion group (n=20). Univariate analysis was used to compare the differences in clinical data between the two groups, and then the binary Logistic regression model was used to analyze the influencing factors of postoperative residual lesions. Result There were statistically significant differences between the complete ablation group and the residual lesion group in terms of the location of the lesions between liver segments, the degree of hepatocyte differentiation, the degree of liver fibrosis, the Child-Pugh grade and the level of alpha-fetoprotein (P<0.05). The results of binary Logistic regression model analysis showed that the location of lesions between liver segments, the degree of hepatocyte differentiation, the degree of liver fibrosis and the level of alpha-fetoprotein ≥200μg/L were independent influencing factors of postoperative residual lesions (P<0.05). Conclusion To analyze the influencing factors of residual lesions after radiofrequency ablation in patients with single hepatocellular carcinoma with a maximum diameter of≤3.0cm, which will help clinicians to formulate treatment plans early before surgery and improve the treatment effect.
[Key words] Hepatocellular carcinoma; Radiofrequency ablation; Residual disease; Influencing factors
射频消融手术具有简单、微创、患者术后恢复快等特点,对治疗肝细胞癌具有重要作用,特别是对肿瘤最大径直径≤3.0cm患者的疗效及安全性已获得众多认同[1-3]。但因受到肝细胞癌位置、病理、医生技术水平及医院条件等因素影响,射频消融手术难免存在无法对病灶进行完全消融的问题,出现术后病灶残留[4]。姚升娟等[5]研究表明,原发性肝癌经射频消融治疗后病灶殘留率高达14.20%。同时,残留病灶内仍可能存在的少量癌细胞,增加了癌症复发风险,而且还可能通过血液、淋巴道转移到新的组织、器官,最终导致疾病进展[6]。因此,射频消融术前准确评估术后病灶残留风险,及时识别高危患者,对指导临床治疗、改善患者预后的重要性不言而喻。但目前国内对于最大径≤3.0cm的肝细胞癌射频消融术后病灶残留危险因素的研究较为少见,本研究拟从该方面作为切入口进行分析。
1 资料与方法
1.1 一般资料
回顾性分析2013年1月至2022年6月金华市人民医院收治的肝细胞癌最大径≤3.0cm的患者239例,所有患者均行射频消融术治疗,按照术后病灶是否完全消融分为完全消融组(n=219)与病灶残留组(n=20)。纳入标准:①单发病灶,且最大径≤3.0cm;②经术前穿刺活检明确诊断为原发性肝细胞癌;③行射频消融手术治疗;④病灶无肝外转移;⑤年龄≥18岁。排除标准:①肝功能Child-Pugh分级C级;②合并其他恶性肿瘤;③合并心、脑、肺、肾等身体器官严重疾病;④射频消融术前已行手术、微波消融、靶向治疗等其他治疗;⑤术后4~6周无随访记录者。其中,男167例,女72例;年龄42~76岁,平均(60.28±14.63)岁;病灶位置:胆囊旁45例,膈肌旁33例,肝段间51例,肝包膜下方27例,非特殊位置83例;病灶直径0.9~3.0cm,平均(2.07±0.51)cm;Child-Pugh分级:A级157例,B级82例;手术引导方式:超声220例,CT 19例。本研究获得金华市人民医院伦理委员会审批(伦理审批号:IBR-20220042-R)。
1.2 方法
1.2.1 资料收集 从电子病历系统调取并收集患者人口学资料(年龄、性别等)、病灶位置、病灶直径、肝病史、血管侵犯情况、肝细胞分化程度、肝纤维化程度、有无肝硬化、肝功能分级、合并症、手术引导方式(超声或CT)、是否运用人工腹水/胸水辅助手术以及反映肝功能的实验室指标(甲胎蛋白、总胆红素、谷丙转氨酶、谷氨酰转移酶、谷草转氨酶)。其中,肝纖维化程度采用ishak分期评分系统[7]进行评价,总积分0~6分,分值越高肝纤维化程度越严重;肝硬化由医生根据相关指南[8],结合病史、病因、实验室检查、病理学检查等结果判断。
1.2.2 射频消融手术方法 使用美国AngioDynamics公司的Rita型射频消融系统,患者行局部麻醉+静脉麻醉,在明确病灶位置、数量及大小后通过超声或CT引导,在穿刺点切开一小切口并将射频消融针刺入病灶合适位置,伞状开启集束电极针并锁定,选择适宜的消融功率对病灶进行消融(范围需>病灶边缘0.50cm),操作过程中尽量避免漏空现象,消融完成后需再次借助增强CT扫描确认病灶完全消融再结束治疗。术后嘱患者静卧12h,给予常规心电监护、吸氧、保肝以及支持治疗等。
1.3 观察指标
患者行射频消融手术后4~6周使用肝脏增强CT或磁共振成像进行复查,对术后病灶残留判定,并借助mRECIST标准评估消融效果。①病灶残留判定标准:动脉期消融区域病灶出现强化;②完全消融判定标准:动脉期消融区域病灶未见强化,病灶已被消融区域全部覆盖,而且覆盖区域超出病灶边缘0.5cm[9]。
1.4 统计学方法
采用SPSS 26.0统计学软件对数据进行处理分析,计量资料以均数±标准差()表示,组间比较采用t检验,计数资料采用例数(百分比)[n(%)]表示,组间比较采用χ2检验,等级资料采用非参数秩和检验,采用二元Logistic回归模型分析术后病灶残留的影响因素。P<0.05为差异有统计学意义。
2 结果
2.1 临床资料比较
两组在病灶位于肝段间、肝细胞分化程度、肝纤维化程度、Child-Pugh分级以及甲胎蛋白水平方面比较,差异有统计学意义(P<0.05),见表1。
2.2 术后病灶残留的影响因素
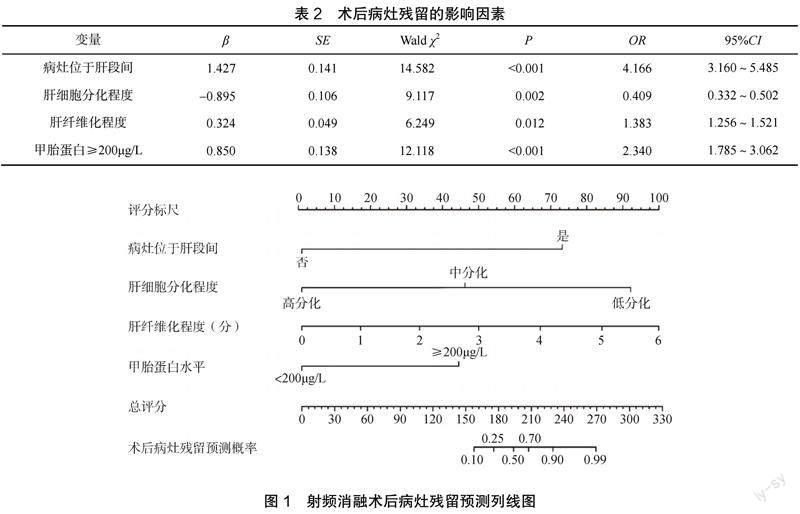
二元Logistic回归模型分析结果显示,病灶位于肝段间、肝细胞分化程度、肝纤维化程度以及甲胎蛋白≥200μg/L是术后病灶残留的独立影响因素(P<0.05),见表2。基于该模型建立列线图,预测术后病灶残留的校准度(χ2=6.187,P=0.486);受试者操作特征曲线下面积为0.886(95%置信区间:0.765~0.930),见图1。
3 讨论
一直以来,射频消融术后病灶残留都是一项值得研究的问题,姚升娟等[5]针对原发性肝癌的研究发现,行射频消融术后病灶残留率高达14.2%。本研究单发肝细胞癌最大径≤3.0cm患者射频消融术后病灶残留率为8.37%,低于上述研究结果,可能与本研究选取的病灶数量、病灶直径、医生术中操作水平、病灶部位等不同有关,而针对既往常规射频消融容易出现残留病灶的特殊部位肝细胞癌(如危险脏器旁等),本研究则借助了人工腹水、胸水等辅助治疗技术,对周围脏器进行隔离保护,并合理设置消融功率,进而降低术后残留病灶风险;同时,超声引导手术的优点为可实时动态查看病灶消融情况,CT引导手术的优点为定位精准,通过合理选择手术引导方式也有助于提高射频消融成功率。但本研究的术后病灶残留率仍然偏高,需引起足够重视。
目前国内指南和专家共识关于特殊部位肝细胞癌的治疗建议相对较少,同时由于病灶位置解剖结构的特殊性和治疗方法的局限性,导致治疗难度大,行射频消融术后残留风险可能更大,特别是病灶位于胆道、大血管附近的肝细胞癌[10-11]。本研究结果发现,病灶位于肝段间是单发肝细胞癌最大径≤3.0cm患者射频消融术后病灶残留的独立影响因素(P<0.05),可能为肝段间病灶与血管相邻导致。因为肝脏分段依据主要为门静脉和肝静脉分布,在对该位置病灶进行射频消融手术时,血管内血流会持续降低消融所产生的温度,导致无法对附近的病灶造成凝固性坏死,进而出现病灶残留,该过程也称为血流“热沉效应”,常常存在于直径≥3.0mm的血管附近,而肝段间刚好有较大血管存在[12-13]。因此病灶位置在肝段间的单发肝细胞癌患者,射频消融术后病灶残留风险也更高。
健康成年人群的血清甲胎蛋白一般<10ng/mL,在肝脏再生或出现癌变时可激活甲胎蛋白相关基因,从而导致血清甲胎蛋白水平增高[14]。既往认为,肝癌的分化程度越低,甲胎蛋白水平越高,肿瘤侵犯微血管的可能性也更大;同时,射频消融术后早期复发以及长期生存也与肝癌患者术前机体高甲胎蛋白水平相关,因此既往常将术前甲胎蛋白作为预测肝癌手术预后的重要指标[15]。本研究结果显示,肝细胞分化程度、甲胎蛋白≥200μg/L是单发肝细胞癌最大径≤3.0cm患者射频消融术后病灶残留的独立影响因素(P<0.05),提示肿瘤分化差、甲胎蛋白水平≥200μg/L的肝细胞癌患者不但需要术前充分评估治疗方案,而且术后还需密切跟踪治疗效果,以便及时增加相应的辅助治疗措施。
肝纤维化是细胞外基质蛋白聚集与慢性肝损害共同作用下的结果,肝纤维化可导致肝星状细胞激活、癌相关成纤维细胞形成等肿瘤微环境异常,对促进肝细胞癌发生、发展具有重要作用[16-17]。杨思维等[18]研究表明,肝纖维化程度是单发肝细胞癌射频消融术后生存期缩短的危险因素。本研究结果显示,肝纤维化程度也是单发肝细胞癌最大径≤3.0cm患者射频消融术后病灶残留的独立影响因素(P<0.05)。分析原因可能为肝纤维化程度通常与机体炎症状态及其持续时间呈正比,可导致癌细胞表型发生变化、血管形成,增殖与侵袭能力增加,进而增加了射频消融手术难度,增高了术后病灶残留风险[19]。
本研究基于多因素回归模型分析结果,进一步构建了预测单发肝细胞癌最大径≤3.0cm患者射频消融术后病灶残留的列线图,该图具有良好的校准度及区分度,有助于在术前及时识别射频消融术后病灶残留的高危患者,并考虑联合其他治疗手段(如立体定向放疗、肝动脉化疗栓塞术等),以减少术后病灶残留率。
此外,还有针对射频消融术后肝癌复发的文献报道提出,病灶大小、Child-Pugh分级、白蛋白等为独立影响因素[15,20]。本研究多因素分析表明病灶大小、引导方法、Child-Pugh等均与单发肝细胞癌最大径≤3.0cm患者射频消融术后病灶残留无关,但本研究样本量偏少,仍有待下一步深入分析。
综上所述,分析单发肝细胞癌最大径≤3.0cm患者射频消融术后病灶残留的影响因素,有助于临床医生术前早期制定治疗方案,提高治疗效果。
[参考文献]
[1]马恒飞, 杨学刚, 周石, 等. 肝动脉化疗栓塞联合射频消融治疗直径≤3cm肝细胞癌的疗效分析[J]. 中华普通外科杂志, 2021, 36(1): 6062.
[2]武世伦, 孔健, 董姝英, 等. 肿瘤相关巨噬细胞极化在肝癌射频消融后残留癌转移中的作用[J]. 中华实验外科杂志, 2020, 37(10): 17931796.
[3]TAN Y, DING X, LONG H, et al. Percutaneous ethanol injection enhanced the efficacy of radiofrequency ablation in the treatment of HCC: an insight into the mechanism of ethanol action[J]. Int J Hyperthermia, 2021, 38(1): 13941400.
[4]张文轩, 尹训波, 孔健, 等. 肝细胞癌不完全热消融后肿瘤发展的研究进展[J]. 中华实验外科杂志, 2021, 38(10): 20812084.
[5]姚升娟, 曲静琦, 曹宇, 等. MRI联合血清miR-204水平对原发性肝癌经皮穿刺射频消融术后疗效及复发的预测价值[J]. 放射学实践, 2022, 37(1): 6267.
[6]黄浩峰, 庞强. 经导管肝动脉化疗栓塞术后原发性肝细胞癌残留状态的增强CT与超声造影比较[J]. 世界华人消化杂志, 2019, 27(18): 11611166.
[7]田爱平, 杨永峰. 慢性肝炎病理学分级分期评分系统比较[J]. 临床肝胆病杂志, 2018, 34(11): 22712277.
[8]徐小元, 丁惠国, 李文刚, 等. 肝硬化诊治指南[J]. 临床肝胆病杂志, 2019, 35(11): 24082425.
[9]GOLDBERG S N, GAZELLE G S, SOLBIATI L, et al. Ablation of liver tumors using percutaneous RF therapy[J]. AJR Am J Roentgenol, 1998, 170(4): 10231028.
[10]沙荣贵, 黄田英, 包仕廷. 特殊部位肝癌的局部治疗[J]. 广东医科大学学报, 2021, 39(2): 233238.
[11]张先舟, 韩风, 聂常富, 等. 人工腹水辅助腔镜超声引导重度肝硬化特殊部位肝癌射频消融术[J]. 中华普通外科杂志, 2019, 34(11): 986987.
[12]KANG T W, LIM H K, CHA D I. Percutaneous ablation for perivascular hepatocellular carcinoma: refining the current status based on emerging evidence and future perspectives [J]. World J Gastroenterol, 2018, 24(47): 53315337.
[13]CASACCIA M, SANTORI G, BOTTINO G, et al. Laparoscopic resection vs laparoscopic radiofrequency ablation for the treatment of small hepatocellular carcinomas: a single-center analysis [J]. World J Gastroenterol, 2017, 23(4): 653660.
[14]龚培贤, 孙涛, 刘金玮, 等. 肝细胞癌根治性切除术患者术前血清AFP、VEGF水平及肿瘤组织Ki-67表达水平与早期复发的关系[J]. 山东医药, 2022, 62(15): 2832.
[15]韩融诚, 马霄虹, 王爽, 等. 肝细胞癌射频消融后早期复发的影响因素分析及列线图预测模型构建[J]. 中华肿瘤杂志, 2021, 43(5): 546552.
[16]BAGLIERI J, BRENNER D A, KISSELEVA T. The role of fibrosis and liver-associated fibroblasts in the pathogenesis of hepatocellular carcinoma[J]. Int J Mol Sci, 2019, 20(7): 1723.
[17]吴美龙, 杨世忠, 于飞, 等肝细胞癌肿瘤微环境的研究进展[J]. 中华肝胆外科杂志, 2019, 25(1): 7073.
[18]杨思维, 张致远, 苏天昊, 等. 肝纤维化对射频消融治疗单发肝细胞癌患者长期预后的影响[J]. 中国介入影像与治疗学, 2021, 18(4): 207211.
[19]罗晓勇, 杜成友, 魏续福, 等. 基于Ishak炎症评分构建的Nomogram肝细胞癌术后复发预测模型的研究[J]. 中华外科杂志, 2018, 56(2): 124129.
[20]龙江, 赵鹏, 杨晓珍, 等. 射频消融治疗中等肝细胞癌5年预后及影响因素分析[J]. 介入放射学杂志, 2019, 28(4): 343346.
(收稿日期:2022–08–23)
(修回日期:2022–09–06)
