基于主题式复习的高三化学课教学实践与思考
——以“高铁酸钾”复习为例
2023-04-16施飞霞
施飞霞
(浙江省海宁市第一中学)
一、问题的提出
高三的复习课内容多、节奏快,在高中课程中起着“回顾与整理、深化与迁移”的重要作用。一轮复习多以“真题剖析—知识整理—方法归纳—迁移运用”的模式展开,环节紧凑,讲练结合,以夯实基础为主。二轮复习则侧重于对重难点知识进行提炼和归纳,完善知识体系,构建解题模型,提升学科核心素养。在教学中,二轮复习要有别于一轮复习模式,避免只是对知识进行简单的重复与再现,而缺乏对知识的整合与提升;避免只是教会学生用碎片化的知识去思考和解决问题,而缺乏对题目的联系与对比。
主题式教学最早由美国教学家哈纳进行首次定义。他提出主题式教学是指围绕具体的一个具体的、有社会意义的主题,展开有目的的学习的过程。本文基于主题式教学模式,在学生已有的知识水平基础上,基于教学目标和学生思维提升的需求,打破传统复习课的局限,确定一个主题,创造一条主线,围绕主线展开复习,实现学生由低阶思维向高阶思维的迁移。
二、设计思路
在金属及其化合物的二轮复习中,学生已经熟悉各物质的相关基础知识,建立了相对完整的知识体系,但对于高铁酸钾这个物质还不太熟悉,学生对于该物质的认识是零散的。同时铁元素除了常见的正二价、正三价,还有正六价,其具有丰富的价态转变关系,是氧化还原反应和离子反应的重要载体,因此有必要对高铁酸钾做一个综合的复习。
以高铁酸钾为主题,以“物质推断—性质分析—制备方法—综合应用”为主线,精选习题,层层递进,逐步深入。既全面复习了高铁酸钾的内容,又从选择、推断、原理、实验等不同题型进行考查,使得复习更全面,更有针对性。通过“高铁酸钾”的复习课,呈现出高三课堂中运用主题式复习模式的流程,探索高三课堂教学的有效模式,完善学生的知识体系,培养学生的思维能力,渗透学科核心素养,切实提高复习课的有效性。
三、教学过程与意图
(一)导入——高铁酸钾的推断
【例1】为探究化合物A(仅含三种元素,摩尔质量为198 g/mol)的组成与性质,设计并完成以下实验:取3.96 g化合物A溶于水中,一段时间后全部转化为B(红褐色沉淀)、C(一种碱)和气体单质D(可使带火星的木条复燃),向溶液中加入100 mL 0.6 mol/L的稀硫酸,再加入含有0.08 mol KOH的溶液,恰好完全反应。过滤,将沉淀洗涤后充分灼烧,得到红棕色固体粉末1.60 g;将所得溶液在一定条件下蒸发可得到一种纯净的不含结晶水的盐。
(1)化合物A的化学式:________;
(2)化合物A与H2O反应的离子方程式为
______________________________。
【参考答案】(1)K2FeO4
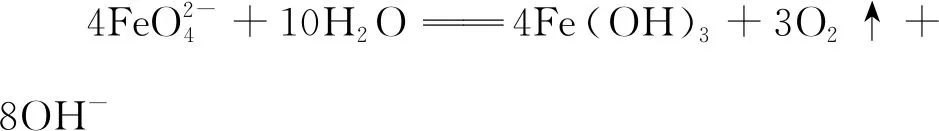
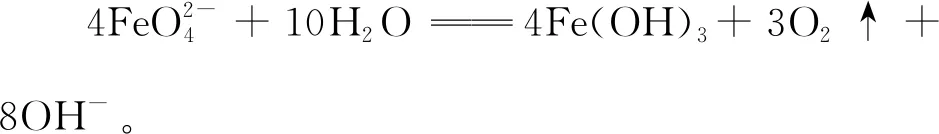
【设计意图】无机推断分析是高考的重难点,选择无机推断题作为高铁酸钾的引入点,通过定性和定量的双重分析,学生可以推导得出高铁酸钾这个物质,进而引出主题,学生通过推断分析得出高铁酸钾,激发了学生对于高铁酸钾的兴趣。第二小问根据题目信息写出高铁酸钾与水反应的离子方程式,自然地过渡到高铁酸钾的性质学习。
(二)深入——高铁酸钾的性质
【知识补充】
1.铁元素的价态
铁元素原子的价电子层结构为3d64s2,一般情况下,铁表现为+2价和+3价,在强氧化剂的作用下,才会反应生成不稳定的+6价(高铁酸盐),从而具有强氧化性。
2.高铁酸钾的性质
高铁酸钾为暗紫色、有光泽的粉末,在198℃以下、干燥空气中稳定存在,加热条件下发生分解反应,极易溶于水,微溶于KOH溶液,在酸性或中性溶液中能快速产生O2,在0~5℃的强碱溶液中稳定存在。高铁酸钾是一种集氧化、消毒、吸附、凝聚、杀菌、去污于一身的新型、高效的多功能水处理剂。
【思考】高铁酸钾具有强氧化性,在使用高铁酸钾进行消毒后,高铁酸钾的产物以什么形式存在呢?请提出猜想,并设计实验验证。
【分析】

实验猜想实验方案猜想1:全部为Fe2+取消毒后的溶液,先滴加硫氰化钾溶液,无明显现象,再滴加少量新制氯水,出现血红色猜想2:全部为Fe3+取消毒后的溶液,滴加硫氰化钾溶液,出现血红色;另取溶液,滴加铁氰化钾溶液,无蓝色沉淀猜想3:Fe2+和Fe3+都有取消毒后的溶液,滴加硫氰化钾溶液,出现血红色;另取溶液,滴加铁氰化钾溶液,出现蓝色沉淀
【思考】高铁酸钾用于杀菌、净水的原理是什么?
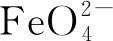
【例2】用高铁酸钾(K2FeO4)对来自河、湖的淡水消毒,是城市饮水处理新技术,下列对高铁酸钾用于饮水处理的分析正确的是
( )
A.K2FeO4在溶液中显酸性,能杀菌消毒
B.在K2FeO4中铁元素显+6价,具有强还原性,能杀菌消毒
C.K2FeO4的还原产物为Fe3+,其易水解产生Fe(OH)3胶体,使水中悬浮物聚沉
D.溶液pH越小,K2FeO4越稳定
【分析】高铁酸钾在溶液中水解显碱性,A不正确;高铁酸钾中铁元素的化合价为+6,具有强氧化性,能杀菌消毒,B不正确;高铁酸钾作氧化剂时,其还原产物为Fe3+,Fe3+水解得到Fe(OH)3胶体,具有强吸附能力可用于净水,C正确;高铁酸钾在酸性条件下不能稳定存在,快速产生O2,D不正确。

( )
A.□处的物质应为KCl
B.每转移1 mol e-,可以得到33 g K2FeO4
C.该反应中铁元素的化合价升高
D.氧化性:Cl2>K2FeO4
【分析】根据化学方程式前后原子守恒可知,□处的物质应为KCl,A正确;根据得失电子守恒可知2K2FeO4~6e-,故每转移1 mol e-,可得到66 g K2FeO4,B不正确;从化学方程式中可知铁元素的化合价从+3升高到+6,C正确;Cl2为氧化剂,K2FeO4为氧化产物,故氧化性:Cl2>K2FeO4,D正确。
【设计意图】从结构到价态到性质,总结归纳高铁酸钾的相关知识。再通过两道选择题用以检测高铁酸钾性质和用途,一道题从净水消毒的角度考查,另一道题从氧化还原的角度考查,从而较全面地考查了高铁酸钾的性质,同时由例3也引出了高铁酸钾的制备方法。
(三)整合——高铁酸钾的制备
【思考】制备高铁酸钾所需要的铁源形式多样,常见的铁源包括单质铁、氧化铁、三价铁盐、二价铁盐等,如图1是制备高铁酸钾的实验装置图,请分析其原理。
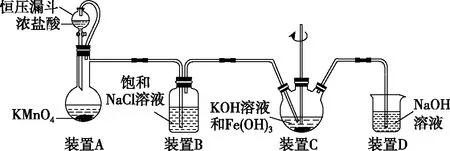
图1
【分析】整个装置利用高锰酸钾和浓盐酸在常温下制备氯气,通过饱和食盐水除去HCl(g)后再通入装置C与KOH溶液反应生成KClO,将Fe(OH)3氧化成K2FeO4,剩余的氯气通入NaOH溶液进行尾气处理。
【思考】装置B的作用有哪些?
【分析】装置B既可以除去氯气中混有的氯化氢气体,又可以观测气体流速,控制通入装置C中的氯气量。
【思考】装置C中除了生成KClO,还可能生成KClO3等,可以采取哪些措施减少副反应的发生?
【分析】采用搅拌,防止局部浓度过大;混入氮气稀释氯气的浓度;将反应置于冷水浴中降低反应温度等。
【例4】高铁酸盐在能源、环保等方面有着广泛用途。湿法、干法制备高铁酸盐的原理如表所示:

湿法强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液干法Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如图2所示:
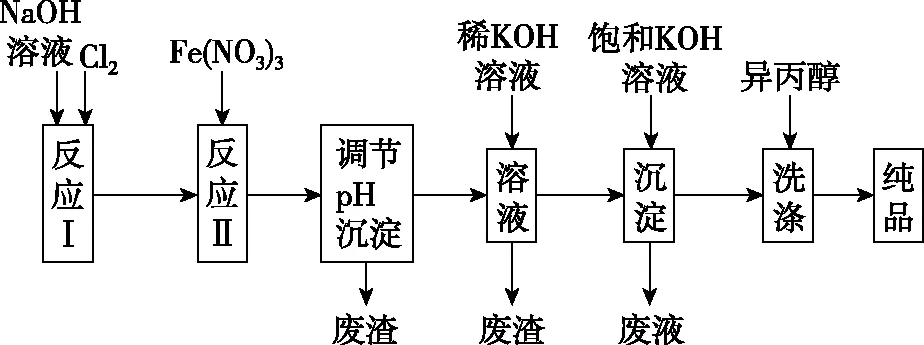
图2
①反应Ⅱ的离子方程式为
;
②加入饱和KOH溶液的目的是
____________。
(2)干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为________。
(3)除湿法、干法制备高铁酸盐外,我国学者还提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如图3所示。
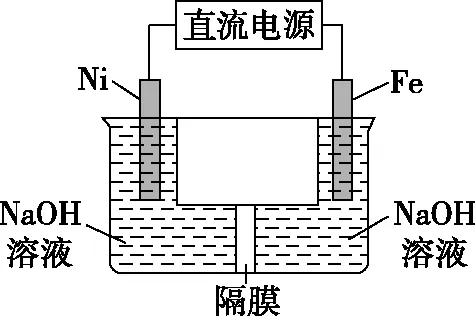
图3
①Ni电极作________(填“阴”或“阳”)极;
②Fe电极的电极反应式:
。

(2)3∶1
【总结】

表1 三种高铁酸钾制备方法比较
【设计意图】从湿法、干法、电解法三种制备方法探究高铁酸钾的制备原理,在复习内容上融入化学反应原理、电化学知识,使得内容和形式更加丰富。以湿法、干法制备高铁酸钾的流程为依托,考查反应方程式的书写和氧化还原反应的相关内容,电解法制备高铁酸钾运用电解池的相关原理,回顾并拓展电化学的知识。对比三种不同的制备方法,干法制备步骤简单,但反应温度难以控制;湿法工艺成熟,但方法复杂;电解法操作简便,但能耗较高,通过对三种制备方法的比较和分析,最终在广度和深度上升华了高铁酸钾的相关内容。
(四)检测——高铁酸钾的应用
【例5】实验小组制备高铁酸钾(K2FeO4)并探究其性质。已知K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)将氯气通入含Fe(OH)3和KOH溶液的混合物中,得到紫色固体A和溶液A。取紫色溶液A,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:

方案Ⅰ取少量a,滴加KSCN溶液至过量,溶液呈红色方案Ⅱ用KOH溶液充分洗涤固体A,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生
①由方案Ⅰ中溶液变红可知a中含有________离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由__________________________(离子用方程式表示)产生。
②方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是
。
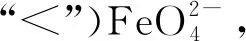
。
。

(2)> 溶液的酸碱性不同
不能说明,方案:向紫色溶液b中滴加过量稀H2SO4,观察溶液紫色快速褪去还是显浅紫色(合理即可)
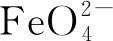

(1)步骤①中发生的离子方程式为
____________________;
(2)原溶液中K2FeO4的物质的量浓度为
________(用含字母的代数式表示)。
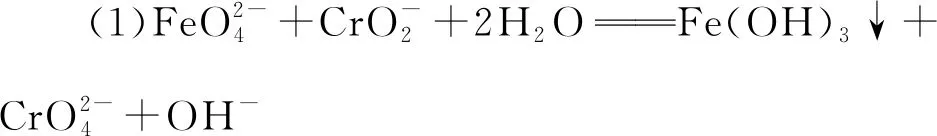


【设计意图】例5、例6考查学生对信息的处理能力和对知识的综合运用能力,涉及陌生氧化还原反应方程式的书写、实验方案的设计、分析计算等内容,同时也有对课堂内容进行延伸,例如比较氯气和高铁酸钾的氧化性,起到了很好的检测作用。这两道题在问题设置上层层递进,多角度考查知识的内在联系,充分体现了化学学科核心素养。
四、反思与感悟
(一)呈现学科特色,发展学科核心素养
重视对教材内容的二次加工与呈现,使教材和试题成为一种动态的课程资源,呈现学科特色。以“物质的推断—物质的性质—物质的制备—物质的应用”为主线复习知识,通过选择题、推断题、原理题、实验题等多种题型从多角度考查知识。高三的二轮复习采取主题式复习模式,立足学生的知识水平,符合学生的认知规律,满足学生的知识需求,让学生更有效地参与课堂教学,落实教学目标,发展学科核心素养。
(二)构建知识网络,培养学生综合能力
“学生保持在记忆里的东西越多,就越有必要进行总结概括,越有必要从具体材料中抽象出真理来,越有必要进行思考和推论。”学生觉得化学难学,很多时候是因为他们的知识是零散的,缺乏知识间的联系。通过主题式复习,以核心物质为中心进行发散,构建知识网络,完善知识体系,活化知识应用。同时也能发挥学生的主体作用,通过不断深入问题,引导学生逐步深入思考,培养学生的思维能力以及提高解决问题的能力。
(三)改变复习模式,促进教师专业发展
在高三的复习课中,教师要改变观念,从“多讲多练”到“精讲精练”,从“一题一讲”到“多题串联”。运用主题式复习模式将同一主题的内容设置一条主线,逐一突破,打造高效课堂,提高复习的有效性。同时对教师自身而言,选择试题、设计主线的过程也是在不断探索、实践和反思的过程,有利于教师专业水平的发展和提升。
