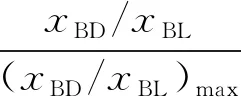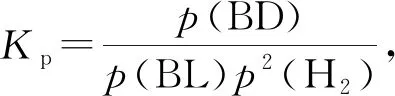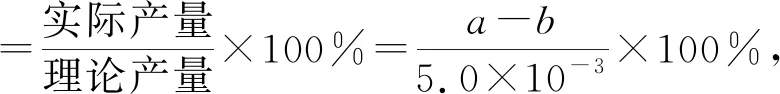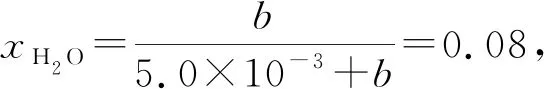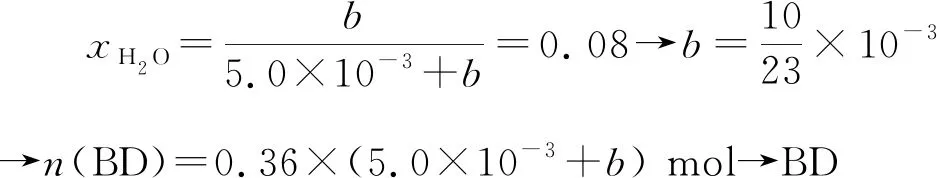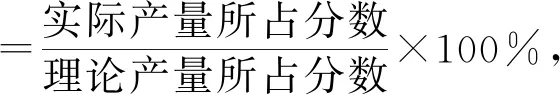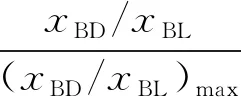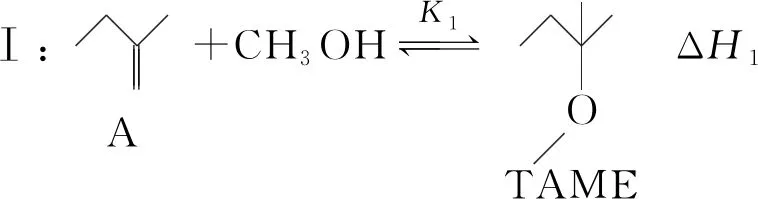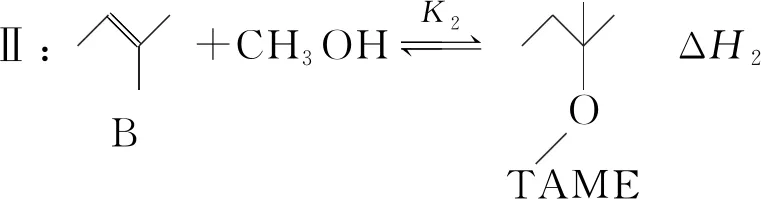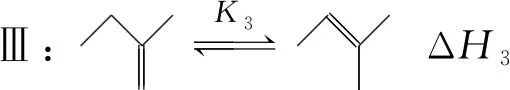研究反应特点,探析解题思路
——以山东高考“化学反应原理综合题”为例
2023-04-16孝衍娇王婷婷
孝衍娇 王婷婷
(山东省北镇中学)
化学反应原理综合题是高考化学中极富挑战性的题目,其综合性强、变式多,难度不言而喻。2022年山东省高考化学试题中化学反应原理综合题以有机反应为载体,且连续反应过程中又包含两个竞争反应,涉及考点有反应热的计算、化学平衡图像分析、平衡常数的计算、产率计算、原因分析,学生纷纷表示“看不懂”“算不对”,化学反应原理综合题真的高不可攀吗?笔者认为并非如此,高考试题给了原本并不复杂的化学反应太多包装,倘若我们认真研究反应的本质及特点,自然可以“去伪求真”,构建解题模型。
接下来笔者将给大家呈现2022年山东卷,20题化学反应原理综合题解题步骤,着重于解题思维的训练与培养过程。
【原题呈现】利用γ-丁内酯(BL)制备1,4-丁二醇(BD),反应过程中伴有生成四氢呋喃(THF)和1-丁醇(BuOH)的副反应,涉及反应如下:
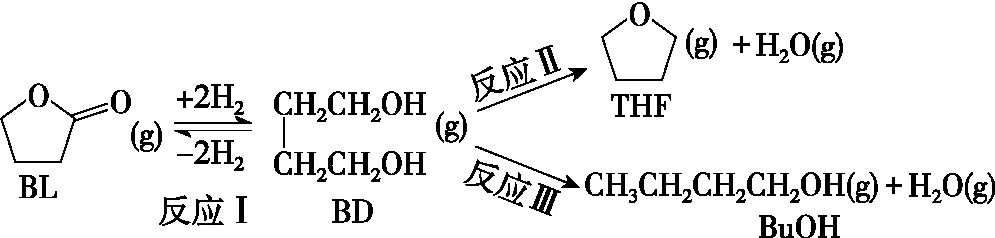
已知:①反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响;②因反应Ⅰ在高压H2氛围下进行,故H2压强近似等于总压。
回答下列问题:
(1)以5.0×10-3mol BL或BD为初始原料,在493 K、3.0×103kPa的高压H2氛围下,分别在恒压容器中进行反应。达平衡时,以BL为原料,体系向环境放热XkJ;以BD为原料,体系从环境吸热YkJ。忽略副反应热效应,反应Ⅰ焓变ΔH(493 K,3.0×103kPa)=________kJ·mol-1。
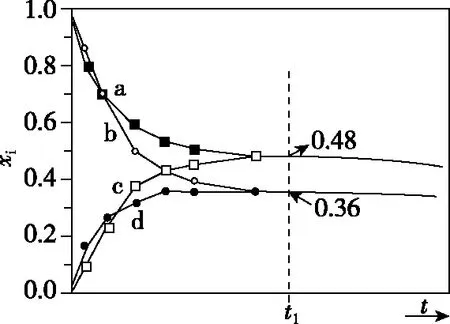
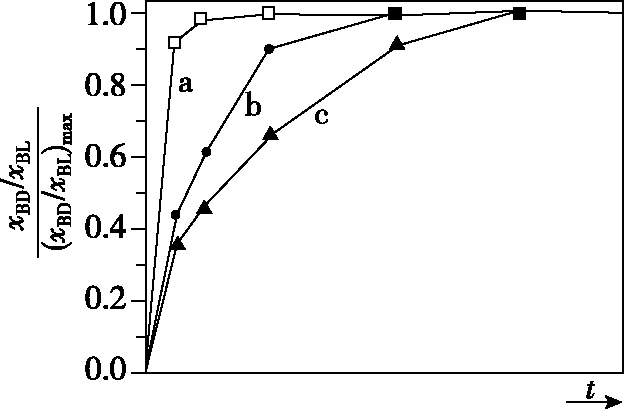
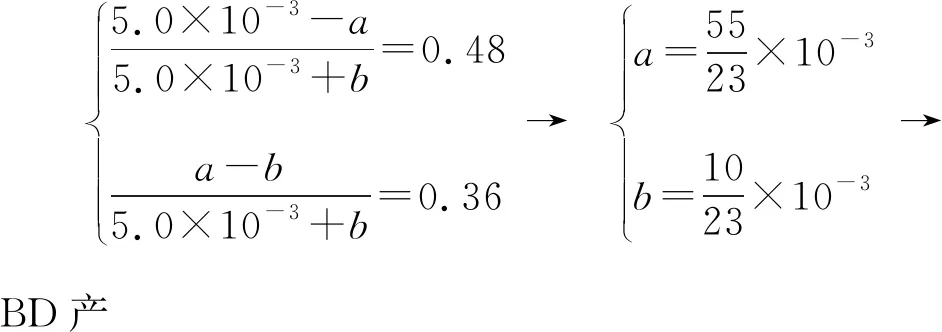
(2)初始条件同上。xi表示某物种i的物质的量与除H2外其他各物种总物质的量之比,xBL和xBD随时间t变化关系如图甲所示。实验测得X 图甲 。 图乙 【分析】本题以1,4-丁二醇(BD)的制备原理为背景进行考查,题干中涉及三个化学方程式,但并不是常见的完整方程式,而是以小流程图的形式给出,给学生以复杂陌生感。通过观察将其转化为熟悉的形式,反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响,即反应Ⅰ是主反应: 图1 平衡常数的计算需要代入各气体组分的分压,而xH2O、BD产率的相关计算过程中由于已知条件②,我们可以将H2看作反应体系的环境,故在平衡体系中除H2后反应又可简化为 这样将反应Ⅱ、Ⅲ看作两个竞争反应,我们观察到其反应特点均为BD等物质的量地转化为某物质与H2O,由此可继续将反应简化为 BD产率的计算是多重平衡体系计算的难点,在多重化学反应体系中各组分的浓度、物质的量和气体的平衡分压等各物理量可以等效为一个数值且相等。 方法一:列“三段式”进行运算,将转化量设成未知数amol、bmol。 起始量(mol) 5.0×10-30 转化量(mol)aa 平衡量(mol) 5.0×10-3-aa 起始量(mol)a0 0 转化量(mol)bbb 平衡量(mol)a-bbb 方法二:三段式与图表信息结合运算 若先分析反应特点求算出xH2O=0.08,再代入求b。 在传统列三段式的基础上充分结合图表信息,减少了计算量。 方法三:结合反应特点,充分利用图表信息 试想,由于题中给出的信息是物质的量占除H2外其他各物种总物质的量的分数,那么是否可以无需计算具体的物质的量,而根据分数去求算? 高考试题体现了“服务选拔”的功能指向,处处渗透着“情境”“素养”“问题”和“知识”,这就对学生提出了更高的要求,不仅要会“解题”,更要学会“解决问题”,从繁杂的题干中找到关键所在,提取有效信息,灵活处理。分析山东省近三年的高考化学题中,化学反应原理综合题均以多重平衡体系为背景,不避热点,规律有迹可循。如2020年山东卷18题,部分题干信息如下: 探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下: 回答下列问题: (1)ΔH3=________kJ·mol-1。 (2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的浓度为________mol·L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为________。 【分析】通过观察以及第一问ΔH3的求算过程可得反应Ⅱ+Ⅲ=Ⅰ,以CO2、H2为原料合成CH3OH,一旦发生反应Ⅱ,相当于Ⅲ转化为Ⅰ,由此,我们就将三个反应简化为两个反应,主反应Ⅰ、副反应Ⅲ,即两重竞争平衡体系,继而列出三段式: 起始量(mol) CO2:1;H2:3;CH3OH、H2O、CO均为0 反应Ⅰ 转化量(mol)a3aaa 转化量(mol)bbbb 平衡量(mol) CO2:1-a-b;H2:3-3a-b;CH3OH:a;H2O:a+b;CO:b 代入便可得出结果。 再如2021年山东卷20题,部分题干信息如下: 2-甲氧基-2-甲基丁烷(TAME)常用作汽油原添加剂。在催化剂作用下,可通过甲醇与烯烃的液相反应制得,体系中同时存在如图反应: 反应Ⅱ+Ⅲ=Ⅰ,由此我们在涉及平衡的计算中仍然认为体系中只存在反应Ⅰ、Ⅲ,大大简化了求算过程。 通过分析,不难发现近几年山东高考反应原理综合题载体均为多重平衡体系,难点为转化率、各组分含量、产率等的计算,多重平衡体系的化学反应看起来盘根错节、眼花缭乱,但细细看来无非是两种关系:竞争反应、连续反应。我们需要分析反应特点,简化反应过程,掌握两重平衡(连续反应、竞争反应)体系中三段式的列式计算,尖锐的问题便在不知不觉中弱化而解。 化学学科从微观角度研究物质,体现了化繁为简、把握根本的大智慧,面对众多化学反应,我们往往把研究重点放在“原理”上,反而忽略了研究对象,因此对于化学反应原理综合题,首要任务是分析其反应特点,知不变,以应万变,成之道也。