安罗替尼+诱导化疗联合同步放化疗治疗晚期鼻咽癌的近期疗效观察
2023-04-10陈浩楠王梦泽姜锋丁忠祥
陈浩楠 王梦泽 姜锋 丁忠祥
鼻咽癌是一种起源于鼻咽部黏膜的肿瘤,我国南方地区发病率相对较高,发病率约为3.26/10万[1-2]。在头颈部癌症中,鼻咽癌是最容易向远处转移的癌症之一[3]。由于鼻咽癌特殊的解剖位置和临床症状,多数患者在就诊时已处于局部晚期,且约75%~85%的鼻咽癌患者存在颈部淋巴结转移[4-5]。既往研究发现,即使使用标准治疗方案——诱导化疗联合同步放化疗,仍有约20%的局部晚期鼻咽癌(locally advanced nasopharyngeal carcinoma,LA-NPC)由于远处转移导致治疗失败,因此如何有效治疗此类患者成为一个研究方向[6]。研究发现,肿瘤细胞内血管内皮生长因子(vascular endothelial growth factor,VEGF)过度表达,促使结构和功能异常的肿瘤血管形成,进而促进肿瘤生长[7-8],67%的鼻咽癌患者存在VEGF 高表达状态[9]。近年来,许多以VEGF、细胞内血管内皮生长因子受体(vascular endothelial growth factor receptor,VEGFR)作为靶点的抗血管生成药物成为肿瘤治疗的研究热点,期待其在相应的“时间窗”内促进异常血管的“正常化”,获得更好的疗效[10]。安罗替尼是一种新型多靶点酪氨酸激酶抑制剂,可以抑制VEGFR、成纤维细胞生长因子受体(fibroblast growth factor receptor,FGFR)、血小板衍生生长 因子受体(platelet-derived growth factor receptor,PDGFR)、干细胞生长因子受体(c-kitproto-oncogeneprotein,c-Kit)、肝 细 胞 生 长 因 子 受 体(hepatocyte growth factor receptor,HGFR)和一种在转化中发生基因重排的原癌基因(rearranged during transfection,Ret)表达,对肿瘤血管的生成、生长具有广泛的抑制作 用[11];目 前 已 在 肺 癌[12]、甲 状 腺 癌[13]、软 组 织 肉瘤[14]、骨肉瘤[15]、神经母细胞瘤[16]等多种恶性肿瘤治疗中开展临床试验,展现了较好的临床效果。目前安罗替尼用于治疗LA-NPC 的报道较少。因此,本研究对LA-NPC 患者在诱导化疗联合同步放化疗的基础上增加安罗替尼抗血管生成治疗,观察疗效及可耐受性,现报道如下。
1 对象和方法
1.1 对象 本研究为一项观察LA-NPC患者服用安罗替尼的疗效与安全性的Ⅱ期临床研究(NCT05232552)。选取2021 年1 至9 月在浙江省肿瘤医院收治的LANPC 患者34 例为研究对象。所有患者肿瘤组织均经病理学检查证实,并治疗前行头颈部体格检查、电子鼻咽镜检查、胸部CT、头颈部MRI、腹部超声、全身骨扫描、PET-CT 和血液学检查评估,根据第8 版美国癌症联合会/国际抗癌联盟(American Joint Committee on Cancer/Union for International Cancer Control,AJCC/UICC)分期标准进行分期。纳入标准:(1)年龄18~70岁;(2)病理证实的初治鼻咽癌患者;(3)分期T3~4N2M0或T1~4N3M0;(4)体能状态评分≤2 分;(5)预计生存预期不少于6 个月;(6)足够的骨髓或肝肾功能储备,预计能顺利完成化疗;(7)能理解本研究,并已签署由国家癌症研究所和参与中心的机构审查委员会批准的书面知情同意书。排除标准:(1)无法行MRI 检查者;(2)入组前曾接受全身治疗,包括化疗或靶向治疗及免疫治疗者;(3)有严重的合并症者,包括心肌梗死、严重的心率失常、严重的脑血管病、溃疡病、精神病和不可控制的糖尿病等;(4)无定期随诊条件者;(5)具有明显大出血倾向者;(6)无法耐受诱导化疗的患者;(7)研究者判断存在其他可能影响临床研究进行及研究结果判定的情况。34 例患者中男28 例,女6 例;年龄<50 岁13 例,≥50 岁21 例;T1分期1 例,T2分期4 例,T3分期16 例,T4分期13 例;N1分期2 例,N2分期13 例,N3分期19 例;AJCC/UICC 分期Ⅲ期4 例,Ⅳ-A 期30 例;存在淋巴结坏死20 例、无淋巴结坏死14 例。
1.2 方法
1.2.1 治疗方案 患者均接受诱导化疗(多西他赛和顺铂)联合同步放化疗+安罗替尼治疗。(1)诱导化疗:多西他赛(扬子江药业集团有限公司,规格:20 mg/支)(75 mg/m2,静脉滴注,d1)、顺铂(齐鲁制药有限公司规格:10 mg/支)(75 mg/m2,静脉滴注,d1)和安罗替尼(正大天晴药业集团股份有限公司,规格:12 mg/粒,国药准字:H20180004;规格:10 mg/粒,国药准字:H20180003;规格:8 mg/粒,国 药 准 字:H20180002)(12 mg,口服,1 次/d,d1~14)治疗,每3 周为1 个周期,治疗3 个周期;(2)同步化疗:诱导化疗结束后3~4 周,顺铂(100 mg/m2,静脉滴注,d1)和安罗替尼(12 mg,口服,1 次/d,d1~14)2 个周期;(3)调强放疗:鼻咽大体肿瘤区计划靶区69 或72 Gy,区域转移淋巴结计划靶区66~69 Gy,鼻咽肿瘤计划靶区63~66 Gy,计划靶区1 60~63 Gy,计划靶区2 51~54 Gy,分30 或33 次进行,放疗1 次/d,每周5 次,调强放疗计划6~6.5 周完成。详细治疗方案参照文献[17]。所有患者在每周期诱导化疗结束后均使用重组人粒细胞刺激因子注射液(杭州九源基因工程有限公司,规格:75 μg/支)2~4 支/次,连用3 d 预防性升白细胞治疗。若患者出现3~4 级不良反应则延期化疗并降低剂量。
1.2.2 安罗替尼剂量调整 当患者出现与安罗替尼相关的2 级以上不可耐受的血液学或非血液学不良反应时,可暂停用药(不超过2 周)直至症状缓解或消失。后一疗程降量为10 mg,再次出现2 级以上毒性反应可再降量为8 mg。若使用8 mg 剂量再出现2 级以上毒性反应或2 周后不良反应仍未恢复至3 级以下,应终止使用安罗替尼。治疗过程中允许多次暂停药物,每次连续暂停时间不得超过14 d。
1.3 疗效及不良反应评估 诱导化疗完成后2 周及同步放化疗结束后4 周,根据实体瘤反应评估标准v1.1[18]对肿瘤反应进行评估,分为为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD),其中客观缓解率(objective response rate,ORR)为CR 和PR 比例之和。患者治疗期间接受常规实验室检查、血液学检查、头颈部MRI 及鼻咽镜检查等,对全身化疗不良反应依据美国国家癌症研究所通用毒性标准3.0 分级。
2 结果
2.1 患者治疗完成情况 34 例患者中,在诱导化疗期间25 例(73.6%)按计划完成3 个周期安罗替尼治疗,8例(23.5%)完成2 个周期治疗,有1 例(2.9%)仅接受1个周期;同步化疗阶段30 例(88.2%)患者完成2 个周期安罗替尼治疗,仅4 例(11.8%)完成1 个周期;按计划完成5 个周期抗血管生成治疗的为23 例(67.6%),3例(8.8%)仅接受3 个周期治疗。在治疗过程中15 例(15/34,44.1%)发生安罗替尼剂量减低,其中5 例(5/15,33.3%)服用剂量减至8 mg。平均每例患者每日接受的安罗替尼剂量为10.4 mg(10.4 mg/12 mg,86.7%),中位剂量为10.8 mg,其中23 例(23/34,67.6%)患者接受了>80%方案剂量的安罗替尼治疗。所有患者均按计划完成3 个周期的诱导化疗序贯2 个周期同步化疗与调强放疗治疗,治疗期间共5 例(14.7%)顺铂减量及1 例(2.9%)多西他赛减量。
2.2 患者近期疗效 患者诱导化疗结束2 周后,经评估10 例(29.4%)鼻咽部病灶达到CR,17 例(50.0%)为PR;颈部淋巴结中20 例(58.8%)达到CR,8 例(23.5%)PR,整体肿瘤ORR 为67.6%,见表1。治疗结束4 周后,鼻咽部病灶及颈部淋巴结CR 率分别为70.6%和73.6%,整体肿瘤ORR 达97.1%。20 例颈部淋巴结坏死患者中阳性淋巴结CR 率为65%,见表2。
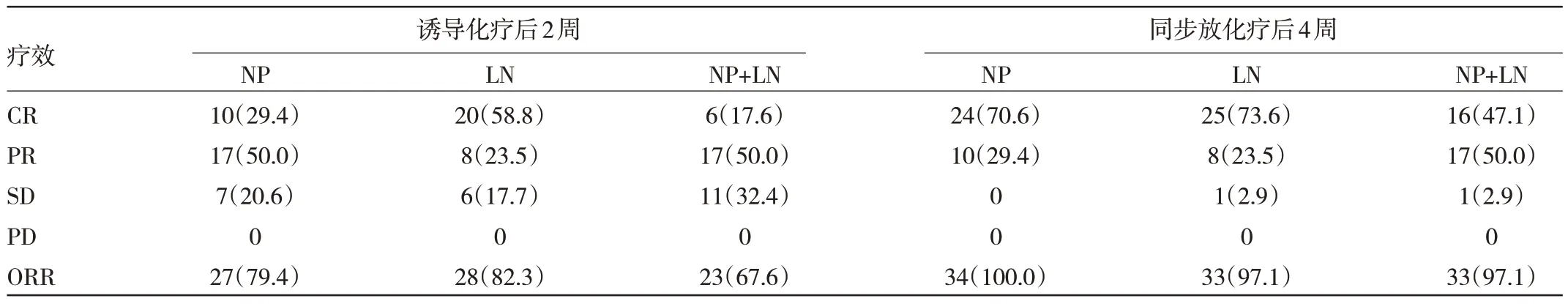
表1 34 例患者近期疗效[例(%)]
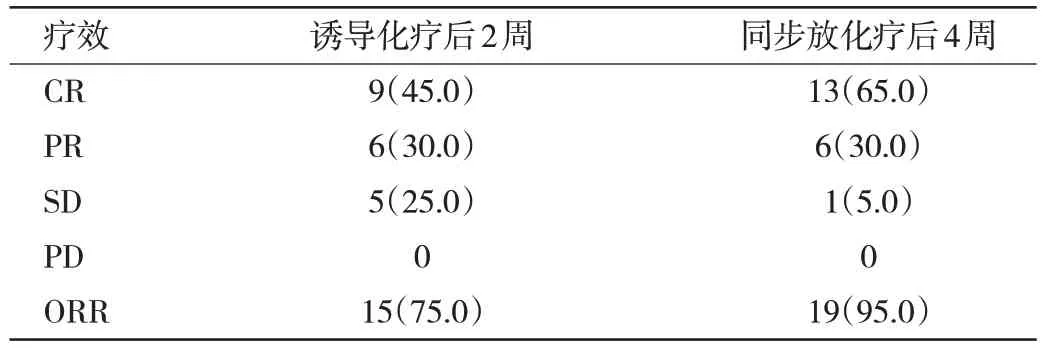
表2 20 例颈部淋巴结坏死患者颈部淋巴结近期疗效评估[例(%)]
2.3 患者不良反应发生情况 患者治疗期间未发生5级不良反应,见表3。所有患者均发生了治疗相关的不良反应。在诱导化疗治疗期间,常见的不良反应是口咽痛38.2%(13/34)和腹泻29.4%(10/34);35.3%(12/34)的患者发生了3~4 级的不良反应,其中最常见的是腹泻(8.8%)和口腔黏膜炎(8.8%)。同步放化疗期间,常见的不良反应是WBC 降低91.2%(31/34)、口腔黏膜炎88.2%(30/34)、口干76.5%(26/34)、口咽痛76.5%(26/34)、疼痛73.5%(25/34);41.2%(14/34)的患者发生了3~4 级不良反应,其中WBC 减少17.6%(6/34)、口腔黏膜炎17.6%(6/34)是常见的3~4 级不良反应。
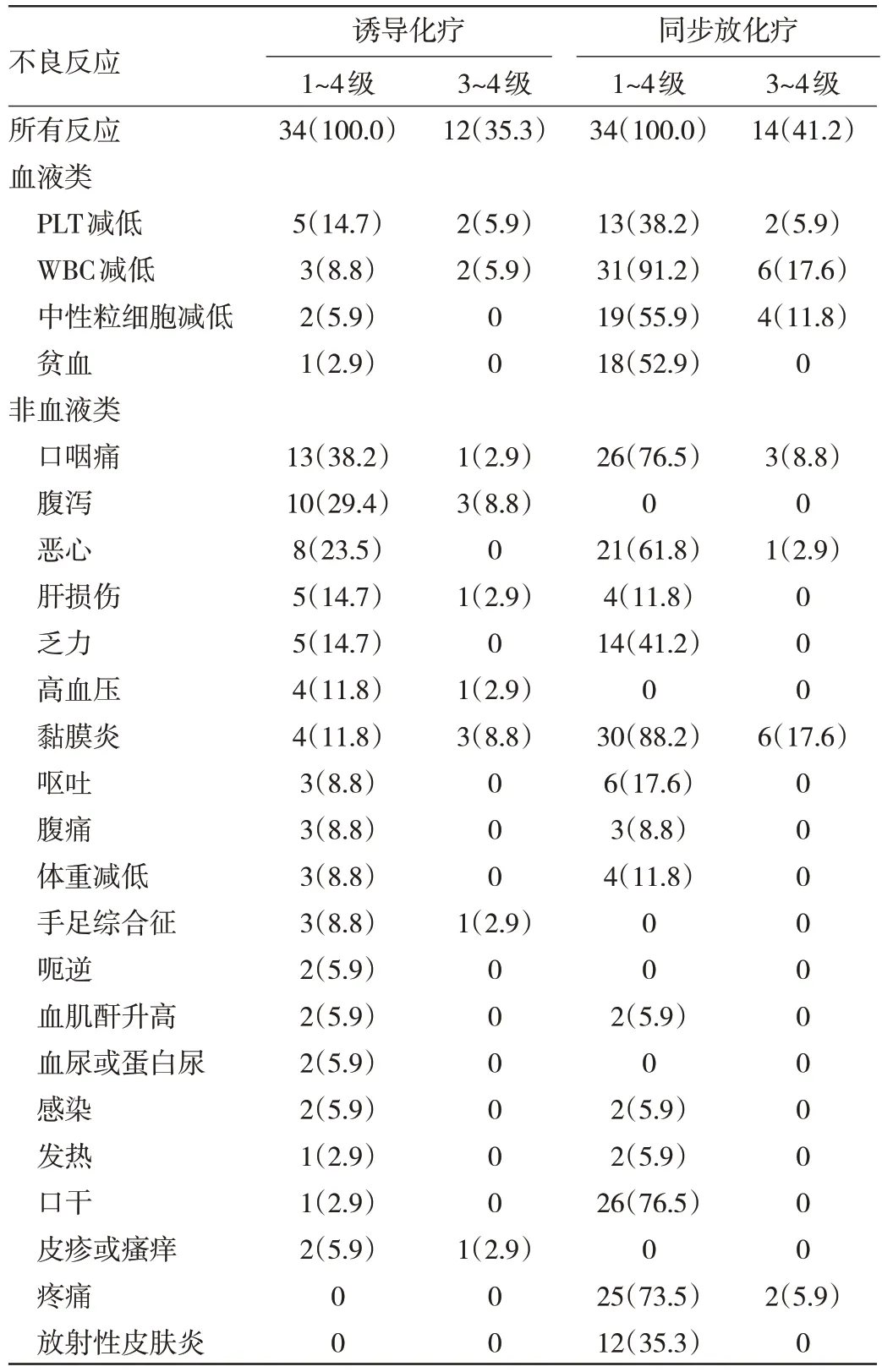
表3 患者不良反应发生情况[例(%)]
在安罗替尼服用期间由于咽痛引起的药物减量最多(3 例,8.8%),骨髓抑制、腹泻、手足综合征及肝损伤各发生2 例(5.9%),剩余由呃逆、异物感、高血压、蛋白尿及胃肠道炎引起。此外,由于消化系统不适导致患者暂停服药发生率最高,为20.6%(7 例),因骨髓抑制3 例(8.8%),其余由乏力、异物感、皮疹及高血压导致各1 例(2.9%)。
3 讨论
本研究探讨了LA-NPC 患者应用诱导化疗联合同步放化疗方案联合安罗替尼抗血管生成治疗的近期疗效及安全性。笔者发现在增加安罗替尼后,没有影响患者的基础治疗,所有患者均按计划完成诱导化疗联合同步放化疗,并且67.6%的患者接受了5 个周期的抗血管生成治疗;诱导化疗及同步放化疗期间未发生治疗相关死亡病例,分别35.3%(12/34)和41.2%(14/34)的患者发生了3~4 级的不良反应,治疗结束后4 周肿瘤ORR 可达到97.1%,这些结果初步证明安罗替尼联合标准治疗在LA-NPC 患者的治疗中是可行的。
自Folkman[19]发现肿瘤细胞会促进非正常的新生血管快速、无序增生,导致肿瘤的快速增长、侵袭和转移,许多以抗血管生成作为靶点的药物研究迅速进展。安罗替尼是一种多靶点受体酪氨酸激酶抑制剂,在抑制肿瘤血管淋巴管生成的同时,调控肿瘤细胞的增殖和转移[20]。一项关于晚期肺腺癌的多中心研究发现安罗替尼能有效抑制肿瘤转移,减少新转移灶的出现;同时在小鼠实验中发现,安罗替尼组肿瘤引流淋巴结出现转移病灶的数量及体积均小于对照组[12]。既往研究证明了抗血管生成在抗肿瘤治疗方面的优越性。
本研究中鼻咽部肿瘤在诱导化疗后2 周和同步放化疗后4 周的评估CR 率分别为29.4%和70.6%,阳性淋巴结CR 率达58.8%和73.6%,相比早前116 例局部晚期鼻咽癌患者接受3 个周期TPF(多西他赛+顺铂+5-氟尿嘧啶)诱导化疗联合铂类同步放化疗治疗研究报道[21],诱导化疗后鼻咽部肿瘤和阳性淋巴结根据Recist 标准评估CR 率分别为24.1%和12.1%,治疗结束3 月后,CR 率分别达到98.3%和97.4%。另一项34 例晚期鼻咽癌患者接受2 个周期TP(多西他赛+顺铂)联合铂类同步放化疗治疗的研究发现,诱导化疗后鼻咽部肿瘤和阳性淋巴结根据WHO 标准评估CR 率为23.5%和53.8%,治疗结束后达到94.1%和80.8%[22]。本研究在诱导化疗后肿瘤CR 率优于既往常规放化疗方案,尤其是对阳性淋巴结。临床研究发现,淋巴管系统是肿瘤细胞向区域淋巴结转移扩散的主要途径[23],淋巴管内皮细胞表达VEGFR-3[24]。安罗替尼可以抑制VEGFR1-3 磷酸化,在一项晚期肺腺癌的安罗替尼应用的研究分析认为,安罗替尼可能在一定程度上抑制肺肿瘤的淋巴管生成从而抑制新的转移,并且在裸鼠腋窝淋巴结附近种植肿瘤细胞的实验中,发现安罗替尼组的肿瘤重量、体积及淋巴管密度均显著小于安慰剂对照组[12]。因此,笔者推测在本组LA-NPC 患者的治疗中安罗替尼同样发挥了显著作用,从而获得优秀的诱导化疗后阳性淋巴结CR 率。此外,早前有研究对399 例鼻咽癌患者在诱导化疗后肿瘤应答率对远期生存的预测价值进行分析,发现CR、PR、SD 这3 个亚组之间在无病生存期、总生存期和局部无复发生存率上均有统计学意义(90.0%比79.0%比58.2%、95.7%比88.7%比70.2%、92.0% 比87.4% 比74.3%)[25]。由此推测本研究患者较高的CR 率有可能进一步转化为生存获益。Lee 等[10]在鼻咽癌标准治疗联合贝伐单抗的研究中获得了较高的2 年无远处转移生存率(90.8%)、总生存率(90.9%)。因此推测本组患者联合多靶点药物安罗替尼的治疗,可能也会获得较好的生存结果。
更重要的是在本研究中,笔者发现在常规放化疗基础上结合安罗替尼,颈部淋巴结坏死患者阳性淋巴结CR 率高达65%,相较于既往Liang 等[26]的鼻咽癌患者伴颈部淋巴结坏死在标准治疗结束的CR 率(59.5%,97/163)有所提升。而颈部淋巴结坏死是鼻咽癌患者不良预后的危险指标,因此这一联合方案对于预后不佳的CNN 患者更具有吸引力。
本研究发现LA-NPC 患者标准治疗联合安罗替尼抗血管生存治疗是安全可行的。一项安罗替尼治疗甲状腺髓样癌的研究中,32.3%(20/62)的患者药物剂量减低,其中10.0%(2/20)减量至8 mg[13]。而本研究中患者治疗剂量减低(15/34,44.1%)得更多,并且其中33.3%(5/15)的患者剂量减至8 mg,因此下阶段研究可能建议10 mg 作为标准治疗剂量,使更多的患者耐受安罗替尼的不良反应。此外,研究中发现安罗替尼会引起较高的口咽痛及乏力发生率,尽管以1~2 级为主,但患者仍感到无法耐受,经过减量或暂停服药均可缓解,治疗过程中仅发生1 例3 级高血压。本研究中以骨髓抑制、消化系统反应更为常见,但3~4 级的不良反应发生率相较其他标准治疗[21-22]并没有明显升高。
本研究存在一定的局限性,这是一项Ⅱ期临床研究,样本量较小,入组患者存在一定的选择性偏差;其次患者随访时间短,目前临床可见较好的近期疗效,但是远期生存获益目前尚不确定,未来需要更大样本量的研究来明确。
综上所述,LA-NPC 患者采用安罗替尼+诱导化疗联合同步放化疗治疗可以获得较好的肿瘤反应率,特别是在诱导化疗治疗后肿瘤CR 率较高,并且不良反应可以耐受。
