耦合TiO2 直接苛化的黑液半焦与石油焦水蒸气共气化特性研究
2023-03-11王贵金袁洪友靳立军胡浩权
王贵金,袁洪友,靳立军,李 扬,杨 赫,胡浩权,*
(1. 大连理工大学化工学院 煤化工研究所 精细化工国家重点实验室,辽宁 大连 116024;2. 中国科学院广州能源研究所 中国科学院可再生能源重点实验室 广东省新能源和可再生能源重点实验室,广东 广州 510640)
黑液是碱法制浆蒸煮过程产生的废液,其固形物中包含约60%的有机物和约40%的无机物[1],其中,有机物主要包括木质素、半纤维素和糖类化合物等,无机物主要为Na2CO3等[2]。根据联合国粮食及农业组织(FAO)统计,2019 年,中国原生纸浆产量约为1635 万吨(干基)。按照每吨纸浆(干基)附带产生1.7 吨黑液固形物估算,黑液固形物产量约为2780 万吨,其中所蕴含的能量超过1000 万吨标准煤。因此,实现黑液这一特殊生物质资源的高效能源化利用对于减少煤炭等化石能源的消耗有积极意义。目前,黑液一般采用传统碱回收工艺进行能源化利用和资源回收。在该工艺中,黑液首先在碱回收炉中燃烧以利用其有机物中的能量,用于生产蒸汽和电力;燃烧残余的无机物通过后续的石灰石苛化工段进行回收,供制浆蒸煮工段循环利用[3,4]。该工艺目前使用广泛,但其中涉及石灰石高温煅烧的高能耗环节,对当前制浆企业践行能耗“双控”产生阻碍,制约企业的低碳绿色发展。
为优化基于直接燃烧法的黑液碱回收工艺,前人开展了许多替代技术的研究。其中,TiO2直接苛化的黑液气化工艺引起了广泛关注[5-8]。在该工艺中,黑液中的有机物在气化炉中转化为富含H2和CO 的合成气(式(1)-(3))(该气体既可用作洁净燃气,也可催化合成高附加值燃料和化学品);其中的Na2CO3则与TiO2同步发生脱碳反应生成钛酸钠(mNa2O·nTiO2)(式(4));mNa2O·nTiO2通过后续的水解反应器,在温和条件下重新生成NaOH 碱液供制浆工艺循环使用[9-11]。
研究表明,TiO2直接苛化的黑液气化工艺取消了高能耗的石灰石苛化段,其发电效率可提高至30%-35%,达到传统碱回收工艺(10%-14%)的2-3 倍[12]。与未添加TiO2的黑液气化过程相比,添加TiO2可有效提高气化反应速率,同时抑制熔融物生成[13]。Zeng 等[14]在700-900 ℃研究了TiO2直接苛化的硫酸盐黑液半焦空气气化,发现有机碳可实现完全转化,过程几乎无Na 元素损失。
综上,TiO2直接苛化的黑液气化工艺优势明显,可作为黑液碱回收替代工艺进一步开发。然而,黑液自身热值较低(10-12 MJ/kg,干基),其单一气化能源输出相对有限,过程工艺经济性仍有待提高。基于此,在黑液气化过程中引入补充燃料是可选方案之一。
石油焦是石油化工过程中延迟焦化的副产物,具有热值高、灰分低、不熔融和成本低等特点[15]。从其自身属性,有望成为黑液气化辅助燃料的备选。目前,石油焦产量逐年递增,将其通过气化进行能源化利用引起了广泛关注[16,17]。石油焦中碳的有序化程度较高、孔隙结构极不发达、氧和矿物含量低,致使其气化反应活性低[18]。因此,石油焦单独气化一般需要较高的反应温度和较长的停留时间[19,20],这对设备材料、设计和运行成本均提出较高要求,严重影响石油焦气化的工业化进程。从提高石油焦气化反应性角度出发,石油焦与煤/生物质的共气化成为研究热点[21,22]。研究表明,在石油焦与煤/生物质共气化过程中,由于煤/生物质灰分中富含碱金属和碱土金属(AAEMs)等,石油焦的气化反应性得到有效提高,原料间也呈现出显著的协同效应[23-25]。另外,黑液自身富含碱金属Na 等,一些学者将其引入到石油焦气化过程[26-28]。对石油焦CO2气化反应动力学的研究发现,添加黑液可显著降低石油焦气化反应的活化能[29]。于德平等[30]借助流化床反应器研究了石油焦水蒸气气化特性,发现黑液的添加可在保证气化反应活性不变的情况下,使气化温度降低200 ℃。Zhang 等[31]关于黑液催化石油焦水蒸气气化的研究也表明,在900 ℃,添加10%的黑液可使石油焦气化完成时间从120 min 缩短至40 min左右。上述的研究证实了在以石油焦为主体的反应体系中,黑液是催化石油焦气化反应的有效催化剂。但从考虑黑液自身的能源化利用和碱回收问题,以石油焦为补充燃料,以TiO2为苛化剂的三元混合物共气化过程的研究仍属空白。
基于此,本研究旨在考察TiO2直接苛化条件下黑液半焦与石油焦的水蒸气共气化特性。通过物理机械方式制备黑液半焦-TiO2-石油焦三元混合物,借助热重分析仪(TGA)和固定床装置进行恒温水蒸气气化实验,同时采用GC、XRD 和SEM等分析方法,对共气化过程的热失重行为、产气特性和残余固体特性等进行系统分析,以期能够为黑液气化工艺的优化、石油焦的能源化利用以及黑液碱回收提供新的技术支持。
1 实验部分
1.1 样品制备与分析
本研究采用的黑液固形物来源于新疆某麦草碱法制浆企业,石油焦由广东某燃料公司提供。两种原料均为粒径≤150 μm 的均匀颗粒。实验前,首先在N2保护下,分别将黑液固形物和石油焦在600 ℃下进行30 min 热解,制得黑液半焦(Black Liquor Char,BLC)和热处理后的石油焦(Petroleum Coke,PC)。待冷却后,存于干燥器中备用。BLC和PC 的元素分析和工业分析数据列于表1。其中,样品的C、H、N 和S 元素含量采用元素分析仪(Vario EL cube,Elementar,Germany)进行测定,其工业分析参照GB/T 28731—2012 进行。由表1可知,BLC 中灰分含量和氧含量均较高,其热值相对较低。与BLC 相反,PC 的灰分含量极低,含碳量高,O/C 较低,其热值约为BLC 的5 倍。因此,BLC 与PC 两者具有良好的原料互补性。采用原子吸收分光光度计(AAS,Z-2000,Hitachi,Japan)对BLC 中碱金属元素Na 和K 的含量进行了分析,其含量分别为24.6%和3.2%。

表1 黑液半焦与石油焦的基本分析Table 1 Fundamental analyses of the black liquor char (BLC) and petroleum coke (PC)
在本研究中,除BLC 和PC 外,通过干法机械混合方式制备了三组样品:一是根据先前的报道[13],参照脱碳反应(式(4))的化学计量比,按照BLC与TiO2质量比5∶3 配备两者的混合物,记为BT;二是按照BLC 与PC 质量比1∶1 配备两者的混合物,记为BP;三是以BLC、TiO2和PC 质量比5∶3∶5 配备三元混合物,记为BTP。
1.2 实验装置与方法
为确定各样品的热失重行为和水蒸气气化反应性,用同步热分析仪(STA 449 F3,NETZSCH,Germany)进行了热重分析实验。实验中每次测试的样品用量为(30.0 ± 0.1) mg,采用高纯N2(99.999%)作为载气,流量设定为40 mL/min,以8 ℃/min 的加热速率从室温升至850 ℃;当温度达到850 ℃时开始通入水蒸气,水的流量设定为5 mL/h;在850 ℃下恒温60 min。
为确定水蒸气气化产气特性和残余固体特性,采用固定床(水平管式炉)进行了系列实验。固定床反应装置与流程如图1 所示。反应管为石英材质,其内径50 mm,长度1100 mm;样品舟为310S 不锈钢材质,其料槽长宽高分别为100 mm ×25 mm × 5 mm。
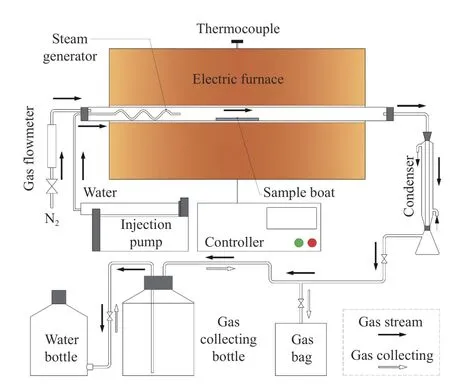
图1 水蒸气气化实验装置流程图Figure 1 Flow diagram of experimental apparatus for steam gasification
实验中,采用高纯N2作为载气,流量设定为250 mL/min;使用注射泵进行水的供给,水的流量为2 mL/min;液态水经由置于石英管内的不锈钢螺旋管汽化为连续稳定的水蒸气;反应区温度设定为850 ℃,样品舟在反应区的停留时间为12 min;每次实验的样品用量为(3.0 ± 0.1) g。反应产生的气体首先经过冷凝管冷却其中的水蒸气,然后通过下游的集气瓶进行收集。集气瓶中预先装满水,产气体积由排水法累计确定。气体经气袋收集后,通过气相色谱仪(GC 7890A,Agilent,USA)分析其主要组分。气化残余固体通过X 射线衍射仪(XRD,X’Pert Pro MPD,PANAlytical,Netherlands)进行物相鉴定,Cu-Kα 射线为辐射源,波长λ=0.15432 nm,轴电压40 kV,轴电流40 mA,扫描10°-80°,扫描步长0.017°。另外,借助扫描电子显微镜(SEM,S-4800,Hitachi,Japan)对气化残余固体进行微观表面形貌的表征,扫描成像的加速电压为2.0 kV。
水蒸气气化产气中各气体组分的产率为单位质量固体反应物气化后所生成的对应气体组分在标准状况下的体积,其计算公式如下:
式中,Yi,V为i组分(H2、CO、CO2和CH4)的气体产率,单位为mL/g;Vi为i组分在标准状态下的体积,单位为mL;W0为参与气化反应的固体原料的质量,单位g;Vtotal为排水法测得的产气总体积,单位为mL;vi为GC 测得的i组分的体积分数,单位%。
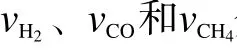
气化过程的碳转化率基于气化反应前后固体中碳元素的质量平衡计算,公式如下:
其中,xC为碳转化率;WC,ini.和WC,res.分别为初始反应物和气化残余固体中碳的质量,可基于反应物和残余物的质量以及它们各自的含碳量(由EA 测得)计算。
本研究反应装置采用电加热管式炉,其与实际工业应用的气化炉存在显著差别,所涉及气化过程的能源输入输出情况差异大,不宜采用诸如冷煤气效率等常规气化炉性能评价参数。在此,提出了能源输出比(Energy Output Ratio,EOR)的概念,用于评价过程的能源转化率。其定义为水蒸气气化过程输出产气的化学能与输入固体原料的化学能的比值,计算公式如下:
其中,LHVgas为单位体积气体的低位热值,单位kJ/m3,计算公式如式(7)所示;Ygas,V为产气总体积产率,单位m3/kg;LHVini.为单位质量初始固体反应物的低位热值,单位kJ/kg。由EOR 的定义可知,其与气化过程的能源转化率呈正比。
2 结果与讨论
2.1 基于 TGA 的热化学转化行为分析
2.1.1 TG-DTG 分析
图2 为TiO2直接苛化的BLC 与PC 在850 ℃恒温水蒸气共气化(a)和升温共热解(b)过程的TG-DTG 曲线。在此,BTPtheo是基于BT 和PC 单独气化和热解的TG-DTG 数据,假设BT 和PC 两者相互独立、互不影响,加权平均计算得到。PC的TG-DTG 数据见先前的研究报道[28]。图2 所示的TG-DTG 曲线均已作扣除TiO2处理,各样品在恒温水蒸气气化段初始时刻也已作归一化处理。
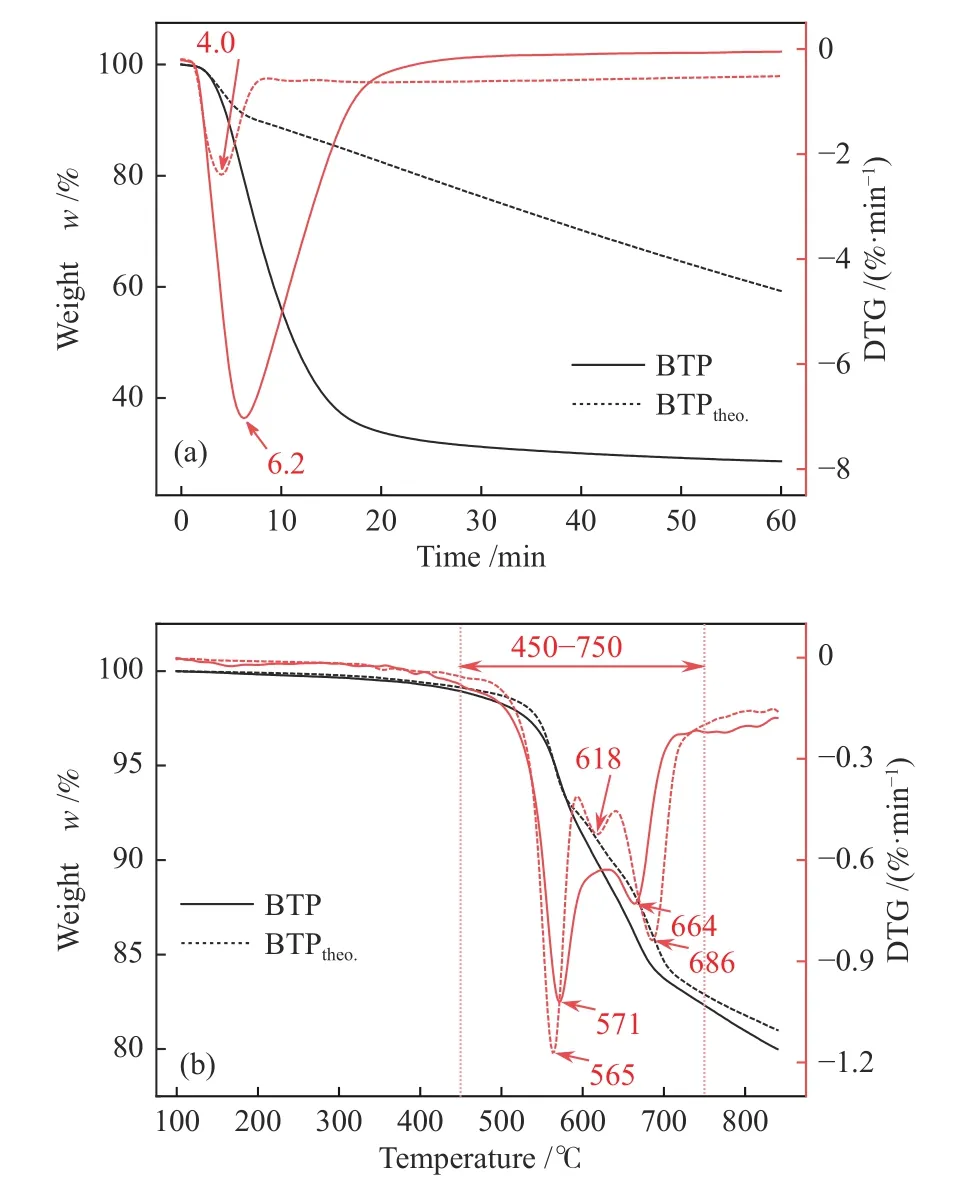
图2 TiO2 直接苛化的BLC 与PC 的850 ℃恒温水蒸气共气化(a)及升温共热解(b)的TG-DTG 曲线Figure 2 Experimental and calculative TG-DTG curves of isothermal steam co-gasification at 850 ℃ (a) and nonisothermal co-pyrolysis (b) of BTP
由图2(a)可知,在850 ℃、60 min 的恒温水蒸气气化过程中,BTP 在约6.2 min 时刻达到最大气化反应速率(记为Rmax)7.0%/min,在30 min 时气化反应基本完成,之后样品质量趋于稳定;BTPtheo在初始的0-8 min 反应速率相对较快,在4.0 min左右达到Rmax≈ 2.4%/min,随后以约0.6%/min 的速率缓慢反应,在60 min 时刻持续失重。对比发现,BTP 和BTPtheo在恒温段的气化行为差异显著,表明BT 与PC 在共气化过程中并非相互独立。在850 ℃、60 min 条件下,PC 自身的水蒸气气化反应速率和进行程度均相对较低[28],因此,在BT 和PC 共气化过程中,PC 是限制反应速率和反应进行程度的瓶颈。研究表明,Na 盐是半焦气化反应的有效催化剂[17,32,33]。BT 中富含Na盐,可有效催化BLC 和PC 中有机碳的气化反应,尤其是使PC的气化反应活性显著增强。因此,BTP 混合燃料体系能够实现完全气化,且Rmax可达加权平均值的2.9 倍。
从图2(b)可知,在升温热解过程中,BTP 在571 和664 ℃附近存在两个显著的失重峰。根据先前的研究可知[13],这主要是TiO2与BLC 中Na2CO3之间的脱碳反应(式(4))所致。该反应为固-固反应,颗粒间接触程度将影响反应速率。当混合PC 时,TiO2与BLC 中Na2CO3之间的接触程度发生变化,因此,BTP 和BTPtheo在升温热解过程中的失重峰大小和位置存在差异。从TG-DTG 曲线变化趋势可知,脱碳反应可在450-750 ℃升温基本完成,表明PC 颗粒的存在不会阻碍这类反应的进行和完成。为确定脱碳反应的发生,同时明确BTP 中Na 的存在形态在升温热解过程中的变化,对850 ℃热处理(N2保护)前后的BTP 进行结构表征,相应的XRD 谱图和SEM 照片分别如图3 和图4 所示。从图3 可看出,热处理前的BTP 中存在未反应的TiO2,含Na 化合物主要以Na2CO3和Na-Si 二元物质(aNa2O·bSiO2)为主。其中,aNa2O·bSiO2主要包括Na2SiO3(Na2O·SiO2)、Na4SiO4(2Na2O·SiO2)和Na6Si2O7(3Na2O·2SiO2)等。850 ℃热处理之后,BTP 的XRD 谱图中的衍射峰以mNa2O·nTiO2为主。其中,T1 为4Na2O·5TiO2,T2为2Na2O·5TiO2,T3 为Na2O·3TiO2。从SEM 结果可知(图4),850 ℃热处理前后BTP 的微观形貌差异显著。热处理前,其微观表面堆积着均匀粒径大小的TiO2颗粒;热处理后,其微观表面则存在具有规则几何形貌的较大粒径尺寸的晶体。这表明,经由850 ℃的升温热处理,BTP 中初始的TiO2与Na2CO3已转化为mNa2O·nTiO2。因此,在后续的恒温气化段,BTP 中PC 气化反应活性增强主要是源于mNa2O·nTiO2的促进作用。也就是说,mNa2O·nTiO2是BT 与PC 在共气化过程中提高反应速率的促进剂,是两类原料间产生协同效应的桥梁。
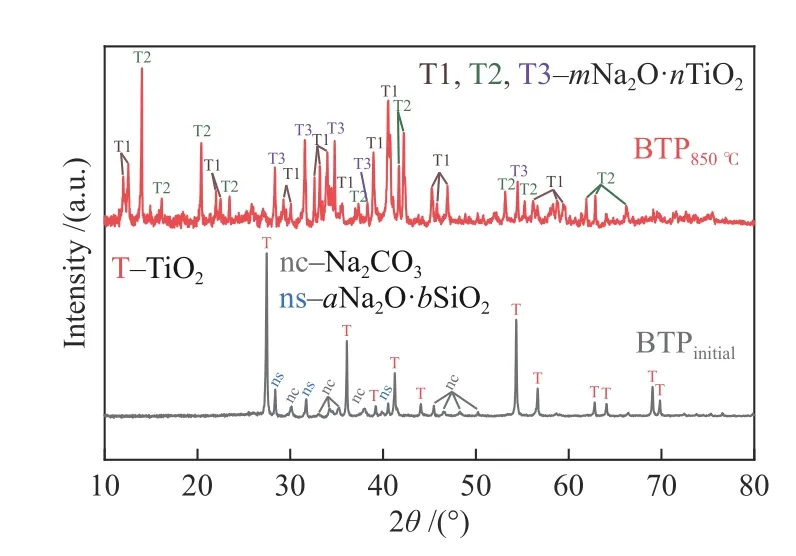
图3 850 ℃热处理前后BTP 的XRD 谱图Figure 3 XRD patterns of BTP before and after heat-treatment at 850 ℃

图4 850 ℃热处理前(a)后(b)的BTP 的SEM 照片Figure 4 SEM images of BTP before (a) and after(b) heat-treatment at 850 ℃
2.1.2 过程无机盐损失分析
Na 作为制浆过程的重要元素,在BLC 完成能源转化后需进行回收以循环利用[34]。根据BLC 单独升温热解与恒温水蒸气气化的TG-DTG 曲线可知[28],其在升温热解和恒温水蒸气气化过程中不仅涉及有机碳的转化,同时还会伴随含Na 无机盐的损失。Na 盐的损失不仅会降低制浆工艺的经济性,同时也会造成严重的设备腐蚀,影响设备运行稳定性和安全性。因此,控制BLC 在热化学转化过程中(热解与气化)的无机盐损失率很有必要。
依据各样品在100-850 ℃升温段和850 ℃恒温段(60 min)的TG 曲线可计算全过程的无机盐相对损失率,计算公式如下:
式中,Lossinorg代表无机盐相对损失率,Mloss,exp代表从TGA 实验得到的失重量,Mloss,theo为假设固体样品在热化学转化过程中挥发分完全释放、直接苛化反应完全进行(式(4))、碳转化率100%和无机盐损失率0 时的理论失重量,Mash为样品中初始的灰分质量。
图5 显示了BLC、BP、BT 和BTP 四组样品在热化学转化(热解+气化)过程的无机盐损失结果。可以发现,BLC 单独转化时的无机盐损失显著,相对损失率高达68.7%;BLC 与PC (BP)共转化过程的无机盐损失有所下降,相对损失率为54.9%;当添加TiO2时(BT),无机盐相对损失率显著下降至1.6%;在三元混合物(BTP)的热化学转化过程中,无机盐损失也得到有效控制,相对损失率为9.4%。

图5 不同添加物对BLC 热化学转化过程无机盐损失的影响Figure 5 Effect of various additives on inorganic salts loss during the thermochemical conversion process of BLC
图6 和图7 分别为850 ℃热处理前后BLC 的XRD 谱图和SEM 照片。由图6 可知,BLC 中的含Na 物质主要以Na2CO3和Na-Si 二元化合物为主。在升温加热过程中,BLC 中的Na2CO3会与有机碳发生碳热还原反应(式(11)、(12)),期间伴随Na 蒸汽的挥发与损失[35]。从XRD 谱图中在28°-32°、36°-40°和45°-49°等的衍射峰强度的变化可知,热处理使BLC 中Na2CO3和Na-Si 二元化合物的分布发生变化。观察图7 的SEM 照片可知,初始状态的BLC 微观表面分散分布着有机碳(表面光滑)和无机盐颗粒,两者之间分离度良好;而850 ℃热处理之后,BLC 微观表面均匀附着熔融的无机盐颗粒,看不到明显的有机碳存在。这表明,Na2CO3在恒温水蒸气气化过程中为熔融态,这将导致Na的飞溅损失加剧。源于碳热还原反应(式(11)、(12))的发生以及Na2CO3的熔融与飞溅,BLC 及BP在整个热化学转化过程中的无机盐损失较为严重。当添加TiO2时,BLC 中的Na2CO3在升温过程中发生脱碳反应(式(4)),碳热还原反应(式(11)、(12))得到抑制,高温易熔融的Na2CO3在热解升温段即转化为高热稳定性的mNa2O·nTiO2(图3),BT 及BTP 在整个热化学转化过程的无机盐损失率随之大幅下降。由此可知,添加TiO2是控制高温蒸汽环境中Na 元素损失的有效措施。
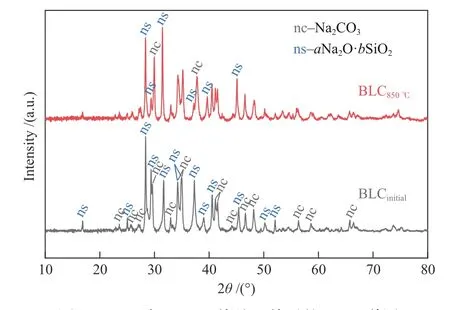
图6 BLC 在850 ℃热处理前后的XRD 谱图Figure 6 XRD patterns of BLC before and after heat-treatment at 850 ℃

图7 BLC 在850 ℃热处理前(a)后(b)的SEM 照片Figure 7 SEM images of BLC before (a) and after (b) heattreatment at 850 ℃
2.2 产气特性及过程能源转化分析
图8 为不同固体反应物850 ℃水蒸气气化产气中各组分的产率(a)、产气组成特性(b)、有效气组分(H2+CO)含量及其产率(c)和产气热值(d)。其中,BTPtheo基于BT 和PC 单独气化的数据加权平均计算得到,PC(包括在此列出的BLC)单独气化的产气特性可见于先前的报道[28]。H2/CO 会影响气化产气作为合成气利用时的催化转化路径,是评价合成气组成特性的常规参数之一[36]。通过反应方程式((1)-(4)、(11)-(12))以及(逆)水煤气变换反应(式(13))可知,过程中可燃气体组分CO 和不可燃气体组分CO2竞争释放,可能影响产气组成。为此,同时采用H2/CO 和CO/CO2这两个参数评价产气组成特性。
如图8(a)所示,各样品气化产气的主要组分为H2、CO 和CO2,另外还有少量的CH4。与BLC相比,BT 的CO 和CO2产率上升,分别提高28.7%和21.4%。添加TiO2后,BLC 中的Na2CO3发生脱碳反应(式(4)),从而促使生成更多的CO2。CO2的原位释放也会促进Boudouard 反应(式(3))和逆水煤气变换反应(式(13))的进行,进而生成更多的CO,同时导致H2产率小幅下降。从产气组成特性,BT 产气的H2/CO 显著下降,CO/CO2则变化较小(图8(b))。另外,由于BT 产气中CO2含量的增大,有效气含量和产气热值分别下降3.7%和2.9%(图8(c)、8(d))。BTP 的H2、CO 和CO2产率分别为1527、532 和466 mL/g;与BTPtheo相比,提高幅度分别达119.7%、208.7%和77.1%;产气的H2/CO 减小,CO/CO2上升。由于H2和CO 产率的大幅提高,BTP 气化产气中有效气组分含量及产率分别达到81.1%和2059 mL/g,气体热值也达到9343 kJ/m3,相对于其理论值分别提高6.8%、137.3%和5.5%。
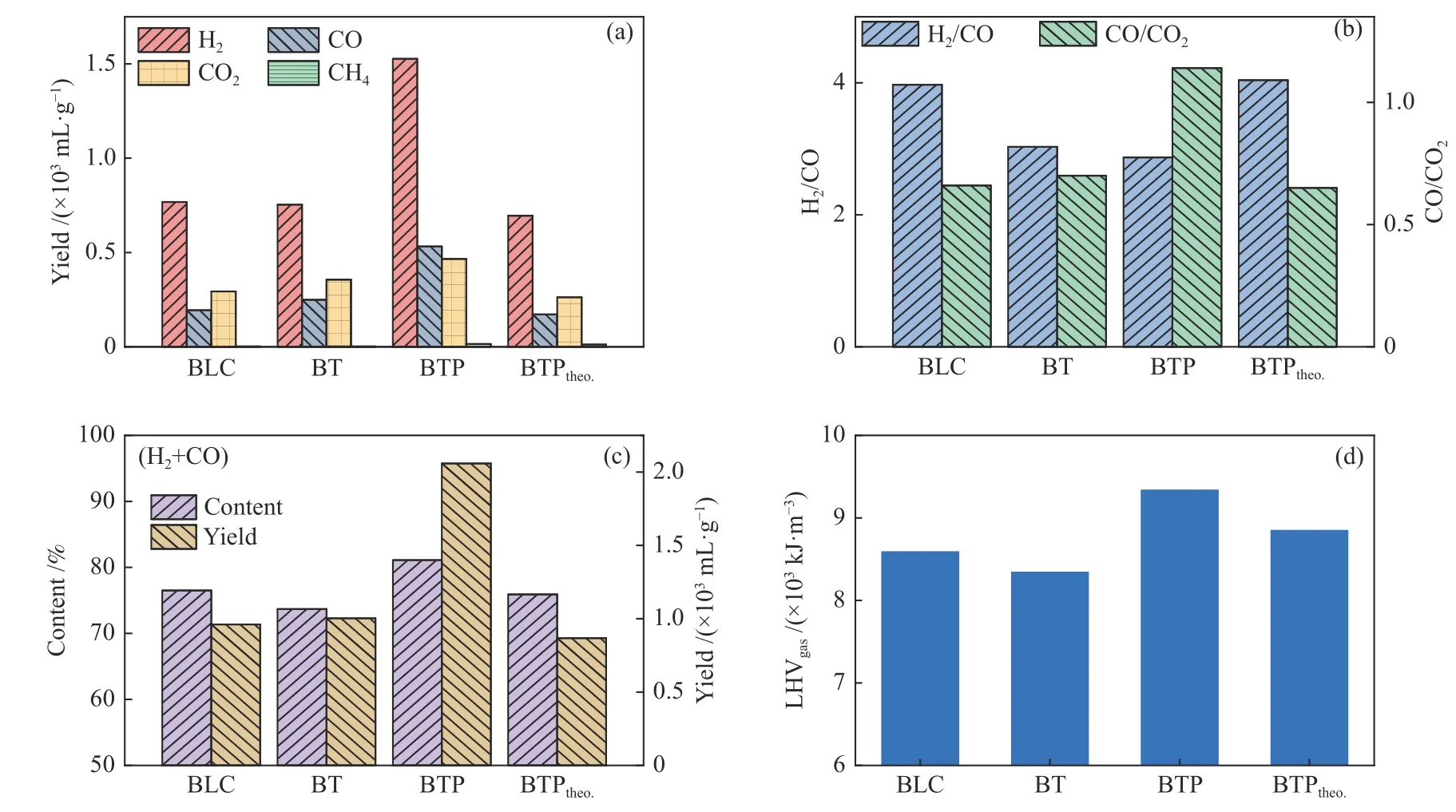
图8 不同固体反应物水蒸气气化的产气特性Figure 8 Characteristics of gaseous products from steam gasification of different solid reactants
图9 为各反应物水蒸气气化过程的碳转化率(xC)和能源输出比(EOR)。如图9 所示,添加TiO2可有效提高BLC 的碳转化率和能源输出比,提升幅度分别为20.7%和4.6%。这表明,与BLC 中Na2CO3对有机碳气化的催化作用相比,mNa2O·nTiO2的促进效果更优。与BTPtheo相比,BTP 的碳转化率和能源输出比分别提高61.6%和135.4%,达到95.0%和1.13。

图9 不同固体反应物水蒸气气化的碳转化率(xC)和能源输出比(EOR)Figure 9 Carbon conversion (xC) and energy output ratio(EOR) for the steam gasification of different solid reactants
PC 单独气化的气体产率相对较低,H2、CO 和CO2的产率仅为637、95 和170 mL/g,碳转化率和能源输出比也仅为18.6%和0.25,均处于较低水平[28]。因此,在BT 和PC 共气化过程中,PC 是限制性因素。从产气特性和能源转化效率,BTP 的实验值与理论值差异显著,表明在三元混合物(BTP)共气化过程中,mNa2O·nTiO2可作为有效的催化剂,显著提高PC 的气化反应性,在提高碳转化率和能源输出比的同时,生成更多的H2、CO 和CO2。
综上所述,在TiO2直接苛化条件下,BLC 水蒸气气化的碳转化率和能源输出比均得到显著提升。然而,脱碳反应会伴随生成更多的CO2,导致BLC 产气中有效气组分含量及气体热值下降,对产气品质产生不利影响。BT 与PC 共气化可突破PC 低气化反应性限制,使得三元混合体系的气体产率、气体热值、碳转化率和能源输出比都达到较高水平;同时可有效调控产气组成,提高产气品质。
2.3 气化残余固体特性分析
气化残余固体(Gasification Residue,GR)不仅需要通过碱回收进行循环利用,而且影响实际气化反应器的设计。因此,其结构特性值得关注。图10 和图11 为各样品水蒸气气化残余固体的SEM 照片和XRD 谱图。

图10 850 ℃水蒸气气化残余固体的SEM 照片Figure 10 SEM images of the steam gasification residues at 850 ℃
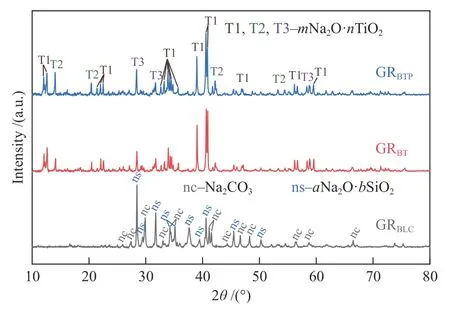
图11 850 ℃水蒸气气化残余固体的XRD 谱图Figure 11 XRD patterns of the steam gasification residues at 850 ℃
SEM 结果显示,BLC 水蒸气气化残余固体已熔融为一体,其微观表面密集分布着细小的无机盐颗粒;添加TiO2后,气化残余固体的熔融现象得到有效抑制,BT 和BTP 的残余固体均呈颗粒状堆积分布,其微观表面也均赋存着具有规则几何形貌的晶体存在,尽管形状和尺寸有所不同。结合图11 的XRD 谱图可知,BLC 熔融为一体主要是其中高温易熔融的Na2CO3所致;而BT 和BTP气化残余固体中以热稳定性较高的mNa2O·nTiO2为主,有助于维持固体颗粒流动性,便于后续的碱回收。由于mNa2O·nTiO2的生成源于固-固反应,颗粒间的接触程度将影响其形成与类型分布[10]。因此,在混合PC 的情况下,mNa2O·nTiO2的生成与分布受到影响,BT 和BTP 气化残余固体中mNa2O·nTiO2晶体的微观形貌存在差异。
3 结 论
在850 ℃的TiO2直接苛化黑液半焦(BLC)和石油焦(PC)水蒸气共气化过程中,体系中的mNa2O·nTiO2可有效促进有机碳的气化反应,使得耦合过程(BTP)与独立的TiO2直接苛化BLC 气化(BT)和PC 气化加权平均(BTPtheo)相比,表现出显著的协同效应。具体如下:
BTP 的最大气化反应速率为7.0%/min,为BTPtheo的2.9 倍,气化反应由60 min 未完成缩短至约30 min完成。BTP 在热化学转化过程中的无机盐损失得到有效控制,相对损失率约9.4%。BTP产气中有效气组分(H2+CO)含量及其产率分别为81.1%和2059 mL/g,气体热值为9343 kJ/m3,相对于BTPtheo分别提高6.8%、137.3%和5.5%,产气品质得到改善。与BTPtheo相比,BTP 的碳转化率和能源输出比分别达95.0%和1.13,相对提高61.6%和135.4%。此外,通过添加TiO2将高温易熔融的Na2CO3转化为高热稳定性的mNa2O·nTiO2,使BTP 气化残余固体维持为流动性颗粒,利于后续的碱回收。综上,TiO2直接苛化的黑液与石油焦共气化工艺是优化单一黑液气化和石油焦气化的有效技术手段,可为不同类型碳资源互补耦合能源化利用以及黑液碱回收提供新的解决方案。
