磺胺嘧啶银/超强碱协同催化CO2/醇耦合反应选择性制碳酸二甲酯
2023-03-11张福灿吉可明张建利宋清文
张福灿,刘 平,张 侃,吉可明,*,张建利,赵 亮,宋清文,*
(1. 中国科学院山西煤炭化学研究所 煤转化国家重点实验室,山西 太原 030001;2. 中国石油大学(北京) 重质油国家重点实验室,北京 102249;3. 宁夏大学 省部共建煤炭高效利用与绿色化工国家重点实验室,宁夏 银川 750021)
CO2是一种丰富、无毒的碳资源,将其转化为化学品是绿色化学的一个重要目标。到目前为止,CO2已成功转化为各种化学品,例如有机碳酸酯、聚碳酸酯、含氮衍生物、甲酸和醇类等[1-5]。但由于CO2的化学惰性,其转化过程面临很多问题,其中,高选择性合成化学品研究在学术界和工业界都备受关注。
DMC 分子中含有丰富的官能团,可作为羰基化或甲基化试剂,代替光气、氯甲烷等剧毒物,用于多种精细化学品的合成。DMC 也可作为电解液,保证低温下的锂电池具有高活性。DMC 分子中的氧含量为53%,可以代替甲基叔丁基醚作为一种绿色汽油添加剂,使汽油得到更高的辛烷值。此外,DMC 还是一种性能优良的溶剂,在农药和涂料中有着广泛的应用[6]。
目前,工业上合成DMC 的主要方法是两步酯交换法和甲醇尿素法。两步酯交换法路线长且原料环氧化物价格高;甲醇尿素法过程中产生的氨气易与DMC 发生副反应,导致产物选择性低[7]。综合考虑,制备DMC 最理想的方法是甲醇和CO2直接反应,其路线最短、原料廉价且副产物只有水,符合绿色化学生产要求(式(1))。然而,直接合成法在热力学上是不利的,一般的催化策略DMC收率往往在5%以下[8]。另外,甲醇和CO2的反应为可逆反应,基于平衡移动原理,移除体系水分将促进平衡向右移动,因此,使用脱水剂将有助于提升反应效率,目标产物收率在很大程度上得到提高。其中,使用缩酮[9]和2-氰基吡啶[10]作为脱水剂最有效,收率达到90%以上。但脱水剂的使用量很大,至少为当量试剂。因此,也相应得到大量的副产物。另外,脱水剂的使用,在很大程度上引进了更多更复杂的副反应,会进一步降低目标产物的选择性。总之,发展新的脱水策略与催化体系是工业界与学术界亟需解决的问题。
α-羟基酮是一类重要的精细化学品合成中间体,研究报道炔丙醇和水分子在CO2氛围下能够高效水合生成α-羟基酮(式(2))[11,12]。另外,通过炔丙醇、CO2与亲核试剂三组分耦合反应的方式,不经过脱水历程,而是间接地将“水分子”转移至炔丙醇分子中。基于此,Zhou 等[13]设计了热力学有利的炔丙醇、邻二醇和CO2三组分反应,炔丙醇做为“间接脱水剂”,高收率得到环状碳酸酯和α-羟基酮(式(3))。Zhou 等[14]以生物质基多元醇作为亲核试剂,合成了手性多环碳酸脂和α-羟基酮。Hu 等[15]报道以一元醇作亲核试剂,定量得到多种非对称性链状碳酸酯。
发展新型高效催化方法以及提升催化效率是未来亟需研究的方向。醇类和CO2的多组分串联反应历程一般是炔丙醇首先与CO2羧化环化得到中间体α-亚甲基环状碳酸酯,然后α-亚甲基环状碳酸酯再与醇发生醇解反应得到目标产物。炔丙醇、一元醇和CO2三组分反应将耦合一元醇类和CO2羰化反应以及炔丙醇水合反应,但不经过水分子产生与再反应的历程。本团队[16]报道了α-位双烷基取代基的炔丙醇(2-甲基-3-丁炔-2-醇)、甲醇和CO2三组分耦合反应(式(4)),由于相当一部分原料停留到了中间产物,致使DMC 合成效率较低。研究发现[17],不同结构的炔丙醇对CO2和炔丙醇的羧化环化反应结果有很大影响。其中,α-位单取代的炔丙醇作底物时,所得单取代基的α-亚烷基环状碳酸酯产物热力学不稳定,反应最终得到链状碳酸酯。基于此笔者猜想,使用α-位单取代的炔丙醇做底物,不稳定的α-亚烷基环状碳酸酯中间产物会与甲醇进行快速后续反应,同时因该中间体参与的副反应会更少,DMC 收率和选择性会同时得到提高。
近年来,银催化剂在炔丙醇与CO2参与的转化反应中表现出色,如AgI/KOAc 协同催化的炔丙醇和CO2的环化羧化反应,在常压条件下α-亚烷基环状碳酸酯收率最高为99%[18];磺胺嘧啶银/季铵盐协同催化的炔丙醇、邻二醇和CO2三组分反应,在常压和80 ℃的条件下多种环状碳酸酯收率超过90%[19]。笔者推测,通过设计金属银协同催化体系,将会有效促进炔丙醇(α-单取代)、甲醇和CO2三组分反应。
1 实验部分
1.1 实验材料
CO2购自山西宜虹气体有限公司(纯度99.99%)。实验中所有原材料均没有经过进一步纯化,直接用于实验。磺胺嘧啶银(98%)、碳酸银(99.9%)、AgCl(99.9%)、AgI(99%)、AgOAc(99.5%)、Ag3PO4(Ag,77%)、CoCO3(99%)、ZnCl2(99.95%)、ZnBr2(99.9%)、ZnI2(99.99%)、Zn(OAc)2(99.99%)、CuBr(99%)、NiBr2(99%)等金属化合物,1-辛炔-3-醇(98%)、3-甲基-1-戊炔-3-醇(98%)、2-甲基-3-丁炔-2-醇(98%)、2-丁炔-1-醇(97%)、1-戊炔-3-醇(>97%)、3-丁炔-2-醇(98%)、2-甲基-3-壬炔-2-醇(97%)等炔丙醇,1,8-二氮杂二环十一碳-7-烯(DBU)、1,5,7-三氮杂二环[4.4.0]癸-5-烯(TBD)、1,5-二氮杂双环[4.3.0]-5-壬烯(DBN)、1,1,3,3-四甲基胍(TMG)等购自阿拉丁试剂有限公司。甲醇(AR)购自天津市风船化学试剂科技有限公司。乙腈(分析纯)购自福晨化学试剂有限公司。乙酸乙酯(分析纯)、甲苯(分析纯)购自天津市光复科技发展有限公司。N,N-二甲基甲酰胺(DMF)和甲苯(分析纯)购自国药集团化学试剂有限公司。石油醚购自天津市科密欧试剂有限公司。
1.2 实验方法
1-辛炔-3-醇、甲醇和CO2的反应在装有磁子的25 mL 的高压反应釜中进行。首先,将1-辛炔-3-醇(630 mg,5.0 mmol)、甲醇(320 mg,10.0 mmol)、DBU(228 mg,1.5 mmol)和磺胺嘧啶银(358 mg,1.0 mmol)依次加入高压反应釜。拧紧釜盖螺纹封闭反应釜,通过充气口连接高压气瓶。室温下充入5 MPa CO2气体后,将反应釜放在预热好的油浴锅中并开始计时。反应过程中无需补气,记录初始压力。反应既定时间后,冷却降温并小心释放出反应釜中的气体,尾气使用DMF 吸收并回收检测。用针式过滤器滤出产物中的催化剂,与吸收尾气的溶液一同移至容量瓶中,用DMF 定容至10 mL,待分析(代表性谱图及分析见图SI.1)。数据结果计算公式定义如下:
DMC 收率和3-羟基-2-辛酮收率分别基于甲醇和1-辛炔-3-醇计算:
1.3 分析方法
产物的收率和底物的转化率使用气相色谱仪进行分析定量。使用定量注射器采样离线分析法,用FID 检测器检测,色谱工作站记录分析数据。色谱型号为BEIFEN 3420A,毛细管柱(DB-17,30 m ×0.25 mm × 0.25 μm),气相色谱升温程序:50 ℃恒温保持5 min,以10 ℃/ min 升温至200 ℃并保持10 min,然后以5 ℃/ min 升温至280 ℃,在此温度下保持30 min。NMR 光谱由Bruker AVANCE III 400MHz光谱仪测定并记录,其中,1H NMR 在400 MHz 使用CDCl3(7.26)作溶剂测得,13C NMR 在100.6 MHz使用CDCl3(77.00)作溶剂进行测试。
1.4 α-羟基酮核磁表征
1H NMR (400 MHz,CDCl3)δ3.50 (s,1H),2.14(t,J=5.3 Hz,3H),1.79-1.73 (m,2H),1.39 (s,1H),1.26 (s,6H),0.84 (t,J=6.4 Hz,3H)。13C NMR(100.6 MHz,CDCl3)δ210.3,77.6,33.7,31.8,25.4,24.6,22.7,14.2。
2 结果与讨论
2.1 催化组分研究
首先,以1-辛炔-3-醇(1a)、甲醇(2a)和CO2三组分耦合反应为模板反应进行研究。以DBU 为共催化剂,在一定条件下合成DMC(3a)和3-羟基-2-辛酮(4a),反应方程式见表1。不使用任何催化剂时,反应不发生(表1,序号1)。随后,考察了一系列过渡金属盐(银盐、锌盐等)对反应的影响(表1)。从整体上看,与2-甲基-3-丁炔-2-醇、甲醇和CO2三组分反应相比[16],该三组分反应DMC 的选择性更好,DMC 与4a 的收率差距更小。
以CoCO3和NiBr2为催化剂时(表1,序号3-4),DMC 和4a 收率很低,且1a 的转化率均低于仅用DBU 的催化体系(表1,序号2),这说明,CoCO3和NiBr2对此反应体系几乎无活性。对一系列的锌盐作出考察发现,锌盐对该三组分体系活性较差,ZnBr2作为催化剂时DMC 收率最高,为33.1%。另外,使用锌盐作催化剂时,1a 的转化率均超过98%,但DMC 选择性不高,且收率与4a 收率差异较大,这说明,大部分原料转化并停留在中间体阶段。
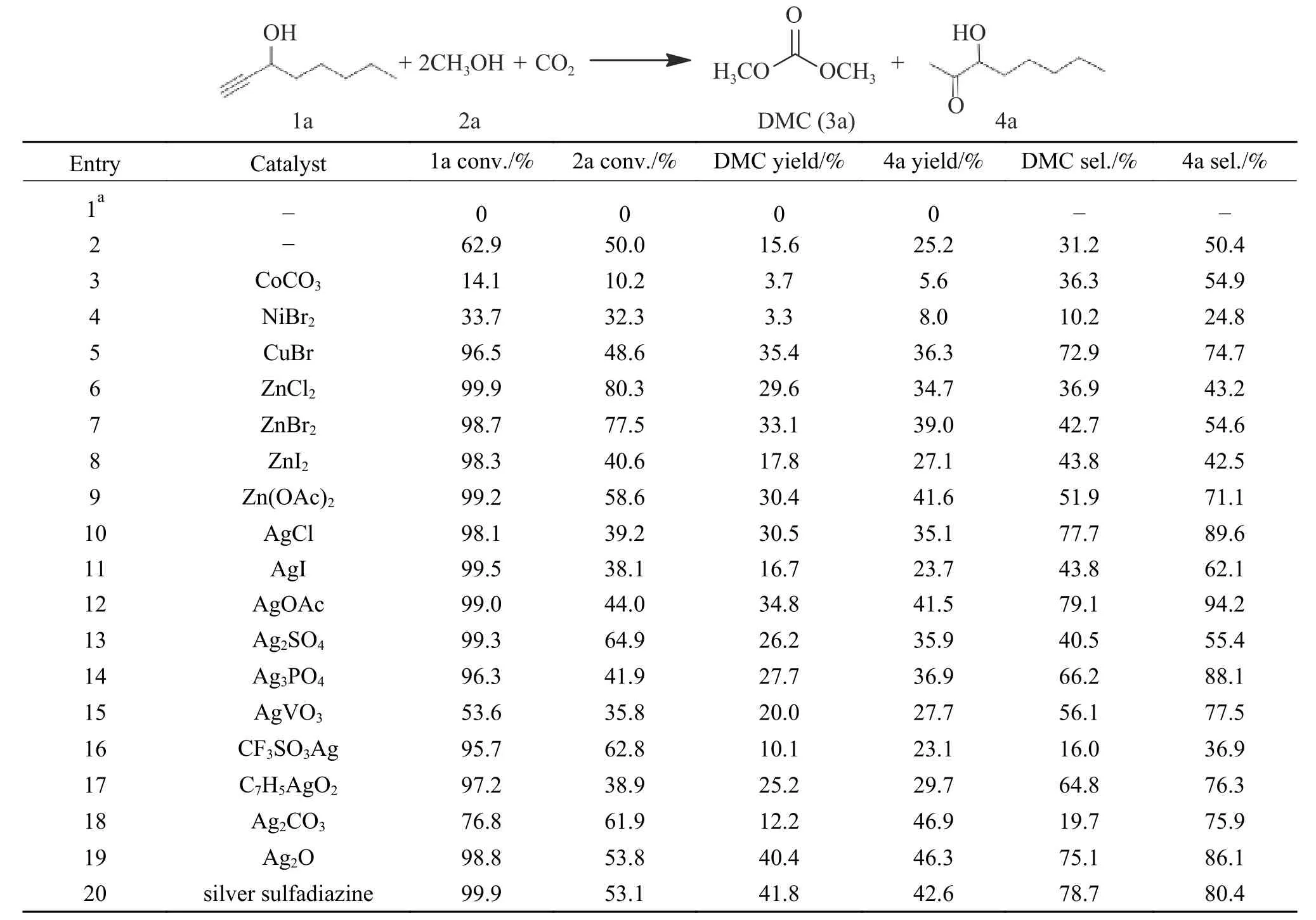
表1 催化剂性能Table 1 Catalysts investigation
银化合物在炔丙醇和CO2合成环状碳酸酯和噁唑啉酮等[1,20]反应中表现出优异的催化性能。基于此,这里优先考察了11 种银盐,其中,以偏酸性(强酸弱碱反应形成)银盐(AgCl、AgI、Ag2SO4、Ag3PO4、AgVO3、CF3SO3Ag)为催化剂时,DMC 收率普遍不高,使用偏酸性最强的CF3SO3Ag 作催化剂时DMC 收率仅为10.1%。AgVO3作催化剂时,底物1a 转化率仅为53.6%,说明AgVO3对碳碳三键(C≡C)的活化效果较差,可能是AgVO3在体系中的溶解度低导致。Ag2CO3作催化剂时,DMC 的收率为12.2%,而大空间位阻的磺胺嘧啶银和与碱性银氧化物Ag2O 作催化剂时,DMC 的收率超过40%。但Ag2O 作催化剂时DMC 与4a 收率差距略大(6%),而以磺胺嘧啶银作催化剂时,DMC 收率41.8%且与4a 收率基本一致,初步推断该体系反应更有利于中间体快速转化,副反应也更少。综合分析,银盐有利于该三组分反应的进行,其中,磺胺嘧啶银作催化剂时,目标产物收率与选择性相符性表现最好。
共催化剂在该反应中也表现出关键的作用。在不使用共催化剂的条件下,DMC 的收率仅为2.2%(表2,序号1),仅使用DBU 作催化剂时收率为15.6%,而磺胺嘧啶银与DBU 共同作用时DMC收率高达41.8%,这说明磺胺嘧啶银与DBU 有很好的协同催化作用,这种作用可能与底物和中间体的活化有关。常见的有机超强碱碱性大小排序为:TBD >TMG >DBN >DBU[21],该次序与同等条件下DMC 收率大小规律相反(表2,序号2-5),这可能是强碱影响了甲醇与中间产物链状碳酸酯的酯交换进而影响了DMC 的收率。另外,随着共催化剂碱性的增强,DMC 和4a 的选择性均呈现下降的趋势(表2,序号2-5),这可是因为体系中碱性的增强加剧了副反应。
季铵盐常作为共催化剂参与CO2的转化反应[1]。在此,首先考察了四丁基溴化铵(TBAB)与四乙基氯化铵(TEAC)对反应的影响(表2,序号6,7),DMC的收率均低于5%,证明季铵盐对该三组分反应活性表现较差。另外,TBAB 和DBU 同作共催化剂时,DMC 收率为22.8%,这可能是因为TBAB 的加入与DBU 形成了竞争关系,降低了磺胺嘧啶银与DBU 的协同催化作用。这一点在加入三苯基膦(PPh3)后也有体现,PPh3与银离子有很强的络合作用[19],因此,PPh3与DBU 联合作共催化剂时DMC 收率仅为2.8%。
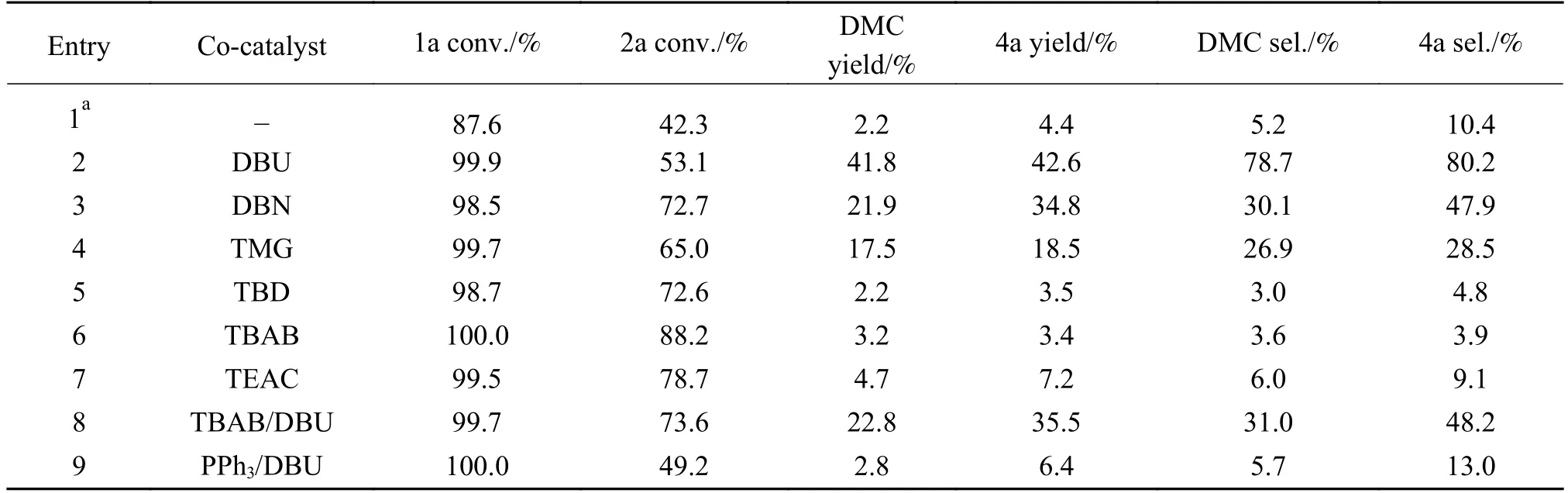
表2 共催化剂性能Table 2 Co-catalyst investigation
基于以上结果分析,共催化剂碱性增强,DMC的收率和选择性均呈现下降的趋势,而磺胺嘧啶银与DBU 的协同催化作用最好,DMC 收率41.8%,选择性78.7%。
得到最优催化剂组合后,考察了磺胺嘧啶银用量对反应的影响,结果如图1 所示。磺胺嘧啶银的摩尔百分比是基于1a,当使用量为1%时,1a 转化率为85.8%,催化剂用量过低导致反应不完全。当催化剂用量低于20%时,随着催化剂量的增加,DMC 的收率增加;而催化剂量大于20%时,继续增大催化剂使用量,1a 转化率几乎未变,但DMC 收率反而降低。强碱环境下α-亚甲基环状碳酸酯的醇解反应更易进行[22],而随着银盐使用量增大,磺胺嘧啶银和DBU 的络合程度增加使得体系的碱性降低,导致后续醇解反应受到一定程度的抑制,部分原料停留在了中间产物阶段,因此,DMC 收率降低。
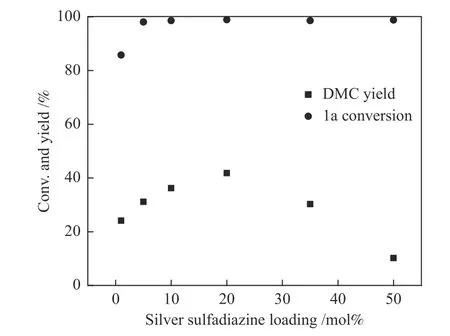
图1 催化剂用量的影响Figure 1 Catalyst loading investigation
2.2 条件参数影响规律研究
有机反应常在溶剂中进行,不同物性的溶剂对反应有较大影响,同时影响因素也很多。在此考察了溶剂二甲基亚砜(DMSO)、二甲基甲酰胺(DMF)、乙腈、乙酸乙酯、甲苯和四氢呋喃对反应的影响,结果如表3 所示。可以看出,与无溶剂体系相比,DMSO 对该三组分反应有较大的促进作用,DMC 的收率高达55.6%,选择性为89.5%。然而,使用乙酸乙酯和四氢呋喃作溶剂时,DMC 的收率均低于30%,这可能是因为体系稀释后,物料浓度降低,分子的碰撞频率变低。另外,磺胺嘧啶银在较高的温度下会分解失活,不同物性的溶剂可能会影响催化剂的热稳定性进而影响催化过程。总体分析,溶剂本身具有的促进或抑制作用与稀释效应等综合效应导致了实际参差不齐的结果,DMSO 作溶剂时,体系效率明显提升,溶剂对体系推动作用占主导地位,总体表现为促进作用。

表3 溶剂对反应的影响Table 3 Solvent effect on the reaction
系统研究溶剂效应的影响后,进一步考察了温度对三组分反应的影响,结果如图2 所示。在40 ℃时,炔丙醇的转化率为99%,说明炔丙醇与CO2的环化反应在低温时就可以顺利进行,但DMC和4a 的收率都低于4%,说明此时产物多为中间产物。在40-120 ℃,随温度升高产物收率明显提高,这可能是因为温度的升高使反应体系中活化分子的数量增多从而加快了反应速率。DMC 和4a 的收率在120 ℃达到最高,当温度超过120 ℃时产物收率锐减。磺胺嘧啶银热稳定性较差,在高温下发生了失活,导致两种产物收率均降低。
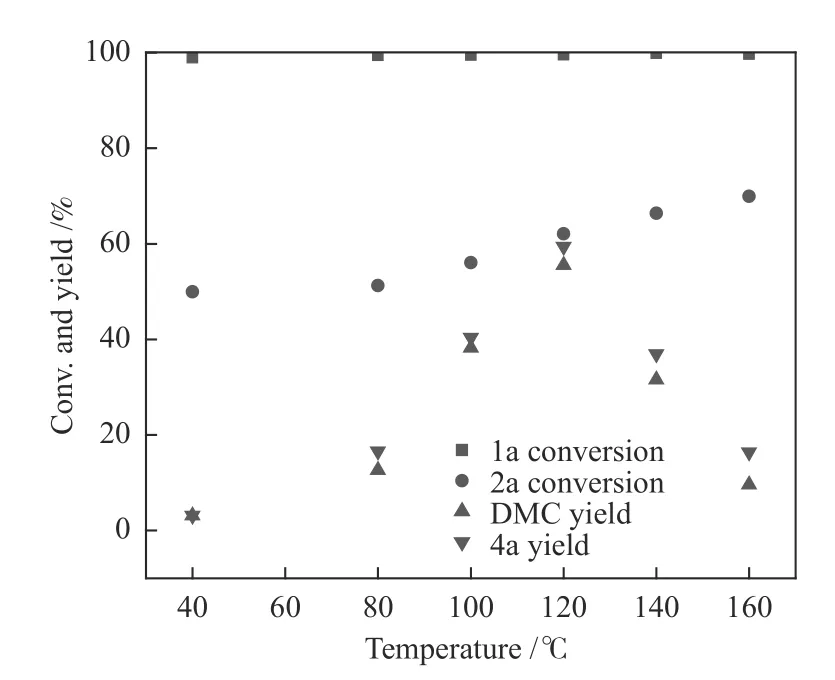
图2 温度对反应的影响Figure 2 Temperature effect on the reaction
从图2 还可以看出,随着温度的升高,DMC与4a 收率的差距逐渐变大,这可能是因为温度升高加剧了副反应。2a 的转化率同样随温度升高而变大,而产物的收率却降低,说明大部分原料转化到了中间态。
DMC 和羟基酮收率随甲醇与炔丙醇的用量比变化如图3 所示。可以看出,原料配比为1 时,4a 收率最高(75.5%),而原料配比为2 时,DMC收率最高(55.6%),说明可以通过调控原料配比高选择性地获取目标产物。当原料配比超过2,此时体系中甲醇过量,DMC 和羟基酮的收率都有所降低,可能是甲醇浓度的提高稀释了反应物或产生溶剂效应,体系中的碱性降低,影响了第二步和第三步的醇解。

图3 原料配比对反应的影响Figure 3 Effect of raw material ratio on reaction
另外,考察了压力对三组分反应的影响,结果如图4 所示。可以看出,随着压力的升高,反应向右移动,2a 的转化率和DMC 的收率均有提高。另外,压力升高,体系的CO2浓度增加,传质增强,DMC 的选择性也随之变大。值得一提的是,当CO2压力降至0.2 MPa,DMC 的收率超过15%,进一步说明了磺胺嘧啶银/DBU 协同催化体系对该三组分反应有较强促进作用。
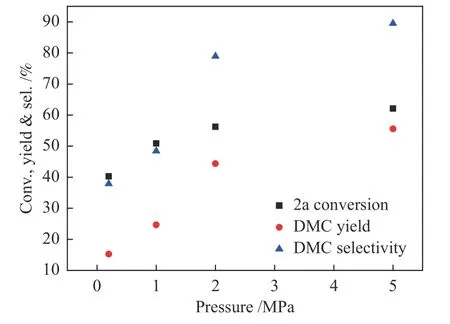
图4 压力对三组分反应的影响Figure 4 Pressure effect on the three-component reaction
图5 为时间对反应的影响,从图5(a)可以看出,反应进行1 h 时,底物炔丙醇转化率接近100%,且随时间延长不发生变化,再次证明了该三组分反应第一步炔丙醇与CO2的羧化环化反应较容易发生。
由图5(b)知,反应在前8 h 内,随时间的延长,DMC 和羟基酮的收率增加,而8 h 后,DMC 和羟基酮的收率随时间延长有所下降,到32 h 时DMC收率仅为21.9%。结合图5(c),时间过长可能导致逆反应程度增加,因此,2a 转化率、产物的选择性和收率均有降低。2011 年,Ca 等[22]系统研究了胍类有机强碱催化的炔丙醇、CO2和一元醇耦合反应,主要产物是β-氧代丙基烷基碳酸酯,研究中并未检测到碳酸二烷基酯的产物。在碱性过渡金属如银[15,23]催化方法中,也显示了同样的产物分布规律。这些研究也预示了β-氧代丙基烷基碳酸酯和一元醇的酯交换反应对金属或非金属催化剂有更高的要求。2020 年,本团队发展了强路易斯酸性的锌盐和DBU 协同活化催化体系[16],实现了CO2、炔丙醇和甲醇三组分串联反应制备DMC 和α-羟基酮路线,在140 ℃和6 MPa CO2条件下,DMC收率达37.3%,定量分析结果显示大部分原料停留在中间产物阶段。在本工作中,通过研究更优的炔丙醇底物结构,在磺胺嘧啶银与超强碱协同活化和催化下,DMC 收率和选择性得到了大幅度的提高(DMC 收率55.6%,选择性高达89.5%)。

图5 时间对反应的影响Figure 5 Effect of the reaction time
炔丙醇结构对反应性以及DMC 收率有很大的影响。鉴于此,考察了磺胺嘧啶银/DBU 催化体系对不同取代基的炔丙醇、甲醇和CO2三组分反应的影响(图6)。首先,对于α-位双取代基的炔丙醇(1c-1e),随着底物炔丙醇碳链的减小,DMC 的选择性和收率皆呈上升趋势。这可能是因为α-位双取代基的炔丙醇做底物时,空间位阻效应占主导地位。炔丙醇空间位阻越大,其对应的中间产物α-亚甲基环状碳酸酯空间位阻越大,亲核反应受到影响,因此,醇解反应的活性降低,导致中间反应速率变慢,DMC 的选择性和收率降低。1h 虽然空间位阻小,但由于炔丙醇末端有取代基,导致C≡C 更加稳定,不容易被活化[20],因此,DMC 的选择性和收率较低。
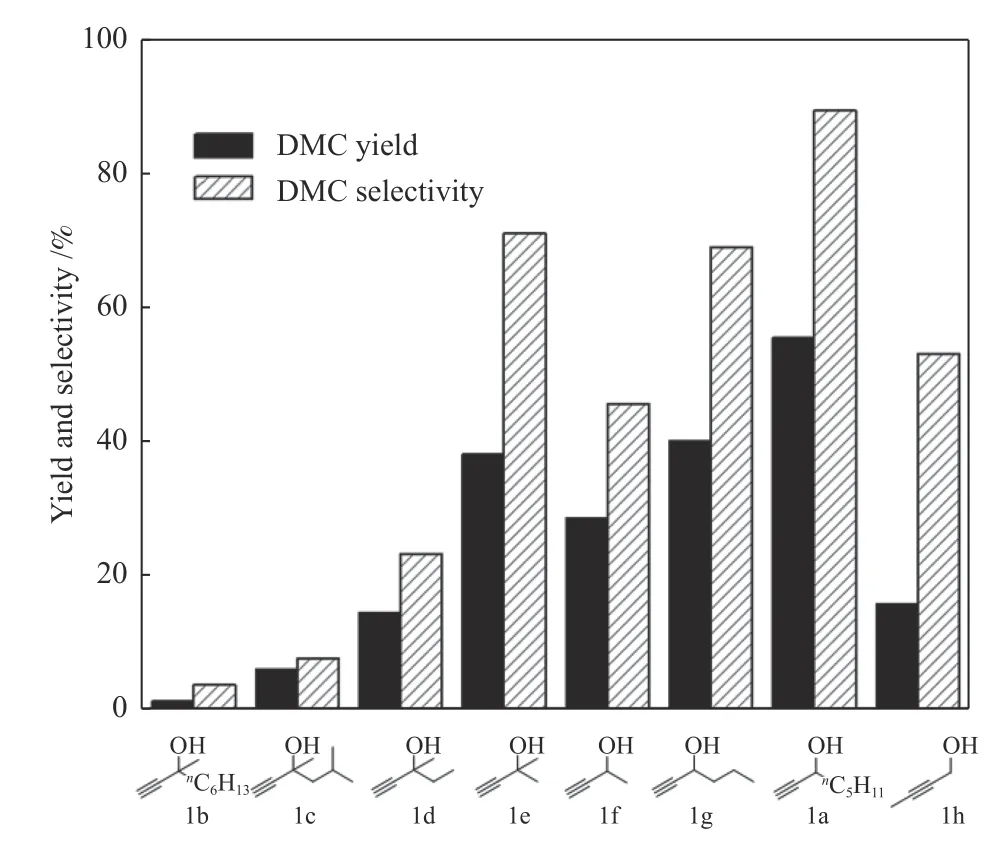
图6 炔丙醇结构与DMC 收率和选择性的关系Figure 6 Relationship between propargyl alcohol structure and the yield/selectivity of DMC
然而,对于α-位单取代基的炔丙醇(1f、1g、1a),随着取代基碳链的增长,DMC 的选择性和收率上升。作者推测α-位单取代基的炔丙醇做底物时,空间效应影响小,电子效应可能占主导地位。随着底物的碳链的增长,对应的中间产物α-亚甲基环状碳酸酯α-位碳键极性增大,诱导效应增强,使其与甲醇进行后续反应更加快速,同时因该中间体参与的副反应会更少,最终DMC 收率和选择性同时得到较大提高。
另外,尽管1a 和1b 都为长链炔丙醇,但α-位双取代基的1b 作底物时,DMC 收率和选择性锐减。实验结果表明,α-位单取代基的炔丙醇更有利于该三组分快速反应。
2.3 机理分析
基于以上研究结果和文献报道[12,16,18],提出了炔丙醇、甲醇和CO2三组分可能的反应机理(图7)。该反应主要分为三步:第一步炔丙醇与CO2羧化环化生成α-亚甲基环状碳酸酯B;第二步B 与甲醇醇解后经互变异构生成β-氧代丙基碳酸酯C;第三步C 和甲醇经酯交换反应后得到DMC 和α-羟基酮。本工作中涉及的α-亚甲基环状碳酸酯B 不稳定,在体系中直接分解转化。β-氧代丙基碳酸酯C 具有一定的稳定性,在色谱分析时能够检测到(图SI.1)

图7 磺胺嘧啶银/DBU 催化炔丙醇、甲醇和CO2 三组分耦合反应机理示意图(修改:炔丙醇底物红色标记的氧原子漏了一个氢原子,氢原子和带负电荷N 原子发生相互作用,实现羟基活化;中间体A 中DBU,修改为DBUH+,DBUH+ 与碳酸酯中带负电荷的蓝色标记的氧原子作用,稳定过渡态)Figure 7 Cascade reaction mechanism of propargyl alcohol,methanol and CO2 catalyzed by silver sulfadiazine/DBU
在第一步反应中,炔丙醇中羟基的氢质子被DBU 和磺胺嘧啶中电负性强的氮原子激活,使得烷氧基中的氧原子亲核攻击CO2变得更容易,因此,可以形成活跃的过渡态A。对于随后的分子内环化过程,因为银离子对C≡C 有很好的活化作用[24],使得过渡态A 中烷基碳酸阴离子的氧原子进攻C≡C 更容易。结果,形成了α-亚甲基环状碳酸酯B。而后B 与甲醇发生醇解反应生成烯醇式链状碳酸酯,再经互变异构得到中间体C。最后,甲醇进攻C 发生醇解反应得到DMC 和α-羟基酮。
基于实验结果,第一步和第二步反应很快完成,第三步为决速步骤。其中,C≡C 和羟基的活化是反应顺利进行的关键,磺胺嘧啶银与DBU 的协同催化作用是反应取得高效的原因。另外,由于体系中有微量水的存在,水与α-亚甲基环状碳酸酯反应生成α-羟基酮,同时还可能发生底物炔丙醇与α-亚甲基环状碳酸酯的醇解与后续的降解反应,最终导致α-羟基酮收率大于DMC[16]。
3 结 论
本研究提出了磺胺嘧啶银/DBU 协同催化方法,建立了高选择性的炔丙醇(α-单取代)、甲醇和CO2三组分耦合反应体系,DMC 选择性最高89.5%,收率55.6%。DMC 收率和选择性受炔丙醇底物结构影响显著,α-位单取代的炔丙醇类底物更适合作为原料,因该类型底物容易形成热力学不稳定的α-亚甲基环状碳酸酯,使其与甲醇进行后续反应更加快速,同时因该中间体参与的副反应会更少,最终DMC 收率和选择性同时得到较大提高。机理研究表明,1-辛炔-3-醇、甲醇和CO2三组分反应在不同阶段所需催化活性物质不同,而磺胺嘧啶银/DBU 恰好可以满足C≡C 与羟基的活化,因此,磺胺嘧啶银/DBU 协同催化对该三组分反应产生了极大促进作用。
