清毒洗液治疗宫颈HR-HPV持续感染的临床疗效研究
2023-02-03刘佳敏周明温丹婷肖静
刘佳敏,周明,温丹婷,肖静
(1.成都中医药大学附属医院,四川成都610032;2.深圳市罗湖区中医院妇科,广东深圳518000;3.广州中医药大学第二附属医院,广东广州 510120)
宫颈癌是威胁全球妇女生命健康的重大疾病之一,其发病率及死亡率在女性肿瘤中均排第四位[1]。我国2020年宫颈癌的新发病例为11.0万,死亡病例为5.9万,均呈现逐年上升趋势[2]。高危型人乳头瘤病毒(high-risk human papilloma virus,HR-HPV)的持续感染是其发生的必要因素,因此清除HR-HPV是阻断病程的关键。目前,预防性疫苗在我国接种覆盖率仍很低,瓶颈问题包括认知度、价格等因素[3-4]。对未达手术级别的HRHPV感染患者,尚无公认有效的治疗药物,临床多选择随访观察,患者常因此而产生焦虑情绪。中医外治法具有简便廉验、不良反应少且轻微的特点,从中挖掘用于治疗HR-HPV感染的有效方法是近年来的研究热点。清毒洗液前身为广东省中医院院内制剂疣毒净,该系列制剂在防治HPV感染的临床及实验研究方面已得到验证[5-7],而原方药味较多,本课题组对其精简优化药物后得出清毒洗液中药方,并将其作为本研究的试验方,观察其对宫颈HPV持续感染、病理诊断为宫颈上皮内瘤变(cervical intraepithelial neoplasia,CIN)Ⅰ级及以下的患者的临床疗效。现将研究结果报道如下。
1 对象与方法
1.1 研究对象及分组选取2020年3月至2021年6月在广东省中医院大学城医院妇科门诊就诊并确诊为HR-HPV感染、病理分级为CIN I级及以下的患者,共61例。根据就诊先后顺序,采用随机数字表法,按照2∶1的比例将患者随机分为治疗组40例和对照组21例。本研究已通过广东省中医院伦理委员会审核批准,于临床试验注册中心处备案,并且所有受试者均签署了相关知情同意书。
1.2诊断标准参照《实用妇产科学》[8]制定诊断标准:①宫颈HR-HPV感染:聚合酶链反应(PCR)法进行HPV-DNA分型检测,高危型基因型为16、18、31、33、35、39、45、52、58、26、51、55、56、59、61、66、68、73、83。②组织病理学诊断:亚临床感染(subclinical human papillomavirus infection,SPI)临床宫颈外观正常,但细胞病理、阴道镜活检和组织病理可见异型性明显的挖空细胞。CINⅠ级属于宫颈癌前病变,病理学检查表现为:不典型增生细胞局限于鳞状上皮的下1/3,可以出现核分裂象但数量不多,上皮下1/3增生的细胞无核异型性,而中表层见到挖空细胞的病变亦归入此范畴。
1.3 纳入标准①PCR方法检测HR-HPV阳性;②HR-HPV感染≥6个月;③病理诊断为CIN I级及以下(包括低度鳞状上皮内病变、慢性黏膜炎、SPI等);④研究者认为适合参加本临床试验;⑤未参加其他药物临床试验,也未使用与本试验药物有类似治疗作用的药物;⑥近期内无生育要求;⑦年龄在21~65岁之间,月经规则或已绝经,但有性生活史;⑧无重大脏器疾患;⑨愿意配合治疗和随诊并签署相关知情同意书的女性患者。
1.4 排除标准①病理确诊宫颈病变程度在CINⅡ级及以上的患者;②有外生殖器部位急性感染的患者;③孕妇或哺乳期妇女;④合并有全身慢性消耗性疾病、严重心血管疾病、肝肾疾病、造血系统疾病的患者;⑤患有精神性疾病的患者;⑥有药物过敏史或变态反应史的患者;⑦近期有生育要求的患者。
1.5 治疗方法
1.5.1 治疗组于非月经期用药,月经干净3 d后用清毒洗液(为医院院内制剂,由大青叶、土贝母等中药组成)冲洗阴道,每晚睡前1次,连用3周,经期停药1周(已绝经妇女与未绝经妇女用药频次一致),共治疗3个月,之后随访3个月。在入组后第4、7个月经周期的月经干净后3~7 d复查HR-HPV和病理活检。
1.5.2 对照组给予无治疗的随访观察6个月,在入组后第4、7个月的月经干净后3~7 d复查HR-HPV和病理活检。
1.5.3 注意事项2组患者观察期间均要求注意经期卫生以及房事必须戴避孕套。
1.6 观察指标
1.6.1 HR-HPV转阴情况治疗前后采集宫颈拭子,采用PCR技术检测HR-HPV分型。
1.6.2 病理变化情况①逆转:如宫颈活检病理显示CIN I级或低度鳞状上皮内病变(low-grade squamous intraepithelial lesion,LSIL)转为宫颈炎性改变;②维持:参与研究前后病理活检级别无变化;③恶化:宫颈活检病理显示CINⅠ级者进展为CINⅡ级及以上,或SPI上升为LSIL及以上,或LSIL上升为高度鳞状上皮内病变(how-grade squamous intraepithelial lesion,HSIL)。
1.6.3 临床症状变化情况记录2组患者治疗前后是否有诸如性交出血、带下异常等不适症状及改善情况。
1.6.4 安全性评价用药期间注意有无不良反应,如阴道内瘙痒、烧灼感等症状,并详细记录不良反应的发生频次及持续时间。
1.7 统计方法采用SPSS 25.0统计软件进行数据的统计分析。计量资料符合正态分布者用均数±标准差(±s)表示,组间比较采用t检验;不符合正态分布者用中位数和四分位数[M(P25,P75)]表示,组间比较采用非参数秩和检验(NPar检验)。计数资料采用率或构成比表示,组间比较采用χ2检验或Fisher精确概率法;等级资料组间比较采用非参数秩和检验。均采用双侧检验,以P<0.05为差异有统计学意义。
2 结果
2.1 2组患者脱落情况及基线资料比较研究过程中,治疗组脱落2例,对照组无脱落病例,最终共有59例患者完成观察,其中治疗组38例,对照组21例。表1结果显示:2组患者的年龄、孕次、产次、流产次数、性生活时间、首次性交年龄等基线资料比较,差异均无统计学意义(P>0.05),具有可比性。
表1 2组高危型人乳头瘤病毒(HR-HPV)感染患者基线资料比较Table 1 Comparison of baseline data between the two groups of patients with high-risk human papilloma virus(HR-HPV)infection [±s或M(P25,P75)]

表1 2组高危型人乳头瘤病毒(HR-HPV)感染患者基线资料比较Table 1 Comparison of baseline data between the two groups of patients with high-risk human papilloma virus(HR-HPV)infection [±s或M(P25,P75)]
组别治疗组对照组合计t值P值例数/例38 21 59年龄/岁40.6±10.2 35.4±10.2 38.5±10.3 1.757 0.085孕次/次3.0(2.0,4.0)2.0(1.0,3.0)3.0(2.0,4.0)0.214产次/次1.0(1.0,2.0)1.0(0.5,1.5)1.0(1.0,2.0)0.252流产次数/次2.0(1.0,2.0)1.0(0.0,2.0)2.0(1.0,2.0)0.308性生活时间/年19.5±10.2 14.8±9.5 18.0±9.4 1.731 0.089首次性交年龄/岁20.0(19.0,22.0)20.0(18.0,23.5)19.0(18.0,20.0)0.727
2.2 2组患者HR-HPV转阴率比较
2.2.1 2组患者入组后第4个月HR-HPV转阴率比较在入组后第4个月(即治疗组用药结束后),对2组患者的HR-HPV进行复查,以评估药物的近期疗效。表2结果显示:治疗组的HR-HPV转阴率为39.47%(15/38),对照组为0;组间比较(χ2检验),治疗组的HR-HPV转阴率明显优于对照组,差异有统计学意义(P<0.01)。

表2 2组高危型人乳头瘤病毒(HR-HPV)感染患者入组后第4个月HR-HPV转阴率比较Table 2 Comparison of HR-HPV negative-conversion rate between the two groups of patients with high-risk human papilloma virus(HR-HPV)infection on the 4th enrollment month [例(%)]
2.2.2 2组患者入组后第7个月HR-HPV转阴率比较入组后第7个月,对2组入组后第4个月HR-HPV未转阴的患者进行复查,以评估药物的远期疗效。表3结果显示:治疗组的HR-HPV转阴率为73.91%(17/23),对照组为9.52%(2/21);组间比较(χ2检验),治疗组的HR-HPV转阴率明显优于对照组,差异有统计学意义(P<0.01)。
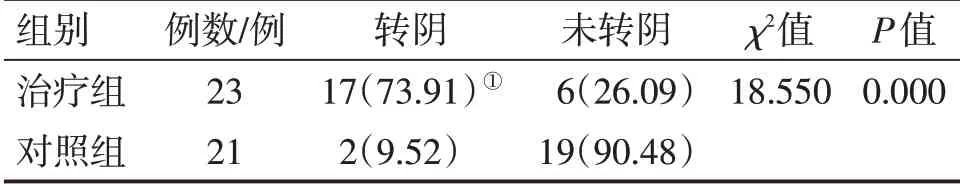
表3 2组高危型人乳头瘤病毒(HR-HPV)感染患者入组后第7个月HR-HPV转阴率比较Table 3 Comparison of HR-HPV negative conversion rates between the two groups of patients with high-risk human papilloma virus(HR-HPV)infection on the 7th enrollment month [例(%)]
2.3 2组患者病理结果比较
2.3.1 2组患者治疗前宫颈病理结果比较表4结果显示:治疗前,2组患者的病理活检结果比较(χ2检验),差异无统计学意义(P>0.05),提示2组具有可比性。

表4 2组高危型人乳头瘤病毒(HR-HPV)感染患者治疗前宫颈病理结果比较Table 4 Comparison of cervical pathological findings between two groups of patients with high-risk human papilloma virus(HR-HPV)infection before treatment [例(%)]
2.3.2 治疗组患者治疗前后自身病理活检结果比较表5结果显示:治疗组患者治疗前后自身病理活检结果比较(NPar检验),差异无统计学意义(P>0.05),提示治疗组的总体病理结局稳定,未见进一步恶化。
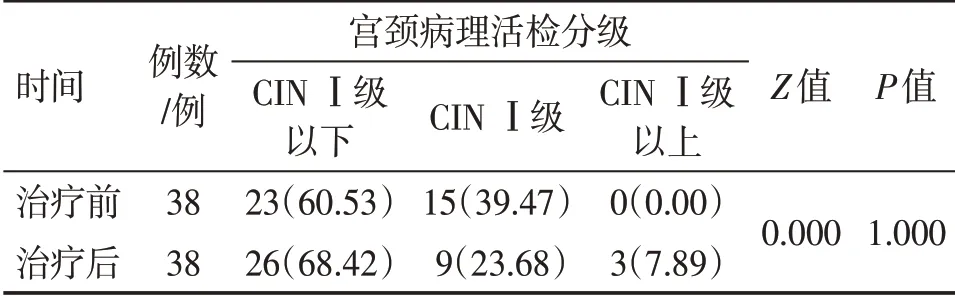
表5 治疗组高危型人乳头瘤病毒(HR-HPV)感染患者治疗前后自身宫颈病理结果比较Table 5 Self-comparison of cervical pathological findings in the treatment group of patients with high-risk human papilloma virus(HR-HPV)infection before and after treatment [例(%)]
2.3.3 对照组患者观察前后自身病理活检结果比较表6结果显示:对照组患者观察前后自身病理活检结果比较(NPar检验),差异有统计学意义(P<0.05),提示对照组的总体病理结局恶化,病理级别升级。

表6 对照组高危型人乳头瘤病毒(HR-HPV)感染患者观察前后自身宫颈病理结果比较Table 6 Self-comparison of cervical pathological findings in the control group of patients with high-risk human papilloma virus(HR-HPV)infection before and after observation [例(%)]
2.3.4 2组患者治疗后宫颈病理结局比较表7结果显示:分别将2组患者进行自身病理结局比较,治疗组入组第7个月病理逆转率为18.42%(7/38),维持率为68.42%(26/38),恶化率为13.16%(5/38);对照组入组第7个月病理逆转率为0,维持率为71.43%(15/21),恶化率为28.57%(6/21)。组间比较(NPar检验),治疗组对宫颈病理结局的改善作用明显优于对照组,差异有统计学意义(P<0.05)。
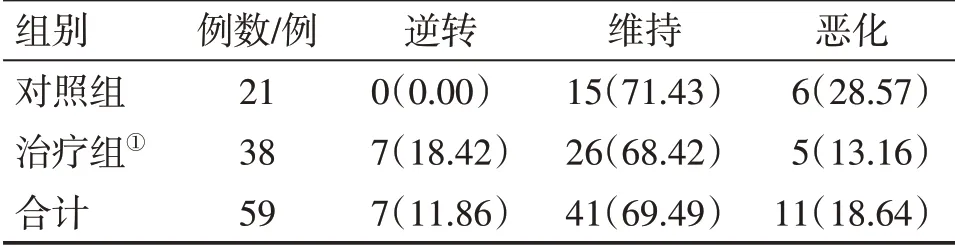
表7 2组高危型人乳头瘤病毒(HR-HPV)感染患者治疗后宫颈病理结局比较Table 7 Comparison of cervical pathological outcomes between the two groups of patients with high-risk human papilloma virus(HR-HPV)infection after treatment [例(%)]
2.4 2组患者治疗前后症状改善情况比较表8结果显示:治疗前,2组患者的性交出血、带下异常、外阴感觉异常等相关症状表现比较(校正χ2检验、Fisher精确概率法),差异均无统计学意义(P>0.05),说明2组具有可比性。治疗后,治疗组对带下异常的改善作用优于对照组,差异有统计学意义(P<0.01)。

表8 2组高危型人乳头瘤病毒(HR-HPV)感染患者治疗前后症状改善情况比较Table 8 Comparison of improvement of symptoms between two groups of patients with high-risk human papilloma virus(HR-HPV)infection before and after treatment [例(%)]
2.5 安全性分析研究期间,治疗组2例患者用药初始期出现外阴瘙痒不适,但程度轻,持续约数分钟,停药后症状缓解,未予特殊处理,因上述不良反应要求退出试验,故最终未纳入统计;其余患者均无不良反应报告,表明清毒洗液具有较高的安全性。
3 讨论
清除高危型人乳头瘤病毒(HR-HPV)是阻断宫颈恶性肿瘤形成的重要途径,迄今为止,国际上暂无公认的确能清除HR-HPV病毒的药物,现有的治疗方案仍处于探索阶段。对于未达手术级别的HR-HPV感染患者,临床可选择定期随访,等待机体自我清除病毒,也可试验性地采用阴道用药、物理及手术治疗方法,如干扰素、保妇康栓等。HPV病毒疫苗应用前景广阔,但预防性疫苗所接种的范围和覆盖率在不同国家或同一国家的不同地区之间仍存在较大的差异[9],治疗性疫苗仍处于研究开发阶段。中医认为,HR-HPV感染的病因病机多为湿热瘀毒蕴结于胞宫子门而成,治法以清热解毒祛湿为主[10]。近年来,中药内、外治法治疗HR-HPV感染的研究均有报道,其中,外治法因其安全便捷、直达病所的特点,近年来已成为临床研究的热点。
清毒洗液包括大青叶、土贝母等药物,是从广东省中医院院内制剂疣毒净优化而来。从1997年开始,对疣毒净制剂在治疗HPV感染的临床疗效、作用机制等方面进行了一系列研究,并用于治疗因HPV致病的多个病种。但原方药味较多,为进一步精简药物,故通过正交优化的方法得出清毒洗液方。在药理作用方面,大青叶性寒,味苦,归心、胃经,功效清热解毒、凉血消斑,现代药理研究[11]表明,其具有较好的抗菌、抗病毒、增强免疫力和抗癌的作用,将其用于治疗扁平疣,可获得良好的疗效。土贝母性凉,味苦,入肺、脾二经,功可清热化痰、散结拔毒,现代研究[12-13]显示,土贝母皂苷对宫颈癌细胞的生长具有较强的抑制作用。
本研究结果显示:治疗组入组后第4个月的HR-HPV转阴率为39.47%(15/38),第7个月的HR-HPV转阴率为73.91%(17/23),组间比较,治疗组的HR-HPV转阴率均明显优于对照组,差异均有统计学意义(P<0.01),提示清毒洗液对HRHPV具有较好的清除作用。治疗组自身治疗前后的病理活检比较,差异无统计学意义(P>0.05),提示患者的病理结局稳定;对照组自身观察前后的病理活检比较,差异有统计学意义(P<0.05),提示对照组的病理结局恶化。这提示外用中药制剂或许是通过清除病毒而达到防治宫颈癌前病变的目的;同时,考虑到HPV感染有自然逆转倾向,故本次研究纳入患者的感染时间均≥6个月,从研究结果我们推测,中药制剂亦可能通过增强局部免疫力,加速自然逆转的过程而达到清除HR-HPV的作用。上述结论还需后期进一步的机制研究加以验证,因HPV病毒对病理的影响是一个长期的过程;另外,本次研究纳入的病例数有限,且未能进一步追踪患者的长期病理结局,从而使得本研究的统计效能和论证强度降低,故确切的结论有待于今后延长观察周期,扩大样本量加以证实。
