迈克F 580与Sysmex XS500i血细胞分析仪检测系统比对研究
2023-02-02佘文婕刘宇董树美张春唐鹤亭
佘文婕 刘宇 董树美 张春 唐鹤亭
摘 要:目的:以美国临床与实验室标准化委员会(CLSI)EP9-A3文件为依据,讨论了国产迈克F 580和日本Sysmex XS500i全自动血细胞分析仪结果的可接受性。方法:参照EP9-A3文件,以Sysmex XS500i为参考系统,以迈克F 580为实验系统,使仪器处于正常状态。测定40份新鲜抗凝全血标本的白细胞计(WBC)、红细胞计数(RBC)、血小板计数(PLT)、血红蛋白(Hb)和红细胞压积(HCT)。用ESD方法对测量结果进行离群值检验和评估偏移。利用最佳回归模型拟合回归方程,计算各项目医学决定水平处的偏移,并以1/2CLIA88允许误差为标准,判断该偏移是否可接受。结果:Hb和Hct在两种血细胞分析仪的检测结果中偏移不被接受。WBC、RBC、PLT偏移均可接受。所有项目的偏移均小于允许误差。结论:根据CLSI EP9-A3标准,临床实验室血细胞分析仪定期比对试验是为临床使用提供准确可靠的试验数据的有力保证之一。
关键词:血细胞分析仪,迈克F 580,Sysmex XS500i,偏移评估
DOI编码:10.3969/j.issn.1002-5944.2023.17.037
基金项目:本文受校级课题项目“基于检验系统性能验证下的国产与进口血细胞分析仪的比对研究”(项目编号:2022JK49)资助。
Comparative Research on Detection System of Maccuras F 580 and Sysmexs XS-500i Automatic Hematology Analyzers
SHE Wen-jie LIU Yu DONG Shu-mei ZHANG Chun* TANG He-ting
(Laboratory of Teaching and Research on Inspection,Yunnan College of Business Management)
Abstract: Objective: Based on the EP09-A3, a document issued by the Clinical and Laboratory Standards Institute (CLSI) in the U.S., this paper discusses the acceptability of the test results of Maccuras F 580 and Sysmexs XS-500i automatic hematology analyzers. Method: Referring to EP09-A3, the paper takes Sysmexs XS-500i as the reference system, takes Maccuras F 580 as the experimental system, and keeps the instrument at the normal state. The white blood cell count (WBC), RBC count (RBC), platelet count (PLT), hemoglobin (Hb), and hematocrit (HCT) were determined in 40 fresh anticoagulated whole blood samples. Outlier test and offset evaluation were performed on these measurements by ESD method. The optimal regression model was used to fi t the regression equation, calculate the offset at the level of medical decision for each item, and determine whether the deviation was acceptable, using 1/2 of allowable error value in the CLIA88. Result: The deviations of Hb and Hct results in the two hematology analyzers are not acceptable. The deviations of WBC, RBC and PLT results are acceptable. Deviations of all items are less than the range of allowable error. Conclusion: According to the CLSI EP09-A3, performing comparative experiments on hematology analyzers regularly by clinical laboratories is one of the powerful guarantees to provide accurate and reliable test data for clinical use.
Keywords: hematology analyzer, Maccura F 580, Sysmex XS-500i, offset evaluation
隨着检验技术和科技创新不断发展,国内自主研发品牌大踏步前进,国产品牌的全自动五分类血细胞分析仪不断涌现,实验室一台血细胞分析仪已不能满足工作量需求,实验室同时采用国产品牌和进口品牌的血细胞分析仪已成为检验科发展的必然趋势。但是,由于仪器检测原理、方法学、精密度和试剂等方面存在差异,可能引起同一检验项目存在差异,要求实验室注意定期对同一实验室不同仪器的结果进行比较和评价,将差异控制在临床可接受的范围内[1-2]。本研究符合美国国家临床实验室标准化委员会(CLSI)EP9-A3文件[3]及国际血液学标准化委员会(ICSH)的要求[4],用迈克F 580与Sysmex XS500i自动血细胞分析仪两台仪器对5个主要指标的结果进行比对分析。两台分析仪的检测结果的偏差和检测结果的一致性符合临床接受范围。
1 材料与方法
1.1 一般资料
每天收集8份新鲜的EDTA-K2抗凝血,来自云南经济管理学院的职工体检样本。连续进行5天,共40个标本。每个样品都使用两台血液分析仪进行测试。每份标本分别用两台血细胞分析仪进行检测。血液标本避免黄疸、溶血、乳糜和其他不合格情况。项目检测结果尽量覆盖高、中、低医学决定水平。比对项目包括5个指标,分别是HCT、PLT、WBC、RBC和Hb。每天对收集到的8个标本在2小时内完成检测。
1.2 仪器与试剂
检测系统(1):Sysmex XS500i全自动血细胞分析仪是国际先进的仪器、配备有高品质的试剂和质控品,作为参比系统。
检测系统(2):迈克F580全自动血细胞分析仪、原装试剂和质控品,作为实验系统。试剂和质控品均在有效期,仪器均在半年内进行了校准,均顺利通过室间质评和每日室内质控。
1.3 方法
1.3.1 标本测定
每天都要使用专业的仪器和质控品在室内环境中进行严格的质量控制。保证各项目质控在控。两套检测系统按照常规标本检测方式对各项指标进行测样。每份样本按照1→8正序测定1次,再按8→1反序测定1次。2小时内完成测样,连续测定5天,共40份样本,结果记录。
1.3.2 离群值检查
根据EP9-A3文件的规定,对离群值进行严格检查,以确保准确性和可靠性。采用ESD(extreme studentized deviate)法进行离群值检查[5-6]。
1.4 统计学处理
采用SPSS 22.0统计软件进行分析。建立回归方程及相关系数(r2≥0.95,作为比对试验的判断标准),回归和偏移分析采用普通线性回归OLR(ordinary linear regression)、加权最小二乘WLS(weightedleastsquares)、P-B(Passing-Bablok)模型计算。根据美国临床实验室修正法案,计算每个参数在医学决定水平上面的偏移(WBC≤±7.5%,R B C≤±3%,H b≤±3 . 5 %,H c t≤±3%,PLT≤±12.5% ) 为标准,判断偏移可否接受[7]。
2 结 果
2.1 离群值检查
对1~40号标本的5项指标的检测结果采用ESD法定量检验,通过最大偏移值ESDmax计算结果显示RBC的ESDmax=2.51、WBC的ESDmax=2.43、Hb的ESDmax=2.51、PLT的ESDmax=2.30和HCT的ESDmax=2.91均小于λi=3.05,无离群值。绘制散点图,目测结果显示均无异常值点。
2.2 偏移结果评价
2.2.1 回归分析
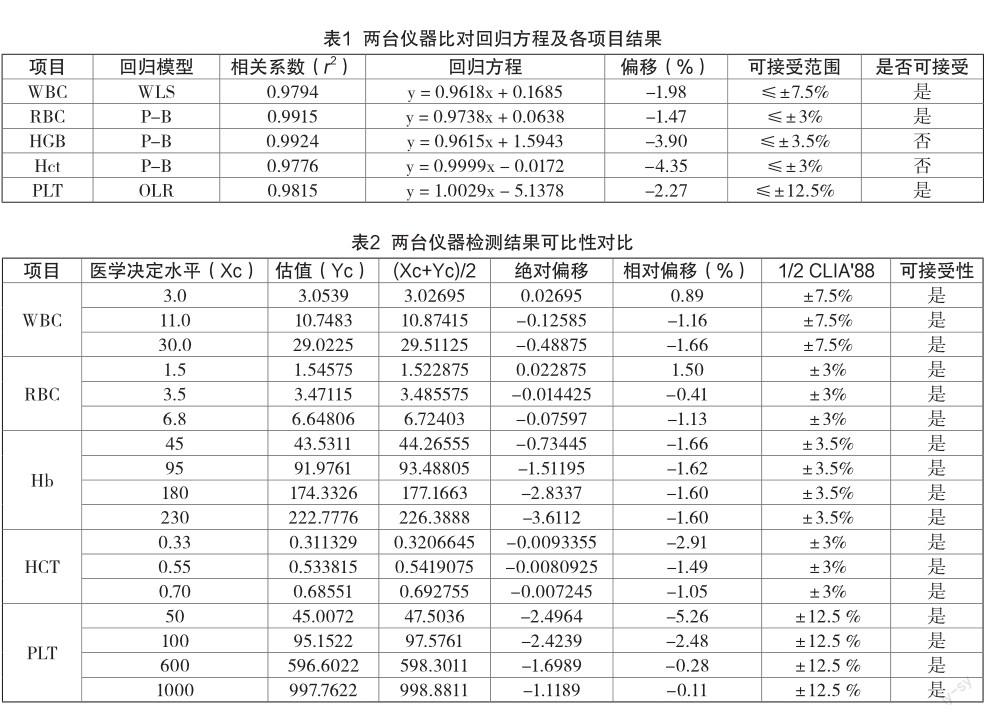
将无离群值德40个点绘制成偏差图,结果显示两套检测系统的差值:PLT采用 OLR模型进行回归分析,差值为恒定 SD。WBC采用 WLS 模型进行回归分析,恒定CV变化。RBC、Hb、Hct均采用P-B回归分析,差值为混合变化。两套检测系统测定结果的相关性比较,相关系数r2均大于0.95,提示具有良好的相关性。回归方程及其各参数见表 1。
2.2.2 偏移初步估算
绘制两套系统的差频直方图结果显示,RBC和PLT是正态分布,并且可以采用平均数来评估偏移。WBC、Hb和Hct是非正态分布,采用中位数法。40份样本差值的平均值估算偏移是-1.47%(RBC)、-2.27%(PLT)。中位数评估偏移是-1.98%(WBC)、-3.90%(Hb)和-4.35%(Hct)。Hb和Hct偏移>1/2 CLIA88允许误差,不可接受。WBC、RBC、和PLT均<1/2CLIA88允许误差,可接受。
2.2.3 医学决定水平的偏移评估
将各参数医学决定水平分别代入回归方程计算偏移。将小于1/2 CLIA88允许误差范围为临界点。以WBC在医学决定水平为3.0×109/L、11.0×109/ L及30.0×109/L时,偏移为临界点(±7.5%)。RBC在医学决定水平为1.5×1012/L、3.5×1012/L及 6.8×109/ L时,偏移为临界点(±3%)。HGB在医学决定水平为45 g/L、95 g/L、180 g/L及230 g/L时,偏移为临界点(±3.5%)。Hct在医学决定水平为0.33、0.55和0.70时,其偏移均小于1/2CLIA88允许误差范围(±3%)。PLT在医学决定水平为50×109/L 、100×109/L、600×109/L及1000×109/L时,偏移为临界点(±12.5%),见表2。
3 讨 论
血常规检查是临床实验室三大常规检查之一,对临床医生在疾病诊治、治疗监测、预后判断等方面具有重要意义。为了满足临床需要,同一实验室在检查同一项目时采用不同系统比较普遍。ISO 15189医学实验室要求,当实验室使用两套或多套检测系统对同一项目进行检测时,应保证系统之间比较结果的一致性[8]。目前,评估结果一致性的方法有很多,大部分采用CLSI EP9-A2方式。根據2013年8月EP9-A3最新版本文件《患者样本的方法比较与偏差评价:批准指南-第三版》,为生产企业和临床实验室提供了最新的方法比较与偏差评价指南[9]。EP9-A3在EP9-A2的基础上提出了“恒定SD”“恒定CV”“混合变化”等数据特征的概念,并指出用差值或百分比表示的平均偏差的选择以及线性回归方法与数据特征有关[10]。EP9-A3实验方案和统计方法进行了较大修改,适用范围更广,可操作性更强,方案设计更合理,统计分析更科学[11]。
本研究对两套血常规分析系统的测定结果进行了回归分析和偏移评估。首先运用ESD方法通过最大偏移值ESD max计算结果均小于λi=3.05。绘制两个检测系统各测量结果的散点图,可视结果中无异常值。对数值偏差图和频率直方图的进一步分析表明,两种系统存在差异。PLT差值为常数SD,采用OLR模型进行回归分析。WBC常数CV采用WLS模型回归分析。Hct、RBC、Hb的差异为混合变化,采用P-B回归分析。对两台血细胞分析仪测定结果的相关性进行比对,结果显示相关系数r2均大于0.95,具有良好的相关性。对两台血细胞分析仪的检测结果进行偏移性评估,Hb、Hct偏移大于1/2CLIA88允许误差,不可接受。WBC、RBC、和PLT均小于1/2CLIA88允许误差,可接受。将各数据的医学决定水平分别代入回归方程式。在HGB、Hb、WBC、RBC和Hct的偏移均小于1/2CLIA88允许误差范围。其中,对Hb、Hct偏移不被接受的原因进行分析,机器老化,未定期保养维护,管道和采样针等堵塞等问题可被考虑。要从根本上寻找原因,首先要对仪器进行充分的清洁保养、疏通管道、更换相应配件乃至检修,做好全面保养和校准。其次校准后在同等实验环境条件下做Hb和Hct的偏移评估。如果评价不合格,可以根据相应的回归方程调整评价体系的相关系数,然后进行比较。比较通过后,即可暂时使用血细胞分析检测系统。此外,应加强质量控制系统,注意患者的标本复查,如有异常应立即向科室领导报告。
4 结 论
根据实验室的研究,在临床工作中,同一项目在不同检测系统下的检测结果会存在一定的偏差。造成这种偏差的原因有很多。必须注意不同测试系统之间的差异[12-13]。因此,临床实验室定期对不同品牌或型号的同类检测仪器进行对比实验研究,有助于保证仪器系统之间良好的相关性和一致性,结果具有可比性,为临床使用提供准确可靠的检测数据,可以满足临床需要。只有全自动血细胞分析仪系统完备、异常提示突出、性价比明显,才能更受客户欢迎[14-15]。
参考文献
[1]孙兵.不同血细胞分析仪检测结果的比对研究[J].饮食保健,2020,7(6):203-204.
[2]陈娟,吴志成,赖小婷,等.D6-CRP型与XN-9000型血细胞分析仪比对的结果分析[J].中国医学装备,2020,17(5):215-218.
[3]Clinical and Laboratory Standards Institute. Measurement procedure comparison and bias estimation using patient samples; Approved Guideline-Third Edition:CLSI EP9-A3[S]. 2013.
[4]ENGLAND J M, ROWAN R M, VAN ASSENDELFT O W, et al. Protocol for evaluation of automated blood cell counters. International Committee for Standardization in Haematology (ICSH) [J]. Clinical and laboratory haematology, 1984, 6(1): 69-84.
[5]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.临床血液学检验常规 项目分析质量要求:WS/T406-2012[S].北京:中国标准出版社,2012.
[6]徐建华,刘冬冬,黄宪章,等.新指南CLSI EP9–A3在方法学比对及偏移评估中的应用[J].中华医學杂志,2015,95(12):894-897.
[7]苏航就,周程艳,阳文辉.CLSI EP9-A3在两种血细胞分析仪检测系统比对中的应用[J].中国临床新医学,2019,12(7):751-754.
[8]BURNETT D. ISO 15189:2003--quality management, evaluation and continual improvement [J]. Clinical Chemistry And Laboratory Medicine, 2006, 44(6): 733-739.
[9]CLSI.Method comparison and bias estimation using patient samples:EP9-A2[S].2nd ed,Wayne PA:CLSI,2002.
[10]石文,戴永辉,邱峰,等.CLSI EP9-A3在血液分析仪比对中的应用[J].临床检验杂志,2016,34(1):67-69.
[11]徐江月.两台不同型号血细胞分析仪比对试验分析[J].智慧健康,2019,5(22):7-8.
[12]WANG N, JIANG J, WANG J, et al. Detection of nucleated red blood cells using the Mindray BC-6800Plus hematology analyzer: a clinical performance evaluation [J]. Annals Of Palliative Medicine, 2021, 10(8): 8808-8017.
[13]LONG Y, LIU J, CHEN F, et al. Evaluation of humoral pattern detection performance of Mindray BC-6000PLUS blood analyzer based on WS/T 662-2020[J]. Annals Of Palliative Medicine, 2021, 10(6): 6446-6454.
[14]JO S Y, PARK S H, KIM I S, et al. Performance evaluation of recently launched Sysmex XN-550 Automatic Hematology Analyzer[J]. International Journal of Laboratory Hematology, 2017, 39(1): e4-e9.
[15]欧阳贵平,王河生.迈瑞BC-5390与Sysmex XN-10两台血细胞分析仪新鲜血检测结果的比对分析[J].实验与检验医学,2019,37(4):638-640.
作者简介
佘文婕,本科,讲师,主要从事临检、生免检验等研究工作。
(责任编辑:张瑞洋)
