磁性煤矸石地质聚合物类芬顿降解苯酚
2023-02-02吴丹蕾吉登高郭精茂曹守发马建超
吴丹蕾,吉登高,郭精茂,曹守发,王 欣,马建超
(太原理工大学 a.矿业工程学院,b.材料科学与工程学院,太原 030024)
煤矸石(CG)是煤炭行业排放量最大的固体废弃物[1]。据统计,我国CG已累计堆存超过70亿t,造成了严重的环境污染[2]。CG富含Si、Al等元素,因此有望替代粉煤灰、矿渣和偏高岭土等物质制备地质聚合物[3]。地质聚合物(简称地聚物)是一种新型硅铝胶凝材料[4],具备耐腐蚀、热稳定好等化学性能和一定的孔道结构,可用于处理废水[5-6]。
苯酚是一种难降解且生物毒性高的有机污染物[7],《污水排入城镇下水道水质标准CJ 343-2010》规定苯酚必须达到1 mg/L或者0.5 mg/L才可排放,但是仅煤加工废水中苯酚浓度便高达9~6 800 mg/L.为此,亟待探寻高效可行的含酚废水处理方法。在众多处理方法中,类芬顿氧化法具有将有机物最终氧化降解为CO2和H2O的优点而受到广泛关注[8],朱佳裔等[9]使用FeOOH作为类芬顿催化剂,其对对氯硝基苯的降解率在30 min可达80%以上。YAN et al[10]使用Fe(OH)2胶体作为类芬顿活化剂,利用胶体和H2O2高效去除罗丹明 B等有机污染物。杨霏等[11]通过将纳米零价铁(nZVI)负载到伊利石上制备出It/CTAB@nZVI,有效降低了nZVI团聚、分散性差的问题,而负载后的材料对头孢哌酮的类芬顿降解率相较于单体nZVI从77%提升至96.4%,且4次循环使用后It/CTAB@nZVI的降解率仍能达到81.0%,而nZVI已降低至37.4%,由此证明载体材料对类芬顿反应活性及稳定性的提升有着关键的作用。但上述材料均通过离心回收导致催化剂活性组分流失、催化性能下降,因此类芬顿反应催化剂中活性组分(例如亚铁、零价铁等)的活性和催化剂回收性能影响了该方法的推广应用[12-13],本课题组通过在水处理材料中添加Fe3O4解决了类芬顿材料回收难题[14-15]。此外,地聚物的三维网状结构可为催化活性组分提供良好的载体,分散催化活性组分,增强类芬顿催化剂的活性[16]。
为此,本文以CG为原料,在制备煤矸石地聚物(CGGP)过程中引入Fe3O4成功制备出磁性煤矸石地聚物(Fe3O4-CGGP),实验探究类芬顿降解苯酚的性能和工艺参数,结合淬灭实验,分析类芬顿降解苯酚的主要作用方式。
1 实验
1.1 实验材料
煤矸石(CG),山西大同煤矿;水玻璃(Na2SiO3),模数3.3,w(Na2O)=8.3%,w(SiO2)=26.5%,w(H2O)=65.2%,山东优索化工科技有限公司;氢氧化钠(NaOH)、浓盐酸(HCl)、双氧水(H2O2,质量分数30%)、对苯醌(C6H4O2)、糠醇(C5H6O2)、叔丁醇(C4H10O)、无水乙醇(C2H6O),分析纯,甲醇(CH3OH),色谱纯,天津市科密欧化学试剂开发中心;六水合三氯化铁(FeCl3·6H2O)、四水合氯化亚铁(FeCl2·4H2O),天津巴斯夫,分析纯;苯酚(C6H6O),天津市大茂化学试剂厂,分析纯;试验用水为去离子水。
1.2 实验仪器
分析天平(BSA224S),赛多利斯科学仪器有限公司;管式炉(SK-G06163),天津中环电炉有限公司;超声波清洗机(KQ5200DE),昆山市超声仪器有限公司;恒温搅拌水浴锅(DF-101S),上海力辰邦西仪器科技有限公司;真空干燥箱(DZF-6050),上海精密实验设备有限公司;pH计(PHS-3C),上海仪电科学股份有限公司;高效液相色谱仪(1260Ⅱ),简称HPLC,安捷伦科技(中国)有限公司。
1.3 材料的制备
1.3.1CGGP的制备
将CG研磨筛分至200目后于800 ℃在管式炉热活化4 h(加热速率为2 ℃/min),随后研磨至200目备用。取0.88 g CG倒入含有0.19 g NaOH和1.00 g Na2SiO3碱激发剂的塑料烧杯中常温下反应30 min.接着将样品于80 ℃干燥 24 h,待干燥完成后洗涤至中性,烘干研磨至200目后即得CGGP.
1.3.2Fe3O4的制备
取5.00 g FeCl2·4H2O和10.00 g FeCl3·6H2O加入到装有100 mL去离子水的三口烧瓶中于80 ℃在N2保护下搅拌30 min[17].待混合均匀后滴入NaOH至pH=9~10后再搅拌60 min,然后通过外部磁铁分离黑色沉淀物。最后,Fe3O4用蒸馏水洗涤3次,并在80℃的真空干燥箱中干燥24 h,待干燥完成后取出研磨备用。
1.3.3Fe3O4-CGGP的制备
取1.50 g与0.88 g CG混合,将其倒入含有0.19 g NaOH和1.00 g Na2SiO3碱激发剂的塑料烧杯中常温下反应30 min.接着将样品于80 ℃干燥24 h,待干燥完成后洗涤至中性,烘干研磨至200目后即得Fe3O4-CGGP.
1.4 分析方法
使用 Bruker D8衍射仪在5°~80°范围内记录X射线衍射(XRD)光谱,识别材料物相组成;在4 000~400 cm-1范围内,采用KBr颗粒法在Thermo红外光谱仪上记录了傅里叶变换红外光谱(FT-IR)来分析材料中官能团的存在和化学键的性质;通过S4800扫描电子显微镜(SEM)结合能量色散光谱(EDS)评估材料形态和元素分析。通过JEOL JEM 2010型透射电子显微镜(TEM)和高分辨透射电子显微镜(HRTEM)获得材料的纳米形态结构。通过K-Alpha型X射线光电子能谱仪(XPS)测得材料表面的元素组成与价态。材料孔性质是通过micromeritics ASAP 2020型比表面积及孔径分析仪(BET)来确定的。材料的磁性由振动样品磁强计(VSM)研究,磁场为±20 000 Oe.
1.5 类芬顿氧化实验
150 mL烧杯中倒入100 mL质量浓度为100 mg/L的苯酚溶液,pH值用0.1 mol/L HCl和NaOH调节,加入Fe3O4-CGGP材料,待吸附60 min至吸附平衡后加入H2O2.分别于3 min、5 min、10 min、15 min、20 min、30 min、45 min、60 min取1.5 mL苯酚溶液,用磁铁将Fe3O4-CGGP分离后过0.22 μm膜过滤器得到待测样品。苯酚浓度用HPLC测定,色谱柱采用ZORBAX SB-C18,流动相为甲醇∶水=1∶1.
苯酚去除率用η来表示,参数由方程式(1)推导而来:
(1)
式中:C0为溶液中苯酚的初始浓度;Ct为催化反应tmin后溶液中苯酚的浓度。实验数据为3次实验后的平均值,保证了最小的相对误差(5%).
2 结果与讨论
2.1 类芬顿氧化效果对照
在pH=4.5,催化剂用量为0.5 g/L,H2O2用量为10 mmol/L的条件下,评估Fe3O4-CGGP的类芬顿氧化降解苯酚效果。结果如图1所示,仅在H2O2存在下,对苯酚氧化去除率为6.37%.CGGP对苯酚只有吸附效果,苯酚去除率为13.49%.Fe3O4在没有H2O2的情况下仅有吸附效果,苯酚去除率仅为7.07%;在Fe3O4-H2O2体系中,对苯酚的去除率只有60.72%.在没有H2O2的情况下Fe3O4-CGGP材料对苯酚去除率为12.52%,与CGGP相比,Fe3O4-CGGP对苯酚分子的吸附能力降低,导致苯酚吸附去除率低。Fe3O4-CGGP材料对苯酚的去除率达到97.79%,这表明其催化活性相比于Fe3O4有明显提高,可能是由于Fe3O4纳米颗粒均匀分散在CGGP表面上,增加了活性点位,从而提高了苯酚降解率。

图1 不同体系降解苯酚的对照实验Fig.1 Comparative experiment of phenol degradation in different systems
2.2 材料的表征分析
2.2.1XRD表征分析
图2中(a)为CGGP的XRD谱图,2θ范围在17°~32°之间可以明显看到“鼓包峰”,这表明材料处于非晶态和半晶态之间的中间状态,证明了CGGP中硅铝酸盐水合物凝胶的形成[18-19],图中显示2θ=26.66°处的最高峰与石英的(011)晶面(JCPDF编号78-1253)相对应,在2θ=20.9°、36.56°、40.34°、50.12°和67.82°时分别对应石英的(100)、(110)、(102)、(11-2)和(21-2)晶面(JCPDF编号78-1253),同时2θ=26.66°处的最高峰与硅酸铝的(021)晶面(JCPDF编号16-0602)相对应,在2θ=39.56°处的衍射峰对应于硅酸铝的(202)晶面,表明成功制备出煤矸石地聚物[3]。图2中(b)为Fe3O4的XRD图谱,2θ=35.65°处的最高峰与(311)晶面相对应,位于2θ=30.14°、43.34°、53.66°、57.32°和62.72°分别对应Fe3O4的(220)、(400)、(420)、(511)和(440)晶面(JCPDF编号99-0073),表明成功制备出Fe3O4[20].图2中(c)为Fe3O4-CGGP的XRD图谱,可以看出Fe3O4-CGGP的“鼓包峰”相较于CGGP的峰形面积有所减小,这可能是由于引入磁性颗粒,地聚物的无定形凝胶相产物相对减少[19]。Fe3O4-CGGP与CGGP的主峰相同,在2θ=20.9°和2θ=50.12°处,对应石英的(100)和(11-2)晶面;Fe3O4-CGGP除保留了CGGP的特征峰外,在2θ=30.14°、35.65°、57.32°和62.72°处,分别对应Fe3O4的(220)、(311)、(511)和(440)晶面,表明Fe3O4-CGGP成功制备。

图2 样品的XRD图Fig.2 XRD patterns of samples
2.2.2FT-IR表征分析
图3中(a)、(b)、(c)分别为CGGP、Fe3O4及Fe3O4-CGGP的FT-IR谱图。从图3中(a)可以看出800~1 200 cm-1对应于Si—O—T键(T代表Si或者Al)不对称拉伸振动,为地聚物的特征峰[3];3 453 cm-1和1 647 cm-1分别归因于水分子的—OH伸缩振动和H—O—H的形变振动,表明材料中含有化学结合水。1 454 cm-1处的振动峰归因于O—C—O的拉伸振动,表明地聚物碳酸化形成碳酸盐。图3中(b)可以看出574 cm-1处的位置出现了Fe—O键特征吸收峰。3 391 cm-1和1 619 cm-1处的峰是由于—OH键的伸缩振动和弯曲振动引起的,这是由于Fe3O4表面羟基形成缔合氢键形成了吸收峰[20]。从图3中(c)可以得出1 007 cm-1处的峰值与CGGP的不对称Si—O—T拉伸振动有关,由于在聚合过程中引入Fe3O4参与聚合,导致吸收峰向低波数移动,增加了振动带的峰强[3];699 cm-1的振动峰归因于SiO4/AlO4四面体屈曲和AlO4对称伸长,证明了CGGP前驱体的地质聚合作用;从450 cm-1到600 cm-1的范围是Fe—O键振动的特征,457 cm-1与699 cm-1处的条带与Si—O—T键屈曲有关[21-22]。
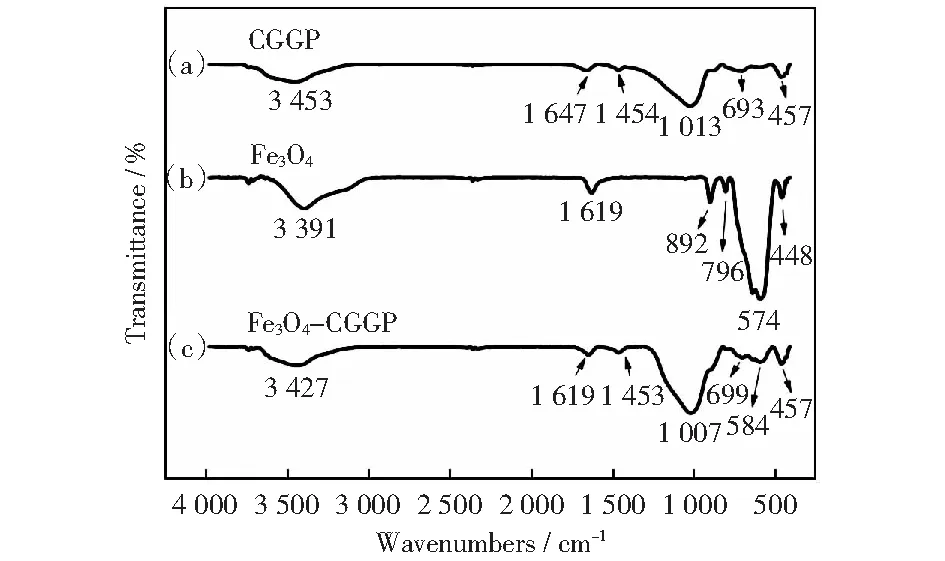
图3 样品的FT-IR图Fig.3 FT-IR spectra of samples
2.2.3形貌表征分析
图4(a)是Fe3O4的SEM图。从图中可以观察到粒径不均匀、形貌不规则的Fe3O4球形颗粒。再对Fe3O4进行HRTEM测试,见图4(b).从图中可以看出合成的磁性Fe3O4颗粒呈现球形结构,表面粗糙,粒径在10~20 nm左右,间距为0.30 nm的晶格与Fe3O4的(220)晶面良好吻合。图4(c)是CGGP的SEM图,由于聚合发生在CG表面,碱激发剂溶解CG以释放Si4+和Al3+用于地聚物,表明CGGP是NASH凝胶、硅铝酸盐凝胶和煤矸石颗粒的混合物[3]。图4(e)是最佳配比下Fe3O4-CGGP的SEM图,从图中可以观察到Fe3O4均匀分散在CGGP表面。

图4 样品的形貌图Fig.4 Morphology of samples
图4(d)是CGGP的EDS图谱,图中出现的这些峰分别对应于O、Si、Al和Na等元素。图4(f)是Fe3O4-CGGP的EDS图谱,图中出现的峰分别对应于O、Fe、Si、Al和Na等元素。结果表明:负载后的材料含Fe元素,与XRD分析结果相结合,可证实材料中存在Fe3O4和CGGP.
图5是Fe3O4-CGGP的EDS mapping图,可以清晰观察到Fe、Si和Al等元素的分布情况,由图可知,CGGP主要由Si、Al元素组成,与XRD、FT-IR分析结果一致;Fe元素分布均匀,证实Fe3O4均匀分散在CGGP表面。

图5 样品的EDS mapping图Fig.5 EDS mapping diagrams of sample
2.2.4XPS表征分析
图6(a)为Fe3O4-CGGP的XPS全谱图,由图可知,Fe3O4-CGGP主要由Na、Fe、O、C、Si和Al元素组成。图6(b)为O 1s的高分辨谱图,在结合能为531.9 eV、530.7 eV和529.2 eV处分别对应Si—OH、Si—O—Si和Si—O—Al键[23],这与文献表述一致,再次证实了CGGP的形成[24-25]。另外,531.1 eV处对应Fe—O键[26]。图6(c)为Fe 2p的高分辨谱图,在结合能为723.9 eV和710.2 eV处分别对应Fe 2p1/2轨道和Fe 2p3/2轨道,在726.5 eV和711.7eV处分别对应Fe3+的2p1/2轨道和2p3/2轨道[27],在723.8 eV和709.9 eV处分别对应Fe2+的2p1/2轨道和2p3/2轨道,因此,复合催化剂中铁的存在形态是Fe2+和Fe3+的氧化物, 对比NIST X射线光电子谱图证明该氧化物为Fe3O4[28].

图6 样品的XPS图Fig.6 XPS diagrams of sample
2.2.5BET表征分析
图7为CGGP和Fe3O4-CGGP的吸附-脱附曲线和孔径分布图。二者的N2吸附-脱附等温线均为Ⅳ型曲线,在p/p0为0.5~1之间均显现出H3型滞后环。从孔径分布图可以看出,CGGP的孔径分布在10 nm周围,Fe3O4-CGGP的孔径分布在13 nm周围,均为介孔材料。

图7 N2吸脱附等温线及孔径分布图Fig.7 N2 adsorption-desorption isotherms and pore size distribution
表1所示CGGP的BET比表面积为5.26 m2/g,负载Fe3O4后增大至9.42 m2/g,Fe3O4-CGGP的孔容较CGGP的0.01 cm3/g增大至0.03 cm3/g,平均孔径从10.74 nm增大至13.25 nm.由于Fe3O4是在地聚物聚合成型过程中引入的,所以CGGP表面和内部因嵌入Fe3O4而使得孔容、孔径相对增大。

表1 比表面积、孔容、孔径一览表Table 1 List of specific surface area, pore volume, and pore diameter
2.2.6VSM表征分析
图8(a)为材料的VSM磁滞回线图。从图中可知,Fe3O4纳米颗粒和Fe3O4-CGGP的饱和磁化强度分别为68.50 emu/g和35.68 emu/g.与Fe3O4相比,Fe3O4-CGGP的磁化强度下降,这是由于引入无磁性的CGGP载体所致。但是仍表现出足够磁性,能够通过外部磁场进行分离(见图8(b)).

图8 样品的磁性能表征Fig.8 Characterization of magnetic properties of samples
2.3 类芬顿氧化实验条件优化
2.3.1pH值对催化性能的影响
将溶液pH值调至2.5、3.5、4.5、6.0和8.0探究pH值对降解苯酚效果的影响。结果见图9,当pH值为2.5时,反应60 min Fe3O4-CGGP对苯酚的去除率达到98.34%;pH值为3.5时,反应60 min苯酚去除率达到99.40%.因为在酸性条件下,H2O2更易聚集在Fe3O4-CGGP上产生·OH,易于发生≡FeIII与≡FeII的转化,但在强酸条件下,负载在材料外表面上的Fe3O4易被腐蚀而导致材料催化性能降低[29]。在pH值分别处于4.5、6.0和8.0时,苯酚的去除率依次为97.79%、36.54%和12.37%.当pH>6.0时,苯酚去除率很低,可能是在碱性条件下水溶液中OH-的数量较多,与≡FeIII极易生成沉淀,阻碍了与≡FeII的转化,不利于H2O2产生·OH.因此苯酚降解的最佳pH值为3.5.

图9 pH值对催化性能的影响Fig.9 Effect of pH values on catalytic performance
2.3.2催化剂用量对催化性能的影响
考察了催化剂投量分别为0.1、0.3、0.5、0.6、0.7、0.8和1.0 g/L对降解苯酚效果的影响。由图10可看出,催化剂投量在0.1~0.8 g/L之间时,苯酚去除率随着催化剂投量的增加而增加,在催化剂投量为0.8 g/L时苯酚去除率达到100%.这是因为Fe3O4-CGGP用量的增加使得活性位点和活性组分的数量增加,吸附更多的苯酚和H2O2到催化剂表面,产生更多的·OH参与到苯酚的降解中,增大苯酚去除率。然而,催化剂投量在0.8~1.0 g/L之间时,苯酚的去除率随着催化剂投量的增加反而减小。这是因为当催化剂投加过量时会导致材料表面的≡FeII消耗了·OH,降低了苯酚的降解率[30]。
≡FeII+·OH→≡FeIII+OH-.
(2)
综合考虑到成本及其他因素,催化剂投量在0.5、0.6、0.7和0.8 g/L时,反应60 min的去除率均达到100%,故选用催化剂投量为0.5 g/L.

图10 催化剂用量对催化性能的影响Fig.10 Effect of catalyst dosage on catalytic performance
2.3.3H2O2用量对催化性能的影响
考察了H2O2投量分别为5、10、15、20、25和30 mmol/L对降解苯酚效果的影响。从图11中可以看出,H2O2投量在5~20 mmol/L时,H2O2投量增加,苯酚降解速率随之增加,在H2O2投量为10~20 mmol/L时均达到最大值100%;当H2O2投量增加到25~30 mmol/L时,苯酚的降解速率随着H2O2投量的增加而减小,此时的降解率为91.03%.

图11 H2O2用量对催化性能的影响Fig.11 Effect of H2O2 dosage on catalytic performance
这是因为过量的H2O2会与·OH反应[31]。
H2O2+·OH→H2O+HO2·HO2· .
(3)
HO2·+·OH→H2O+O2.
(4)
综合考虑经济效益最大化原则,选用H2O2最佳投量为10 mmol/L.
2.3.4苯酚初始质量浓度对催化性能的影响
考察了苯酚初始质量浓度分别为50、100、125、150、200和250 mg/L对降解苯酚效果的影响,结果见图12.在60 min内,Fe3O4-CGGP对50和100 mg/L苯酚的降解率为100%;当质量浓度升高至125~250 mg/L时,苯酚的降解率分别为87.08%、76.05%、69.02%和64.32%,呈现苯酚降解率随苯酚浓度升高而降低的趋势。这是由于当Fe3O4-CGGP和H2O2的投加量恒定时,苯酚初始质量浓度升高后,在Fe3O4-CGGP表面形成的·OH的初始浓度是恒定的,苯酚初始质量浓度过高会阻碍活性物质与苯酚分子的有效结合,导致苯酚的降解率降低[32]。故选择100 mg/L为最佳苯酚初始质量浓度。

图12 苯酚浓度对催化性能的影响Fig.12 Effect of phenol concentration on catalytic performance
2.4 催化材料稳定性
为了研究 Fe3O4-CGGP催化剂的可重复性能,在最佳条件下进行7次重复催化实验,结果见图13.

图13 Fe3O4-CGGP的重复使用性能Fig.13 Reusable performance of Fe3O4-CGGP
从图中可以看出,Fe3O4-CGGP连续使用6次后对苯酚的去除率可达87.44%.铁离子溶出实验表明,浸出液中总铁的溶出量为1.473 mg/L,其中Fe3+为1.049 mg/L,Fe2+为0.424 mg/L,与Fe3O4-CGGP的投加量0.5 g/L相比,可以忽略铁离子的溶出量。说明Fe3O4-CGGP具有较好的稳定性。
2.5 淬灭实验

图14 淬灭剂及叔丁醇浓度对催化性能的影响Fig.14 Effects of quenchers and tert-butyl alcohol concentration on catalytic performance
3 结论
1) 以固体废弃物煤矸石为原料,经800 ℃热活化、氢氧化钠和硅酸钠混合碱激发后成功制备出CGGP,在CGGP成型过程中引入磁性Fe3O4材料成功制备出Fe3O4-CGGP.
2) Fe3O4-CGGP的XRD谱图出现地聚物的“鼓包峰”及Fe3O4的特征峰,FT-IR谱图中显示出地聚物Si—O—Si和Si—O—Al的振动峰以及Fe3O4的Fe—O振动峰;从SEM形貌推断出材料表面为N—A—S—H凝胶和硅铝酸盐凝胶及均匀分布的纳米Fe3O4,10~20 nm的Fe3O4均匀分散在CGGP表面;VSM表明Fe3O4-CGGP的饱和磁化强度为35.68 emu/g.
3) 在pH=3.5,催化剂投量为0.5 g/L,H2O2投加量10 mmol/L的条件下,反应60 min,100 mg/L的苯酚降解率为100%.Fe3O4-CGGP使用6次后苯酚降解率为87.44%,表明Fe3O4-CGGP具有良好磁性及稳定性。叔丁醇淬灭实验表明,·OH在Fe3O4-CGGP催化降解苯酚中占主导作用。
