新型固体储氢材料的研究进展
2023-02-02金之钧苏宇通
王 璐, 金之钧,3, 苏宇通
(1.北京大学 能源研究院,北京 100871;2.北京大学 地球与空间科学学院,北京 100871; 3.中国石化 石油勘探开发研究院,北京 100083)
能源供给是经济增长的重要保障,对人类生活质量起着至关重要的作用。世界人口的增长伴随着能源需求的大幅增长,仅从2000年到2019年,能源消耗从408 EJ增加到585 EJ,2000年—2018年每年持续增长约2%[1-2]。目前,大部分能源需求由石油、煤炭和天然气等化石燃料满足,导致全球气候变化、空气和水污染以及臭氧层损耗[3]。因此,全球加速寻找可能替代化石燃料的替代能源。而在如今中国碳中和的背景下,寻找清洁能源变得十分重要。
太阳能、核能、风能、海浪能、地热能、水电等已成功应用于多种用途[4],然而,这些能源不能直接作为燃料用于如陆地运输、航空运输和远洋船舶等应用[5]。氢气具有极高的单位质量能量(热值为142 MJ/kg)、低质量密度(标准状态下密度0.0899 g/L)、巨大的环境和经济效益(无毒无污染,燃烧产物是水),作为地球上最常见的元素之一,以多种形态存在(可以气态、液态或固态形式存在,能够在不同的环境下储存),损耗小,可以避免高压远距离输电造成的能量损失,并且可以反复循环使用,因此被认为是未来最有希望的化石燃料替代品,被称为“未来燃料”[6-9]。氢气的用途也比较广泛,可以用于炼油厂、热工业、钢铁业、建筑动力、交通如氢能汽车,以及航空、深海船等。还有一个很重要的用途就是将二氧化碳加氢生成甲醚、甲醇等,可实现二氧化碳的消耗,有利于实现碳中和。据McKinsey公司[9]预测,到2050年氢气的需求量将比2022年增加5倍,主要用于钢铁业、深海船、航空等方面。因此氢能有望在能源转型中发挥主要作用。
发展氢能需要解决氢的制取和储运问题。由于在环境温度和常压下,氢气的密度只有0.09 kg/m3,且氢气易燃、易爆、易扩散,因此在实际应用中要优先考虑氢储存和运输中的安全、高效和无泄漏。近年来,氢燃料电池汽车的快速发展有效促进了储氢技术的进步,但高效、安全、经济的储氢技术仍是现阶段氢能应用的瓶颈问题。
1 储氢技术概况
目前,储氢方法按照氢气的相态可以分为气态储氢、液态储氢和固态储氢。气态储氢是将氢气压缩于高压容器罐中,优点是其充放氢速率快并且成本较低;缺点是储量小且在运输途中容易发生泄漏,安全性差,而且要求容器材料能够承受氢气可能产生的脆化,并且要轻质、耐燃、耐高温和耐降解[10-11]。液态储氢是将氢气低温液化后储存在特殊容器中,是一种轻巧紧凑的存储方法,多用在火箭、飞船等领域,优点是储能密度较高,缺点是氢气液化的能耗大,约为液化氢能的30%~40%。固体储氢是指利用物理或化学吸附的方法将氢气储存在固体材料中,固体储氢因其具有安全性、经济性等优点,目前在国内外都受到了广泛研究。固体储氢包括金属及合金储氢、多孔碳材料储氢、水合物储氢、络合物储氢等多种方式[12]。
金属化合物储氢是储存氢的最紧凑的方法之一,是目前研究较多的储氢方法。氢与某些金属或合金(Ti、Mg、Ni、Fe、Mn、La等)在一定温度和压力下反应生成金属氢化物。在加热条件下,其又可分解释放出氢气[13-15]。虽然金属氢化物的单位体积储氢量较高,但是其质量储氢密度(质量分数,下同)较低,大多数低于3%[15],例如,LaNi5H6的质量储氢密度仅为1.4%[16]。虽然MgH2的质量储氢密度达到7.6%,但在吸、放氢过程中有不可逆损伤,影响了储氢材料的使用寿命,限制了该方法的应用。另外,许多合金成本较高也是金属氢化物应用的主要缺点[16-18]。
此外,H2化学吸附到金属表面需要一定的活化能,需要升高压力,且是一个放热反应会产生热量。而释放储存的氢气,必须降低压力,并对系统施加热量。形成的金属氢化物越稳定,放氢时需要的能量就越多,即吸放氢条件不温和,这也限制了金属氢化物在储氢上的应用。虽然一些金属氢化物在接近环境的温度就可以释放氢气,但它们的储氢能力较低;而有一些络合氢化物具有较高的氢气储存能力(NaBH4、LiBH4、Mg(BH4)2的理论氢质量分数均为5.5%~21%),但其反应动力学缓慢,需要高温处理才能从氢化物中释放H2[16-18]。有机化合物储氢,其优点是储氢量高、安全和储运方便,不足之处是化学反应难以控制,距离商业化应用还有很远距离[19]。
2 新型固体储氢材料研究进展
近年来,由于物理吸附储氢具有安全可靠、储存效率高、能够在温和条件下吸附/解吸附氢气等特点而迅速发展。目前物理吸附储氢材料研究的热点是多孔碳材料(如分子筛、碳纳米管、富勒烯、活性炭等)、硅纳米管、金属有机骨架材料(MOFs)、共价有机材料(COFs)等[20-21]。
2.1 生物质多孔碳材料
与金属有机骨架化合物和分子筛等吸附剂相比较,多孔碳材料由于其本身优异的物理化学性能如质量轻、吸附量大、可重复使用、对少量气体杂质不敏感,同时具有来源广、制备工艺简单等优点,从而成为高效储氢材料的研究热点,如碳纳米材料和活性炭[22-23]。
碳纳米材料主要包括碳纳米管和碳纳米纤维[24]。由于不同学者制备的碳纳米管材料不同、采用的氢吸附条件不一,致使目前文献中关于碳纳米管储氢效果的报道差别较大[25],且质量储氢密度高于10%的数据很难重复,多出于样品污染或错误测量。诸多研究者对碳纳米管进行了研究,证明其有一定的储氢能力,但目前碳纳米管的制备方法为激光法和电弧法,均无法满足大规模生产的要求。另外,碳纳米管需要5 h达到最大吸附容量(质量分数4.2%),碳纳米纤维需要14 h才能达到其最大吸附容量[26],这极大地限制了碳纳米材料在储氢上的大规模应用。活性炭是一种很好的吸附剂,其比表面积大、原料来源广泛,且经过表面化学改性或金属负载改性后的吸附性能将有很大提高。与其他储氢材料相比,高比表面积的活性炭储氢量大、吸放氢条件温和、解吸快,是一种较有潜力的储氢材料[27]。但总的来说,多孔碳材料的成本较高,制约了其商业应用,降低多孔碳的制备成本,将进一步推动多孔碳材料在储氢方面的应用。
生物质由于其在全球普遍存在且成本很低,是一种很有前途的可再生能源,目前在国外已经有很好的发展。研究人员为了降低多孔碳的成本,利用生物质废弃物作为廉价的碳前驱体,以获得成本较低的多孔碳。其中微藻是一类分布广泛的藻类植物,已在许多领域得到开发和应用。小球藻作为一种著名的绿色微藻,被认为是优质的生物质来源,具有巨大的生物技术潜力,可生产各种高性能产品[28]。Seifi等[29]采用水热法将小球藻制备成多孔碳。在经过热液处理之前,原料首先水解成许多中间产物,然后通过脱水和聚合重新转化为微球核。微球核通过周围分子的吸附形成分散的胶体颗粒结合成的碳微球。微藻发生相分离,通过离心分离上溶液和底沉淀。在KOH电解质中经过40次循环后,制备出的微藻基多孔碳具有良好的孔结构(介孔)、高比表面积(718 m2/g)和适当的表面官能团(C—OH、C—O—S和COO—),其电化学储氢能力达到1040 (mA·h)/g(质量储氢密度≈3.9%)。以上结果表明,微藻生物质可以成功地应用于电化学储氢。
近年来,国内研究人员也开始寻找含碳量丰富的生物质废弃物作为廉价的碳前驱体,以获得成本较低的多孔碳,并逐渐在一些企业投资生产,以改善生物质资源被浪费并造成环境污染的现状。随着生物质多孔碳研究的深入,有学者对生物质多孔碳的吸附储氢性能展开了研究。如刘雪岩[30]用蓝藻制备了活性炭,周向阳等[31]用生物质玉米芯制备了活性炭,李长明等[32]用坚果壳制备了多孔碳材料,并对其储氢性能进行了研究,用氨水改性方法制备的蓝藻基活性炭在 77 K、0.1 MPa下,最高的储氢量达到 2.52%。以生物质玉米芯为原料,采用氢氧化钾活化的方法制备的活性炭,当碱/碳质量比为4、活化温度为850 ℃时,样品在-196 ℃、4.0 MPa下储氢性能最好。证明碱/碳质量比不仅对样品的比表面积和总孔体积有影响,而且影响其孔径分布,最终影响储氢性能。以坚果壳为原料进行活化后,制得的生物质多孔碳材料的比表面积大于1000 cm3/g,电流密度5A/g下充放电10000次后,其储氢容量保持在90.625%[30-33]。Wang等[34]利用氢氧化钾对各种真菌基进行化学激活(见图1),制备的多孔碳材料具有高表面积(1600~2500 m2/g)和孔隙体积(0.80~1.56 cm3/g),各种真菌制备的多孔碳在0.1 MPa和-196 ℃条件下实现了较好的H2吸收,饱和H2吸收质量分数最高达2.4%;在高压条件下(3.5 MPa),各种真菌基多孔碳在-196 ℃时,饱和H2吸收质量分数为4.2%~4.7%。此外,Zhao等[35]利用蒲公英管制备多孔碳材料,进行碳化后保留了其管状形貌,该材料的电化学性能和储氢性能都较好。Wang等[36]用花生皮通过用氢氧化钾化学活化制备多孔碳,制备处理片状形貌、比表面积较大(2500 m2/g)的材料。Wang等[37]以生物质玉米芯为原料,采用热解炭化和KOH活化法制备了玉米芯活性炭。通过改变活化条件,可获得大孔体积、超高BET比表面积的样品。样品在4 MPa和-196 ℃条件下取得了最高的吸氢能力,为5.80%。此外,研究人员还利用青蒿壳、甘蔗渣、棉花、稻壳、竹笋壳、莲梗、丝蛋白、香蒲和木材等废弃生物质制备多孔碳材料,以实现低成本储氢[38-40]。

图1 多种真菌制备的多孔碳材料[34]Fig.1 Porous carbon prepared by various fungi[34](a) Fungi such as auriculariale, Coprinus comatus, lentinus edodes, agarics; (b) Photograph and SEM image of the fungi-based porous carbon.
生物质多孔碳吸附氢气的原理有物理吸附和化学吸附两大类。物理吸附主要是通过范德华力吸附,主要取决于材料本身,材料的比表面积和孔隙结构会影响材料对氢气的吸附能力。此外可以通过在制备过程中采用水热碳化、活化等方法来增加材料的比表面积来提供更多的表面活性位点,从而增强材料对氢气的吸附能力,如采用氢氧化钾化学活化材料。化学吸附主要是利用官能团作用力或者分子间π-π相互作用力等来吸附。所以综合衡量生物碳的成本与环境效益(可以使用废弃物)、可持续性、表面活性、孔径分布、能量密度、稳定性、氢气吸附速率等因素,以生物质作为碳前驱体制备多孔碳有望成为理想的储氢材料并实现工业化[41-43]。
2.2 矿物储氢材料
矿物储氢材料是指自然界中具有结构性纳米孔道的天然多孔矿物,晶体内有大量的空穴和孔道[44-45],如沸石、黏土矿物(包括坡缕石、海泡石、蒙脱石、伊利石)等,其纳米孔道具有一维、二维或三维的尺度。由于矿物表面粗糙、比表面较大、表面能较高、通常具有极性,从而对氢分子产生吸引,所以矿物储氢的原理除有物理吸附外,还有化学吸附[46-48]。矿物储氢材料的吸附性能一般与其比表面积成正相关,其中内表面的贡献远大于外表面[49]。矿物储氢的优点是储氢方式简单,成本较低。此外,对矿物进行改性,可以进一步提高储氢性能。
沸石具有良好的热稳定性、整齐的孔道结构、分子大小的孔径尺寸、强吸附性、高比表面积等特点,是常见的实现工程应用的天然矿物材料之一,已被广泛用作吸附剂、重金属和放射性元素固定、离子交换剂和催化剂,并用于氨-氮吸附以及气体的净化、污水的处理等[50-55]。沸石的表面积高达100~500 m2/g,按照孔道特征可以分为一维、二维和三维体系。但对沸石能否作为理想的储氢材料,众学者分歧很大[54-58]。有研究人员发现,磨细的沸石样品具有较高的氢吸附能力,吸附氢气质量分数可达7%[59]。Vitillo等[60]发现在77K 时,沸石的储氢质量密度最大为1.81%。Weitkamp等[61-62]发现,含Na+、K+、Rb+等可交换阳离子的A型沸石(除CsA沸石)均有氢气吸附性能,但效果并不理想。Anderson等[63]发现,在低温77 K、压力4 MPa下,沸石Na-X的储氢质量密度最大为2.55%。
针对实验中沸石储氢性能的不同,有学者认为这主要是由于沸石复杂的微孔结构所造成的,沸石的微孔结构被沸石的化学成分、骨架特征及其所含的阳离子所影响,而形成独特的孔笼或孔道组成的二维或三维的复杂孔道体系。一些学者从理论上进行研究,通过采用巨正则蒙特卡罗(GCMC)和分子动力学等手段模拟氢气分子在沸石中的吸附扩散行为。Vitillo等[64]采用分子动力学模拟预测77 K时沸石质量储氢密度为2.65%~2.86%。Du等[65]采用巨正则蒙特卡罗方法模拟了ZSM-5分子筛中分子氢在过临界温度时的吸附特性,发现随着温度的降低和压力的增加,氢的吸附量增加。在25 K和10 MPa时,吸氢质量分数最高为2.24%。总之,目前报道的沸石的储氢量差别较大,因此沸石是否可以作为良好的储氢材料还有待加深研究。但总的来说,沸石单位质量相对较大,内部还有许多不能吸附氢气的大直径的空间,可能不是最好的矿物储氢材料的选择。
具有纳米通道的黏土矿物,有高纯度、结构一致性、粒径可精细控制和可用简单廉价的设备提纯等优点。黏土易于制备以及在空气中稳定、安全性的特点为研究其物理吸附H2提供了一个理想的环境[66-68]。层状硅酸盐黏土(Layered silicate clay) 是由[SiO4]4-四面体以角顶连接而成的有规律的二维无限延伸的层状硅氧骨架的硅酸盐矿物,其层状结构见图2[69]。根据晶体结构类型的不同,层状硅酸盐矿物主要分为2∶1型层状结构如蒙脱石族(蒙脱石)、海泡石族(海泡石、凹凸棒石)、云母石族(伊利石)等和1∶1型层状结构如高岭石族(高岭石、埃洛石)和蛇纹石族(蛇纹石)等[70-71]。层状硅酸盐矿物晶体结构中的络阴离子[SiO4]4-为层状硅氧骨架,称为四面体片,与四面体片结合的阳离子均位于活性氧和OH-组成的八面体空隙中,构成八面体片,四面体片与八面体片构成层状硅酸盐的结构单元片层[72]。结构单元片层厚度及片层间距大约为1 nm,层间可以由水分子或阳离子填充。层状硅酸盐矿物自身具有特殊的分子结构和大的比表面积,具有较好的吸附能力。
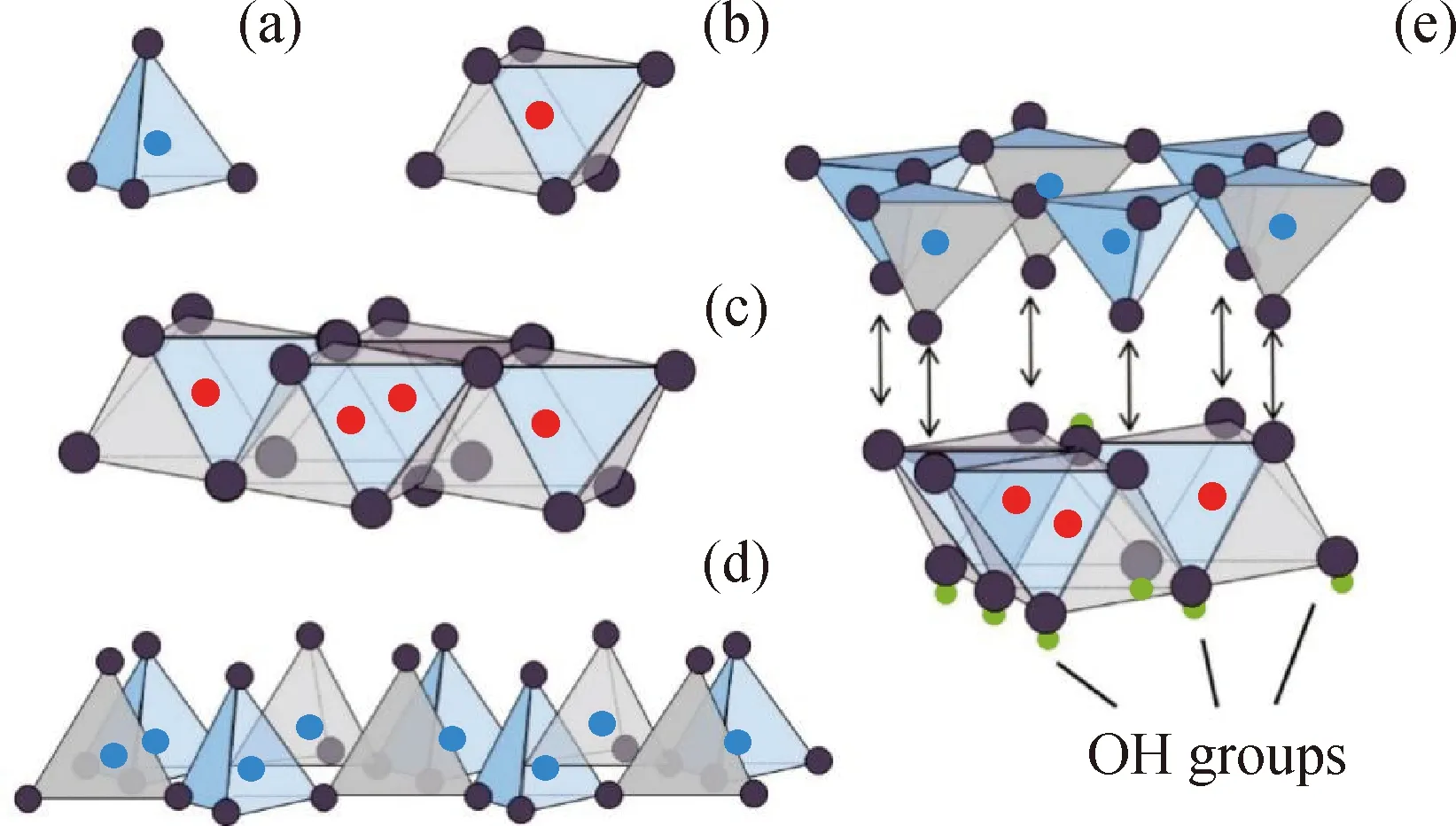
Blue circle—Silicon atom; Red circles—Aluminum atom; Dark purple circle—Oxygen atom; Green circle—Hydrogen atom图2 黏土矿物层状结构[69]Fig.2 Layered structure of clay minerals[69](c) Connected octahedral sheet of AlO8; (d) Connected tetrahedral sheet of SiO4; (e) Tetrahedral sheet connected to octahedral sheet forming a 1∶1 layer
国外学者对黏土矿物的微孔结构进行了研究,认为一些黏土矿物具有分子筛特征[73-74]。Hizal等[75]研究了蒙脱石对Cu(Ⅱ)、Cd(Ⅱ)和Pb(Ⅱ)的吸附及其表面络合动力学,发现了蒙脱石良好的吸附能力。Wang等[76]研究了三维网状蒙脱石水凝胶对Pb(Ⅱ)的吸附能力。陆银平、杜春芳、程伟等[67-71]的研究结果均表明,蒙脱石、高岭石、海泡石等黏土矿物具有很好的吸附性能。
在这些黏土矿物中,高岭石和滑石没有层电荷,不能吸引层间阳离子,没有结合位点可以吸附H2。伊利石和云母主要以钾离子为层间阳离子,层间空间对于氢气来说太小,从而限制了对氢气的吸附[73]。而蒙脱石有希望成为良好的储氢材料,因为它具有高的比表面积与易于可调的层间区域,层间空间的大小可由阳离子控制交换较大的离子或通过调整水蒸气压力来调节。通过对Ca2+和Mg2+等离子进行交换,可以进一步调整层间的结合势能,从而来提供合适的H2吸附位点[74-78]。天然一维多孔海泡石族矿物——海泡石和坡缕石,具有2∶1型的链状结构,在尺寸、形状和结构构造上都与人工合成的纳米材料(碳纳米管)十分相似,为纤维状黏土矿物,具有较高的比表面积,较高的孔隙率、较多的表面电荷,因此具有良好的吸附性能和较好的储氢能力[79-81]。其中海泡石比表面积(420 m2/g)比坡缕石的比表面积(298 m2/g)大,具有更好的吸附氢气的性能。此外,黏土矿物由于固体表面极性与氢分子发生强烈相互作用,会吸收更多的氢。木士春等[81]发现,增加压力,海泡石的储氢量会增加[81]。矿物的比表面积和孔径会影响氢气的吸附,从而推测矿物储氢的机理为物理吸附。综上,矿物对氢气的吸附能力较强,但对于矿物吸附氢气的机理还需要更深入的研究。
此外,对天然矿物进行加工改造可以提高其储氢能力。有研究人员研究了NH4-蒙脱石的储氢特征,发现与蒙脱石相比,其储氢性能提高[77]。铁-蒙脱石具有较高的储氢释氢能力、可回收性和优异的热稳定性,是一种具有广阔应用前景的化学法储氢材料。钯负载有机蒙脱石也可提高蒙脱石储氢的性能(见图3)[82]。因此加工改造天然矿物也不失为一种好的制备储氢材料的途径。
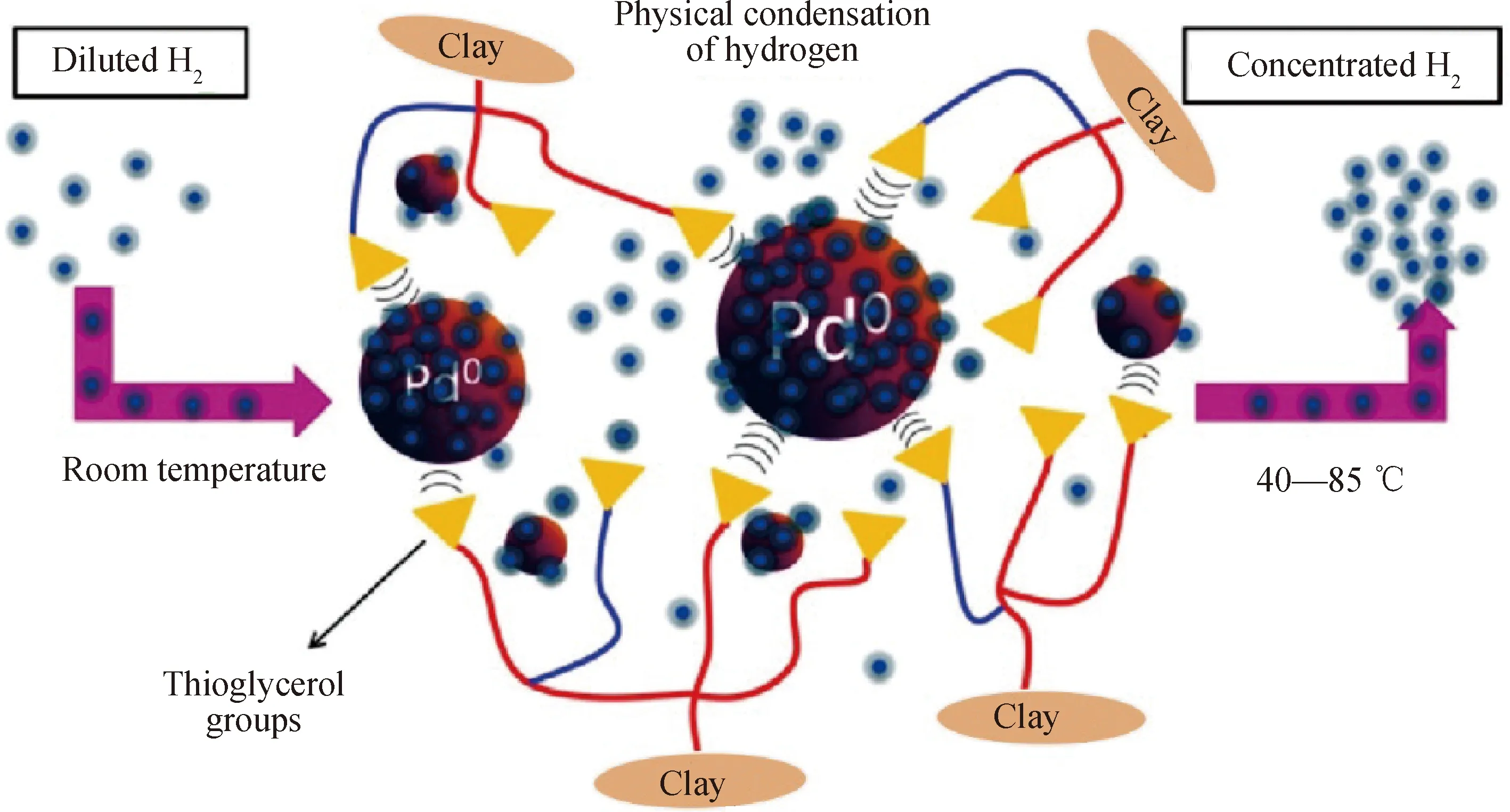
图3 钯负载有机蒙脱石示意图[82]Fig.3 Schematic diagram of palladium-supported organic montmorillonite[82]
2.3 沸石-冰储氢
“沸石-冰”是由水分子通过氢键结合而形成的空洞结构,其结构与沸石的结构类似,因此被叫做“沸石-冰”。Wang等[83]提出用“沸石-冰”储氢,它是由丙烷作为促进剂形成水合物,然后将水合物中的丙烷去除而形成。“沸石-冰”成为储氢材料的具体的制备过程见图4。研究人员在250 ~ 270 K和30~70 MPa条件下进行了一系列模拟,结果表明,压力和温度会影响“沸石-冰”的储氢性能,在270 K时,随着压力的增加,进入水合物相的氢分子数量增加,在250、260 K时,储氢量在质量分数1.0%~1.5%波动。
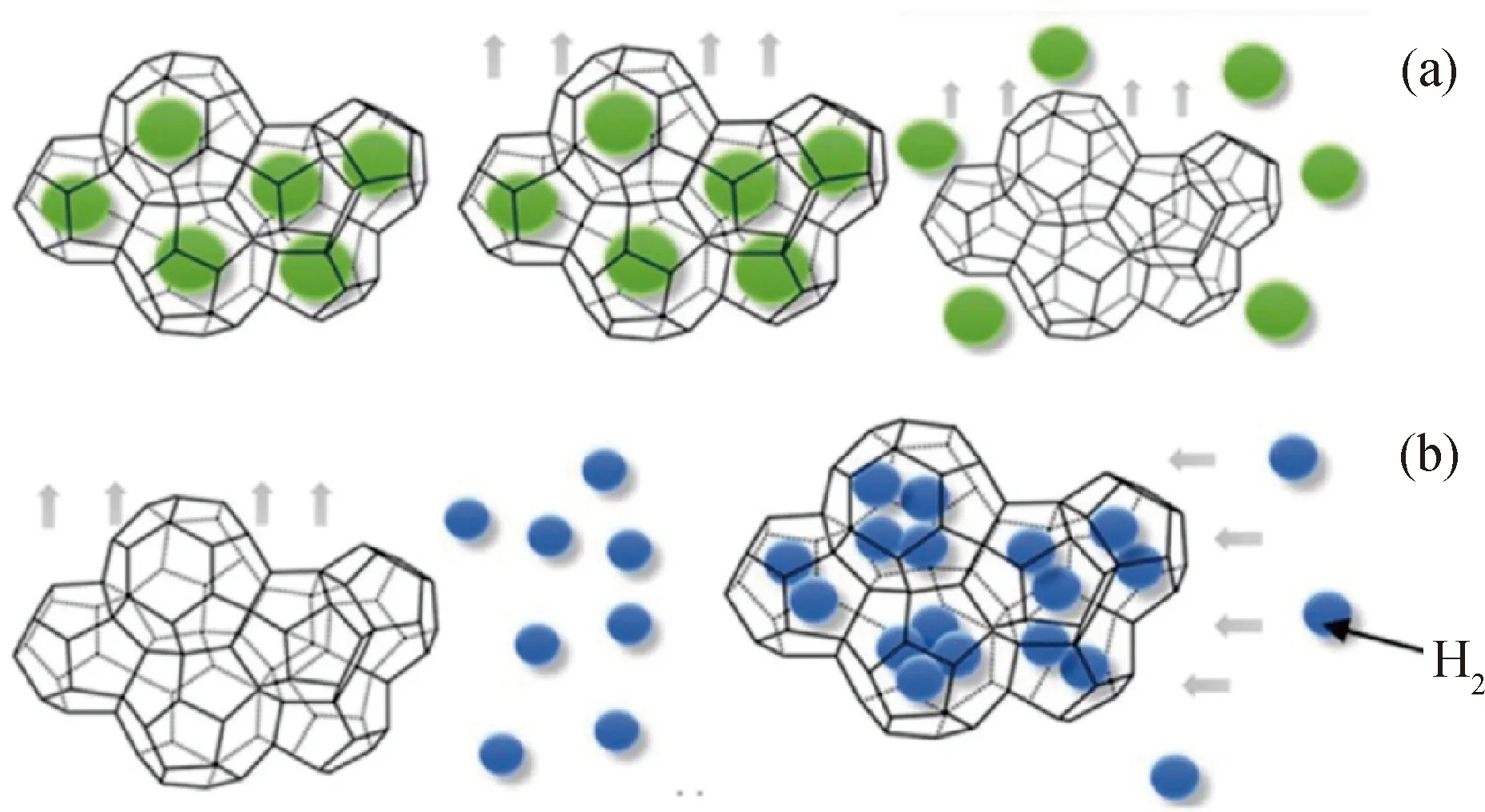
图4 “沸石-冰”的形成及成为储氢材料的过程[94]Fig.4 Process of forming "zeolite-ice" and making it a hydrogen storage material[94](a) Synthesis of propane hydrate and form “zeolite-ice”; (b) Diagram of hydrogen pressurized into “zeolite-ice”
以“沸石-冰”作为储氢材料,具有成本低、安全性好、充放电能耗低、对环境影响小等优点[84],与纯氢水合物相比,该技术解决了纯氢水合物操作压力和温度范围严格(300 MPa,249 K)的缺点。虽然加入促进剂也有助于在较低的压力下形成水合物来储存氢,但它会损害水合物的储氢能力,如四氢呋喃(THF)的加入可以使氢气水合物的生成压力降低到100 MPa[85-86]。甲烷(CH4)和环戊烷(CP)作为有效的促进剂,也可以降低氢气水合物的生成压力[87-92]。目前的研究大多集中在CH4-H2或THF-H2二元水合物的直接生成,但促进剂分子会占据水合物的空腔,从而限制水合物的储氢能力[85-93]。“沸石-冰”储氢与直接用丙烷、氢气的混合气体形成水合物相比,提高了储氢能力且省时、高效[84]。但其缺点是与多孔碳等方法相比,储氢量仍较低,未来仍需探索更合适的促进剂。
3 结语和展望
氢气因为燃烧后的产物为水,并具有较高的热值,被认为是替代化石燃料的环境友好型能源。目前,全球已有包括加拿大、日本、欧盟等20多个国家和地区发布了氢能发展战略,高度重视氢能产业发展。储氢技术作为目前氢能产业中的卡脖子技术,寻求经济高效的储氢材料将在未来较长时间内成为关注与研究的热点。
(1)在多孔碳储氢材料方面可以寻找原材料简单易得、成本低廉的生物质材料。如稻壳、玉米秆等制备多孔碳,其不仅具有高表面积和孔隙体积等优点,而且来源丰富,具有耐热、无毒、良好的化学稳定性和可逆性。同时,从环境友好性和持续可用性的角度来看,以生物质为基础材料是多孔碳更有前途的碳来源。
(2)探索廉价的比表面积高、氢气吸附能力强的天然矿物可有效降低储氢成本,具有很好的发展前景。可以通过对矿物进行改性、负载不同的离子以达到超越原矿物的储氢性能。
(3)利用“沸石-冰”作为储氢材料是一条新颖的储氢途径。研究表明,“沸石-冰”可以提高储氢效率,实现温和高效储氢。但仍需在促进剂的合成及选择方面进行探索,从而提高其储氢量以实现工业化应用。
