基于环介导等温扩增技术的川贝母快速真伪鉴别技术研究*
2023-01-11徐晓可邓华明余至兴黄逸仪徐发莲梁惠倩黄启红
徐晓可,邓华明,余至兴,黄逸仪,徐发莲,梁惠倩,黄启红
(1.广东岭南职业技术学院,广东 广州 510663;2.广东省科学院测试分析研究所,广东 广州 510070)
川贝母是我国传统名贵中药材,具有化痰止咳、抗菌和抗病毒等功效,广泛用于中成药[1-2]。川贝母的正品包括川贝母、甘肃贝母、暗紫贝母、瓦布贝母、梭砂贝母和太白贝母。易与川贝母混淆的有伊贝母、平贝母浙贝母和湖北贝母。由于川贝母的药用价值高,疗效显著,但资源锐减,市场上以浙贝母、伊贝母、平贝母和湖北贝母等伪品混充川贝母的现象十分普遍,影响了药品的安全有效性[3]。药典规定川贝母的鉴别包括了性状鉴别和PCR-RFLP法。传统的性状鉴别方法需要丰富的经验积累,PCR-RFLP鉴别步骤繁杂、耗时长,且需要大型仪器。因此,建立一种快速和特异的方法鉴别川贝母,对中药材市场的监管及中医中药的健康发展至关重要。
环介导等温扩增技术(Loop Mediated Isothermal Amplification ,LAMP)[4]是一种新颖的核酸扩增技术,特点是针对靶基因的6 个区域设计4 条特异引物,利用一种链置换DNA 聚合酶在等温条件(63 ℃ 左右) 反应30~60 min,可通过肉眼直接观察反应结果,具有操作简单、快速、特异性强和灵敏等优点。该技术已广泛应用于临床疾病的诊断、细菌以及病毒等的检测[5-8]。
本文通过比较分析川贝母保守性序列及其常见伪品的序列差异,设计LAMP引物,并筛选LAMP引物,构建LAMP反应体系,建立川贝母LAMP快速、特异和操作简单的鉴别技术,为中药材市场的监管提供技术支撑,促进中医中药的健康发展。
1 材料与方法
1.1 药材
川贝母(批号 121000-201108)、伊贝母(批号 120929- 201005)、平贝母(批号 120924-201410)、浙贝母 (批号 120972-201405)和湖北贝母(批号 120962-201005),均购自中国食品药品检定研究院;太白贝母和暗紫贝母购自药材店,均经过药典方法鉴定。其他市售川贝母样品30 批(编号依次为GZ-1至GZ-30),购自广州市各药材店。
1.2 主要试剂
新型植物基因组DNA 提取试剂盒(DP320),购自北京天根生化科技有限公司;环介导等温扩增法 DNA 扩增试剂盒,购自广州迪奥生物科技有限公司;DNA Marker和GelRed 核酸染料,购自生工生物工程(上海)股份有限公司;PrimeSTAR Max Premix(2×)和SmaI限制性核酸内切酶,购自TaKaRa公司。
1.3 主要仪器
移液枪,德国Eppendorf公司;低温高速离心机(SIGMA 3K30),德国sigma公司;恒温水浴锅(XMTD-8222),上海精宏实验设备有限公司;PCR仪(Mini3220),杭州朗基科学仪器有限公司;电泳仪(DDR-6B),北京六一生物科技有限公司;酶标仪(EPOCH2),美国BioTek公司;凝胶成像系统(Tanon-4600SF),上海天能科技有限公司。
1.4 方法
1.4.1 DNA抽提
1)样品前处理:川贝母、伊贝母、平贝母、浙贝母和湖北贝母粉末直接用于 DNA 提取。其他样品依次用75%乙醇 1 mL、灭菌超纯水 1 mL 清洗,吸干表面水分,置研钵中研磨成极细粉,备用。
2) DNA抽提:按照试剂盒说明书提取基因组DNA。
1.4.2 引物设计
1)LAMP引物设计:比较分析川贝母保守性序列及其常见伪品的序列差异,利用LAMP软件设计LAMP引物(表1),由上海生物工程公司合成。

表1 本研究用引物序列
2)PCR-RFLP引物:参考《中华人民共和国药典》,由上海生物工程公司合成。
1.4.3 LAMP扩增
LAMP反应体系 25 μL,包括 12.5 μL 2×反应液(RM)、 0.5 μL 上游外引物F3(10 μmol/L)、0.5 μL 外引物B3(10 μmol/L)、2 μL 上游内引物FIP(40 μmol/L)、2 μL 下游内引物BIP(40 μmol/L)、1 μL Bst DNA聚合酶(8U)、2 μL DNA模板,加dd H2O至体积 25 μL,加入 1 μL 显色剂在PCR管盖。扩增反应条件:63 ℃ 恒温水浴 1 h,不用开盖,通过颜色直接观察结果。
1.4.4 PCR-RFLP反应
PCR反应体系和酶切反应参考《中华人民共和国药典》[9]。
1.4.5 LAMP引物筛选
以川贝母和伊贝母基因组 DNA为模板,进行LAMP 反应,观察结果,筛选3套候选引物。
1.4.6 LAMP特异性验证
分别以 3种川贝母和7 种常见混淆品基因组DNA为模板,进一步验证筛选引物LAMP的特异性。
1.4.7 LAMP灵敏度评价
DNA抽提试剂盒抽提川贝母DNA,酶标仪测定DNA浓度,梯度稀释DNA,LAMP扩增,评价其灵敏度。
1.4.8 市售川贝母样品的检测
购买广州药店市售川贝母样品30份,提取DNA,分别进行LAMP和PCR-RFLP检测,比较结果。
2 结果与讨论
2.1 LAMP引物筛选
以川贝母和伊贝母基因组DNA为模板,进行LAMP反应(图1)。检测结果显示,Set1和Set2套引物不能区分川贝母和伊贝母,都出现了绿色阳性结果,可能会将川贝母伪品鉴定为正品。Set3套引物可以区分川贝母和伊贝母,其中川贝母显示绿色阳性结果,伊贝母显示橙色阴性结果。因此确定选择引物 Set 3为川贝母LAMP鉴定引物。

1.Set1引物川贝母模板;2.Set1引物伊贝母模板;3.Set2引物川贝母模板;4.Set2引物伊贝母模板;5.Set3引物川贝母模板;6.Set3引物伊贝母模板。图1 LAMP引物筛选
引物设计对LAMP特异性鉴定至关重要。刘香香等[10]基于川贝母保守性序列及其常见伪品的序列差异,通过突变方式设计了 1 对川贝母特异性引物,建立了川贝母 PCR 鉴定技术。错配碱基的引入增加了鉴别的特异性和准确性。本文分别以川贝母JF778850序列和川贝母GQ205120序列设计了两套LAMP引物(Set1和Set2套引物),结果特异性都不理想。然后对比川贝母及其混伪品的ITS序列的差异,本文在Set2套引物的基础上,设计了1条川贝母特异性引物(Set3FIP)。该引物在 3′端引入了1个错配碱基(5-CCGCAAATCGTGCCCGGAGCACTATGCCCGCCCTACC-3’,引入的错配碱基标记下划线)。实验表明,Set3套引物能准确的鉴别川贝母和伊贝母,可以用于下一步的特异性和灵敏度实验。
2.2 LAMP特异性
利用筛选的Set3套引物分别扩增3种川贝母和 7 种常见混淆品基因组DNA,检测结果如图2 所示。其中,3种川贝母均为阳性,显色反应呈现绿色;7 种常见混淆品均为阴性,显色反应呈现橙色。说明该LAMP引物仅针对川贝母产生特异性扩增,对伊贝母、平贝母和浙贝母等的DNA未产生扩增反应,LAMP扩增的特异性良好,可用于川贝母的特异检测。
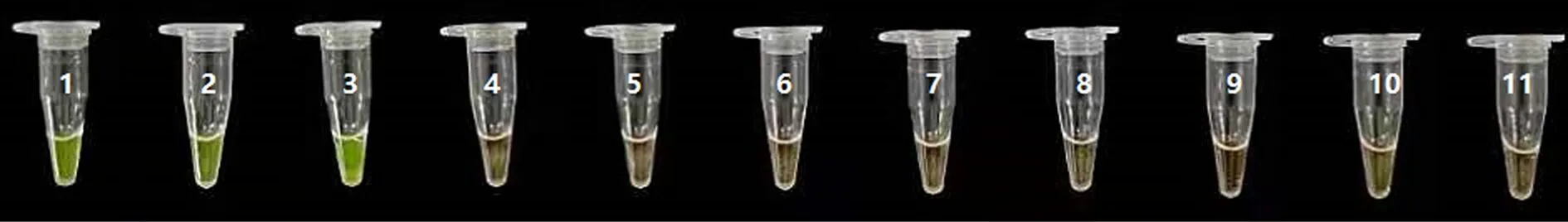
1.川贝母;2.暗紫贝母;3.太白贝母;4.平贝母;5.伊贝母;6.浙贝母;7.湖北贝母;8.土贝母;9.新疆贝母;10.东贝母;11.空白对照。图2 LAMP特异性结果
2.3 LAMP灵敏度
川贝母基因组DNA的质量浓度为 40 mg/L。梯度稀释DNA,LAMP扩增。结果表明,LAMP的灵敏度为 32 μg/L(图3),即该方法的灵敏度可达到 0.1%。

1. 3.2 mg/L;2. 0.32 mg/L;3. 32 μg/L;4. 3.2 μg/L ;5. 0.32 μg/L;6.空白对照。图3 LAMP DNA灵敏度实验结果
2.4 市售川贝母样品的检测
30份市售川贝母样品,LAMP方法检出29份川贝母阳性样品,结果与PCR-RFLP方法一致,但比传统方法的检测时间大大缩短(部分结果见图4和图5)。

1.GZ-1;2.GZ-2;3.GZ-3;4.GZ-4;5.GZ-5;6.GZ-6;7.空白对照;8.阳性对照。图4 市售川贝母样品LAMP检测结果

M.从上往下片段大小依次是:600 bp、500 bp、400 bp、300 bp、200 bp、100 bp;1.阳性对照;2.阳性对照;3.GZ-4;4.GZ-4;5.空白对照。图5 市售川贝母部分样品PCR-RFLP检测结果
3 结论
本研究建立了川贝母的LAMP检测方法。建立的方法具有操作简单、快速和特异性强的优点。灵敏度为 32 μg/L,应用于市售川贝母样品快速筛查检测,结果与《中华人民共和国药典》PCR-RFLP方法一致,简便快捷,具有较好的推广应用前景。
