T790M突变与TKI获得性耐药的晚期肺腺癌患者预后的相关性
2023-01-05李书凡王玉秀姜正华
李书凡,王玉秀,姜正华
(1.扬州洪泉医院,江苏 扬州 225200;2.苏北人民医院 呼吸与危重症医学科,江苏 扬州 225000)
在全球各种癌症类型中,肺癌的发病率和死亡率均居首位[1]。非小细胞肺癌 (NSCLC)占所有肺癌的80%~85%[2]。表皮生长因子受体(EGFR)激活突变,主要包括19外显子(19del)和21外显子(L858R)突变,这2种常见突变已被证实是NSCLC靶向治疗临床结果的主要预测因子[3]。第一代EGFR-TKI的初始反应的平均有效持续时间为3~7个月[4]。大多数患者经过一段治疗时间后会对第一代EGFR-TKI产生获得性耐药[5],在导致对先前的第一代或第二代EGFR-TKI获得性耐药的众多机制中,EGFR第20 外显子Thr790Met(T790M)突变是一个主要的突变,占48%~62%[6]。
奥希替尼(AZD9291)作为不可逆的第三代EGFR-TKI,能够通过在ATP结合位点的半胱氨酸797残基处与EGFR激酶结合来克服获得性T790M介导的耐药性[7]。然而,在第一代EGFR-TKI进展后未获得EGFR T790M突变的患者中,化疗仍然是美国国家综合癌症网络(NCCN)指南推荐的策略。根据IMPRESS研究的结果,不建议继续使用EGFR-TKI联合化疗。一线使用吉非替尼进展后,继续使用吉非替尼,与后线接受化疗的患者相比,并不会延长PFS(5.4个月 vs 5.4个月)[8],甚至与化疗加安慰剂相比对总生存期不利(13.4个月 vs 19.5个月,P=0.016)[9]。
然而,在临床实践中,一些患者在一线EGFR-TKI进展后无法耐受化疗,因此,即使没有检测到EGFR-T790M,也接受了奥希替尼。此外,组织再活检的临床应用通常受到缺乏可用组织、成本、并发症风险和周转时间的限制[10]。血液循环肿瘤 DNA(ctDNA)检测在上述方面优于组织活检,并且被推荐用于检测获得性T790M突变[11]。Cobas测试、液滴数字聚合酶数字链反应(ddPCR)和下一代基因测序(NGS)可用于检测源自ctDNA的肿瘤DNA中的T790M突变,以确定患者是否可以继续接受奥希替尼治疗[12]。在现实世界中,奥希替尼作为第一代EGFR-TKI进展后的后续治疗在复杂情况下(例如贝伐单抗联合或不伴有T790M突变)的疗效仍然值得探索。
我们研究的目的是全面研究不同临床因素在接受奥希替尼治疗的具有获得性T790M突变的真实中国NSCLC队列中的预后价值。
1 资料与方法
1.1病例选择 本前瞻性研究分析选自2009年8月至2020年3月在扬州苏北人民医院经病理学或细胞组织学确诊的Ⅳ期或术后复发转移的肺腺癌患者,经过筛查获得符合入组标准的肺腺癌患者93例,入组标准为:①所有患者病理均通过电子纤维支气管镜、经皮肺穿刺、胸腔积液细胞学或手术诊断为肺腺癌;②所有患者均经NGS测出EGFR敏感突变,且为19外显子19del或21外显子L858R敏感性突变;③所有病例至少有1处可测量病灶以便评估疗效;④所有入组患者在一线治疗时选择的治疗方案为第一代EGFR-TKI单药治疗;⑤所有患者均签署知情同意书。本研究经苏北人民医院伦理委员会批准。
1.2治疗方案 一线用药选择:标准剂量的一代EGFR-TKI治疗(包括吉非替尼250 mg,1次/d;埃克替尼125 mg,3次/d;厄洛替尼150 mg,1次/天);经一代EGFR-TKIs治疗后出现疾病进展,所有患者行二次活检肿瘤组织或血液循环肿瘤细胞或胸水肿瘤细胞的NGS检测,根据检测结果及药物的可及性,部分患者选择第三代EGFR-TKI药物奥希替尼作为二线治疗,部分患者行全身化疗(AC或AP或TP方案)和(或)抗血管生成(贝伐单抗)、局部放疗作为二线治疗。所有患者疾病再次进展后行T790M基因检测并更换治疗方案。奥希替尼的治疗方案为:80 mg每天1次清晨空腹口服,直至疾病进展,未出现不可耐受的不良反应则不调整用药。放化疗方案则根据药物的标准剂量进行。所有患者治疗6~8周后评估首次疗效。治疗期间定期检查患者肝肾功能、血常规、心电图、CT及MRI,观察评价疗效及不良反应。
1.3NGS检测 所有患者均采集9 ml左右的全血送至燃石医学基因检测公司进行基因检测,采用经过国家食品药品监督管理总局认证的Illumina@公司的TrusightOne@的临床外显子组测序板,按照说明,遵循TruSigh-tOne@方案,将扩增样品加载到MIseq仪器上,通过Variantstudio软件@(IIlumina◎)进行数据分析[6]。
1.4评价指标 疗效判定采用实体肿瘤疗效评价标准RECIST(Response Evaluation Criteria in Solid Tumor)1.1标准评价近期疗效,在患者服药6~8周后重复同种影像学检查,比较病灶大小以进行第1次疗效评价,之后每2个月进行1次疗效评价。总体疗效分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。客观缓解率(ORR)=(CR+PR)/总例数×100%,疾病控制率(DCR)=(CR+PR+SD)/总例数×100%。无疾病进展生存期(PFS)被定义为选择该治疗方案的第1天开始直到第1次出现疾病进展、任何原因引起的死亡时间(以月为单位)。按世界卫生组织的毒副反应标准评价药物不良反应。
1.5统计学方法 所有统计分析均使用SPSS 26.0版(IBM Corp.,Armonk,NY,USA)进行。用描述性统计分析患者的临床特征和对治疗的反应。连续和分类数据分别表示为中位数[四分位数1(Q)和四分位数3(Q3)]和数字(百分比)。非正态分布数据比较采用Mann-WhitneyU检验,分类变量采用χ2检验。用Kaplan-Meier 曲线用于比较不同组患者的生存时间。使用Cox比例风险模型计算风险比(HR)和95%CI。P<0.05表示差异有统计学意义。
2 结 果
2.1病例的临床特征 患者年龄46~84岁,中位年龄63岁。其中男性42例(45.16%),女性51例(54.84%)。患者身体状态的ECOG评分为0~1分者61例(65.59%),2~3分者32例(34.41%);不吸烟者68例(73.12%),吸烟者25例(26.88%);所有患者的病理类型均为腺癌。74例(79.57%)患者初治时为Ⅳ期,19例(20.43%)患者为术后复发。在使用第三代EGFR-TKI治疗的肺癌患者中, 42例(45.16%)患者为二线治疗(一线治疗为一代TKI药物吉非替尼、厄洛替尼、埃克替尼),51例(54.84%)患者为三线治疗(一线治疗为一代TKI药物,二线治疗为化疗、抗血管生成药物或放疗)。除第三代EGFR-TKI奥希替尼使用线数与T790M的状态差异有关外,其他人口统计学特征与T790M的状态无关,见表1。
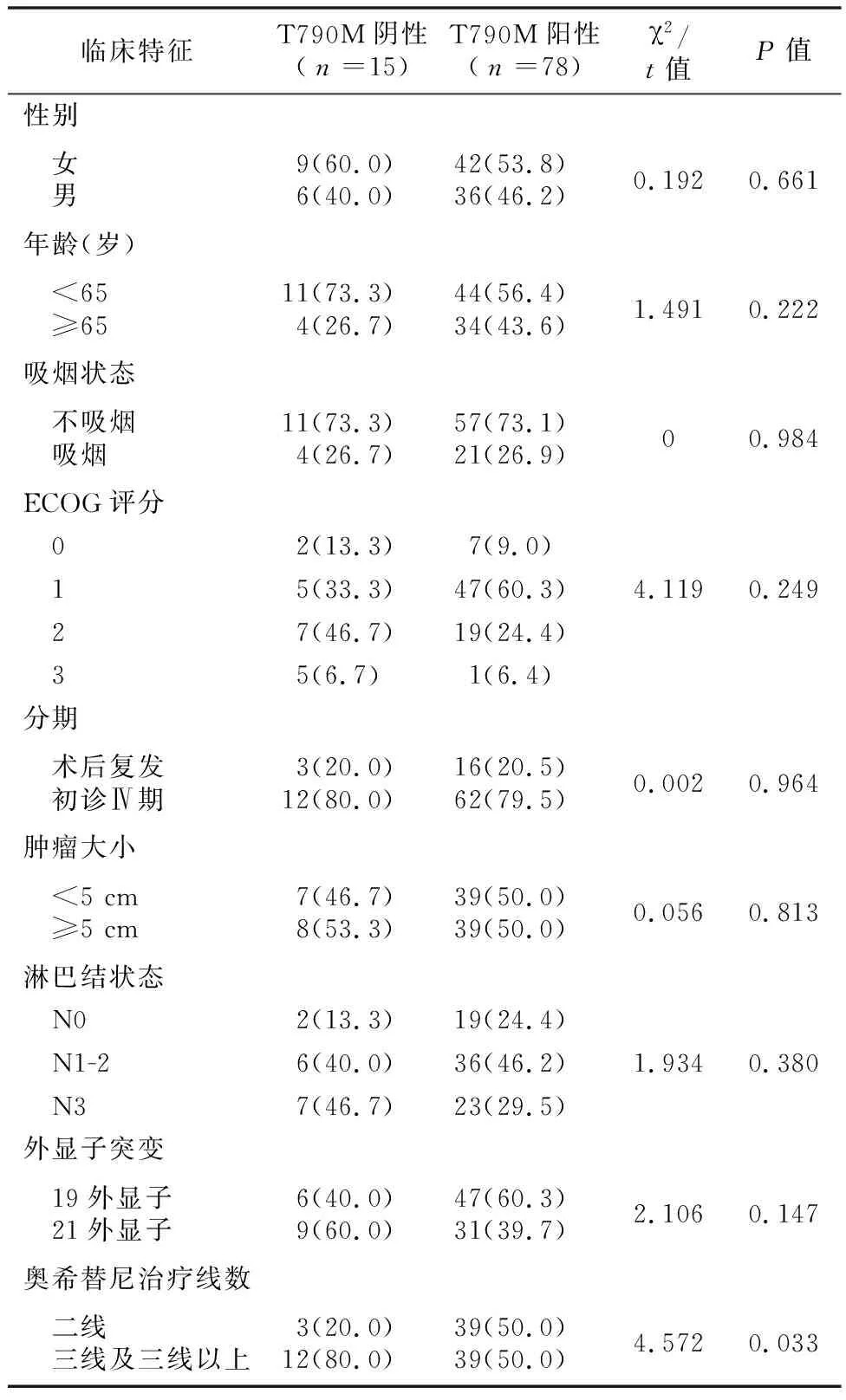
表1 两组临床特征比较
2.2临床治疗疗效与T790M状态的关系 所有入组患者均经病理诊断为复发/转移性非小细胞肺癌,携带敏感的EGFR外显子19缺失或外显子21突变,并在一线EGFR -TKI(埃克替尼、吉非替尼或厄洛替尼)后进展。所有患者在应用奥希替尼治疗前均行T790M检测,其中T790M突变阳性的有78例,T790M突变阴性的15例。因药物的可及性,并非所有T790M阳性的患者都选择奥希替尼作为二线治疗方案。在所有线数治疗的T790M阳性患者中,有PR 48例,PD 2例,SD 28例,CR 0例,ORR为61.54%,DCR为97.44%;在T790M阴性患者中,有PR 2例,PD 4例,SD 9例,CR 0例,ORR为13.33%,DCR为73.33%。T790M阳性组和阴性组的ORR差异无统计学意义(P=0.084),而DCR(P=0.01)差异有统计学意义。二线使用奥希替尼在T790M的两种不同状态下,ORR(P=0.022)和DCR(P=0.016)差异均有统计学意义。三线使用奥希替尼,同样发现ORR(P=0.016)和DCR(P=0.011)差异也具有统计学意义,见表2。

表2 T790M突变与临床治疗疗效[例(%)]
通过Mann-WhitneyU检验提示,T790M的突变与PFS显著相关,其中所有人群中(P<0.01)、二线治疗人群中(P=0.022)和三线治疗人群中(P=0.016),见表3。
2.3KM生存分析与多变量COX回归分析 对所有的患者进行KM生存分析,观测到总体的PFS与T790M的突变状况有关(P<0.01)。T790M阳性的中位PFS为12.50个月(IQR 9.40~17.25)。T790M阴性的中位PFS为6.00个月(IQR 1.50~8.00),见图1。对T790M进行分层分析,可以观测到在T790M阴性组中,患者基因检测中出现EGFR 19外显子和21外显子的PFS差异无统计学意义(P=0.679),见图2。在T790M阳性组中,患者基因检测中出现EGFR 19外显子和21外显子的PFS差异有统计学意义(P=0.05),见图3。在T790M阳性组中,EGFR 19外显子亚组的中位PFS为12.80个月(IQR 9.80~18.00),而在EGFR 21外显子亚组的中位PFS为10.4个月(IQR 8.00~15.50)。同样对T790M的状态及奥希替尼使用线数分层,在T790M阴性组中,二线与三线使用奥希替尼治疗的PFS差异无统计学意义(P=0.923),见图4。在T790M阳性组中,二线与三线使用奥希替尼治疗的PFS差异无统计学意义(P=0.850),见图5。
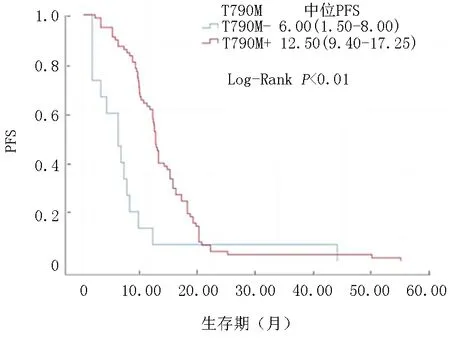
图1 两组总体人群PFS

图2 T790M阴性人群分外显子PFS
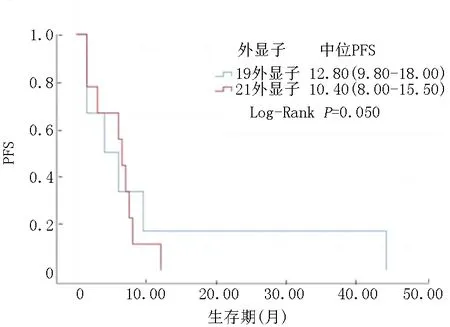
图3 T790M阳性人群分外显子PFS
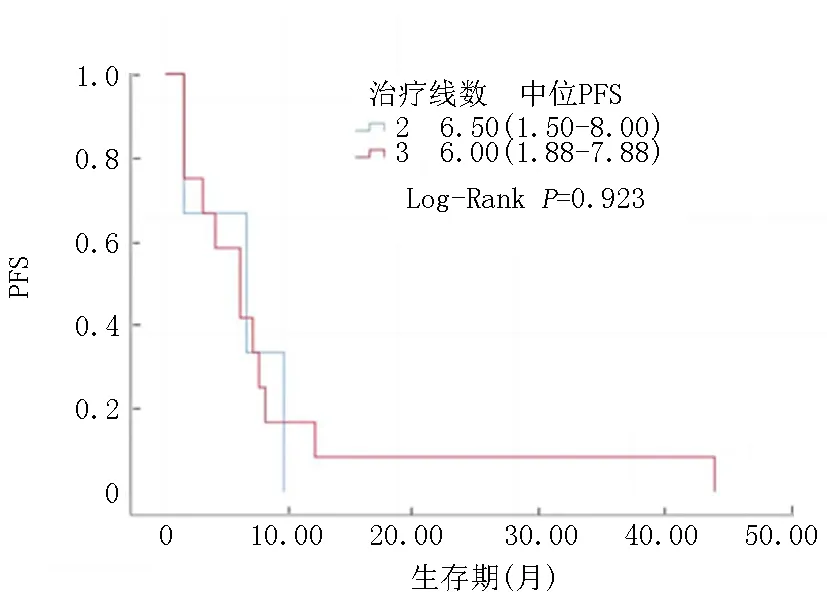
图4 T790M阴性人群分线治疗PFS
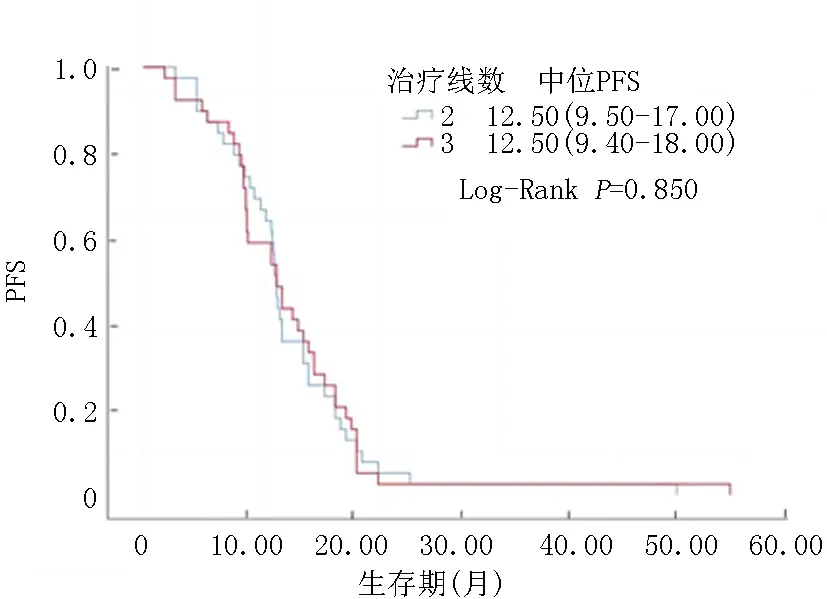
图5 T790M阳性人群分线治疗PFS
使用Cox比例风险回归分析对入组的所有患者进行单因素变量分析,可以发现,肿瘤直径<5 cm患者PFS略优于肿瘤直径≥5 cm患者(P=0.056)。而EGFR外显子的突变情况,EGFR 19外显子突变患者的PFS优于EGFR 21外显子突变患者(P=0.013)。T790M阳性患者的PFS优于T790M阴性患者(P=0.01),见表4。
结合肿瘤直径,EGFR外显子的突变情况,T790M的突变状况进行多因素Cox比例风险回归分析。我们依旧发现EGFR外显子的突变情况,EGFR 19外显子突变患者的PFS优于EGFR 21外显子突变患者(P=0.007)。T790M阳性患者的PFS优于T790M阴性患者(P<0.01)。原本与PFS弱相关的肿瘤直径,在进行多因素COX分析后,我们发现肿瘤直径<5 cm患者优于肿瘤直径≥5 cm患者(P=0.012),见表4。

表4 单因素及多因素Cox比例风险回归分析
2.4不良反应 93例患者中,出现皮疹的16例,为Ⅰ~Ⅱ级,占比17.20%(16/93);出现腹泻20例,为Ⅰ~Ⅱ级,占比21.55%(20/93);出现肝功能损害的6例,为Ⅰ~Ⅱ级,占比6.45%(6/93);心脏损害(QTC间期延长)1例,为I级,占比1.08%(1/93);血液系统损害(血小板降低)10例,为Ⅰ~Ⅱ级,占比10.75%(10/93),总的不良反应发生率56.99%(53/93),未出现3~4级不良反应,患者均无未因不良反应而停药或减量。
3 讨 论
奥希替尼是一种标准治疗方法,用于治疗在具有获得性T790M突变的第一代EGFR -TKI后出现进展的肺腺癌患者,与传统化疗相比,可提高生存率和反应率[13]。 建议使用一线EGFR-TKI后出现进展的患者进行二次活检以检测T790M突变,该突变可以占该亚群的50%左右。对于在一线期间或之后出现进展的患者,NCCN 指南建议没有T790M突变的患者进行全身化疗,但更好的后续方案仍在探索中。在临床实践中,获取肿瘤组织总是困难且昂贵,尤其是在复发或转移性疾病患者中,这使得液体活检成为检测获得性耐药突变的替代方法。但是,仍有一批T790M阴性患者对细胞毒性药物不耐受或不愿接受化疗,因而,第三代EGFR-TKI作为一线EGFR-TKI耐药后或者二线全身化疗失败后的新选择。依旧有一些患者因为种种原因,在做出进一步治疗决定之前甚至不知道他们的基因状态。因此,在如此复杂的情况下,奥希替尼是否可以为EGFR敏感突变的肺腺癌患者,在一线EGFR-TKI治疗进展后可以提供更多的选择和优化策略还是值得探索的。
此前在一项全球真实世界研究中,奥希替尼显示出与临床试验相似的临床疗效,在3 015名T790M阳性NSCLC患者中观察到mPFS为11.1个月(95%CI=11.0~12.0)[14]。在本研究中,93例伴有EGFR敏感性突变的19外显子和21外显子的患者中,分别选择奥希替尼作为他们的二线或三线治疗。
在一项探索奥希替尼作为后续治疗对94名NSCLC患者的疗效的研究中,mPFS 为8.6个月(二线治疗为8.5个月,≥三线治疗为9.1个月)[15]。对于可检测到T790M突变的患者,DCR和中位PFS分别为91.9%和8.6个月(95%CI=7.2~10.0),而没有检测到T790M突变的患者,DCR和中位PFS分别为80.0%和3.2个月(95%CI=0.5~5.9)[15]。在另一项回顾性分析使用奥希替尼治疗携带EGFR敏感性突变的NSCLC患者的疗效中,在携带EGFR 19外显子缺失或21外显子L858R突变的患者中,使用第一代EGFR-TKI后出现进展后,用NGS或ddPCR检测有无T790M突变。所有入组患者的奥希替尼mPFS为17.0个月(HR=1.744, 95%CI=13.534~20.382),与之前的研究相比较长[13],有26.2%的患者在化疗或其他类型的化疗后接受奥希替尼作为三线治疗。在至少有一处可测量病灶的60名患者中,ORR为35.0%,DCR为98.3%。尽管ORR率似乎低于AURA3研究中的(71%)[13],这项研究不仅包括携带T790M突变的患者,还包括那些在现实世界环境中结果为阴性甚至未知状态的患者,以及接受奥希替尼作为三线治疗的患者,这可能会影响反应率。
同样也有其他2项关于奥希替尼的研究,这些研究中都纳入了一部分T790M阴性或者未知的患者。在Jänne等[16]的研究中,对于那些没有检测到的T790M突变的患者,其中位PFS为2.8个月,这表明奥希替尼也可能对此类患者具有中等疗效。 在2期TREM 研究中,无论是否存在T790M突变,至少一种既往EGFR-TKI进展的NSCLC患者接受奥希替尼治疗,T790M阳性患者的ORR为60% (51%~69%),T790M阴性患者的ORR为28%(15%~41%)(P<0.01);T790M阳性和T790M阴性患者的中位PFS分别为10.8个月和5.1个月(HR=0.62,P=0.007);T790M阳性和T790M阴性患者的中位OS分别为22.5个月和13.4个月(HR=0.55,P=0.002)[17]。
在此次研究中,所有入组人群的mPFS为12.0个月(二线治疗为12.3个月,≥三线治疗为9.3个月)。对于T790M阳性突变的患者,ORR为61.54%,DCR为97.44%,中位PFS 12.50个月。而T790M阴性突变的患者,ORR为13.33%,DCR为73.33%,中位PFS 6.00月。另外,在本研究中有1名通过血液检测出T790M阴性的患者,其PFS达到了12个月,这已经很接近T790M阳性患者的中位PFS了,可见通过血液检测T790M状态的检测方法虽说已经精确了不少,但还是未能做到100%的准确。在本次研究中,在没有T790M突变的患者中观察到奥希替尼活性的原因仍不清楚,部分原因可能是由于肿瘤异质性导致的活检假阴性。此外,局部治疗或抗血管生成药物的组合也可能有助于改善 PFS。本研究结果提示,奥希替尼可能代表选定的T790M阴性患者的潜在治疗选择。尽管如此,长期生存仍需要随访。
脑转移瘤 (BMs) 是晚期肺癌患者中最常见的远处转移灶之一并且预后不理想。有人提出,在靶向治疗期间携带EGFR突变的NSCLC患者中,BM 的发生率随着时间的推移而增加。研究表明,早期EGFR -TKI 显示出比化疗更好的中枢神经系统疗效,但颅内进展的高频率仍然是不可抗拒的。与第一代EGFR相比,第三代EGFR - TKI 在中枢神经系统 (CNS) 中的渗透性和疗效更好。在 ASTRIS Korean Subset 的一项真实世界研究中,颅内ORR和颅内DCR分别为62.5%和93.8%,中位颅内PFS为13.0个月(95%CI=7.21~18.8)。
此次研究有几个优势。由于它是在现实世界环境中设计的,因此考虑了复杂的情况,以便研究后续奥希替尼在现实世界中的疗效,并为更大的人群提供更多信息。但是,这项研究仍然存在一些局限性。首先,截至目前,OS数据尚未成熟,需要进一步随访以探索长期生存率。其次,绝大多数T790M阳性的患者使用了奥希替尼,仅有少部分患者因为药物的可及性并未选择奥希替尼。但是,与使用NGS检测相比,使用ddPCR检测T790M可能具有不同的敏感性[12],我们并未对所有患者同时使用NGS和ddPCR两种检测方法来确定T790M的准确性,测定结果的不同,会导致不同比例的患者对奥希替尼的选择性也会不同。其他限制包括未能证明伴随基因的存在是否会影响后续奥希替尼的疗效和接受该方案的患者的生存率。根据先前的研究,基线时伴有除EGFR敏感性突变的NSCLC患者的PFS比不伴有其他基因突变的患者更短(6.20个月 vs 18.77个月)[18],但是,具有EGFR和VEGFR双重通路的突变可能会改善患者的PFS[19]。由于本研究提供的基因组检测信息有限,我们未能确定伴随基因与后续奥希替尼疗效之间的关系,以及贝伐单抗联合用药是否会提高此类患者的生存率。获得更多基因组检测信息并设计进一步的前瞻性研究以进一步阐明遗传替代物与生存的关系仍然至关重要。奥希替尼的耐药机制仍需进一步研究。
