伴或不伴C3 沉积原发性膜性肾病的临床病理特点及预后分析
2022-12-28潘林林包蓓艳
潘林林 包蓓艳
1.宁波大学医学院,浙江宁波 315300;2.宁波市泌尿肾病医院肾内科,浙江宁波 315300
原发性膜性肾病(primary membranous nephropathy,PMN)是成人肾病综合征常见病理类型之一,是由上皮细胞下及基底膜免疫复合物沉积所致的肾小球基底膜增厚。过去10 余年间,M 型磷脂酶A2 受体(m-type phospholipase A2 receptor,PLA2R)[1]、血小板反应蛋白7A 域(thrombospondintype1 domain-containing 7A,THSD7A)[2]及神经表皮生长因子样1 蛋白(neural epidermal growth factor-like 1 protein,
NELL-1)[3]等已被确定为PMN 的靶抗原。靶抗原与其对应的抗体结合形成免疫复合物后启动补体3(complement3,C3)的激活、补体C5 的转化形成,最终导致足细胞损伤、蛋白尿漏出。因此补体系统是PMN 患者组织损伤及蛋白尿漏出的先决条件。本研究回顾性分析2016 年1 月至2021 年12 月在宁波市泌尿肾病医院行肾穿刺确诊的280 例PMN 患者的临床资料,旨在探讨肾小球伴或不伴C3 沉积对PMN患者临床病理特征及预后的影响。
1 对象与方法
1.1 研究对象
选取2016 年1 月至2021 年12 月在宁波市泌尿肾病医院行肾穿刺确诊的PMN 患者280 例,收集其临床及病理资料。纳入标准:①年龄≥18 岁;②随访>6 个月且临床病理资料完整;③肾穿刺活检肾小球≥8 个。排除标准:①通过评估抗核抗体谱、乙肝三系、丙肝抗体等血液指标、肾小球乙肝表面抗原(hepatitis B surface antigen,HBsAg)、乙肝核心抗原(hepatitis B core antigen,HBcAg)沉积等病理特征排除继发性膜性肾病相关疾病者:②自身免疫性疾病,包括系统性红斑狼疮、干燥综合征、原发性小血管炎、过敏性紫癜等;③感染:乙型或丙型病毒感染、感染性心内膜炎、梅毒、艾滋病等。
1.2 资料收集
收集患者的人口学资料,包括性别、年龄;一般临床资料包括收缩压、舒张压、合并高血压、体质量指数(body mass index,BMI)、空腹血糖、24h尿蛋白定量(24h urinary protein quantity,24h UTP)、尿白蛋白肌酐比值(urine albumin creatine ratio,UACR)、尿镜下红细胞、血白蛋白、血肌酐、估算的肾小球滤过率(estimated glomerular filtration rate,eGFR)、血红蛋白、谷丙转氨酶、尿素氮、尿酸、总胆固醇、低密度脂蛋白、免疫球蛋白(immunoglobulin,Ig)G、IgM、IgA、C3、C4、抗PLA2R 抗体、抗核抗体谱、乙肝三系、丙肝抗体及药物使用情况;病理资料包括膜性肾病病理分期、肾小球球性硬化、节段性硬化、新月体及免疫荧光、C1q 和纤维蛋白原沉积。
1.3 分组
根据肾穿刺时肾小球C3 沉积强度对患者进行分组,将(-)定义为不伴C3 沉积,(+)、(++)及(+++)定义为C3 沉积[4]。
1.4 终点事件
①肾脏复合终点:eGFR 下降≥30%或进展至终末期肾病(end-stage renal disease,ESRD),肾脏存活率为未达到肾脏复合终点的人数比例[5];②临床缓解:24hUTP<3.5g 或24h 尿蛋白峰值降低>50%[6]。随访终点为患者达到上述终点事件,未达到终点事件的患者随访截止至2022 年7 月。
1.5 统计学方法
采用SPSS 21.0 统计学软件对数据进行分析和处理,正态分布的计量资料以均数±标准差()表示,采用独立样本t检验,非正态分布的计量资料以中位数(四分位数间距)[M(Q1,Q3)]表示,采用非参数检验。计数资料以例数(百分率)[n(%)]表示,采用Pearsonχ2检验或Fisher 精确检验进行组间比较,两组肾脏存活率和临床缓解率采用Kaplan-Meier 法,分析终点事件的影响因素采用Cox 回归,将单因素分析中P<0.1 的参数纳入多因素分析,P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者的一般资料比较
280 例PMN 患者分为不伴C3 沉积组(n=129)和伴C3 沉积组(n=151)。肾小球不伴C3 沉积组的24h UTP、肾病综合征比例、抗PLA2R 抗体阳性比例低于C3 沉积组,而血白蛋白高于伴C3 沉积组(P<0.05),两组患者的年龄、男性比例、收缩压、舒张压、高血压比例、BMI、空腹血糖、超大量蛋白尿比例、血尿比例、血肌酐、eGFR、血红蛋白、谷丙转氨酶、尿素氮、尿酸、胆固醇、甘油三酯、低密度脂蛋白、血IgG、IgM、IgA、C3、C4 比较,差异无统计学意义(P>0.05),见表1。
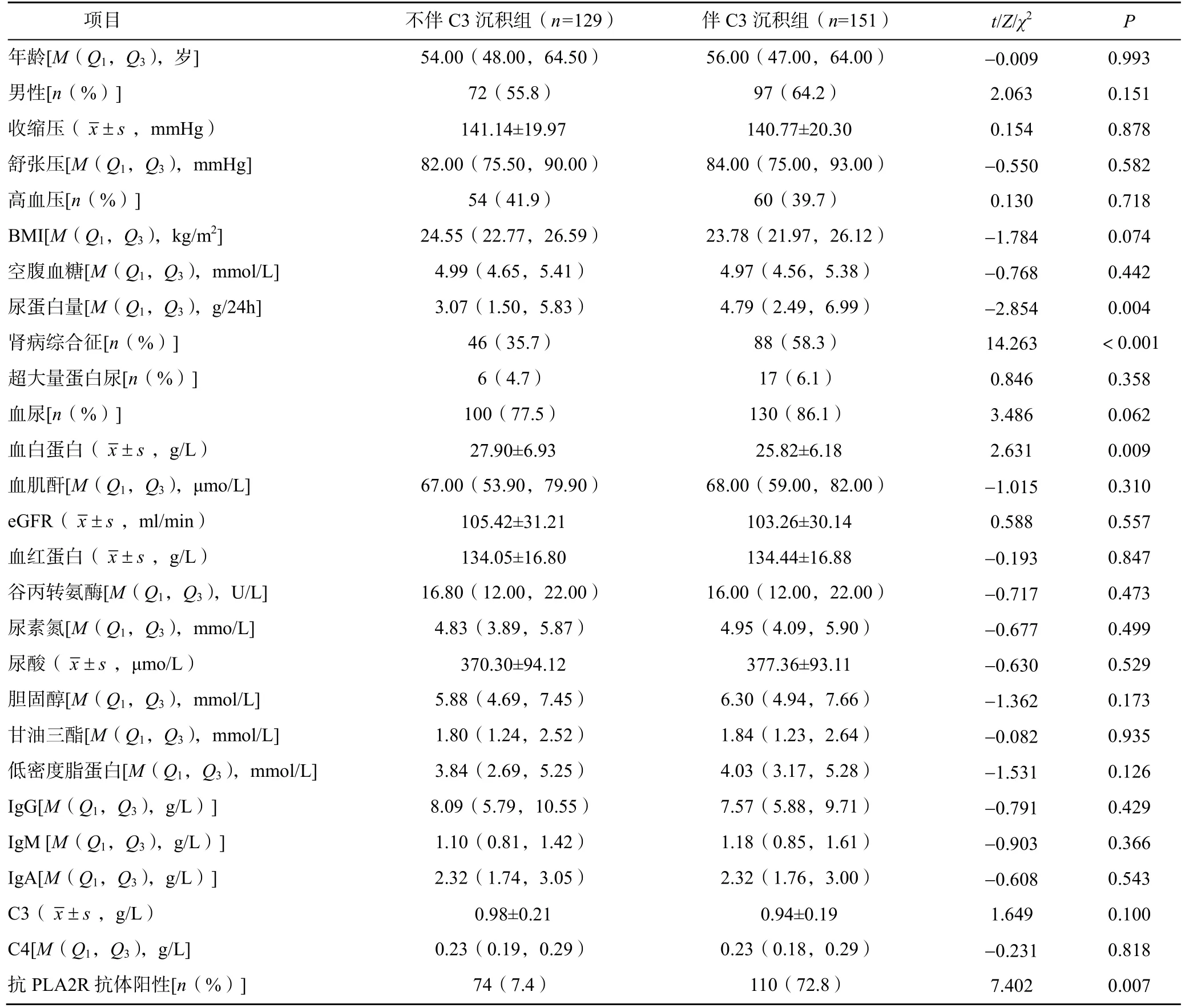
表1 两组患者的一般资料比较
2.2 两组患者的病理资料比较
肾小球不伴C3 沉积组的节段性硬化比例、免疫荧光IgG、IgM、IgA、C1q 及纤维蛋白原沉积比例均低于伴C3 沉积组(P<0.05),两组的PMN 分期、球性硬化比例、新月体比例、C4 沉积比例比较,差异无统计学意义(P>0.05),见表2。

表2 两组患者的病理资料比较[n(%)]
2.3 两组患者的药物使用情况及终点事件比较
不伴C3 沉积组PMN 患者的临床缓解率高于伴C3 沉积组(P<0.05)。两组患者的随访时间、使用激素比例、使用免疫抑制剂比例、发生肾脏复合终点比例比较,差异无统计学意义(P>0.05),见表3。

表3 两组患者的药物使用情况及终点事件比较
2.4 肾脏复合终点
共40 例(14.29%)患者达到肾脏复合终点,中位时间为15.00(6.00,26.25)个月。单因素回归分析结果显示,年龄和男性是肾脏复合终点的影响因素,见表4。将P<0.1 的参数纳入多因素Cox回归分析中,结果显示,年龄和男性仍是肾脏复合终点的影响因素,Kaplan-Meier 法比较两组的累积肾脏存活率,差异无统计学意义(P=0.805)。

表4 PMN 患者达到肾脏复合终点的单因素Cox 回归分析
2.5 预后
单因素回归分析显示,伴C3 沉积、年龄、男性、肾病综合征、抗PLA2R 抗体阳性是PMN 患者临床缓解的影响因素,见表5。将P<0.1 的参数纳入多因素Cox 回归分析中,结果显示,伴C3 沉积、年龄、男性是PMN 患者临床缓解的影响因素。Kaplan-Meier 法比较两组的累积临床缓解率,不伴C3 沉积组的临床缓解率高于伴C3 沉积组,差异有统计学意义(P=0.009)。

表5 PMN 患者达到临床缓解的多因素Cox 回归分析
3 讨论
补体系统在膜性肾病的发生发展中起着重要作用。补体共有三条激活途径,包括经典途径、旁路途径及甘露醇结合凝集素途径,目前研究认为PMN的发病机制早期有经典途径参与,后期由旁路途径和甘露醇结合凝集素途径激活补体,而C3 均参与此三条激活途径[4,5]。海曼肾炎模型是海曼建立的膜性肾病大鼠模型,早期研究表明肾小球C3 和C5b-9 与免疫沉积物共定位[6,7]。在海曼肾炎模型中,尽管存在IgG 的上皮细胞下沉积,但注射眼镜蛇毒消除血清补体C3 可预防蛋白尿[8]。本研究结果显示,肾小球C3 沉积的PMN 患者表现出更严重的蛋白尿[9],表明补体激活与疾病严重程度具有一定的相关性。
在临床特征方面,本研究发现肾小球伴C3 沉积组PMN 患者的血白蛋白低于不伴C3 沉积组,24h UTP、肾病综合征比例、抗PLA2R 抗体阳性比例高于不伴C3 沉积组,与既往研究结果一致[10-12]。膜性肾病病情严重程度与蛋白尿、低白蛋白血症程度及抗PLA2R 抗体滴度相关[13],说明肾小球C3 沉积者临床表现更加严重,肾小球C3 沉积的PLA2R与IgG 结合可能是疾病发生的开始,随后的补体激活能更有效地诱导肾脏病理性损伤,最终导致蛋白尿漏出。
在肾脏病理方面,本研究发现伴C3 沉积组PMN患者的节段性硬化比例高于不伴C3 沉积组,与Chen等[14]的研究结果一致,且伴C3 沉积组患者的免疫荧光IgG、IgM、IgA、C1q 及纤维蛋白原沉积比例均高于不伴C3 沉积组。IgG、IgM、IgA、C3、C1q 及纤维蛋白原均沉积于系膜区和毛细血管壁,被称为“满堂亮现象”,通常见于继发性肾炎,如狼疮性肾炎、过敏性紫癜性肾炎、乙肝病毒相关性肾炎、梅毒相关性肾炎等[15]。本研究中所有患者均经肾穿活检确诊PMN 且排除继发因素,中位随访时间19.00(10.00,34.00)个月,所有患者均未诊断为系统性红斑狼疮、慢性乙型肝炎、肿瘤等疾病。临床中许多抗PLA2R 抗体阳性的PMN 患者肾小球中也有IgM、IgA 和(或)C1q 的沉积[16]。PMN 的主要致病抗体为抗PLA2R 抗体和抗THSD7A 抗体,主要类型为IgG4,而IgG4 具有“半抗体交换”特性,交换重组后的IgG4 的两个Fab 臂结合不同的抗原,即失去结合补体的能力,不能激活补体系统,故不能排除PMN 患者中存在其他抗体激活补体系统。肾小球C1q 沉积表明部分膜性肾病患者存在经典途径的补体激活,C1q 有6 个可与免疫球蛋白结合的位点,只有在2 个以上位点结合时才会被激活。作为五聚体,IgM 比单体的IgG 具有更高的激活C1q的能力,且研究证实IgM 沉积通常伴有C3、C4 和C1q 的沉积[17]。
已有研究表明,C3 沉积在IgA 肾病是不良预后的独立影响因素,与其活动性炎症有关[18,19]。研究发现,膜性肾病患者的肾小球C3 沉积越多,血清C3水平越低,预示患者肾功能不全[10]。但本研究并未发现C3 沉积是肾脏不良预后的影响因素,与Zhang等[11]的研究结果一致,考虑可归因于人种的不同、随访时间及C3 沉积强度的差异。
本研究表明,年龄及男性是影响患者肾脏不良预后的因素,男性、高龄、就诊时eGFR 的降低和持续性严重蛋白尿已被确定为影响预后的危险因素[20-22]。因此,了解影响PMN 患者预后的因素对疾病的恢复至关重要。本研究还发现,C3 沉积、高龄及男性是PMN 临床缓解的影响因素,Kaplan-Meier分析发现伴C3 沉积组达到临床缓解的时间晚于不伴C3 沉积组。
综上所述,伴C3 沉积PMN 患者的临床及病理表现更加严重,不伴C3 沉积PMN 患者的临床缓解率更高,但伴与不伴C3 沉积的PMN 患者的预后无差异。
