木丹颗粒通过miR-146a调控对糖尿病周围神经病变大鼠TLR4通路的影响*
2022-12-27姚伟洁赵香妍
姚伟洁,赵香妍
1首都医科大学附属北京妇产医院北京妇幼保健院,北京 100006;2北京市和平里医院
糖尿病周围神经病变(diabetic peripheral neuropathy,DPN)作为糖尿病的常见并发症之一,在病程后期易导致患者肢端溃烂甚至造成截肢,严重影响患者的生活质量[1]。DPN的发病机制复杂,至今尚未完全阐明,有研究发现,炎症反应参与了DPN的发生发展[2]。木丹颗粒作为临床治疗DPN的常用中药,治疗效果显著[3-4]。前期研究发现,木丹颗粒治疗DPN的机制与抑制Toll样受体4(toll-like receptor 4,TLR4)相关通路,从而抑制炎症反应有关,然而木丹颗粒是通过何种途径调控TLR4通路的至今尚未有深入研究。
相关研究发现miR-146a参与了DPN的发生,并与炎症反应密切相关[5]。但是木丹颗粒能否通过影响miR-146a的表达,调控TLR4通路改善DPN,至今尚未有研究。本实验以木丹颗粒为治疗药物,以链脲佐菌素(streptozotocin,STZ)诱导的DPN大鼠和高糖环境下培养的雪旺细胞(schwann cells,SCs)为研究对象,将miR-146a作为切入点,探讨木丹颗粒调控TLR4通路的机制。
1 材料与方法
1.1 实验动物40只SD雄性大鼠,SPF级,周龄6~8周,体质量(200±20)g,购于北京维通利华实验动物技术有限公司,实验动物许可证编号:SCXK(京)2016-0006。饲养条件:动物饲养于SPF级饲养室,12 h/12 h昼夜交替、温度(23±2)℃、湿度(55±10)%,自由进食饮水。
1.2 实验细胞雪旺细胞选择大鼠RSC96细胞株(American type culture collection),选用dmem(dulbecco's modified eagle medium)完全培养基(培养基中含有4 mM谷氨酰胺,25 mM葡萄糖,1 mM丙酮酸钠,1500 mg/L碳酸氢钠,10% FBS及1%青链霉素混合液)培养细胞,培养环境为37℃和5%CO2的培养箱中。
1.3 药品及试剂链脲佐菌素(streptozotocin,STZ)(Sigma-Aldrich,批号:S0130);α-硫辛酸(Puritan's Pride,批号:6007);木丹颗粒(辽宁奥达制药有限公司,国药准字Z20080033,规格:7 g/袋);D-葡萄糖(Sigma,批号:D7021);澳洲胎牛血清(Gibco,批号:10099-141);Trizol试剂(Invitrogen,批号:15596-025);TransStart Tip Green qPCR SuperMix,TransScript First-Strand cDNA Synthesis SuperMix(全式金,批号:AQ141-02、AT301-03);小鼠单克隆β-actin抗体,兔单克隆TRAF6抗体,兔多克隆IRAK1抗体(Abcam,批号:ab8226、ab33915、ab238)
1.4 实验仪器CareSens血糖仪(i-SENS);3K15型低温离心机(Sigma);全波长酶标仪(Molecular Devices,SpectraMax Plus 384);CFX96TM型实时荧光定量PCR仪(Bio-Rid);PowerPac™型基础电泳仪电源(Bio-Rid);Mini-PROTEAN® Tetra电泳槽(Bio-Rid);小型Trans-Blot®转印槽(Bio-Rid);371型二氧化碳培养箱(Thermo);MLS-3020型高压灭菌器(SANYO)。
1.5 动物实验
1.5.1 造模与分组将SD大鼠40只适应性饲养1周后,随机分为2组,设10只为空白对照组,其余30只大鼠腹腔注射60 mg/kg的STZ溶液诱导糖尿病模型,稳定1周后空腹血糖(fasting blood glucose,FBG)≥16.7 mmol/L的大鼠表明糖尿病模型建立成功。将模型大鼠随机分为模型组、α-硫辛酸组和木丹颗粒组,每组10只。
1.5.2 给药方法α-硫辛酸组给予20 mg/(kg·d)的α-硫辛酸溶液,木丹颗粒组给予2.3 g/(kg·d)的木丹颗粒溶液,空白对照组和模型组给予10 mL/(kg·d)剂量的饮用水,连续给药12周。末次给药1 h后处死大鼠,收集坐骨神经。
1.6 细胞实验
1.6.1 含药血清制备另选SD大鼠30只适应性饲养1周后,随机分为3组,空白血清组15只,α-硫辛酸含药血清组5只,木丹颗粒含药血清组10只。连续干预7天,末次干预1 h后腹主动脉取血,离心半径13.5 cm,3000 r/min离心10 min,4℃分离血清,60℃水浴灭活后除菌(0.22 μm微孔滤膜过滤除菌),分装后用于后续实验。
1.6.2 细胞处理RSC96细胞以4×105细胞/孔的数量接种于6孔板中,将细胞于培养箱中放置过夜,待细胞贴壁后,分别使用空白组大鼠血清、150 mM葡萄糖(Sigma)+空白组大鼠血清、150 mM葡萄糖+10% α-硫辛酸(ALA)含药血清和150 mM葡萄糖+不同浓度(10%、1%和0.1%)木丹颗粒含药血清孵育细胞48 h。
1.7 观察指标
1.7.1 RT-PCR法测定基因表达使用Trizol法分别提取大鼠坐骨神经和RSC96细胞中的总RNA,参照反转录试剂盒说明书,将RNA反转录为cDNA,继续使用SYBR预混系统和特异性引物将cDNA进行RT-PCR扩增,确定每个基因的mRNA表达水平。每个样本设置3个平行复孔,以β-actin作为内参,对各样本miR146、TRAF6和IRAK1进行相对表达量分析,计算2-△△Ct目的基因相对表达量,结果以倍数形式表示。引物序列见表1。

表1 基因引物序列
1.7.2 Western blot法测定蛋白表达使用RIPA裂解液分别提取坐骨神经和RSC96细胞中总蛋白,并使用BCA蛋白定量试剂盒测定蛋白质浓度。在SDS-PAGE凝胶中使用电泳分离蛋白质,并通过湿式转移系统(Bio-Rad,USA)将蛋白转运至0.45 μm PVDF膜上。使用脱脂奶粉室温封闭蛋白2 h后,加入相应一抗4℃孵育过夜。然后加入相应二抗,室温孵育1 h后,加入电化学发光(ECL)试剂并在凝胶成像系统(Bio-Rid)中形成图像。使用Image J软件计算样品灰度值,计算蛋白表达,将β-actin作为内标蛋白,结果以倍数的形式表示。使用了以下一抗:兔单克隆TRAF6抗体,兔多克隆IRAK1抗体,小鼠单克隆β-actin抗体。
1.8 统计学方法使用SPSS 17.0软件进行数据分析。计量资料采用±s表示,多组独立样本比较使用One-Way ANOVA,非正态分布数据使用非参数检验方法,P<0.05表示差异有统计学意义。
2 结果
2.1 大鼠坐骨神经miR-146a、IRAK1、TRAF6mRNA及蛋白表达与空白对照组比较,模型组miR-146a表达显著降低(P<0.01),IRAK1、TRAF6蛋白和mRNA表达均显著升高(P<0.01);与模型组比较,木丹颗粒组miR-146a表达显著升高(P<0.01),IRAK1、TRAF6蛋白和mRNA表达均显著降低(P<0.01)。见图1、表2。
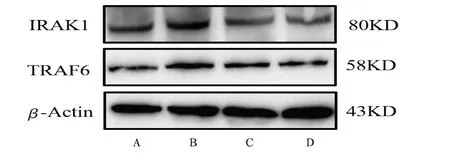
图1 各组大鼠坐骨神经IRAK1和TRAF6蛋白表达电泳图
表2 各组大鼠坐骨神经miR-146a,IRAK1、TRAF6蛋白及mRNA表达比较(±s)
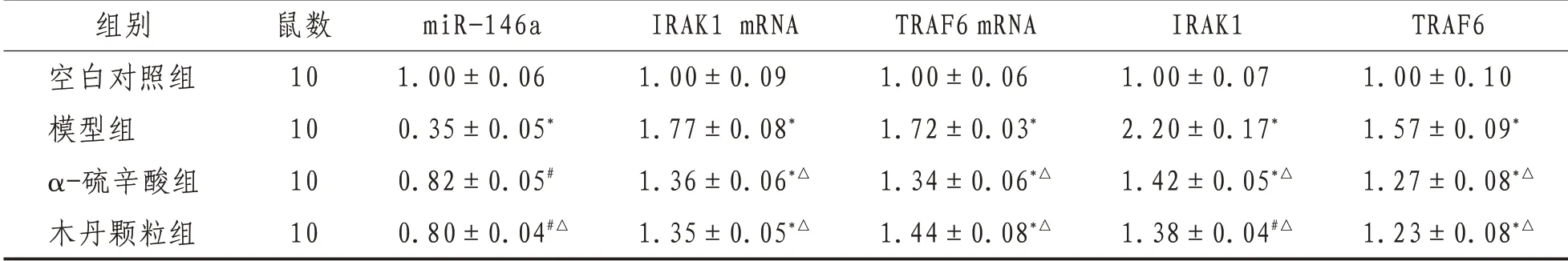
表2 各组大鼠坐骨神经miR-146a,IRAK1、TRAF6蛋白及mRNA表达比较(±s)
注:与空白对照组比较,*表示P<0.01,#表示P<0.05;与模型组比较,△表示P<0.01
组别空白对照组模型组α-硫辛酸组木丹颗粒组鼠数10 10 10 10 miR-146a 1.00±0.06 0.35±0.05*0.82±0.05#0.80±0.04#△IRAK1 mRNA 1.00±0.09 1.77±0.08*1.36±0.06*△1.35±0.05*△TRAF6 mRNA 1.00±0.06 1.72±0.03*1.34±0.06*△1.44±0.08*△IRAK1 1.00±0.07 2.20±0.17*1.42±0.05*△1.38±0.04#△TRAF6 1.00±0.10 1.57±0.09*1.27±0.08*△1.23±0.08*△
2.2 高糖环境下雪旺细胞miR-146a、IRAK1、TRAF6蛋白及mRNA表达与25 mM组比较,150 mM组miR-146a表达显著降低(P<0.01),IRAK1、TRAF6 mRNA及蛋白表达均显著升高(P<0.01);与150 mM组比较,木丹颗粒含药血清组miR-146a表达显著升高(P<0.01),10%和1%木丹颗粒含药血清组IRAK1和TRAF6mRNA及蛋白表达均显著降低(P<0.05),0.1%木丹颗粒含药血清组IRAK1 mRNA表达显著降低(P<0.05)。见图2、表3。
表3 各组含药血清对高糖环境下雪旺细胞miR-146a、TRAF6、IRAK1蛋白及mRNA表达比较(±s)
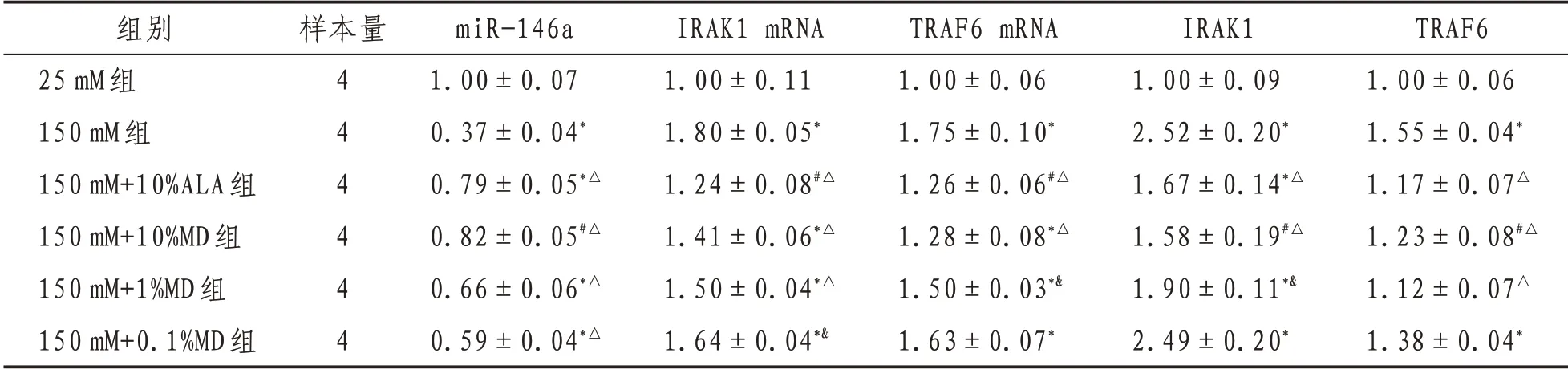
表3 各组含药血清对高糖环境下雪旺细胞miR-146a、TRAF6、IRAK1蛋白及mRNA表达比较(±s)
注:与25 mM组相比,*表示P<0.01,#表示P<0.05;与150 mM组相比,△表示P<0.01,&表示P<0.05
组别25 mM组150 mM组150 mM+10%ALA组150 mM+10%MD组150 mM+1%MD组150 mM+0.1%MD组样本量4 4 4 4 4 4 miR-146a 1.00±0.07 0.37±0.04*0.79±0.05*△0.82±0.05#△0.66±0.06*△0.59±0.04*△IRAK1 mRNA 1.00±0.11 1.80±0.05*1.24±0.08#△1.41±0.06*△1.50±0.04*△1.64±0.04*&TRAF6 mRNA 1.00±0.06 1.75±0.10*1.26±0.06#△1.28±0.08*△1.50±0.03*&1.63±0.07*IRAK1 1.00±0.09 2.52±0.20*1.67±0.14*△1.58±0.19#△1.90±0.11*&2.49±0.20*TRAF6 1.00±0.06 1.55±0.04*1.17±0.07△1.23±0.08#△1.12±0.07△1.38±0.04*
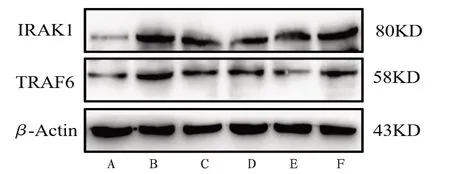
图2 各组含药血清高糖环境下雪旺细胞IRAK1和TRAF6蛋白表达电泳图
3 讨论
SCs是周围神经的髓鞘形成细胞[6],其代谢紊乱易导致神经纤维出现髓鞘脱失,是DPN的主要病理特征[7]。研究发现,SCs容易受高血糖的影响,高糖环境下SCs的损伤和线粒体的功能障碍会导致轴突萎缩,髓鞘脱失等病理改变[8],因此,可将高糖环境下培养的SCs作为DPN研究的体外模型。含药血清是由姜廷良教授引入中国的药理学实验技术,能够真实地反映药物的药效及其作用环境,在体外实验中可信度优于中药粗制剂[9]。因此本实验的体外实验采用高糖环境培养的SCs为研究对象,使用木丹颗粒含药血清为治疗药物干预SCs,结合体内实验,共同探讨木丹颗粒对TLR4通路的调控机制。
DPN的中医病机以气滞血瘀为主[10],木丹颗粒在临床治疗DPN疗效显著[3-4]。方中黄芪为君药,可使气旺血行;三七、延胡索为臣药,功效为活血止痛;佐以赤芍、丹参、川芎、红花、苏木和鸡血藤,共同达到活血化瘀,通络止痛的作用[11]。我们在前期实验中对木丹颗粒治疗DPN的机制进行了研究,实验结果显示,木丹颗粒能够抑制DPN大鼠TLR4/MyD88/NF-κB通路和TLR4/p38 MAPK通路,进而抑制炎症反应,改善周围神经结构和功能的损伤。
微RNA(MicroRNA,miRNA)是高度保守的内源性非编码单链小分子RNA,长度20~25 nt,能够通过靶向信使RNA(messenger RNA,mRNA)的3’UTR区域碱基互补配对,从而抑制或降解靶标mRNA的翻译和表达[12]。miRNA在病理过程中发挥了重要的作用,能够作为疾病预警和早期诊断的生物标志物[13]。miR-146a参与急性和慢性炎症反应的调节已被广泛证明,有研究发现在miR-146a缺陷型小鼠中观察到炎症反应标志物的高表达[14-15]。此外,研究发现miR-146a参与了DPN的发生,并与炎症反应密切相关[5]。
IRAKl和TRAF6是miR-146a调控的两个主要靶基因,能够对炎症进行负反馈调控[16]。IRAK1和TRAF6是TLR下游通路中的两个重要分子[17],TLR4/MyD88/NF-κB通路的激活能够诱发炎症反应[18],其 中MyD88能 够 与IRAKl和TRAF6形 成MyD88-IRAKs-TRAF6复合体进行信号转导,IRAK1和TRAF6的活化会引发NF-κB的核移位,从而促进炎症反应发生[19-20]。体内实验和体外实验均证明,木丹颗粒能够促进miR-146a的表达,并抑制IRAK1和TRAF6的蛋白和基因表达。
综上所述,木丹颗粒能够通过促进miR-146a的表达,进而抑制IRAK1和TRAF6的表达,从而调控TLR4/MyD88/NF-κB通路,抑制炎症反应,防治DPN。
