基于网络药理学探讨当归治疗阿尔茨海默病的机制
2022-12-16叶长青罗洪斌
叶长青,罗洪斌,2*,詹 杰,杨 娇,周 戈
1.湖北民族大学医学部(湖北 恩施 445000)2.湖北民族大学神经精神共患病研究所(湖北 恩施 445000)
阿尔茨海默病(Alzheimer’s disease,AD)是一种慢性中枢神经认知障碍性疾病,其最主要的病理改变是β淀粉样蛋白沉积导致的老年斑(Senile Plaques,SP)及tau蛋白过度磷酸化导致的神经原纤维缠结(Neurofibrillary tangles,NFTs)[1]。神经原纤维缠结由过度磷酸化的tau蛋白形成的成对的螺旋型结构构成[2],老年斑由折叠结构的淀粉样多肽聚集形成[3],周围围绕着损伤的神经突触[1],临床主要表现为记忆力逐渐减退、多领域认知功能障碍、行为异常和社交障碍[4]。目前,AD的临床诊断需要询问病史、神经心理学评估、各种放射学检查等[5]。
AD作为老年人最常见的精神障碍性疾病,随着人口老龄化,中国的痴呆发生率也将呈增长趋势。由于患者常伴有不同程度的记忆缺失和认知功能障碍,导致其生活不能自理,不但对患者本人的生活质量产生影响,还会给照护者、家人和社会带来巨大的负担[6],如何应对人口老龄化和相伴随的AD对社会经济发展带来的挑战是全球面临的共同课题[7]。
目前西医治疗AD的药物主要包括乙酰胆碱酯酶抑制剂、免疫治疗药物及NMDA受体拮抗剂等药物,可在一定程度上缓解患者的症状,但无法阻止AD的进程[8],并可引起恶心、呕吐、头晕等诸多不良反应[9]。因此寻找疗效更确切,而副作用更小的药物成为AD治疗的热点之一。AD属中医学“呆病”“健忘”“郁证”等范畴,为本虚标实之证,以肾精亏虚、脑髓失养为本,痰瘀闭阻脑络、神机失用为标。近年研究认为,中药含有多种有效成分,可以发挥多种作用靶点的药理特点,符合AD多因素、多种病理机制的发病特点[10],且不良反应少,易被患者接受,在AD的防治中得到广泛应用。
当归(Angelicasinensis)是伞科植物当归的根,入肝、脾、心经,性温、甘、辛,具有补血活血、调经止痛、润肠通便等功效,研究表明当归有效成分具有保护损伤后脑细胞、抗炎作用、抗衰老及氧化作用、延缓记忆减退、降低血小板聚集和抗血栓形成、抗氧化清除自由基作用[11]。目前关于当归治疗AD作用机制方面的报道较少。
网络药理学是基于医学生物学、信息学、计算机科学等多学科理论和研究手段,构建“药物-靶点-疾病”网络,分析药物对机体的可能作用机制,为研究中药与疾病的关系提供有效手段,为传统中医药防病治病的现代医学研究提供新的途径[12]。本研究拟运用网络药理学方法对当归防治AD的作用靶点、信号通路进行预测,采用分子对接进行验证,为深入研究当归防治AD提供理论依据、为实验研究提供指导。
1 材料与方法
1.1当归化学成分筛选及靶点预测通过中药系统药理数据库(TCMSP,http://ibts.hkbu.edu.hk/LSP/tcmsp.php,v2.3)检索当归的活性成分,按照生物利用度(OB)≥20%,类似度(DL)≥0.1,进行活性成分的筛选,把TCMSP数据库中的当归活性成分CAS号在Pub Chem数据库进行检索,获得每个成分的Canonical SMILES,再将SMILES的结构式依次导入Swiss Target Predition数据库中,选择物种为智人,对筛选的当归活性成分进行靶点预测。
1.2AD相关靶点筛选在Genecards数据库(https://www.genecards.org),以“Alzheimer’s disease”作为关键词对AD进行检索,根据Relevance Score≥10进行筛选,对检索出的AD靶点进行汇总,将筛选结果导入Excel文件备用。
1.3当归成分-AD靶点PPI网络构建将筛选的当归有效成分靶点与AD靶点进行比较匹配处理,二者靶点取交集,保留其交集靶点,删除其它靶点,将交集靶点导入Cytoscape 3.7.2,对当归-AD靶点PPI网络构建。
1.4当归-AD靶点功能与通路的富集分析将当归作用于AD的潜在靶点导入Metascape平台,进行GO与KEGG的分析,保存分析数据,并对结果进行可视化处理。
1.5当归成分-AD靶点-通路网络图的构建将当归活性成分、疾病靶点、信号通路导入Cytoscape 3.7.2构建当归活性成分-AD靶点-信号通路网络,根据网络图分析当归活性成分、疾病靶点及信号通路之间的相互作用关系。
1.6分子对接验证在TCMSP数据库根据药物成分名称下载化学成分结构,转换成mol2格式。从PDB网站获得的AD相关靶点蛋白三维结构导入Autodock,对蛋白结构进行去水分子、去配体,加氢原子、添加电荷,并保存PDBQT格式。选取对接能量最低且有结合位点的构象靶点蛋白与药物成分用于分子对接,并以pdbqt的格式保存。利用PyMol对对接结果进行可视化。
2 结果
2.1当归活性成分及活性成分靶点的筛选根据TCMSP数据库初步提取出当归有效成分125种,经筛选后得到活性成分10种,分别以DG1-DG10表示(见表1),通过PubChem和Swiss Target Prediction数据库查找当归相关结构和靶点,去除重复值得到活性成分作用靶点206个。

表1 当归主要成分
2.2AD相关靶点的获取利用Genecards数据库对AD进行检索,获得AD相关靶点10 707个,通过Genecards数据库所得到的AD靶点相关性值最高为158.4,最小0.10,设定相关值≥10的靶点为AD潜在靶点,最终得到AD靶点1 445个。
2.3当归成分-AD靶点PPI网络的构建当归成分-AD靶点交集75个,绘制韦恩图(见图1)。将公共靶点蛋白导入STRING 11.5数据库,物种设置为Homo sapiens进行构建,可信度设置为Medium confidence,进行蛋白相互作用分析,构建当归-AD蛋白相互作用关系网络图(见图2)。图中涉及75个节点,而且这些节点相互联系,通过多途径、多靶点协同作用,其中丝裂原活化蛋白激酶14(MAPK14)、丝氨酸/苏氨酸激酶 1(AKT1)、前列腺内过氧化物合成酶2(PTGS2)是Degree值较大的3个节点,表明这些蛋白可能是当归治疗AD的关键靶点。

图1 当归成分-AD靶点韦恩图
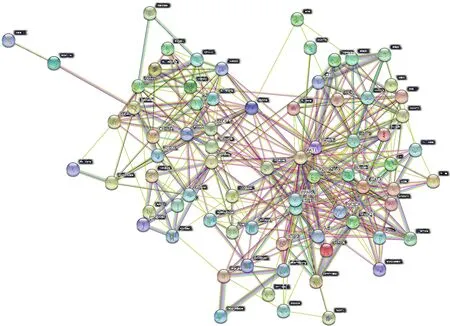
图2 当归-AD靶点PPI网络图
2.4GO功能富集和KEGG通路分析应用Metascape数据平台对当归治疗AD的相关靶点进行信号通路分析,靶点通路富集结果见表2,由结果可见当归多个靶点与AD关系密切。

表2 当归治疗AD靶点通路富集结果
KEGG通路分析提示,当归治疗AD的机制可能与神经活性配体-受体相互作用(Neuroactive ligand-receptor interaction)、多巴胺能突触(Dopaminergic synapse)、阿尔茨海默病(Alzheimer disease)、5-羟色胺能突触(Serotonergic synapse)、神经退行性变的途径-多种疾病(Pathways of neurodegeneration-multiple diseases)、CGMP-PKG信号通路(CGMP-PKG signaling pathway)、NF-kB信号通路(NF-kappa B signaling pathway)、突触小泡循环(Synaptic vesicle cycle)等有关,见图3A。
生物过程分析显示,这些靶点主要涉及无机物的反应、离子传输的调节、对激素的反应、有机羟基化合物代谢过程、激酶活性正向调节等,见图3B。
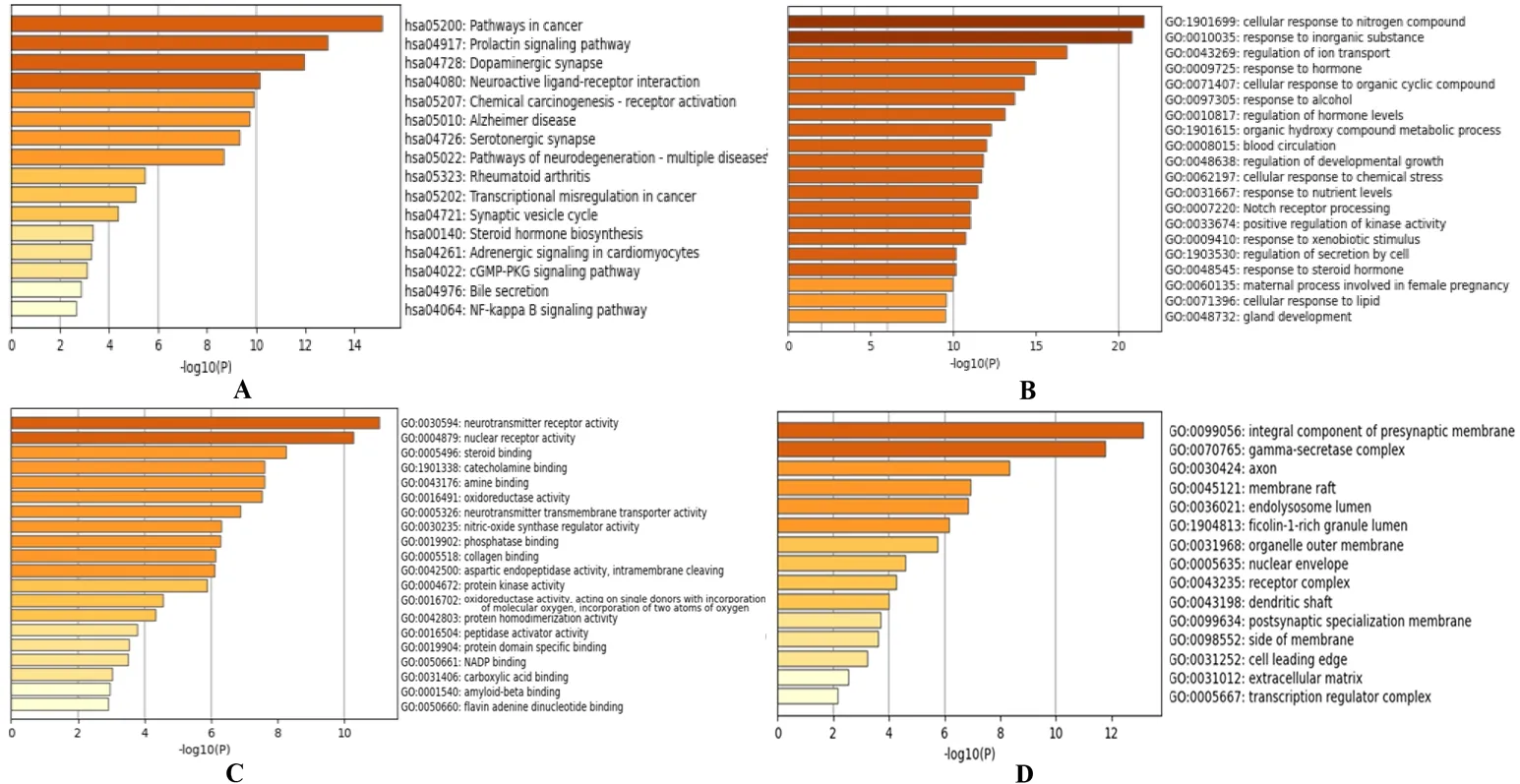
注:A:KEGG;B:GO-BP分析;C:GO-MF分析;D:GO-CC分析。
分子功能分析显示,其靶点主要涉及神经递质跨膜转运蛋白活性、神经递质受体活性、磷酸酶结合、蛋白激酶活性、肽酶活化剂活性、β淀粉样蛋白结合等,见图3C。
细胞组分分析表明,这些靶点主要涉及突触前膜的有机组成部分、轴突、膜筏、突触后膜、核被膜等,见图3D。
2.5当归成分-AD靶点-通路网络图的构建将当归活性成分、靶点信息及信号通路导入CytoScape 3.7.2,构建当归-当归活性成分-AD-通路网络,见图4。
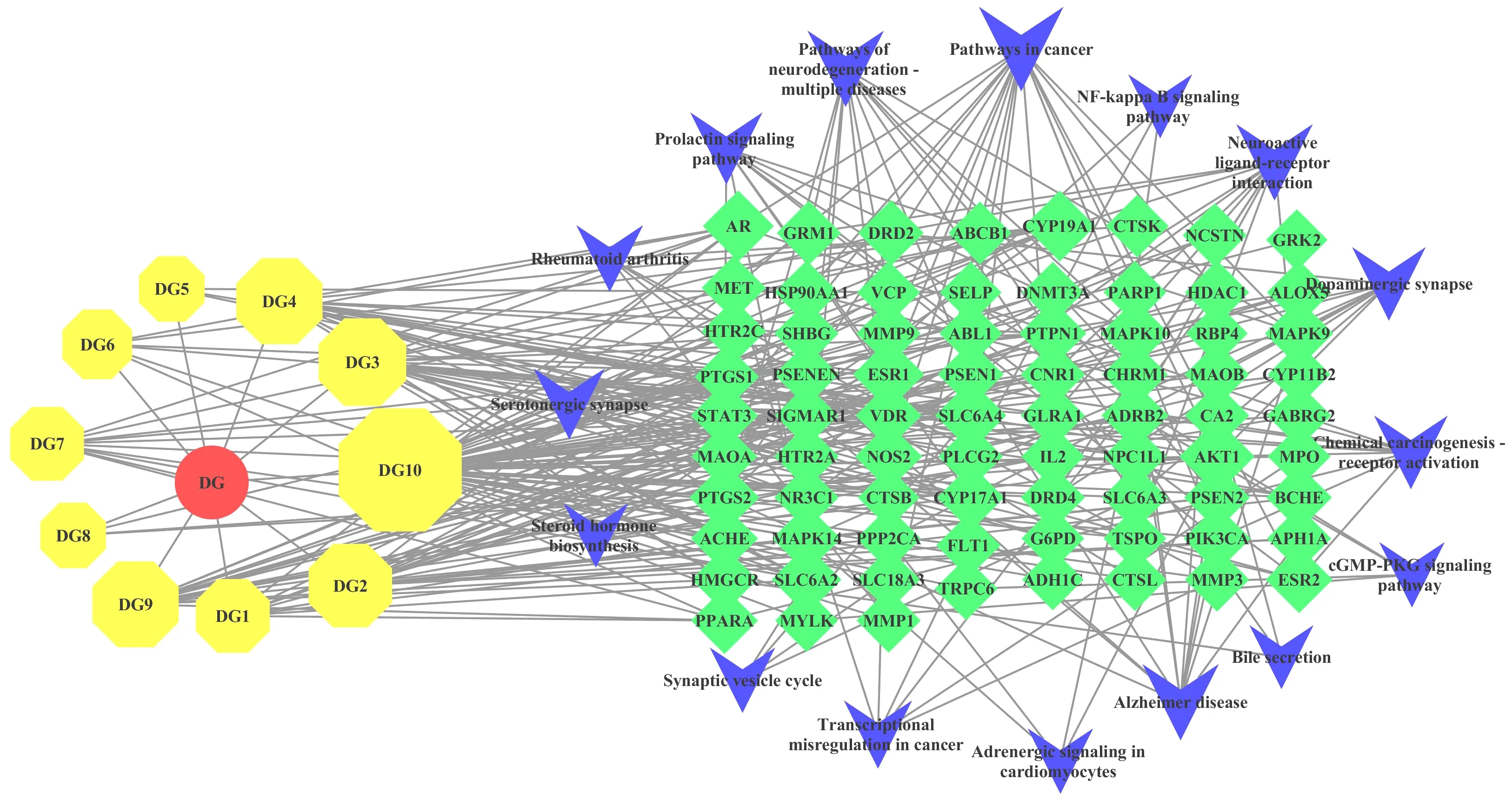
图4 当归-当归活性成分-AD靶点-通路网络图
2.6分子对接将筛选的关键靶点AKT1、PTGS2、MAPK14与当归的主要活性成分豆甾醇(stigmasterol)、西托糖苷(sitogluside)、β-谷甾醇(beta-sitosterol)进行分子对接,结果表明,AKT1与stigmasterol对接能量值为-16.99 kJ/mol,AKT1与sitogluside对接能量值为-10.67 kJ/mol,AKT1与beta-sitosterol对接能量值为-19.41 kJ/mol,PTGS2与stigmasterol对接能量值为-17.15 kJ/mol,PTGS2与sitogluside对接能量值为-8.62 kJ/mol,PTGS2与beta-sitosterol对接能量值为-18.83 kJ/mol,MAPK14与stigmasterol对接能量值为-11.21 kJ/mol,MAPK14与sitogluside对接能量值为-8.58 kJ/mol,MAPK14与beta-sitosterol对接能量值为-11.63 kJ/mol。利用PyMol软件对对接结果进行可视化,见图5。

注:A:AKT1_stigmasterol;B:AKT1_sitogluside;C:AKT1_beta-sitosterol;D:PTGS2_stigmasterol;E:PTGS2_sitogluside F:PTGS2_beta-sitosterol;G:MAPK14_stigmasterol;H:MAPK14_sitogluside I:MAPK14_beta-sitosterol.
3 讨论
AD病因复杂,目前尚未完全明确,主要以各种假说为主,比较公认的如胆碱能假说、tau蛋白假说、β-淀粉样蛋白假说等[13],临床上用于治疗AD的药物效果不显著,因此,寻找能够更有效缓解AD进展的药物具有重要意义。而网络药理学为治疗AD药物的研究提供了新的思路。通过“当归活性成分-作用靶点”网络分析,豆甾醇、β-谷甾醇、西托糖苷可能是当归的主要活性成分。豆甾醇具有抗氧化活性、抗炎、抗肿瘤、保护精神状态等药理作用[14],对神经炎症引起的神经退行性疾病具有治疗作用,还可激活雌激素受体以增强胆碱能神经传递系统,从而改善AD患者认知功能、发挥抗AD的作用[15]。β-谷甾醇能影响炎症、氧化应激、凋亡等多种信号通路,在抗AD方面体现出很好的生物活性[16]。西托糖苷属于甾体活性成分,在其四环核周围的基团作用下,生物活性非常广泛[17]。有报道[18]指出西托糖苷的苷元的同分异构体—β-谷甾醇通过增加中枢神经系统中的血清素和去甲肾上腺素水平而具有抗抑郁活性。
通过构建PPI网络分析得出PTGS2、AKT1、MAPK14可能是当归治疗AD的核心靶点。PTGS2在炎症过程中释放,PTGS2的过表达会危及大脑神经元的存活,PTGS2可激活NF-kB信号通路,与AD的发生密切相关[19],研究发现[20]多种神经退行性疾病中观察到NF-kB通路被激活。大鼠脑皮质注射Aβ1-42,部分反应性星形胶质细胞中检测到NF-kB活化,同时PTGS2和IL-1β也活化[21]。AKT1是一种丝氨酸/苏氨酸蛋白激酶,主要参与细胞增殖和生长的调控,磷脂酰肌醇-3-激酶(PI3K)信号通路是调节细胞生长、迁移功能的主要下游信号分子[22],当其被激活时,能够磷酸化下游蛋白,发挥抗凋亡的作用[23]。MAPK可将细胞膜受体信号传到细胞核,参与调节神经元增殖、凋亡等,其与学习记忆等能力关系密切,可参与调控神经毒性、神经炎症和突触功能障碍等与AD密切相关的病理机制[24]。丝裂原活化蛋白激酶14(MAPK14/p38α)是MAPK的亚型,是一种对炎症和氧化刺激敏感的激酶,激活后能有效调高tau蛋白的磷酸化[35]。研究表明,APP-PS1转基因AD小鼠脑内MAPK14/p38α蛋白表达上调,并进一步证明MAPK14基因缺失在APP-PS1小鼠中刺激自噬中的巨自噬,然后通过增加BACE1的自噬-溶酶体降解导致淀粉样蛋白病理减少,表明抑制MAPK14酶活性有可能作为一种治疗方法来缓解AD[26]。
通过KEGG通路分析当归活性成分治疗AD的信号通路,cGMP-PKG信号通路、NF-kB信号通路、神经配体-受体相互作用信号通路等是当归治疗AD的关键信号通路。
cGMP是细胞转录中的第二信使,促进细胞分化,cGMP-PKG信号通路在细胞内Ca2+释放和细胞外Ca2+内流中起着重要作用[27],AD患者的淀粉样斑块和神经原纤维缠结与细胞内Ca2+浓度动态平衡紊乱有关[28]。cGMP和下游靶蛋白PKG介导抗凋亡作用,可溶性鸟苷酸环化酶的抑制和基础cGMP水平的降低会导致无应激神经细胞发生凋亡。cGMP/PKG通路可能在阻止促凋亡通路激活方面发挥重要作用,从而促进神经细胞存活[29]。
NF-kB是一种转录因子,由P50、P52、REL、REL-A和REL-B组成,这些蛋白质二聚体化后可形成有功能的NF-kB[30],其在炎症应激反应、细胞免疫应答、细胞分裂、生长和凋亡等多种细胞通路中发挥重要作用,其信号通路被激活,会导致AD患者的神经元变性[31]。
神经活性配体-受体相互作用信号通路与AD密切相关,该通路主要利用 5-HT、谷氨酸、ACh、多巴胺、γ-氨基丁酸等神经递质作为前体物质,从而影响后续的信号转导[32]。
分子对接结果表明,当归主要活性成分谷甾醇、托糖苷、β谷甾醇与核心靶点PTGS2、AKT1、MAPK14的结合活性强,表明当归可能是通过谷甾醇、托糖苷、β谷甾醇等发挥抗AD的作用。
综上所述,当归10个主要活性成分可能作用于MAPK14、PTGS2、AKT1等靶点,通过cGMP-PKG信号通路、NF-kB信号通路、神经活性配体-受体相互作用等信号通路减缓神经元损伤,从而达到延缓AD的作用,但所预测的当归治疗AD的重要靶点及信号通路还需在实验中进行验证。
