促性腺激素释放激素拮抗剂灵活方案中促黄体生成素一过性早升对新鲜周期IVF/ICSI-ET 患者妊娠结局的影响
2022-12-15颜晓红李友筑
高 红, 林 莉, 颜晓红, 陶 萍, 李友筑
(厦门大学附属第一医院生殖医学科, 福建 厦门 361003)
控制性促排卵 (controlled ovarian hyperstimulation, COH)方案主要关键点在于控制内源性促黄体生成激素(luteinizing hormone, LH)峰, 防止卵泡早排或者黄素化, 在此基础上促进多个卵泡发育和诱导卵子成熟, 从而获得相对较多的成熟卵子。目前常用的两类COH 方案有长方案和拮抗剂方案。长方案中促性腺激素释放激素激动剂(gonadotropin releasing hormone agonist, GnRH-a)通过垂体“降调节”发挥作用, 使LH 长时间处于较低水平, 内源性LH 峰出现概率极低;拮抗剂方案中促性腺激素释放激素拮抗剂(gonadotropin releasing hormone antagonist, GnRH-A) 可与垂体促性腺激素释放激素(gonadotropin releasing hormone, GnRH)受体特异性结合, 迅速抑制LH峰。拮抗剂方案以其无需降调、周期短、 用药少和使用方便等特点受到医生的青睐, 成为更经济安全的卵巢刺激方案。但是拮抗剂方案中内源性早发LH 峰出现概率较高, 在高反应患者中内源性LH峰出现概率为8%~38%[1-2]。绝大部分患者在使用拮抗剂后, 内源性早发LH 峰得到有效控制。但是这种一过性的内源性早发LH 峰对妊娠结局的影响尚存在争议。已有文献报道内源性早发LH 峰可降低患者种植率、临床妊娠率、活产率[1]和继续妊娠率[3], 而近期的专家共识[4]提出控制良好的早发LH 峰对临床结局无明显影响。本文作者比较拮抗剂灵活方案中LH 一过性早期升高(早升)与未出现LH 早升患者新鲜周期体外受精/卵胞浆内单精 子 注 射- 胚 胎 移 植 (in vitrofertilization/intracytoplasmic sperm injection-embryo transfer, IVF/ ICSI-ET)妊娠结局的区别, 探讨一过性LH早升是否对妊娠结局有不良影响。
1 资料与方法
1.1 研究对象收集2017 年1 月—2021 年12 月于本科行IVF/ICSI-ET 且采用拮抗剂灵活方案助孕治疗患者的临床资料。根据患者是否出现LH 早升分为无LH 早升组(n=105)和LH 早升组(n=40)。纳入标准:①采用拮抗剂灵活方案;②添加拮抗剂日和日均HCG<1.5 μg·L-1;③夫妻双方染色体正常;④移植日子宫内膜厚度≥8 mm。排除标准:复发性流产;子宫畸形;宫腔粘连。所有夫妇均知情同意并签署PPOS 治疗知情同意书。本研究经本院伦理委员会批准[科研伦审字2022(039)号]。
1.2 COH 方案拮抗剂灵活方案:于月经周期第2~3 天起启动促性腺激素(gonadotrophin, Gn), 皮 下 注 射 重 组 卵 泡 刺 激 素 (follicle stimulating hormone, FSH)(商品名普丽康, 300 IU/支, 荷兰欧加农制药公司) 或丽申宝(75 IU/支, 珠海丽珠制药公司)100~300 IU·d-1, 同时可添加人绝经期促性腺激素75 IU(75 IU/支, 珠海丽珠制药公司), 根据患者年龄、抗苗勒管激素(anti-Mullerian hormone, AMH)、基础-窦卵泡(antral follicles, AFC) 数 和 体 质 量 指 数(body mass index, BMI)等调整用药剂量, 4 d 后复查阴道B 超 和血LH、雌二醇(estradiol, E2) 和孕 酮(progesterone, P) 水平, 后每隔1~3 d 回诊, 当最大卵泡直径为12~14 mm, 或者E2≥0.3 pg·L-1开始每日皮下注射0.25 mg GnRH-A(药品名醋酸西曲瑞克, 商品名思则凯, 德国默克雪兰诺制药公司), 直至扳机当日。若出现LH 早升, 当日立即予以皮下注射0.25~0.50 mg GnRH-A, 后每隔1~2 d 监测LH、E2和P 水平, 并且每日皮下注射0.25 mgGnRH-A 直 至 扳 机 当 日。 当1 个 卵 泡直径≥18 mm 或3 个以上卵泡直径≥17 mm 时, 给予GnRH-a(药品名醋酸曲普瑞林, 商品名达必佳, 德国辉凌制药公司)0.1 mg 皮下注射加联合人 绒 毛 膜 促 性 腺 激 素 (human chorionic gonadotropin, hCG, 1 000 IU/支, 珠海丽珠制药公司)2 000 IU 肌肉注射扳机, 根据男方精液情况行体外受精(in vitrofertilization, IVF)或卵胞浆内单精子注射(intracytoplasmic sperm injection, ICSI)受精, 常规胚胎培养, 取卵后开始给予地屈孕酮(10 mg/片, 每次10 mg, 每日2 次, 荷兰雅培制药公司)和黄体酮阴道缓释凝胶(商品名雪诺酮, 每次90 mg, 每日1 次, 德国默克雪兰诺制药公司) 进行黄体支持, 至孕10~12 周。胚胎移植(embryo transfer, ET) 后12~14 d 检测血β-人绒毛膜促性腺激素(β-human chorionic gonadotropin, β-HCG)水平确定生化妊娠, 移植后28 d 阴道B 超可见妊娠囊定义为临床妊娠。超过孕12 周后的临床妊娠定义为继续妊娠。
1.3 体外受精-胚胎培养取卵前要求男方禁欲3~7 d, 取卵当日采用手淫法留取精液或者附睾/睾丸穿刺获得精子, 根据当日取精方法和结果采用密度梯度离心或者上游法处理精液。取卵日行超声引导下经阴道卵泡穿刺术, 在体视显微镜下分拣出卵丘复合物, 于GIVF 培养液(瑞典Vitrolife 公司)中培养4 h 后行短时受精, 若发现卵母细胞均未受精或受精率较低时, 行补救ICSI 处理。次日观察原核情况, 以两原核(2PN)为正常受精, 洗涤后换 用G1 培养液(瑞典Vitrolife 公司)。第3 天(D3)观察胚胎, 计数D3 可用胚胎数和D3 优质胚胎数并进行常规评分。
1.4 卵裂期胚胎(D3 胚胎)中优质胚胎和可用胚胎的判定标准根据胚胎卵裂球大小、形态和碎片百分率将胚胎分为4 级:Ⅰ级, 胚胎卵裂球大小均匀, 形态规则且胞质清晰, 无碎片或碎片百分率≤10%;Ⅱ级, 胚胎卵裂球大小基本均匀, 形态欠规则, 10%<碎片百分率≤25%;Ⅲ级, 胚胎卵裂球大小不均等, 25%<碎片百分率≤50%;Ⅳ级, 胚胎卵裂球大小严重不均匀, 碎片百分率>50%。本研究优质胚胎定义为Ⅰ级或Ⅱ级胚胎。评级为Ⅲ级以上胚胎为可移植胚胎[5]。
1.5 LH 早升的判定标准LH 早升定义为在超过同一月经周期的基础LH 水平的3 倍[6]或LH 绝对值>10 IU·L-1[7]。
1.6 观察指标主要观察指标为继续妊娠率(继续妊娠率=大于孕12 周的妊娠周期数/移植周期数×100%);次要观察指标包括添加拮抗剂日的Gn 天数、添加拮抗剂日E2水平、添加拮抗剂日最大卵泡直径、获卵数、成熟卵(metaphase Ⅱ, MⅡ)数、成熟卵率(成熟卵率=MII 卵数/获卵数×100%)、正常受精率(正常受精率=2PN 受精卵数/MII 卵总数×100%)、D3 可用胚胎率(D3 可用胚胎率=D3Ⅲ级及以上胚胎数/2PN 卵裂胚胎总数×100%)、D3 优质胚胎率(D3 优质胚胎率=D3 Ⅰ级和Ⅱ级胚胎数/2PN 卵裂胚胎总数×100%)、种植率(种植率=孕囊数/移植的胚胎数×100%)和临床妊娠率(临床妊娠率=妊娠周期数/移植周期数×100%)。
1.7 统计学分析采用SPSS 25.0 统计软件进行统计学分析。患者平均年龄、BMI、基础FSH 水平、基础LH 水平、基础E2水平、添加拮抗剂日的Gn 天数、拮抗剂使用天数、拮抗剂日LH 水平、添加拮抗剂日E2水平、添加拮抗剂日卵泡直径、Gn使用天数、Gn 总量、扳机日E2水平、P 水平、扳机日内膜厚度、获卵数、成熟卵数、正常受精数、D3 可用胚胎数和D3 优质胚胎数以±s表示, 组间样本均数比较采用两独样本t检验;患者不孕年限、AMH、基础AFC 数和平均移植胚胎数以M(P25, P75) 表示, 组间比较采用Mann-WhitneyU检验;卵巢低储备患者百分率、多囊卵巢综合征(polycystic ovarian syndrome, PCOS) 患 者 百 分率、成熟卵率、正常受精率、D3 可用胚胎率、D3优质胚胎率、移植囊胚比例、胚胎种植率、临床妊娠率和继续妊娠率以百分率表示, 组间比较采用χ2检验。将是否发生LH 早升作为因变量, 建立多因素二元Logistic 回归模型, 采用向前逐步回归分析法以Logistic 回归模型的比值比(odds ratio, OR)及其95%置信区间(confidence interval, CI)评估各指标与LH 早升的关联。以P<0.05 为差异有统计学意义。
2 结 果
2.1 2 组患者基本特征本研究共纳入患者145 例, 其 中 无LH 早 升 组105 例, LH 早升组40 例。2 组患者平均年龄、不孕年限、BMI、基础FSH 水平、基础LH 水平、基础E2水平、AMH 水平、基础AFC、卵巢低储备患者百分率和PCOS患者百分率比较差异均无统计学意义(P>0.05)。见表1。
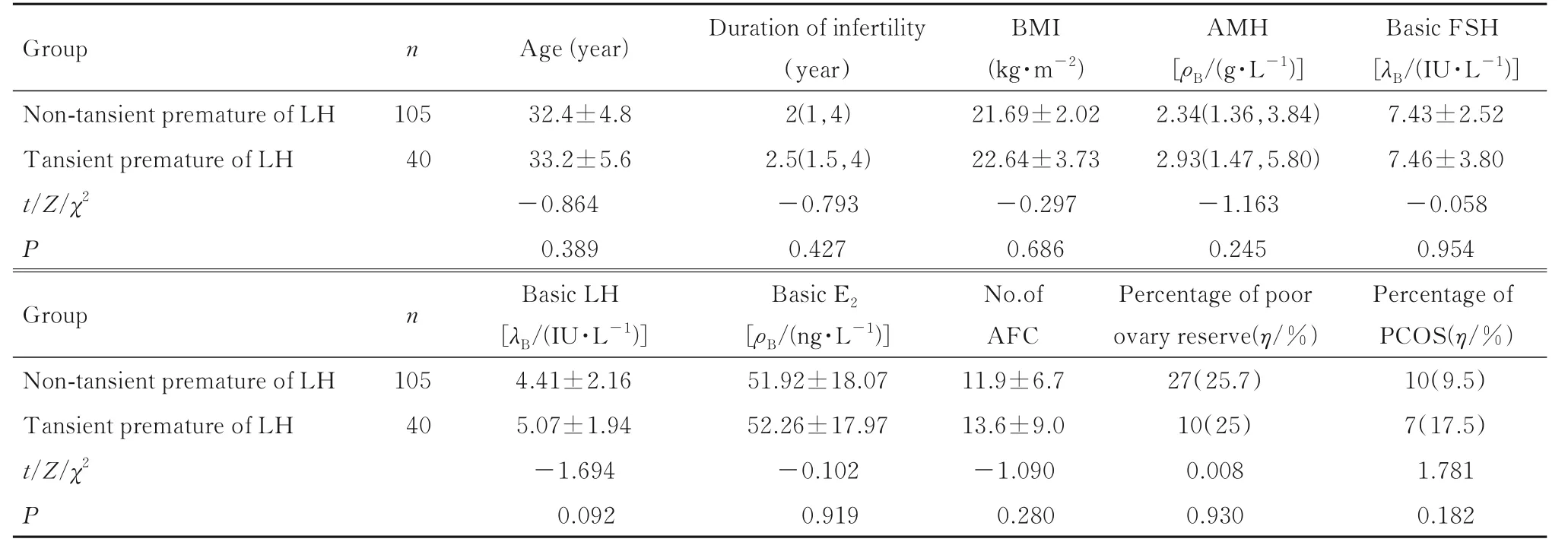
表1 2 组患者基本情况Tab.1 Basic informations of patients in two groups
2.2 2 组患者的促排卵情况LH 早升组患者添加拮抗剂日的Gn 天数、添加拮抗剂日LH 水平和添加拮抗剂日E2水平均大于无LH 早升组(t=-3.251,P=0.001;t=-10.198,P<0.001;t=3.233,P=0.002), 而拮抗剂使用天数小于无LH 早升组(t=3.090,P=0.003)。2 组患者其他促排卵情况比较差异无统计学意义(P>0.05)。见表2。
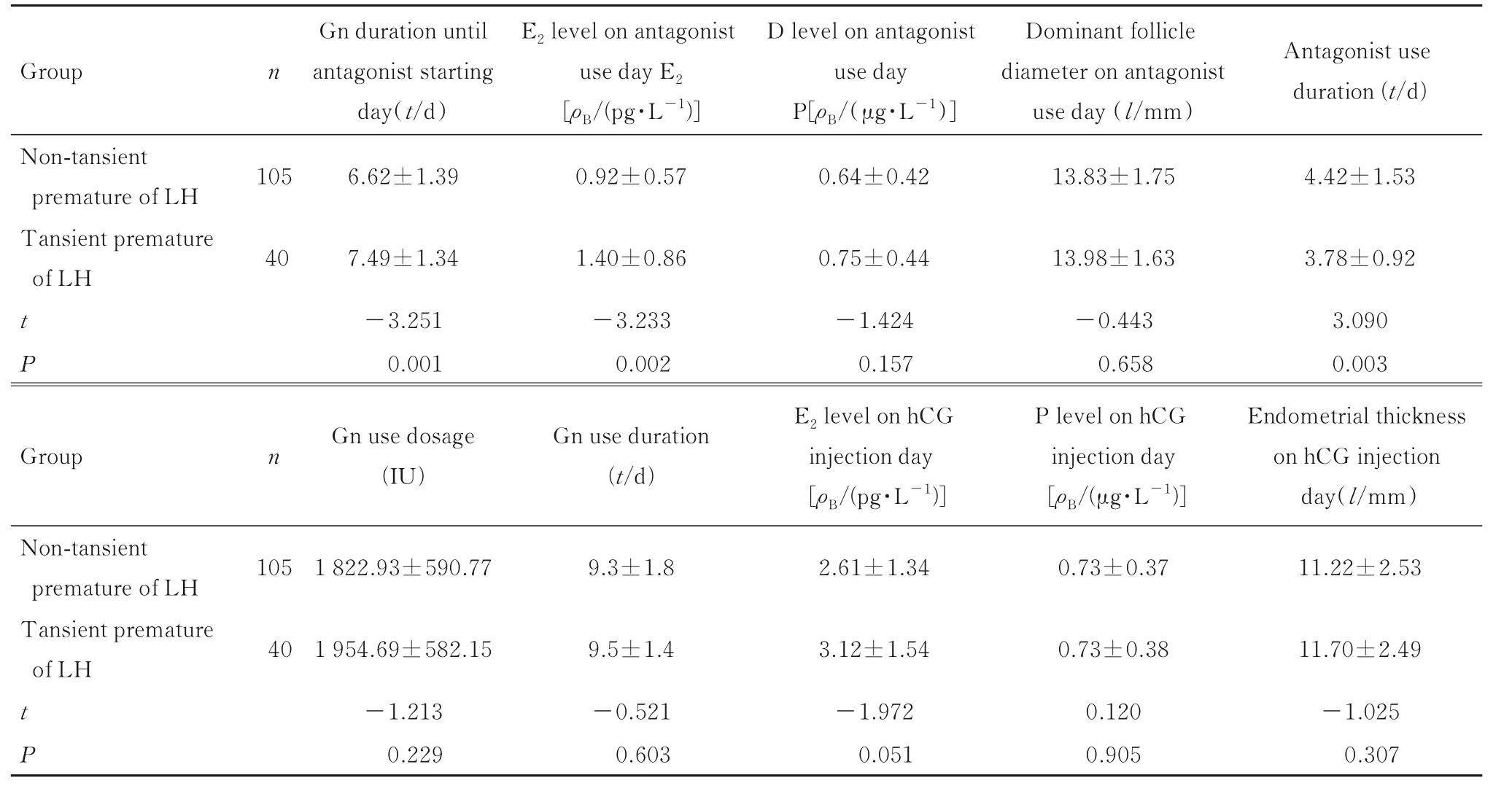
表2 2 组患者促排卵情况的临床指标Tab.2 Clinical indexes of ovarian stimulation of patients in two groups
2.3 2 组患者的促排卵结局2 组患者获卵数、成熟卵数(率)、正常受精数(率)、D3 可用胚胎数(率)和D3 优质胚胎数(率)比较差异无统计学意义(P>0.05)。见表3。
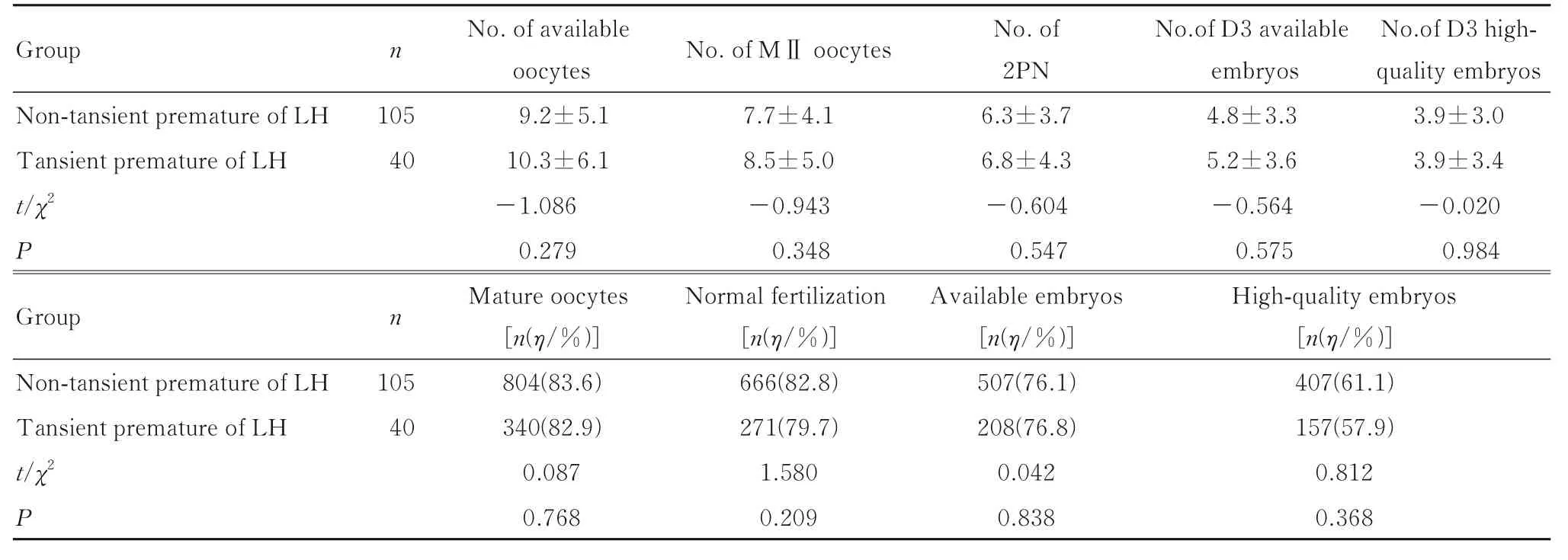
表3 2 组患者促排卵结局指标Tab.3 Outcome indexes of ovarian stimulation of patients in two groups
2.4 2 组患者新鲜IVF/ICSI-ET 周期的妊娠结局2 组患者平均移植胚胎数、移植囊胚百分率、胚胎种植率和临床妊娠率、继续妊娠率比较差异无统计学意义(P>0.05)。见表4。
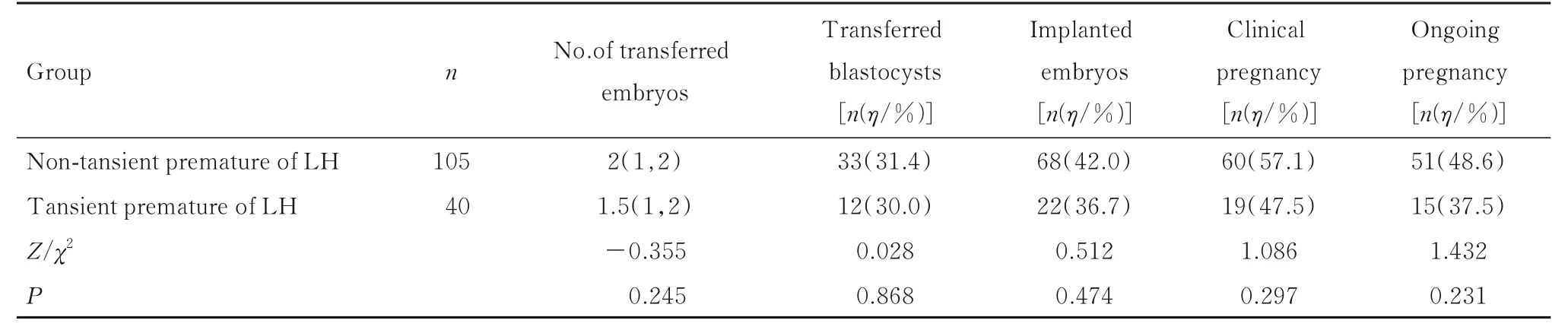
表4 2 组患者新鲜IVF/ICSI-ET 周期移植妊娠结局指标Tab.4 Indexes of pregnancy outcomes of patients underwent fresh IVF/ICSI-ET cycle transplantation in two groups
2.5 影响新鲜IVF/ICSI-ET 周期GnRH 拮抗剂灵活方案中LH 早升的多因素Logistic 回归分析将单因素分析中P<0.1 的变量(包括基础LH 水平、添加拮抗剂时E2水平、添加拮抗剂时最大卵泡直径和添加拮抗剂的Gn 天数)纳入多因素Logistic 回归方程, 分析结果显示:添加拮抗剂的Gn 天数和添加拮抗剂当日E2水平是新鲜IVF/ICSI-ET 周期拮抗剂灵活方案中 LH 早升的危险因素[OR (95%CI) =1.516 (1.128~2.038),P=0.006;OR (95%CI) =2.424 (1.345~4.371),P=0.003]。见表5 和6。

表5 多因素Logistic 回归分析变量赋值Tab. 5 Assignments of multivariate Logistic regression analysis
3 讨 论
20 世纪90 年代以来, 越来越多生殖工作者将拮抗剂方案应用于临床超促排卵。国内各中心中拮抗剂的使用率不断升高。研究[8]显示:拮抗剂方案在超促排卵方案中的百分率从2012 年的8.30%升至2016 年的26.39%, 而激动剂长方案的百分率则从58.31%降至43.69%;但采用拮抗剂方案患者的妊娠率低于采用激动剂长方案者(29.21%~39.41%vs48.56%~52.90%), 提示拮抗剂方案仍不完善, 仍需要进一步探索和规范。内源性LH控制是拮抗剂方案的一个关键点。内源性LH 早升未加以控制, 会引起颗粒细胞过早黄素化[9]或者小卵泡排卵, 损伤卵母细胞质量, 影响妊娠结局。但一过性内源性的LH 早升对妊娠结局的影响尚不明确。本研究探讨新鲜移植周期患者的妊娠情况数据, 其孕酮在拮抗剂添加日和HCG 日其P 水平均<1.5 μg·L-1, 提示卵泡颗粒细胞尚未黄素化;同时在添加拮抗剂后LH 均降至正常水平, 提示本中心对早发的内源性LH 峰控制良好。在此基础上, 本文作者发现:无LH 早升组和LH 早升组患者成熟卵数(率)、正常受精数(率)、D3 可用胚胎数(率)、D3 优质胚胎数(率)、胚胎种植率、临床妊娠率和继续妊娠率组间比较差异无统计学意义, 提示控制良好的早发LH 峰对新鲜移植周期妊娠结局无不良影响。
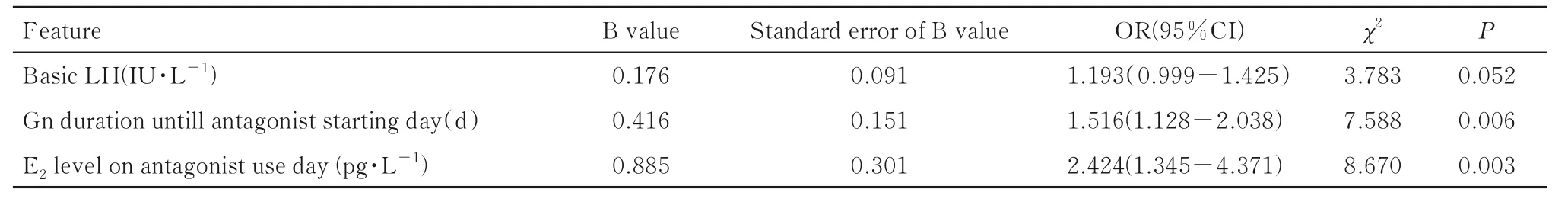
表6 GnRH 拮抗剂灵活方案中LH 一过性早升的多因素Logistic 回归分析Tab.6 Multivariate Logistic regression analysis on transient premature of LH in GnRH antagonist flexible protocol
目前关于早发LH 峰对于患者妊娠结局的影响仍存在争议。肖珊等[10]发现:PCOS 患者拮抗剂方案中早发LH 升高不影响IVF-ET 的临床结局;叶虹[11]提出:仅血清LH 水平升高提示卵泡未黄素化, 其原因可能是LH 刚开始上升或卵泡较小时, 颗粒细胞中LH 受体少, 不能对升高的LH 产生反应。若此时给予拮抗剂抑制早发LH 峰, 可挽救该助孕周期, 而获得相对满意的妊娠结局。中国女医师协会生殖医学专业委员会专家共识编写组[4]在最近发布的辅助生殖领域拮抗剂方案标准化应用专家共识中提出:当发生早发LH 峰时, 控制良好的LH 水平对临床结局无明显影响, 无需取消周期, 这与本研究结论相似。但也有研究[3]显示:在拮抗剂灵活方案中新鲜移植周期中, 即使患者未出现P 早升, 早升的LH 仍然影响其种植率、妊娠率和活产率;DOVEY 等[1]研究显示:采用拮抗剂方案的IVF-ET 患者中, 早发LH 峰会降低其继续妊娠率。因此, 仍需要进一步排除混杂因素, 加大样本量进行研究。
根据拮抗剂添加的时机不同, 拮抗剂方案分为灵活方案和固定方案2 种方案。固定方案:一般在Gn 使用的第5 日或第6 日开始加用0.25 mg 拮抗剂, 每日1 次至扳机日。灵活方案:拮抗剂添加时机根据优势卵泡直径、E2和LH 水平[12]来判断。灵活方案中拮抗剂添加无统一标准, 可以在优势卵泡直径在14 mm 或15 mm 时, 也可以在优势卵泡直径>12 mm 和血清E2>300 ng·L-1时[4]。本研究采用拮抗剂灵活方案当最大卵泡直径≥14 mm, 或者E2≥300 ng·L-1即添加拮抗剂。研究[13-14]显示:固定方案和灵活方案中出现内源性LH 峰的概率无差别, 而灵活方案中拮抗剂使用时间较短或用量较少。ZHANG 等[3]研究显示:拮抗剂灵活方案中未LH 早升和LH 早升组患者拮抗剂使用的Gn 天数为6.9~7.1 d, 均大于6 d, 长于固定方案, 提示固定方案比灵活方案添加拮抗剂时间早。本研究采用多因素Logistic 回归分析, 结果显示:添加拮抗剂的Gn 天数仍然是新鲜IVF/ICSI-ET 周期拮抗剂灵活方 案 中LH 早 升 的 危 险 因 素[OR (95%CI) =1.516(1.128~2.038),P=0.006], 结果预示拮抗剂使用的Gn 天数越长, 越容易产生早发LH 峰;而较早添加拮抗剂可能降低早发LH 峰发生率[15-17]。
自然周期时, 发育成熟卵泡分泌雌激素达到阈值并维持一定时间, 即可发生正反馈而形成LH峰[18]。在COH 中, 多卵泡发育使雌激素过早升高, 在卵泡未发育成熟前即出现早发LH 峰[19], 多见 于 高 反 应 患 者, 如PCOS 患 者[1, 10, 20-21]。 研究[22-23]显示:较低雌激素水平时添加拮抗剂可以改善妊娠结局;WERTHEIMER 等[24]认为:在添加拮抗剂日, 较低雌激素水平使成熟卵率提高, 其原因可能是减少内源性LH 峰的出现。本研究中LH 早升组患者E2水平明显高于无LH 早升组, 多因素Logistic 回归分析结果显示:添加拮抗剂日E2水平仍然是LH 早升的危险因素[OR(95%CI)=2.424(1.345~4.371),P=0.003], 提示在较低E2水平时添加拮抗剂可能减少内源性LH 峰的发生率。除此之外, 早发LH 峰在卵巢低储备患者中发生率较高[25], 其原因可能与卵巢储备低, 小卵泡数量少, 导致促性腺激素分泌峰抑制因子活性低, 不能抑制LH 分泌有关[26]。
综上所述, 拮抗剂灵活方案中内源性LH 一过性早升不影响妊娠结局, 但需要及时控制升高的LH, 避免卵泡早排或者黄素化;在雌激素较低水平时较早添加拮抗剂可以减少早发LH 峰。但是如何精准判断添加拮抗剂时机仍需要继续探索。本研究样本量较少, 未来还需加大样本量行进一步研究。
