乌天麻二氯甲烷萃取部位化学成分及其胆碱酯酶抑制活性的研究
2022-12-08段晓燕陈贻芳罗吉凤丁培超田孟华王跃虎
段晓燕,阎 慧,陈贻芳,罗吉凤,丁培超,田孟华*,王跃虎*
乌天麻二氯甲烷萃取部位化学成分及其胆碱酯酶抑制活性的研究
段晓燕1,阎 慧1,陈贻芳1,罗吉凤1,丁培超2,田孟华2*,王跃虎1*
1. 中国科学院昆明植物研究所 云南省真菌多样性与绿色发展重点实验室和植物化学与西部植物资源持续利用国家重点实验室,云南 昆明 650201 2. 昭通市天麻研究院,云南 昭通 657000
研究乌天麻二氯甲烷萃取部位的化学成分及其胆碱酯酶抑制活性。采用Ellman法测定了二氯甲烷萃取部位对乙酰胆碱酯酶(acetyl cholinesterase,AChE)和丁酰胆碱酯酶(butyryl cholinesterase,BuChE)的抑制活性;利用硅胶柱色谱、Sephadex LH-20柱色谱、半制备高效液相色谱等方法进行分离纯化;利用NMR、MS等技术鉴定化合物结构;测定所有单体化合物的胆碱酯酶抑制活性。乌天麻二氯甲烷萃取部位对AChE和BuChE均有显著的抑制活性,半数抑制浓度(median inhibition concentration,IC50)分别为10.45、9.20 μg/mL;从中分离得到11个化合物,分别鉴定为环[甘氨酸-l--(4ʹʹ-羟基苯基)半胱氨酸](1)、5ʹ-甲硫基腺苷(2)、对羟基苄胺(3)、对羟基苯甲醇(4)、对羟基苯甲醛(5)、2-甲基-3-羟基吡啶(6)、4-乙酰氧甲苯基-β--吡喃葡萄糖苷(7)、4-(乙氧基甲基)苯酚β--吡喃葡萄糖苷(8)、小檗碱(9)、(+)-thalirugidine(10)和(+)-海兰地嗪(11)。化合物1~3和9~11为首次从天麻属中分离得到。化合物9(IC50=5.93 μmol/L)和10(IC50=42.49 μmol/L)对AChE有抑制活性,化合物10(IC50=21.20 μmol/L)对BuChE有抑制活性。
兰科;乌天麻;生物碱;胆碱酯酶抑制活性;小檗碱;(+)-thalirugidine;(+)-海兰地嗪
天麻又名赤箭、独摇芝、定风草、合离草,为兰科植物天麻Blume的干燥块茎[1],主产于贵州、云南、陕西、四川等省,是我国名贵中药材之一[2]。根据天麻块茎形状、块茎含水量、花及花茎的颜色特点,将天麻划分为4个类型,即红天麻Bl. f.、绿天麻Bl. f.Makino、乌天麻Bl. f.S. Chow和黄天麻Bl. f.S. Chow[3-4]。前人已对天麻的化学成分及其药理作用进行了大量研究[5-7],在治疗神经系统疾病方面的研究尤其受到关注[8-9]。有研究报道,天麻醋酸乙酯部分对小鼠学习记忆获得障碍有改善作用,还能降低脑胆碱酯酶的活力及保护脑缺氧,但是起作用的活性成分并不清楚[10]。另有研究表明,天麻超微粉能够改善血管性痴呆大鼠的学习记忆障碍,其作用机制与上调胆碱乙酰转移酶(choline acetyltransferase,ChAT)蛋白,抑制乙酰胆碱酯酶(acetyl cholinesterase,AChE)蛋白,提高脑内乙酰胆碱的作用密切相关[11]。
主产于我国云南省昭通市彝良县小草坝地区的乌天麻,具有较高的药用价值和食用价值[12-13]。目前对乌天麻的生物碱类成分还缺乏系统的研究。本研究在制备乌天麻总生物碱,即二氯甲烷萃取部位后,评价了其对AChE和丁酰胆碱酯酶(butyryl cholinesterase,BuChE)的抑制活性,结果显示,二氯甲烷萃取部位对AChE和BuChE均有显著的抑制活性,半数抑制浓度(median inhibition concentration,IC50)分别为10.45、9.20 μg/mL。因此开展了二氯甲烷萃取部位的化学成分研究,分离得到11个化合物(图1),分别鉴定为环[甘氨酸-l-- (4ʹʹ-羟基苯基)半胱氨酸] {cyclo[glycine-l--(4ʺ- hydroxybenzyl)cysteine],1}、5ʹ-甲硫基腺苷(5′--methyl-5′-thioadenosine,2)、对羟基苄胺[4-(aminomethyl)phenol,3]、对羟基苯甲醇[4-(hydroxymethyl)phenol,4]、对羟基苯甲醛(4-hydroxybenzaldehyde,5)、2-甲基-3-羟基吡啶(2-methylpyridin-3-ol,6)、4-乙酰氧甲苯基-β--吡喃葡萄糖苷{4-[(acetyloxy)methyl] phenyl β-- glucopyranoside,7}、4-(乙氧基甲基)苯酚β--吡喃葡萄糖苷[4-(ethoxymethyl)phenol β--glucopyra- nosid,8]、小檗碱(berberine,9)、(+)-thalirugidine(10)和(+)-海兰地嗪[(+)-hernandezine,11]。其中,化合物1~3和9~11为首次从天麻属中分离得到。胆碱酯酶抑制活性测试结果显示,化合物9(IC50=5.93 μmol/L)和10(IC50=42.49 μmol/L)对AChE有抑制活性,化合物10(IC50=21.20 μmol/L)对BuChE有抑制活性。

图1 化合物1~11的化学结构
1 材料与仪器
薄层色谱硅胶板和柱色谱硅胶(80~100、200~300、300~400目)为青岛海洋化工厂生产;中性氧化铝(100~200目)为上海五四化学试剂有限公司生产;反相(RP)C18硅胶(40~63 μm)、色谱级甲醇、乙腈为德国Merck公司生产;分析纯石油醚、甲醇等为北京化工生产;高效液相色谱仪为Agilent 1200型,检测器为二极管阵列检测器(DAD),半制备柱为Welch Ultimate AQ-C18(250 mm×7.8 mm,5.0 µm),Agilent ZORBAX RX-C8(250 mm×9.4 mm,5.0 µm),YMC-Pack SIL(250 mm×10.0 mm,5.0 µm);凝胶色谱为Sephadex LH-20(GE Healthcare Bio-Xciences AB);1D和2D NMR用AVANCE III 500 MHz和AV 600 MHz型核磁共振仪测定,内标为TMS;电喷雾电离质谱(ESI-MS)UPLC-IT-TOF型质谱仪(日本岛津公司);高分辨电喷雾电离质谱(HR-ESI-MS)Agilent G6230质谱、Agilent Applied Photophysics型数字式圆二色光谱仪(美国安捷伦公司);Shimadzu UV2401PC型紫外可见分光光度计(日本岛津公司);Jasco P-1020型全自动数字旋光仪(日本Jasco公司);酶标仪Multiskan FC(美国Thermo公司);人AChE(≥1000单位/毫克蛋白质)、人BuChE(≥50单位/毫克蛋白质)、碘化硫代乙酰胆碱、二硫代二硝基苯甲酸(DTNB)、阴性对照溶剂二甲基亚砜(DMSO)和阳性对照药物他克林均购自Sigma公司。
乌天麻产自云南省昭通市彝良县小草坝镇小草坝村海子组,于2019年12月采收后加工储存;由中国科学院昆明植物研究所周铉研究员鉴定为乌天麻Bl. f.S. Chow,凭证标本(YJ2021040)存放于中国科学院昆明植物研究所资源植物与生物技术重点实验室。
2 提取与分离
乌天麻干燥块茎20 kg粉碎,用95%乙醇加热到60 ℃超声提取30 min,减压浓缩得到粗提物(1.8 kg)。将其混悬于3 L水中,用等体积石油醚萃取3次,有机相经减压蒸馏回收溶剂后,得到石油醚萃取部分(142.2 g)。剩余水相用1.5% HCl将pH值调至2左右,用等体积醋酸乙酯萃取3次,有机相经减压蒸馏回收溶剂后,得到醋酸乙酯萃取部分(104.4 g)。剩余酸性水相溶液用5% NaOH将pH值调至9左右,用等体积二氯甲烷萃取3次,有机相经减压蒸馏回收溶剂后,得到二氯甲烷萃取部位,即总生物碱(14.1 g)。
二氯甲烷萃取部位用硅胶柱色谱以CH2Cl2/MeOH(1∶0→0∶1)进行梯度洗脱,经TLC检查后合并得6个流分(Frs. 1~6)。Fr. 1(1.4 g)经RP C18硅胶柱色谱(30%→100%甲醇)和Sephadex LH-20柱色谱(甲醇)纯化,得到化合物3(66.0 mg)和5(120.0 mg)。Fr. 2(0.7 g)经硅胶柱色谱(石油醚-丙酮8∶1→0∶1)梯度洗脱得化合物6(26.0 mg)、Fr. 2-2和Fr. 2-3。Fr. 2-3(0.3 g)经Sephadex LH-20柱色谱(三氯甲烷-甲醇1∶1)和半制备HPLC(Ultimate AQ-C18,体积流量3 mL/min,乙腈-水25∶75)得到化合物4(5.5 mg,R=6.998 min)。Fr. 5(0.4 g)经RP C18硅胶柱色谱(20%→100%甲醇)得到Frs. 5-1~5-4,Fr. 5-1经Sephadex LH-20柱色谱(甲醇)纯化,得到化合物1(16.0 mg)和2(14.0 mg);Fr. 5-3(116.0 mg)经半制备HPLC(Ultimate AQ-C18),体积流量2 mL/min,甲醇-水80∶20)得到化合物10(4.1 mg,R=15.405 min);Fr. 5-4经半制备HPLC(Agilent RX-C8,体积流量2 mL/min,甲醇-水78∶22)得到化合物11(2.4 mg,R=9.761 min)。Fr. 6(0.9 g)经RP C18硅胶柱色谱(20%→100%甲醇)得到Fr. 6-1~6-4,Fr. 6-1经半制备HPLC(YMC-Pack SIL,体积流量2 mL/min,正己烷-异丙醇40∶60)得到化合物8(1.6 mg,R=19.127 min)和7(2.8 mg,R=21.907 min);Fr. 6-4经氧化铝柱色谱(石油醚-醋酸乙酯2∶1)和半制备HPLC(Agilent RX-C8,体积流量2 mL/min,甲醇-水30∶70)得到化合物9(2.4 mg,R=12.592 min)。
3 结构鉴定
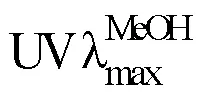
化合物2:白色无定形粉末,分子式C11H15N5O3S;[α]20 D+1.9 (0.26, MeOH);ESI-MS (+)/: 320 [M+Na]+。1H-NMR (500 MHz, methanol-4): 8.32 (1H, s, H-8), 8.20 (1H, s, H-2), 6.00 (1H, d,= 5.1 Hz, H-1ʹ), 4.77 (1H, t,= 5.1 Hz, H-2ʹ), 4.32 (1H, dd,= 5.1, 4.8 Hz, H-3ʹ), 4.21 (1H, m, H-4ʹ), 2.94 (1H, dd,= 14.1, 5.7 Hz, H-5ʹa), 2.86 (1H, dd,= 14.2, 6.1 Hz, H-5ʹb), 2.11 (3H, s, 5ʹ- SCH3);13C-NMR (125 MHz, methanol-4): 157.3 (C-6), 153.9 (C-2), 150.7 (C-4), 141.4 (C-8), 120.5 (C-5), 89.9 (C-1ʹ), 85.5 (C-4ʹ), 74.9 (C-2ʹ), 74.0 (C-3ʹ), 37.4 (C-5ʹ), 16.5 (5ʹ-SCH3)。以上数据与文献报道数据[15]比较,鉴定化合物2为5ʹ-甲硫基腺苷。
化合物3:无色片状晶体(甲醇),mp 115~118 ℃,分子式C7H9NO;ESI-MS (+)/:124 [M+H]+。1H-NMR (500 MHz, methanol-4): 7.05 (2H, brd,= 8.5 Hz, H-2, 6), 6.72 (2H, brd,= 8.5 Hz, H-3, 5), 3.53 (2H, s, H2-7);13C-NMR (125 MHz, methanol-4): 158.0 (C-1), 131.7 (C-3, 5), 129.6 (C-4), 116.1 (C-2, 6), 43.6 (C-7)。以上数据与文献报道数据[16]比较,鉴定化合物3为对羟基苄胺。
化合物4:白色无定形粉末,分子式C7H8O2;ESI-MS (-)/123 [M-H]⁻。1H-NMR (500 MHz, methanol-4): 7.16 (2H, brd,= 8.5 Hz, H-2, 6), 6.74 (2H, brd,= 8.5 Hz, H-3, 5), 4.47 (2H, s, H2-7);13C-NMR (125 MHz, methanol-4): 157.9 (C-1), 133.4 (C-4), 129.8 (C-3, 5), 116.0 (C-2, 6), 65.1 (C-7)。以上数据与文献报道数据[17]比较,鉴定化合物4为对羟基苯甲醇。
化合物5:白色无定形粉末,分子式C7H6O2;ESI-MS (-)/: 121 [M-H]⁻;1H-NMR (500 MHz, methanol-4): 9.75 (1H, s, H-7), 7.76 (2H, brd,= 8.5 Hz, H-2, 6), 6.91 (2H, brd,= 8.5 Hz, H-3, 5);13C-NMR (125 MHz, methanol-4): 192.8 (C-7), 165.2 (C-1), 133.4 (C-3, 5), 130.3 (C-4), 116.9 (C-2, 6)。以上数据与文献报道数据[17]比较,鉴定化合物5为对羟基苯甲醛。
化合物6:黄色油状物,分子式C6H7NO;ESI-MS (-)/: 108 [M-H]⁻。1H-NMR (500 MHz, methanol-4): 7.84 (1H, dd,= 4.6, 1.3 Hz, H-6), 7.13 (1H, dd,= 8.0, 1.3 Hz, H-4), 7.07 (1H, dd,= 8.0, 4.6 Hz, H-5), 2.39 (3H, s, CH3-7);13C-NMR (125 MHz, methanol-4): 153.8 (C-3), 147.6 (C-2), 139.4 (C-6), 123.6 (C-5), 123.1 (C-4), 18.4 (C-7)。以上数据与文献报道数据[18]比较,鉴定化合物6为2-甲基-3-羟基吡啶。
化合物7:白色无定形粉末,分子式C15H20O8;[α]20 D-27.2 (0.27, MeOH);ESI-MS (+)/: 351 [M+Na]+。1H-NMR (600 MHz, methanol-4): 7.29 (2H, brd,= 8.6 Hz, H-3, 5), 7.07 (2H, brd,= 8.6 Hz, H-2, 6), 5.03 (2H, s, H2-7), 4.91 (1H, d,= 7.5 Hz, H-1ʹ), 3.89 (1H, dd,= 12.1, 2.0 Hz, H-6ʹa), 3.69 (1H, dd,= 12.1, 5.4 Hz, H-6ʹb), 2.04 (3H, s, H3-9);13C-NMR (150 MHz, methanol-4): 172.7 (C-8), 159.1 (C-1), 131.5 (C-4), 130.9 (C-3), 130.3 (C-5), 117.7 (C-2), 117.6 (C-6), 102.2 (C-1ʹ), 78.2 (C-3ʹ), 78.0 (C-5ʹ), 74.9 (C-2ʹ), 71.4 (C-4ʹ), 67.0 (C-7), 62.5 (C-6ʹ), 20.9 (C-9)。以上数据与文献报道数据[19]比较,鉴定化合物7为4-乙酰氧甲苯基-β--吡喃葡萄糖苷。
化合物8:白色无定形粉末,分子式C15H22O7;[α]20 D-59.4 (0.16, MeOH);ESI-MS (+)/: 337 [M+Na]+。1H-NMR (600 MHz, methanol-4): 7.26 (2H, brd,= 8.4 Hz, H-2, 6), 7.07 (2H, brd,= 8.4 Hz, H-3, 5), 4.88 (1H, d,= 7.2 Hz, H-1ʹ), 4.43 (2H, s, H2-7), 3.88 (1H, dd,= 12.1, 2.2, H-6ʹa), 3.69 (1H, dd,= 12.1, 5.5 Hz, H-6ʹb), 3.51 (2H, q,= 7.1 Hz, H2-8), 1.19 (3H, t,= 7.1 Hz, H3-9);13C-NMR (150 MHz, methanol-4): 158.8 (C-1), 133.6 (C-4), 130.3 (C-3, 5), 117.6 (C-2, 6), 102.3 (C-1ʹ), 78.2 (C-3ʹ), 78.0 (C-5ʹ), 74.9 (C-2ʹ), 73, 3 (C-7), 71.4 (C-4ʹ), 66.5 (C-8). 62.5 (C-6ʹ), 15.4 (C-9)。以上数据与文献报道数据[20]比较,鉴定化合物8为4-(乙氧基甲基)苯酚β--吡喃葡萄糖苷。
化合物9:黄色粉末,分子式C20H18NO4;ESI-MS (+)/336 [M]+。1H-NMR (500 MHz, methanol-4): 9.76 (1H, s, H-8), 8.70 (1H, s, H-13), 8.11 (1H, d,= 9.1 Hz, H-11), 7.99 (1H, d,= 9.1 Hz, H-12), 7.66 (1H, s, H-1), 6.96 (1H, s, H-4), 6.10 (2H, s, OCH2O), 4.91 (2H, t,= 6.4 Hz, H2-6), 4.19, 4.10 (各3H, s, 2×OMe), 3.25 (2H, t,= 6.4 Hz, H2-5);13C-NMR (125 MHz, methanol-4): 152.2 (C-3), 152.0 (C-9), 149.9 (C-2), 146.4 (C-8), 145.8 (C-10), 139.7 (C-14), 135.2 (C-12a), 131.9 (C-4a), 128.1 (C-13), 124.5 (C-12), 123.3 (C-14a), 121.9 (C-8a), 121.5 (C-11), 109.4 (C-4), 106.5 (C-1), 103.7 (OCH2O), 62.5 (9-OCH3), 57.6 (10-OCH3), 57.2 (C-6), 28.2 (C-5)。以上数据与文献报道数据[21]比较,鉴定化合物9为小檗碱。
化合物10:白色无定形粉末,分子式C39H46N2O8;[α]20 D+88.1 (0.10, MeOH);ESI-MS (+)/671 [M+H]+;ECD (0.01, MeOH)max(Δ) 230 (+10.13) nm。1H-NMR(500 MHz, methanol-4) 和13C-NMR (125 MHz, methanol-4) 数据见表1。光谱数据与文献报道数[22]据比较,鉴定化合物10为(+)-thalirugidine。该化合物的参考文献中只给出了氢谱数据,没有碳谱数据,本研究根据它的2D NMR相关,对其1D NMR数据进行了完整的归属。
化合物11:白色无定形粉末,分子式C39H44N2O7;[α]20 D+75.1 (0.14, MeOH);ESI-MS (+)/653 ([M+H]+);UV (MeOH)max(log) 282 (3.61) nm;ECD (0.01, MeOH)max(Δ) 218 (+17.24) nm;1H-NMR (500 MHz, methanol-4) 和13C-NMR (126 MHz, methanol-4) 数据见表1。光谱数据与文献报道[23]数据比较,鉴定化合物11为(+)-海兰地嗪。该化合物的参考文献中只给出了氢谱数据,没有碳谱数据,本实验根据它的2D NMR相关,对其1D NMR数据进行了完整的归属。

表1 化合物10和11的1H-NMR和13C-NMR数据

续表1
4 胆碱酯酶抑制活性研究
采用Ellman法测定所分离化合物的AChE和BuChE抑制活性[24]。样品溶解在DMSO中;取150 μL磷酸盐缓冲液(pH 8.0)、10 μL测试样品和40 μL AChE(0.1 U/mL)或80 μL BuChE(0.04 U/mL)于96孔板中,37 ℃放置10 min后,分别加入10 μL DTNB(0.625 mmol/L)和40 μL乙酰基碘化硫代胆碱(0.625 mmol/L)或丁基碘化硫代胆碱(0.625 mmol/L)充分混匀,每隔30 s在405 nm下监测乙酰/丁酰硫代胆碱的水解情况,持续1 h。阳性对照组为他克林,终浓度为0.333 μmol/L;对照组为DMSO溶剂,终浓度为0.1%;所有反应均进行了3个重复。测定吸光度()值并按公式计算各浓度下的抑制率,并计算得到样品对AChE和BuChE的IC50值。
抑制率=1-样品/对照
实验结果(表2)显示,化合物9和10具较好的AChE抑制活性;化合物10具较好的BuChE抑制活性;其他化合物均未表现出明显活性。
5 讨论
云南省昭通市彝良县小草坝拥有独特的气候和地理条件,该地区主产的乌天麻天麻素平均含量为1.42%[25],多糖含量为26.53%[26],具有较高的药用和食用价值。为了充分挖掘其潜在利用价值并提供科学的理论依据,本研究对乌天麻二氯甲烷萃取部位进行胆碱酯酶抑制活性测定,结果显示该部位有较好的胆碱酯酶抑制活性;并对二氯甲烷萃取部位的化学成分进行系统研究,共分离鉴定了11个化合物,其中化合物1~3和9~11为首次从天麻属中分离得到。化合物9~11为异喹啉生物碱,异喹啉生物碱主要分布于罂粟科(Papaveraceae)、巴比特科(Berbidaceae)、毛茛科(Ranunculaceae)和防己科(Menispermaceae)中[27],其结构类型复杂,药用价值大,具有镇痛、抗心律失常、降血压、抗肿瘤、抗抑郁等多方面的生理活性;本研究首次从天麻属中分离出异喹啉生物碱。
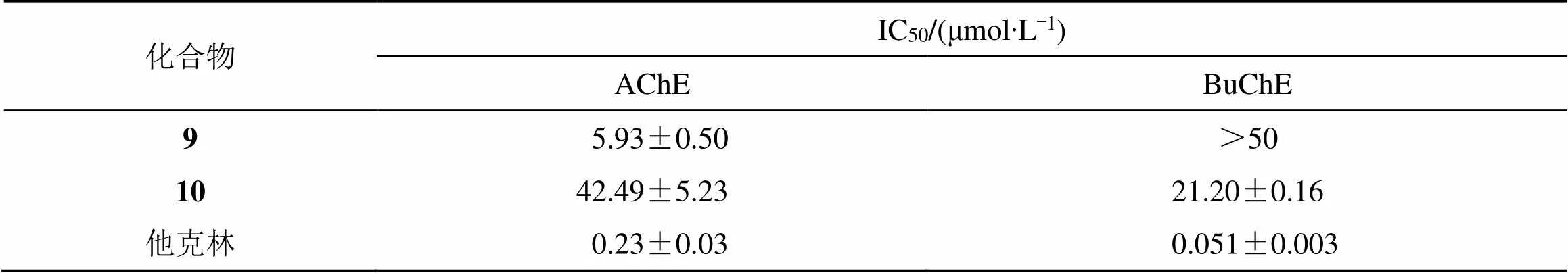
表2 化合物9、10对胆碱酯酶的抑制活性a
a其余化合物在50 μmol/L或100 μg/mL时,对AChE和BuChE抑制率低于50%
ainhibitory rates of other compounds on AChE and BuChE were lower than 50% at 50 μmol/L or 100 μg/mL
胆碱酯酶是参与中枢神经系统的一种关键酶,阿尔茨海默病(Alzheimer’s disease,AD)等神经退行性疾病与大脑内乙酰胆碱的缺失有关,胆碱酯酶抑制剂能有效缓解AD的症状。所有单体化合物均进行了胆碱酯酶抑制活性测试,结果显示化合物9和10有较好的AChE抑制活性,化合物10还有较强的BuChE抑制活性。化合物9、10均为异喹啉类生物碱,此类生物碱的胆碱酯酶抑制活性值得关注。
本研究初步揭示了乌天麻二氯甲烷萃取部位及其化学成分的胆碱酯酶抑制活性,为从乌天麻中发现具有神经保护活性的先导分子提供了新的思路。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典[S]. 一部. 2020: 59.
[2] 李梁, 张艺, 成群芝. 中药天麻产区生态环境分析与评价 [J]. 中药研究与信息, 2004, 6(6): 14-16.
[3] 吴尊华, 王绍柏, 余昌俊. 天麻不同品种商品形态和质量性状比较分析 [J]. 食用菌, 2011, 33(3): 24-26.
[4] 李振斌, 邓薇, 徐大东, 等. 不同品种天麻的形态组织学对比研究 [J]. 华西药学杂志, 2016, 31(1): 51-53.
[5] Kim H M, Kwon J, Lee K,. Constituents ofand their neuroprotective effects in HT22 hippocampal neuronal, R28 retinal cells, and BV2microglial cells [J].(), 2020, 9(8): 1051.
[6] 王志刚, 程俊伟. 天麻钩藤汤加减治疗肝阳上亢型原发性高血压疗效观察及对神经递质节律的影响[J]. 世界中医药, 2020, 15(1): 81-84.
[7] 魏富芹, 黄蓉, 何海艳, 等. 天麻的药理作用及应用研究进展 [J]. 中国民族民间医药, 2021, 30(11): 72-76.
[8] 付亚轩, 孟宪钰, 李明超, 等. 天麻抗抑郁药效物质及其作用机制研究进展 [J]. 中草药, 2020, 51(21): 5622-5630.
[9] 南一楠, 王少卿. 天麻素对神经系统疾病作用的基础研究进展 [J]. 中西医结合心脑血管病杂志, 2020, 18(22): 3811-3813.
[10] 林青, 田闯, 李立纪, 等. 天麻不同提取部位对学习记忆的影响 [J]. 中药药理与临床, 2002, 18(1): 12-13.
[11] 陈婷婷, 周雪, 徐旖旎, 等. 天麻超微粉调控胆碱能系统改善血管性痴呆大鼠学习记忆能力 [J]. 中国实验方剂学杂志, 2020, 26(15): 26-32.
[12] 冯晋, 徐娅玲, 孟庆婷, 等. 云南昭通不同产地天麻质控成分的含量测定 [J]. 云南中医中药杂志, 2021, 42(3): 76-79.
[13] 代玉洁, 李啸浪, 宋雪, 等. 云南天麻产业发展特点分析 [J]. 农业与技术, 2020, 40(12): 141-144.
[14] Zi J C, Lin S, Zhu C G,. Minor constituents from the tubers of[J]., 2010, 12(6): 477-484.
[15] Robins M J, Hansske F, Wnuk S F,. Nucleic acid related compounds. 66. Improved syntheses of 5'-chloro- 5'-deoxy- and 5'--aryl (or alkyl)-5'-thionucleosides [J]., 1991, 69(9): 1468-1474.
[16] 孙爱静, 庞素秋, 王国权. 白及化学成分与抗肿瘤活性研究 [J]. 中国药学杂志, 2016, 51(2): 101-104.
[17] 王亚威, 李志峰, 何明珍, 等. 天麻化学成分研究 [J]. 中草药, 2013, 44(21): 2974-2976.
[18] 段洁, 李巍, 胡旭佳, 等. 九子参化学成分研究 [J]. 中草药, 2009, 40(4): 528-530.
[19] 李海燕, 郑萍, 谢笑天. 合成天麻素中微量二组分的分离和鉴定 [J]. 中国新药杂志, 2006, 15(15): 1278-1281.
[20] Huang Z B, Wu Z, Chen F K,. The protective effects of phenolic constituents fromon the cytotoxicity induced by KCl and glutamate [J]., 2006, 29(11): 963-968.
[21] 汪冶, 杨小生, 赵超, 等. 滇产偏翅唐松草化学成分 [J]. 天然产物研究与开发, 2002, 14(5): 24-25.
[22] Wu W N, Beal J L, Fairchild E H,. Alkaloids of. 25. six new bisbenzylisoquinoline alkaloids fromrugosum [J]., 1978, 43(4): 580-585.
[23] Shamma M, Dudock B S, Cava M P,. Revised structures of hernandezine and thalsimine. mass spectrometry of a bisbenzylisoquinoline alkaloid [J].(), 1966(1): 7.
[24] Ellman G L, Courtney K D, Andres V Jr,. A new and rapid colorimetric determination of acetylcholinesterase activity [J]., 1961, 7: 88-95.
[25] 李德勋, 陈桂, 李辅碧, 等. 天麻不同变异类型药材中天麻素含量比较 [J]. 现代中药研究与实践, 2007, 21(3): 23-24.
[26] 吴刚, 秦民坚, 康继川, 等. 不同产地天麻质量评价 [J]. 现代中药研究与实践, 2007, 21(1): 40-43.
[27] 邵顺波. 异喹啉类生物碱的生理活性及研究进展 [J]. 安徽医药, 2007, 11(3): 254-255.
Chemical constituents and cholinesterase inhibitory activity of dichloromethane-soluble fraction fromf.
DUAN Xiao-yan1, YAN Hui1, CHEN Yi-fang1, LUO Ji-feng1, DING Pei-chao2, TIAN Meng-hua2, WANG Yue-hu1
1. Yunnan Key Laboratory for Fungal Diversity and Green Development and State Key Laboratory of Phytochemistry and Plant Resources Sustainable Use in West China, Kunming Institute of Botany, Chinese Academy of Sciences, Kunming 650201, China 2. Zhaotong Tianma Research Institute, Zhaotong 657000, China
To study the chemical constituents and cholinesterase inhibitory activity of the dichloromethane (CH2Cl2)-soluble fraction fromf.(Orchidaceae).The Ellman method was used to determine the inhibitory activity of CH2Cl2-soluble fraction on acetylcholinesterase (AChE) and butyrylcholinesterase (BuChE). Silica gel column chromatography, Sephadex LH-20, semi-preparative HPLC and other methods were used for separation and purification. NMR and MS were used to identify the structures of the compounds. The cholinesterase inhibitory activity of all compounds was determined.The CH2Cl2-soluble fraction off.showed significant inhibitory activities on AChE (IC50= 10.45 μg/mL) and BuChE (IC50= 9.20 μg/mL). Eleven compounds were isolated from the CH2Cl2-soluble fraction by chromatography and identified as cyclo[glycine-l--(4ʺ-hydroxybenzyl)cysteine] (1), 5′--methyl-5′-thioadenosine (2), 4-(aminomethyl)phenol (3), 4-(hydroxymethyl)phenol (4), 4-hydroxybenzaldehyde (5), 2-methylpyridin-3-ol (6), 4-[(acetyloxy)methyl] phenyl β--glucopyranoside (7), 4-(ethoxymethyl)phenol β--glucopyranoside (8), berberine (9), (+)-thalirugidine (10) and (+)-hernandezine (11) by spectroscopic methods.Compounds 1—3 and 9—11 are isolated fromf.for the first time. Compounds 9 (IC50= 5.93 μmol/L) and 10 (IC50= 42.49 μmol/L) showed AChE-inhibitory activity, while 10 (IC50= 21.20 μmol/L) also showed inhibitory activity against BuChE.
Orchidaceae;Bl. f.S. Chow; alkaloids; cholinesterase-inhibitory activity; berberine; (+)-thalirugidine; (+)-hernandezine
R284.1
A
0253 - 2670(2022)23 - 7324 - 07
10.7501/j.issn.0253-2670.2022.23.002
2022-06-12
中国科学院科技扶贫项目(KFJ-FP-201905);云南省科技入滇项目(202003AD150005)
段晓燕,女,助理研究员,研究方向为药用植物化学。E-mail: duanxiaoyan@mail.kib.ac.cn
王跃虎,男,副研究员,研究方向为民族药物学和民族植物学。E-mail: wangyuehu@mail.kib.ac.cn
田孟华,男,高级工程师,研究方向为天麻栽培、质量评价及天麻健康产品研发。E-mail: tianmenghua@126.com
[责任编辑 王文倩]
