海藻酸钠和硅酸钠对废镁合金粉尘产氢的抑制作用
2022-12-02李嘉欢许开立张毓媛
李嘉欢, 许开立, 张毓媛, 王 犇
(东北大学 资源与土木工程学院, 沈阳 110819)
镁合金是目前世界上最轻的可用金属工程结构材料[1],被广泛应用于设备制造、航空航天等众多领域.然而,在镁合金的打磨、抛光等加工过程中会产生具有爆炸性的镁合金粉尘,为预防镁合金粉尘爆炸事故的发生,湿式除尘系统被应用到镁合金粉尘收集工作中[2].值得注意的是,加工过程中产生的粒径为微米级的镁合金粉尘颗粒进入湿式除尘系统后,能够与水发生反应,产生氢气[3].同时,工业用水经消毒处理后由Cl-形成的酸性环境会腐蚀镁合金粉尘表面的氧化保护膜Mg(OH)2,增加水与颗粒内部单质镁的接触机会,促进产氢反应[4].由此可见,镁合金粉尘进入湿式除尘系统后具有持续产氢的能力.更为重要的是,氢气的爆炸极限为4%~75%,点火能量仅为0.03 mJ,是一种燃爆性较高的气体[5].氢气的存在给湿式除尘系统带来了火灾、爆炸的风险.目前工业上多采用检测报警、连锁排风、防爆电气等工程技术手段预防氢气爆炸事故的发生,尽管经济投入较高,但无法从本质上消除氢气爆炸的危险.因此,抑制镁合金粉尘遇水产氢对降低湿式除尘系统氢气爆炸风险具有重要意义.
目前,关于抑制金属粉尘遇水产氢方面的研究极少,且主要集中在铝粉尘方面.如Xu,Wang等[6-7]使用CeCl3、铬酸盐Cr(NO3)3·9H2O 等抑制铝粉尘与水的产氢反应,但研究中用的抑制剂毒性较强且对环境污染极其严重.Wang,Xu等[8-10]使用葡萄糖酸钠、大豆异黄酮和L-苹果酸等环境友好型抑制剂,解决了抑制剂对环境的污染问题;其作用机理是利用抑制剂为含铝粉尘颗粒表面的Al3+提供电子,从而生成新物质并形成保护膜,阻止产氢反应的进行.但镁可用的空轨道少,与铝相比更难失去或得到电子[11];对铝粉尘有效的抑制剂对镁粉尘几乎无效.因此,需要开展针对抑制镁合金粉尘与水反应产氢的研究.
本文中采用环境友好型的海藻酸钠(SA)和硅酸钠(SS)的复配抑制剂,通过产氢曲线和化学动力学对比分析各抑制剂溶液的作用效果,结合扫描电子显微镜(SEM)、能谱仪(EDS)、傅里叶变换红外光谱(FTIR)和X 射线衍射(XRD)分析反应产物及其表面形态、各元素质量分数,建立二者协同抑制机理,以预防湿式除尘系统中镁合金粉尘产生氢气而导致氢气爆炸事故的发生,对提高镁合金加工企业的本质化安全水平具有重要意义.
1 实 验
1.1 实验材料及设备
Mg-Zn 合金因具有比强度高等性能优势,被广泛应用于新能源汽车、航空航天及生物材料等领域[12].本文中选取Mg-Zn 合金粉尘作为实验用镁合金粉尘,其中Mg 的质量分数约为95%,余量为Zn.图1 显示了Mg-Zn 合金粉尘的粒径分布.实验采用3.5%NaCl(质量分数,下同)溶液模拟企业现场湿式除尘器的工业用水消毒液中Cl-对Mg-Zn 合金粉尘产氢的影响.图2 为作者所在团队自主研发的产氢测试仪(反应釜).
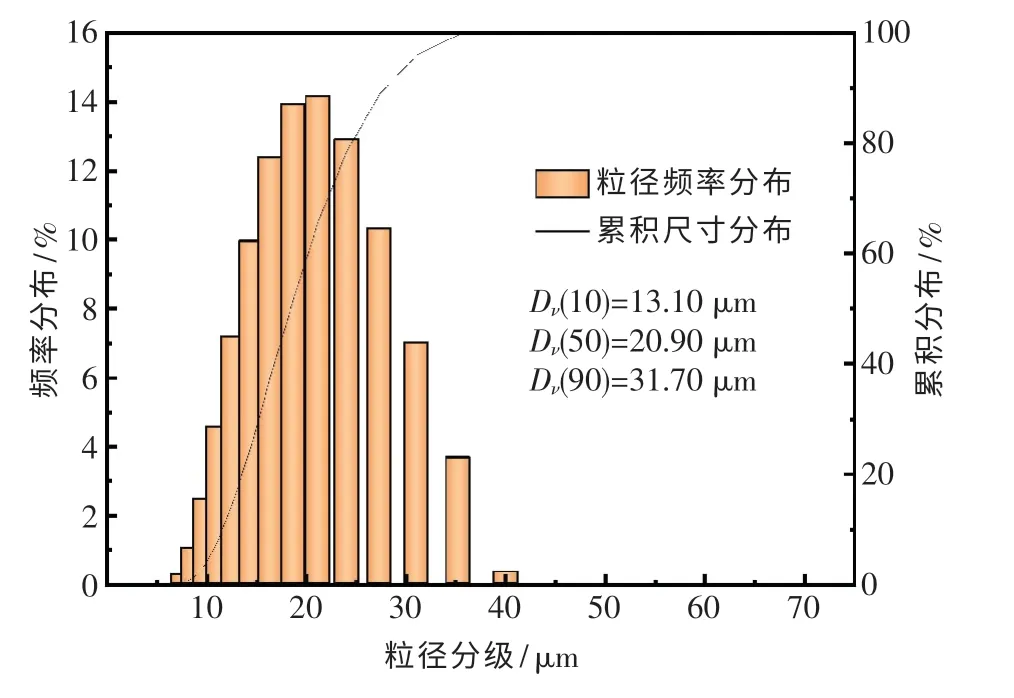
图1 Mg-Zn 合金粉尘的粒径分布Fig.1 Particle size distribution of Mg-Zn alloy dust particles
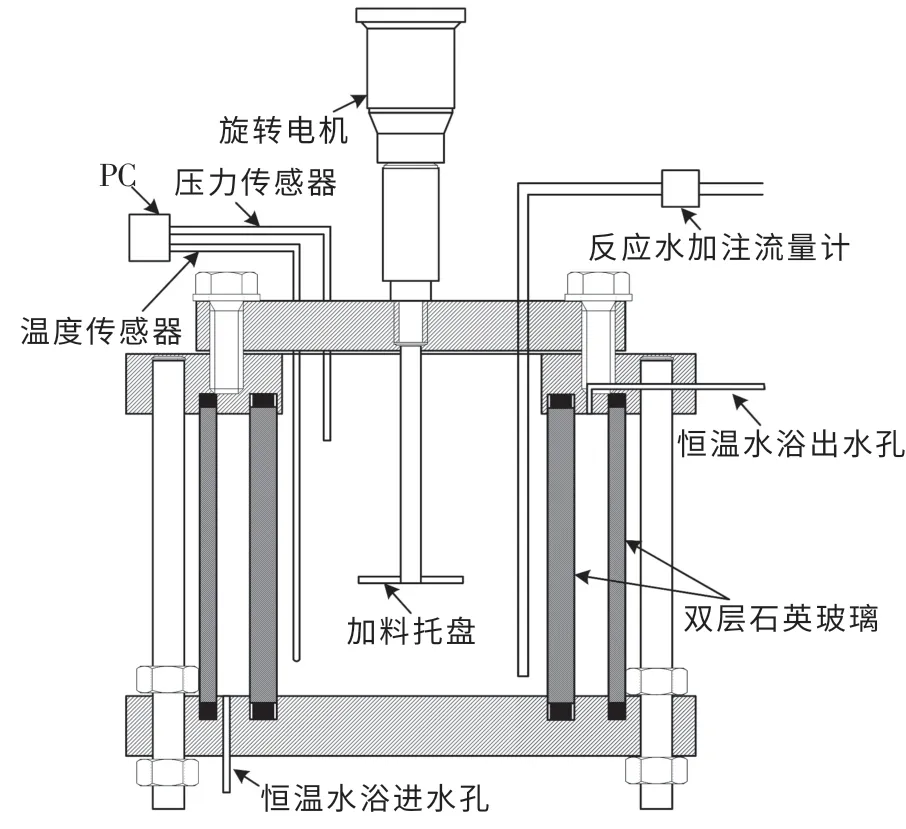
图2 反应釜Fig.2 Reactor structure diagram
1.2 实验步骤
分别配制200 mL 含3.5%NaCl 的SA 和SS各浓度梯度的单一抑制剂溶液,以及200 mL SA和SS 不同浓度配比的复配抑制剂溶液,放入产氢测试仪中,调节水浴温度为60 ℃,各放入1.5 g Mg-Zn 合金粉尘颗粒,收集各反应产物并进行过滤、干燥.实验温度设置为60 ℃,此时氢气产生的速率较大且抑制剂的脱附过程得到促进[13],能够更好地探究高温条件下的氢气抑制效果.
1.3 分析方法
根据理想气体方程及相关研究[7],产氢速率α 的计算公式可表述为
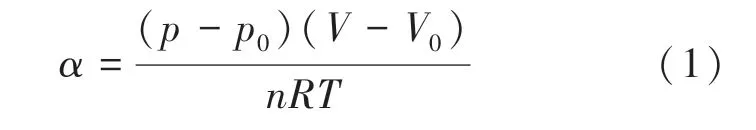
式中:p 为反应器内的压力,kPa;p0为反应器内的初始压力,kPa;V 为反应器体积,取值为1 L;V0为加入反应器的溶液体积,L;n 为实验所用合金粉尘颗粒的物质的量,mol;R 为理想气体常数,取值为8.314 J/(mol·K);T 为实验设定温度,K.
2 实验结果与分析
2.1 产氢曲线
图3 为SA 及SS 各自单一作用时的产氢曲线图.由图可知,SA 和SS 均可对产氢反应起到一定程度的抑制作用,SS 在Mg-Zn 合金粉尘与水快速反应阶段能够迅速抑制氢气的产生,而SA 在平稳反应阶段抑氢效果更稳定.将9 种不同浓度配比下SA 及SS 复配作用后的产氢曲线绘于图4.由图可知,当3 g/L SA 和2 g/L SS 复配时,抑氢效果最好且最稳定.
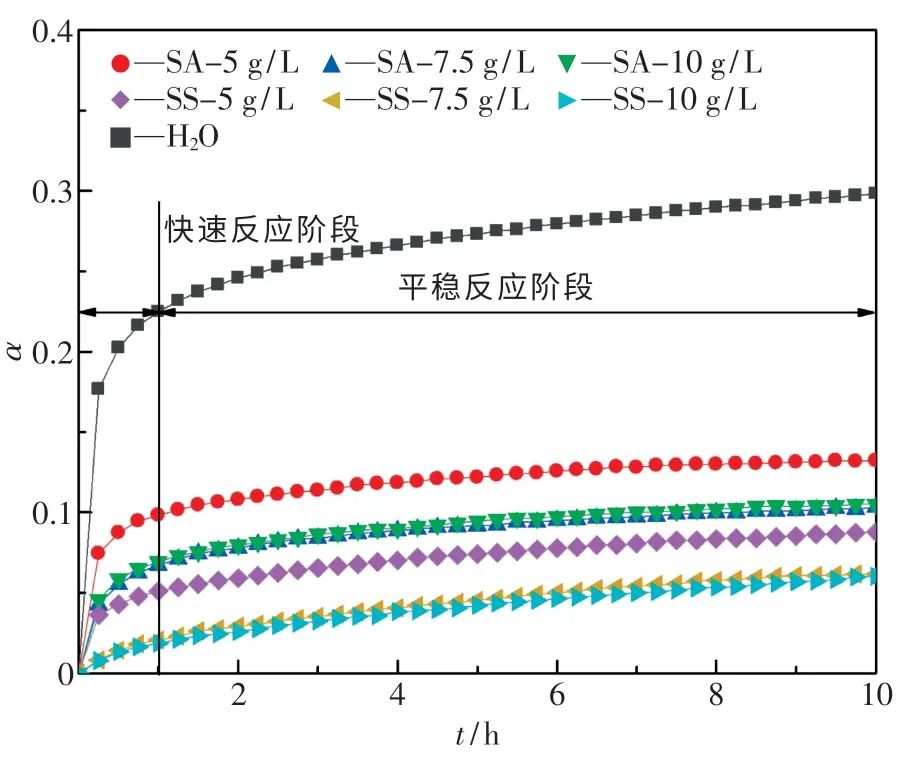
图3 单一抑制剂作用下的产氢曲线Fig.3 Hydrogen evolution curve with single inhibitor
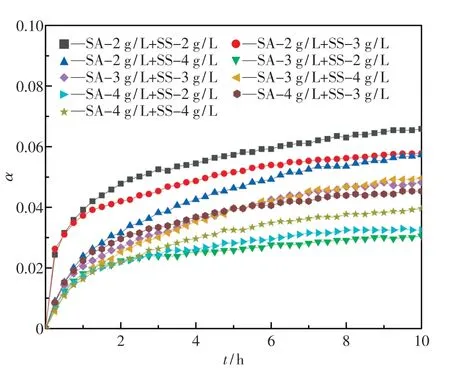
图4 复配抑制剂作用下的产氢曲线Fig.4 Hydrogen evolution curve with compound inhibitor
图5 为SA 及SS 单一作用时最佳浓度下的产氢曲线与二者最佳复配作用下的产氢曲线对比图.由图可知,3 g/L SA 和2 g/L SS 复配可协同抑制Mg-Zn 合金粉尘与水的产氢反应,不仅改善了SA 快速反应阶段作用的滞后性,也降低了SS 平稳反应阶段作用的不稳定性,优化了抑制效果.
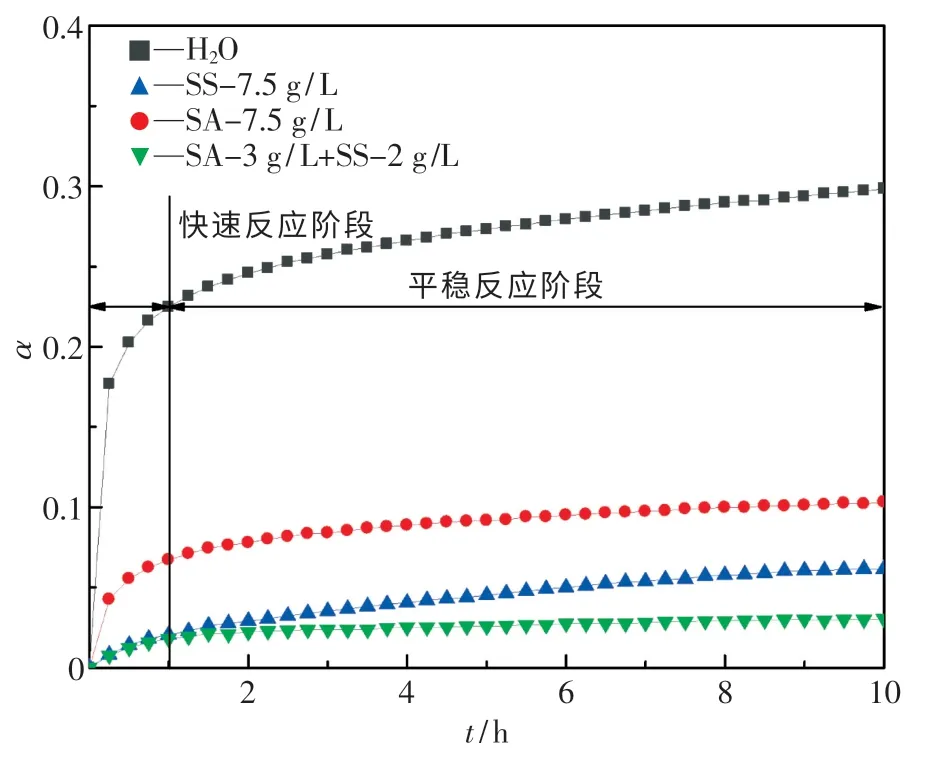
图5 单一及复配抑制剂作用下的产氢曲线对比Fig.5 Comparison of hydrogen evolution curves between single inhibitor and compound inhibitor
2.2 化学动力学分析
金属粉尘与水反应的化学动力学模型符合收缩核模型的特征,可对其进行化学动力学分析.将产氢速率α 和反应速率常数k 的关系用公式(2)表示[7]:
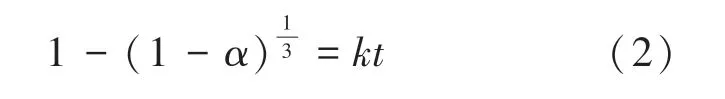
式中:t 为时间,h;k 为反应速率常数,h-1.
经计算,当3 g/L SA 和2 g/L SS 复合作用时,k 值最低,为2.771 98×10-4h-1,几乎为0;此时的复配抑制剂对Mg-Zn 合金粉尘与水产氢反应的抑制效果最好,这与图4 相符.
2.3 SEM-EDS 分析
对Mg-Zn 合金粉尘颗粒及各反应产物进行SEM 表征,如图6 所示(其中右侧小图为SEM 图的局部细节图).图6(a)显示Mg-Zn 合金粉尘颗粒反应前表面光滑;图6(b)显示Mg-Zn 合金粉尘颗粒与水反应后表面粗糙,呈花瓣状.有研究结果表明[14],镁合金与水接触会发生产氢反应,生成Mg(OH)2,如化学式(3)~(5)所示.Mg(OH)2作为保护膜在一定程度上阻止了合金被腐蚀,但其多孔且易破裂,对镁合金基体的保护作用有限,水分子也会穿过Mg(OH)2膜进一步腐蚀合金.同时,溶液中的Cl-也会穿过孔隙使镁合金持续发生点蚀,造成溶液中有少量MgCl2存在,如化学式(6)所示.因此,Mg-Zn 合金粉尘与水反应后的产氢量在初期激增后出现缓慢增长.


图6(c)为最佳复配抑制剂(3 g/L SA+2 g/L SS)复合作用后反应产物的形貌图.由图可知,反应产物表面光滑无裂缝,说明此抑制剂可有效阻断Mg-Zn 合金粉尘与水的产氢反应.对Mg-Zn 合金粉尘与水、最佳复配抑制剂的反应产物分别进行EDS 分析,Mg 和O 的质量分数如表1 所列.Mg-Zn 合金粉尘与水反应后,Mg 的质量分数由94.79%下降至58.33%,O 的质量分数高达36.63%.当SA 和SS 复合作用后,O 的质量分数下降到10.02%,Mg 的质量分数达到84.18%.该结果表明SA 和SS 复合作用下形成的致密保护膜已将Mg-Zn 合金基体保护完好,换言之,即复配抑制剂有效抑制了Mg-Zn 合金粉尘与水的产氢反应.

图6 Mg-Zn 合金粉尘颗粒反应前后及局部细节的SEM 图Fig.6 SEM images of particles and local details of Mg-Zn alloy dust before and after reaction

表1 EDS 结果(质量分数)Table 1 EDS results(mass fraction) %
2.4 FTIR 分析
SA 是一种天然多糖, 分子式为(C6H7O6Na)n,含有大量羧基(—COOH)和羟基(—OH),分子结构如图7 所示.图8 为SA 本身、SA 单一作用后,以及SA 和SS 复配作用后产物的FTIR 图.如图8 所示:SA 本身的红外光谱在1 417和1 609 cm-1处的吸收峰分别对应—COOH 的对称和不对称伸缩, 在3 438 cm-1处的宽带及1 093 cm-1处的吸收峰表征了—OH 的伸缩振动,在1 300 cm-1处的吸收峰为—OH 的可变角振动;在2 932 cm-1处的吸收峰是C—H 键的伸缩振动;糖苷键(1→4 键)吸收峰位于1 029 cm-1[15].
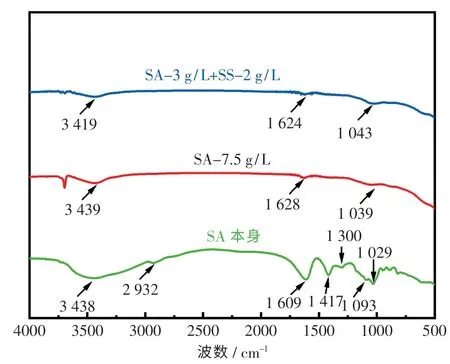
图8 SA 及各抑制剂作用产物的FTIR 图Fig.8 FTIR diagrams of SA and inhibitor action products
SA 单一作用后产物的FTIR 图显示,—COOH在1 609 cm-1处不对称伸缩的吸收峰发生偏移,向低频移动,而在1 417 cm-1处对称伸缩的吸收峰消失,说明SA 的—COOH 与Mg2+发生配位作用.—OH 在1 093 cm-1处的吸收峰消失,在3 438 cm-1处的吸收峰变窄且向低频移动,说明SA 中仅部分羟基参与配位,降低了O—H 的键能.1 300 cm-1处大分子六元环上O—H 键的吸收峰消失是因为生成的金属螯合物的环状结构限制了O—H 键的弯曲振动.—CO 在1 029 cm-1处的吸收峰变宽且向低频移动( 从1 029 到1 039 cm-1),说明部分糖苷键中的—O—C 键参与配位.2 932 cm-1处大分子六元环上C—H 键伸缩振动的吸收峰(是糖类的特征峰)在SA 分子中吸收能力较强,而在反应后的产物的红外光谱中该吸收峰难以观察到.这是因为SA 本身具有能够与金属阳离子结合的交联特性,Mg2+与SA 的多齿配体所生成的螯合物限制了六元环上C—H 键的伸缩振动,螯合物所具有的环状结构使C—H键偶极矩变化较小,所以未能观察到吸收峰.
根据软硬酸碱原理[16],Mg2+属于硬酸,有较高的正电荷,SA 属于硬碱,羧基、羟基等配合官能团中的O 配位原子电负性大,可与硬酸生成稳定配合物.有研究结果表明[17],Mg2+有6 个配位点可与SA 生成比单齿化合物更为稳定的六齿螯合物.SA 中大量的羟基、羧基及糖苷键与Mg-Zn 合金粉尘颗粒表面的Mg2+、反应产物[Mg(OH)2]生成螯合物离子,使氧化膜Mg(OH)2脱附,从而生成SA 的螯合物[SA-Mg].这种特征性螯合交联被称为“卵盒连接”[17].Mg2+半径小于Ca2+,说明Mg2+可以进入蛋盒结构中形成近似海藻酸钙的结构,如图9 所示.
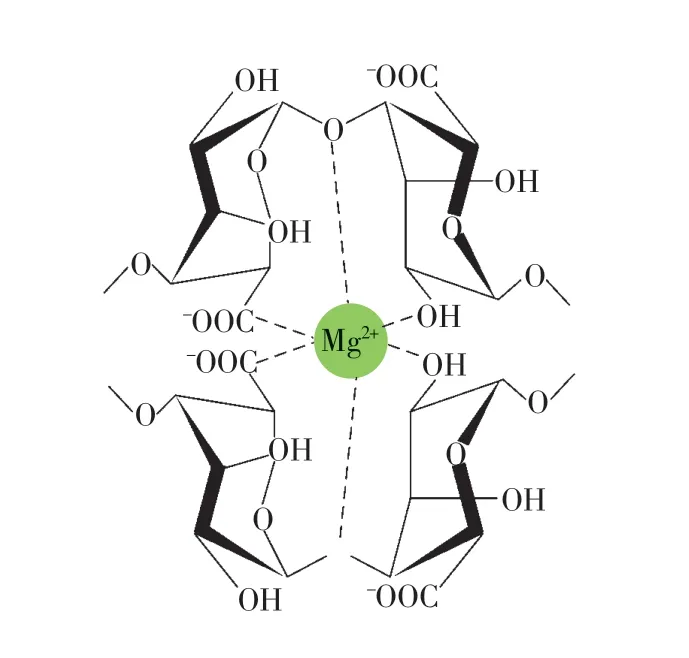
图9 六齿螯合物[SA-Mg]的结构示意图Fig.9 The structure of the hexagon chelate [SA-Mg]
综上所述,SA 抑氢的机理是通过SA 和Mg2+的螯合作用,在Mg-Zn 合金粉尘颗粒表面形成保护膜,防止Mg-Zn 合金粉尘与水接触,从而抑制产氢反应.Mg2+与SA 的螯合作用如下:
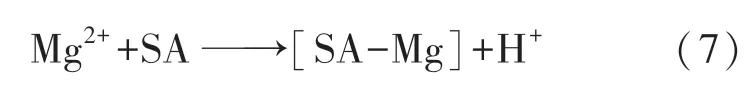
然而,SA 分子链较长、体积较大,易发生缠绕,不能作用于Mg-Zn 合金粉尘颗粒表面所有的活性位.这就导致表面膜内形成许多缺陷,表面有缝隙(即未作用到的活性位),反应生成的产物不能完全覆盖在Mg-Zn 合金粉尘颗粒表面,不能完全抑氢,仍有氢气集聚的可能,进而有氢气爆炸的风险.
2.5 XRD 分析
对Mg-Zn 合金粉尘三种不同反应条件下的产物进行XRD 分析,如图10 所示.Mg-Zn 合金粉尘中含有Mg 基体和第二相合金相MgZn2.与水反应后,产物主要为Mg(OH)2,第二相合金相MgZn2并未参与任何化学反应.复配抑制剂作用后,Mg 的衍射峰非常高,表明产物中存在大量Mg,这说明Mg-Zn 合金基体被生成的保护膜(即水合硅酸镁)很好地保护着.

图10 SS 单一作用、复配抑制剂作用后产物的XRD 图Fig.10 XRD diagrams of the products after the reaction of single and complex inhibitors
根据图10 中复配抑制剂作用后的XRD 分析结果可知:加入SS 后,SS 水解出的Si—OH 基团与Mg-Zn 合金粉尘颗粒表面的Mg—OH 基团进行脱水反应,生成稳定的Si—O—Mg 键;同时,分子间的Si—OH 基团缩合成Si—O—Si 键,在Mg-Zn 合金粉尘颗粒表面生成水合硅酸镁(3MgO·2SiO2·2H2O).但水合硅酸镁的衍射峰非常弱,这是因为Mg-Zn 合金粉尘与SS 之间的反应生成的水合硅酸镁非常少,覆盖在SA 单一作用下Mg-Zn合金粉尘颗粒表面未被覆盖的活性点上,二者产生协同抑氢的效果,使Mg-Zn 合金粉尘与水之间的反应进一步受到抑制,这与图3 相符.SS 的作用如下所示:
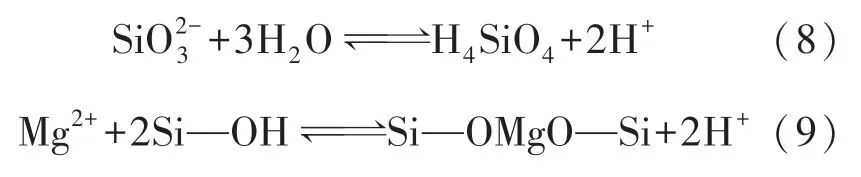
3 吸附模型
有研究结果表明[7],抑制剂在金属表面上的作用可以用Langmuir 吸附等温线来解释,如下所示:
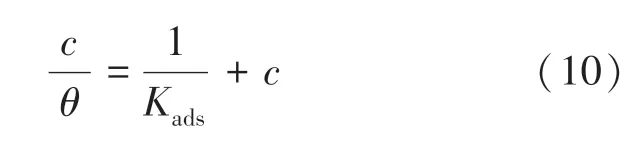
式中:c 为抑制剂的质量浓度,g/L;Kads为吸附热力学常数,L/g;θ 为表面覆盖率.
图11 为SA 和SS 的Langmuir 吸附等温线图.SA 和SS 的相关系数分别为0.999 41和0.998 56,均接近1,表明SA 和SS 在Mg-Zn 合金粉尘颗粒表面的作用机理符合Langmuir 吸附模型.
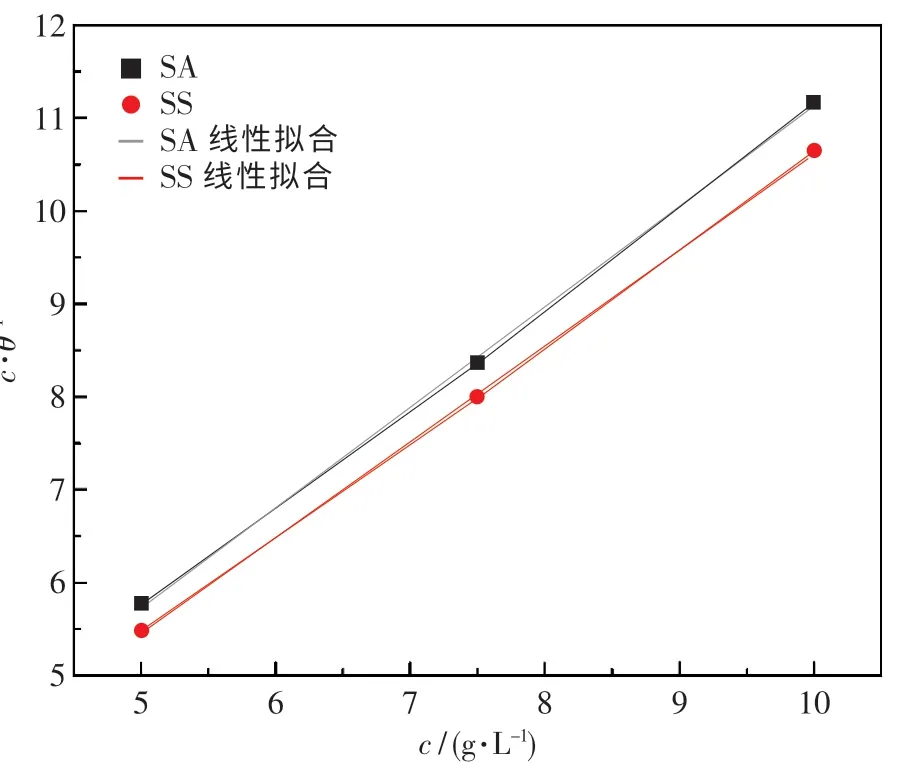
图11 Langmuir 吸附等温线Fig.11 The Langmuir adsorption isotherm curve
标准吉布斯自由能可反应SA 和SS 在Mg-Zn合金粉尘颗粒表面发生的吸附类型,如下所示:

式中:55.5 为溶剂水的浓度,mol/L.
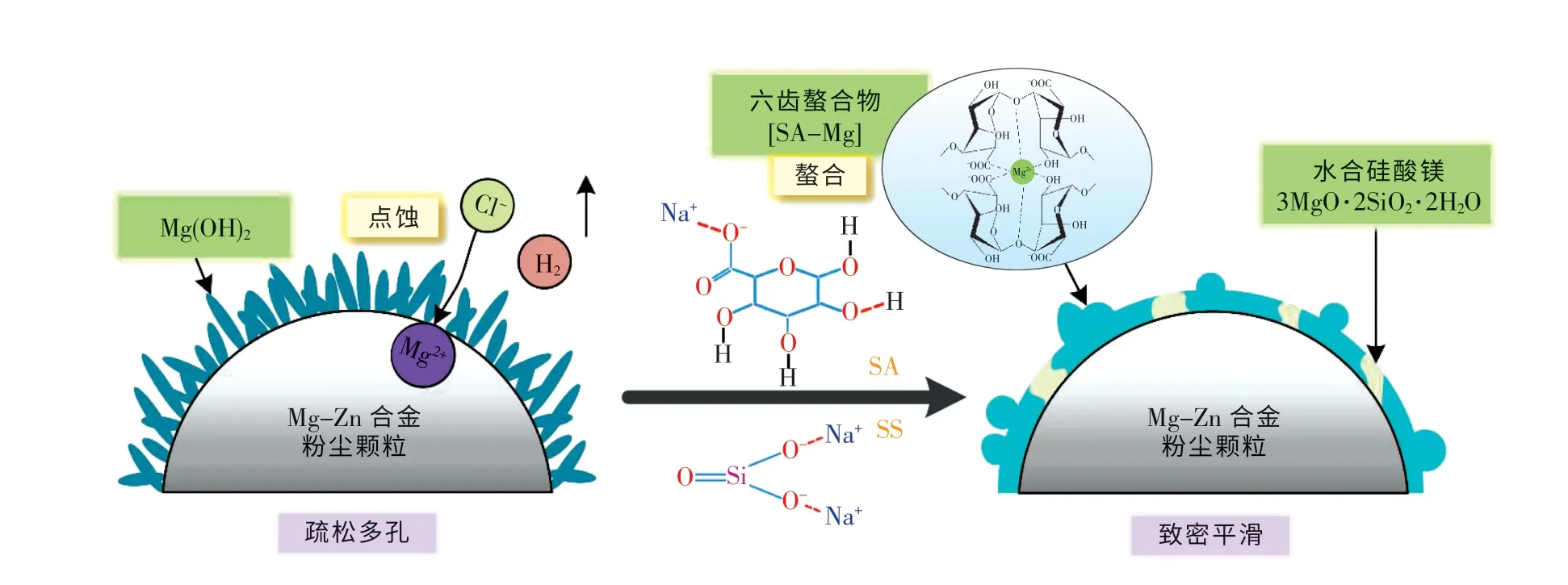
图12 SA 和SS 协同抑制Mg-Zn 合金粉尘与水产氢的作用原理Fig.12 The schematic of SA and SS synergistically inhibiting the hydrogen production of Mg-Zn alloy dust particles and water
4 结 论
(1)SS 在Mg-Zn 合金粉尘与水反应的快速反应阶段作用效果更好,能够快速抑氢;SA 则在Mg-Zn 合金粉尘与水反应的平稳反应阶段作用更好,能够稳定抑氢.
(2)3 g/L SA 和2 g/L SS 复配是最佳抑制剂.二者协同作用可改善SA 快速反应阶段的滞后性以及SS 平稳反应阶段的不稳定性,彻底抑制Mg-Zn 合金粉尘和水的产氢反应,降低湿式除尘系统中遇水产氢导致的氢气爆炸风险,有效提升Mg-Zn合金加工车间湿式除尘系统的本质安全.
(3)SA 和Mg2+反应生成稳定的六齿螯合物[SA-Mg],SS 和Mg2+反应生成水合硅酸镁,二者共同在Mg-Zn 合金粉尘颗粒表面形成致密光滑的保护膜,阻断合金粉尘与水的反应途径,从而实现抑氢,为提高湿式除尘系统的本质安全设计提供一种新的方法.
