海藻酸钙﹣羟基磷灰石复合材料制备及其对Pb2+的吸附性能
2022-11-25吴汉福
田 玲 吴汉福 喻 贵
(六盘水师范学院化学与材料工程学院,贵州 六盘水 553004)
Pb2+是工业废水中的一种毒性高且难以去除的污染物之一[1,2],已被原国家环保部列为五种水体中优先控制排放的重金属污染物,工业污染物排放标准(GB25466—2010)规定Pb2+的排放浓度为0.5 mg·L-1。如果Pb2+排放到环境,人体可以通过食物链摄入积累而引起贫血、头晕、高血压和肾脏疾病等[3-6]。因此,含Pb2+废水在排放之前必须进行有效处理达标排放[7]。
目前,含Pb2+废水处理的方法主要有沉淀法、交换法、吸附法等[7-10],其中吸附法因为方法简单、去除率高、成本低等优点而被广泛运用。工业上常使用的吸附剂有活性炭、硅胶、沸石、分子筛、活性氧化铝等,但这些都普遍存在吸附能力较弱、吸附分离困难等的问题,所以研究开发具有优异性能的吸附剂是吸附法的重点。羟基磷灰石(HAP)被证明是一种优良新型环境友好功能材料,对大多数重金属离子具有良好的吸附固定作用,并且不会造成二次污染。但是单一组分的羟基磷灰石存在易聚团而造成吸附能力下降,固液分离能力差等问题。海藻酸钠是从海带或海藻中提取的一种天然多糖类化合物,其分子链上含有大量的羟基、羧基,可以通过配位、离子交换等吸附重金属离子,还可以与二价金属离子交联形成三维网络的水凝胶[11]。这种三维网络结构不仅可以很好地固定颗粒吸附剂,又可以提高吸附性能。因此,海藻酸钠被广泛运用于包裹碳纳米管、活性炭、二氧化硅等颗粒材料。利用海藻酸钙包覆生物炭制备复合材料吸附污染物已有相关报道[12],但是海藻酸钙固定羟基磷灰石复合材料吸附污染物研究报道较少。
本文通过超声共沉淀法合成羟基磷灰石,进而制备海藻酸钙包覆羟基磷灰石制备复合材料,考察海藻酸钙﹣羟基磷灰石复合材料对Pb2+的吸附性能,该研究可为开发含Pb2+废水处理新型环境友好功能材料提供参考。
1 实验
1.1 主要试剂
CaCl2、Na2HPO4·12H2O、葡萄糖、海藻酸钠(分析纯,天津市科密欧化学试剂有限公司),硝酸铅、HCl、NaOH、无水乙醇(分析纯,国药集团化学试剂有限公司)。
1.2 主要仪器
AA800型原子吸收分光光度计(美国PE公司),JSM-5900LV型扫描电子显微镜(日本电子株式会社),ZWYR-2102C恒温培养振荡器(上海智城分析仪器有限公司),Bruker D8 X射线粉末衍射仪(德国Bruker AXS公司),PHSJ-3C pH计(上海雷磁仪器有限公司),Nicolet-5700傅里叶变换红外光谱仪(美国热电公司),Autosorb-iQ-3 型 BET 比表面全自动物理吸附分析仪 (美国康塔仪器公司),ZNCLG磁力搅拌加热器(巩义市予华仪器有限公司),DHG-914TA电热恒温鼓风干燥箱(上海索域实验设备),KQ-250E 台式超声波清洗器(上海仪天科学仪器有限公司)。
1.3 复合材料(SA/HAP)的制备
1.3.1 羟基磷灰石制备
分别配制一定浓度的CaCl2溶液和Na2HPO4溶液,取200 mL 0.2 g/mL葡萄糖溶液,并将pH值调为11,超声下将CaCl2溶液和Na2HPO4溶液缓慢滴入葡萄糖溶液中(Ca与P摩尔比为1.67),滴加完成后持续超声40 min,陈化12 h、过滤、用蒸馏水和无水乙醇分别清洗3次,在80℃干燥4h,研磨得到HAP备用。
1.3.2 复合材料(SA/HAP) 制备
称取15g羟基磷灰石(HAP)加入到200 mL 海藻酸钠溶液(质量浓度分别为0.5%、1%、1.5%、2%、3%)中持续超声40 min,然后剧烈搅拌30 min形成均匀混合乳状液,然后用注射器缓慢将混合乳状液滴加到5% CaCl2溶液中,交联固化4h,过滤、用超纯水和无水乙醇反复冲洗数次,85℃下干燥4h,得复合材料(SA/HAP-0.5、SA/HAP-1、SA/HAP-1.5、SA/HAP-2、SA/HAP-3)。
1.4 吸附实验
在转速为150 r/min,采用单因素实验分别考察吸附剂SA/HAP的投加量(0.4~2 g/L)、pH(2.0~6.0)、吸附时间(0~90 min)、Pb2+初始浓度(1000~1500 mg/L)、温度(303.15~313.15 K)对 Pb2+的吸附影响。实验中Pb2+浓度采用原子吸收光谱法测定,将实验结果进行吸附动力学、等温、热力学模型的拟合。所有实验数据均为3次平行实验取平均值。
平衡时吸附量用式(1)计算,去除率用式(2)计算。
(1)
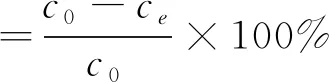
(2)
式中:c0—初始浓度,mg/L;ce—平衡浓度,mg/L;V—溶液体积,L;m—吸附剂量,g。
1.5 吸附再生实验
303.15 K下,将Pb2+溶液与SA/HAP-1.5材料进行饱和吸附,吸附完成后,固液分离回收集SA/HAP-1.5材料,用1 mol/L盐酸溶液浸泡5h进行脱附,然后用蒸馏水洗至中性烘干,连续进行4次吸附解析试验,分别计算每次解吸后复合材料的吸附量。
2 结果与讨论
2.1 对Pb2+吸附材料(SA/HAP)优选
在不调pH情况下,Pb2+溶液为50 mL、初始质量浓度为1000 mg/L,各SA/HAP复合材料均为0.1g,温度为30 ℃,吸附时间70 min,各复合材料对Pb2+吸附效果见图1。
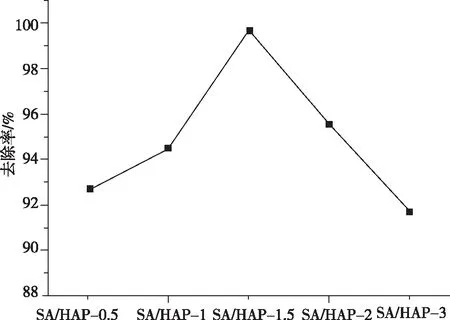
图1不同SA/HAP复合材料对Pb2+吸附效果
由图1可知,随着海藻酸钠浓度的增加,复合材料对Pb2+的去除率增加,当海藻酸钠浓度为1.5%,去除率达最高,为99.7%;随后,继续增加海藻酸钠浓度,去除率下降。造成海藻酸钠浓度低、去除率低的原因可能是因为海藻酸钠不能包裹住全部的HAP粉末,致使部分HAP粉末在制备微球的过程中流失,未能充分利用。而高浓度海藻酸钠制备的复合材料吸附率降低原因可能是海藻酸钠浓度高,造成制备的微球表面致密,孔容较小。因此,后续实验选择SA/HAP-1.5作为吸附剂研究吸附Pb2+的性能。
2.2 材料的XRD、FTIR、SEM、EDS和BET表征
2.2.1 HAP和SA/HAP-1.5的XRD和FTIR分析
HAP和SA/HAP-1.5的XRD和FTIR图见图2。
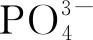

图2 HAP和SA/HAP-1.5的XRD(a)和FTIR(b)谱图
2.2.2 HAP和SA/HAP-1.5的SEM和DES分析
HAP和SA/HAP-1.5的SEM和DES图见图3。
由图3a可知,羟基磷灰石(HAP)为不规则的颗粒物,粒径较小,团聚现象较为严重;与HAP相比,图3b可看出,复合材料(SA/HAP-1.5)颗粒较大,表面较粗糙,表面粗糙有利于吸附。如图3c和3d所示,羟基磷灰石(3c)与复合材料(3d)能谱图在0.52、2.01和3.69keV的吸收峰为O、P、Ca元素的吸收峰,复合材料在0.26keV处还有C元素的吸收峰,这是海藻酸钙中的C元素。
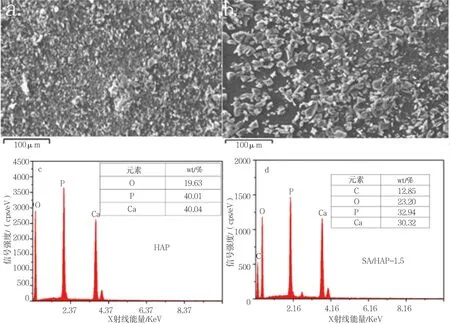
图3 HAP(a)和SA/HAP-1.5 (b)的SEM图以及HAP(c)和SA/HAP-1.5(d)的EDS
2.2.3 BET分析
SA/HAP-1.5的N2吸脱附等温线和BJH孔径分布对应于图4。从图4可以看出,SA/HAP-1.5的吸附等温线属于IUPAC分类中的IV型等温线。在相对压力为0~1.0范围内,根据介孔回滞环的类型,判断为H3型回滞环,说明SA/HAP-1.5材料是典型的介孔材料。从SA/HAP-1.5的孔径分布图可知,其孔径主要分布在1.4~15.5 nm 范围内。根据BET测试结果得到,SA/HAP-1.5吸附剂的比表面积为256.4 m2/g,孔容为0.41 cm3/g。
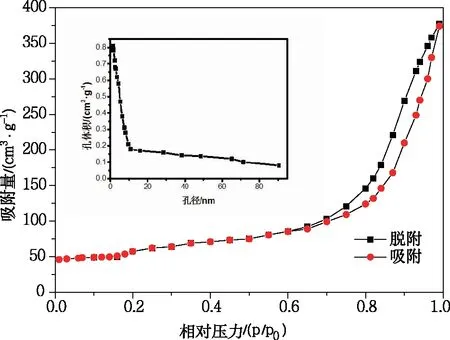
图4 N2吸脱附等温线和BJH孔径分布图
2.3 溶液pH和SA/HAP-1.5复合材料的投加量对Pb2+的吸附影响

在Pb2+溶液为50 mL、初始质量浓度为1000 mg/L,pH为6,温度为30 ℃,吸附时间70 min,SA/HAP-1.5对Pb2+吸附影响见图5b。随着投加量的增加,去除率也明显增加,当投加量达到2 g/L时,去除率达99.7%,此后增加SA/HAP-1.5的投加量,去除率几乎不变。因此,在后续实验过程中,选择最佳吸附pH为6,投加量为2 g/L。
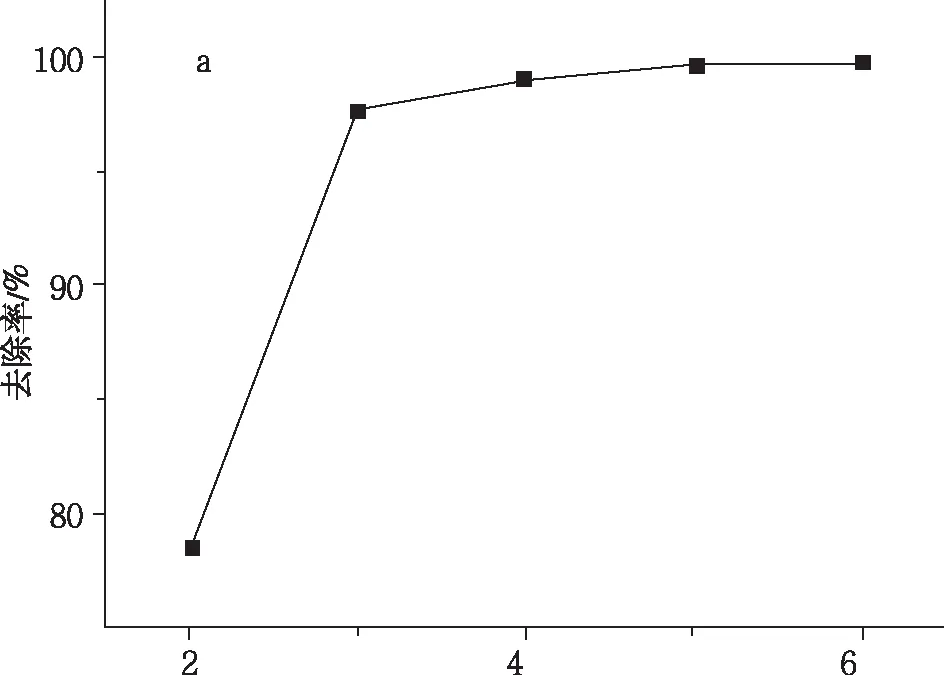
溶液pH
2.4 SA/HAP-1.5复合材料接触时间对Pb2+吸附的影响
图6为接触时间对Pb2+吸附的影响情况。由图可知,开始复合材料对Pb2+的吸附速度较快,30 min内对Pb2+去除率可达90%。在接触时间为60 min时,吸附基本达到平衡。由于在吸附开始时,吸附位点较多,Pb2+迅速占据吸附位点,随着吸附时间的延长,吸附位点逐渐减少。复合材料对Pb2+的吸附过程可分为吸附快速期和吸附慢速期,前30 min为吸附快速期,30 min后为吸附慢速期,直到达到吸附平衡。

图6 接触时间对Pb2+吸附的影响
2.5 吸附动力学模型、等温模型和热力学模型
2.5.1 吸附动力学模型
在30℃(303.15K)下,溶液pH为6,SA/HAP-1.5投加量为2 g/L,考察吸附时间对Pb2+吸附影响,采用准一级动力学模型(3)式,准二级动力学模型(4)式和粒子内扩散模型(5)式对实验数据拟合,拟合结果见图7,拟合参数结果见表1和表2。
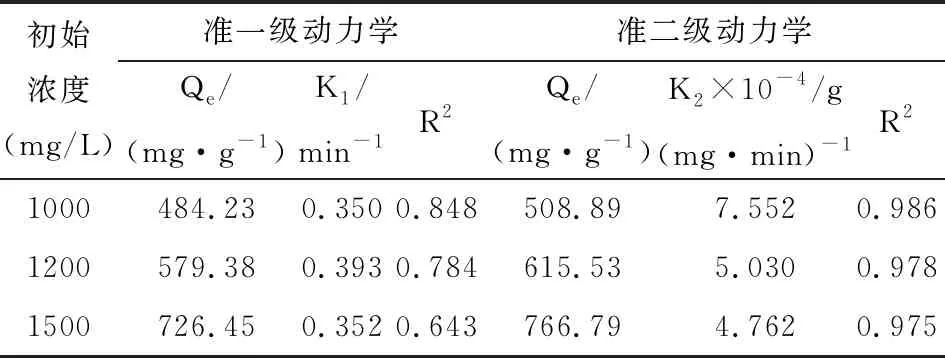
表1 不同浓度下复合材料吸附Pb2+的动力学拟合参数

表2 复合材料吸附Pb2+子内扩散模型拟合参数
准一级动力学模型:Qt=Qe(1-e-k1t)
(3)
(4)
(5)
式中:Qt为t时刻的吸附量,mg/g;Qe为吸附平衡时的吸附量,mg/g;k1为速率常数,min-1;k2为速率常数,g·mg-1·min-1;kp为速率常数,g·mg-1·min-1/2;C为与边界层有关的常数。
由图7a可见,SA/HAP-1.5对不同初始浓Pb2+的吸附在60 min前随着吸附时间增加,吸附量增大;60 min后,吸附量基本不变,趋于平衡状态,吸附量最大,表明60 min达到了吸附平衡。由表1可知,准二级动力学模型(R2=0.975~0.986)较准一级模型(R2=0.643~0.848)能更好描述SA/HAP-1.5对Pb2+的吸附行为,拟合曲线的Qe值与实验值较为接近,吸附过程主要是化学吸附。
颗粒内扩散模型通常用来判断是否为吸附速率控制步骤。由图7b可见,SA/HAP-1.5对Pb2+吸附分为2个阶段,斜率较大的部分为第1阶段-粒子膜扩散;斜率较小的部分为第2阶段-粒子内扩散。由表2可知,第1阶段各初始浓度吸附速率kp分别为28.32、34.6、34.85,Pb2+通过溶液扩散进入吸附剂表面的过程;第2阶段各初始浓度吸附速率kp分别为2.92、6.79、5.66,Pb2+通过吸附剂表面的微孔进入吸附剂内部进行扩散的过程,相应的吸附速率kp都是第1阶段大于第2阶段。因此表明SA/HAP-1.5对Pb2+吸附量主要发生在吸附的初始阶段,当接近吸附平衡后,才由粒子内扩散控制吸附速率,即第2阶段为控速步骤。同时拟合曲线未过原点,说明粒子内扩散并不是唯一控制吸附速率的步骤。

(a)准一级动力学模型和准二级动力学模型
2.5.2 吸附等温模型
在溶液pH为6,SA/HAP-1.5投加量为2 g/L,考察温度对Pb2+吸附影响,采用Langmuir等温模型(6)式,Freundlich等温模型(7)式对实验数据拟合,拟合结果见图8,拟合参数结果见表3。

图8 复合材料吸附Pb2+吸附等温线
(6)
(7)
式中:Qm为吸附剂最大吸附量(mg/g);kL为Langmuir常数(L.mg-1);kF为表征吸附能力的常数(L/g-1);n是表征吸附趋势大小的常数。
由图8可见,随着温度升高,吸附量越大,这说明升高温度有利于吸附反应的进行。由表3可知,Langmuir模型 (R2=0.995~0.997) 较 Freundlich模型(R2=0.925~0.943) 更能描述SA/HAP-1.5对Pb2+的吸附行为,说明吸附主要为单分子层均匀吸附。在Freundlich模型中,1/n代表吸附强度,通常 1/n数值越小,说明吸附能力越强[13],当 0.1<1/n<1 时,表明吸附反应容易发生。在实验温度条件下, 1/n的值分别为 0.10、0.11、0.13。这说明温度升高有利于SA/HAP-1.5对Pb2+的吸附。

表3 复合材料吸附Pb2+吸附等温线参数
2.6 吸附热力学
为了进一步研究温度对SA/HAP-1.5吸附 Pb2+的影响,采用 (8)式和(9)式对吸附等温模型数据进行热力学拟合,结果如表4所示。
ΔG=-RTlnK
(8)
(9)
式中:ΔG为吸附吉布斯自由能,kJ·mol-1;ΔH为吸附焓变,kJ·mol-1;ΔS为吸附熵变,J·mol-1·k-1;R—气体常数,8.314J·mol-1·k-1;T为热力学温度,K;K为吸附平衡常数。
K可通过ln(Qe/Ce)对Ce作图得到,CA/HAP-1.5对Pb2+的吸附热力学参数如表4。
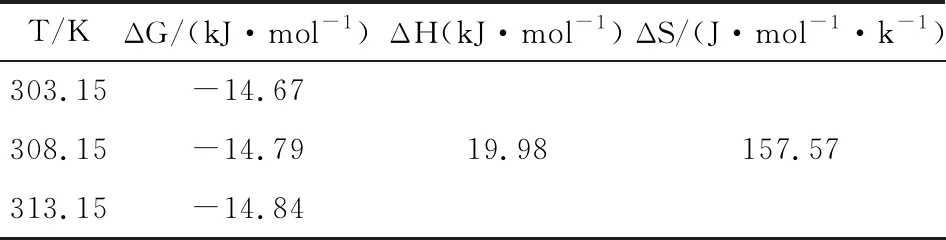
表4 复合材料吸附Pb2+吸附热力学参数
由表4看出,ΔH>0,说明吸附过程是吸热过程,这与吸附等温实验结果一致。ΔS>0,温度增加,说明吸附过程中体系混乱度也增大。当温度增加,ΔG变小,且ΔG<0,表明吸附过程是一个自发的过程。
2.7 吸附再生性能
再生性能见图9。由图9可知,随着再生次数增加,吸附量有所下降。当使用第5次,Pb2+吸附量为450.23 mg/g,吸附量下降率仅为11.5%,说明SA/HAP-1.5具有较好的重复使用性和再生性能。

图9 SA/HAP-1.5的再生性能
3 结论
首先用超声共沉淀法制备了羟基磷灰石(HAP),然后用海藻酸钙固定羟基磷灰石制得吸附剂(SA/HAP-1.5),SA/HAP-1.5吸附剂对Pb2+具有优良的吸附性能。当Pb2+初始质量浓度分别为1000 mg/L、1200 mg/L、1500 mg/L,pH=6.0,SA/HAP-1.5投加量为2 g/L时,吸附量分别为508.89 mg/g、615.53 mg/g、766.79 mg/g。 SA/HAP-1.5对Pb2+的吸附过程符合准二级动力学模型和 Langmuir 等温吸附模型,吸附主要为单分子层的化学吸附,吸附是自发、吸热且熵增过程。SA/HAP-1.5具有良好的再生性能,经过4次再生循环使用,SA/HAP-1.5对Pb2+的吸附量仍可达 450.23 mg/g,吸附量仅下降率11.5%。因此,SA/HAP-1.5复合材料是一种吸附性能和再生性能均优良的吸附剂,可以用于高浓度含Pb2+废水的处理。
