牛肝素脱色工艺研究
2022-11-25刘力波李志敏周银星田志鹏
刘力波,李志敏,周银星,田志鹏
(河北常山生化药业股份有限公司,河北 石家庄 050800)
肝素是一种高度硫酸化的糖胺聚糖,作为抗凝剂和抗血栓药物广泛应用于临床[1]。肝素可以从牛、猪、羊的肠黏膜和牛肺中提取[2]。目前,国际主流市场均使用猪肝素药品,少数国家批准了牛、羊肝素的使用。牛肝素曾是美国食品药品监督管理局最先批准上市的肝素药品,但由于疯牛病的出现,牛肝素退出主流市场[3]。近年来,疯牛病已被有效控制,随着全球对肝素需求的不断增长及穆斯林国家对牛肝素的强烈需求,牛肝素重返市场的呼声不断。
相较于猪肝素,牛肝素存在一定劣势,如效价不到猪肝素的75%[2],颜色更深。由于物质的颜色主要是物质对光选择性吸收的结果[4],肝素的颜色主要与肝素本身的化学结构和残留的有色杂质相关。另外,在放置过程中,肝素的颜色逐渐加深,这是由于,肝素中的氨基化合物和羰基化合物经缩合、聚合发生美拉德反应生成类黑精等褐色物质[5]。因此,选择合适的脱色工艺提升牛肝素产品质量尤为重要。鉴于此,作者将牛源粗品肝素经脱蛋白处理后,分别采用双氧水工艺、过氧乙酸工艺、高锰酸钾工艺等3种氧化工艺精制牛肝素,探讨不同氧化工艺对牛肝素脱色效果和结构的影响,以期筛选出最佳的牛肝素脱色工艺。
1 实验
1.1 材料、试剂与仪器
牛源粗品肝素,Kin Master公司;绵羊血浆,东营博丰生物科技有限公司。
肝素酶,北京艾德豪克国际技术有限公司;肝素钠标准品,欧洲药品质量管理局(EDQM)和美国药典(USP);氘代水、氘代甲醇,Cambridge Isotope Laboratories,Inc.;双氧水、高锰酸钾、过氧乙酸、高氯酸钠、氯化钙、醋酸钙、醋酸铵、氯化钠、磷酸、磷酸钾、氢氧化钠、硼氢化钠、盐酸等,均为国产分析纯试剂。
JJ6000型电子天平,常熟双杰测试仪器厂;AR2140型电子分析天平,美国奥豪斯仪器有限公司;S10-2型恒温磁力搅拌器,上海司乐仪器有限公司;HH-WO型智能数显多功能油水浴锅,巩义予华仪器有限公司;FE28型pH计,METTLER TOLEDO;DZF-6210型真空干燥箱,上海一恒科学仪器有限公司;OS20-S型数显顶置式电子搅拌器,大龙兴创实验仪器(北京)有限公司;AVANCE Ⅲ HD 500MHz型核磁共振波谱仪,德国布鲁克;UV-8000型紫外可见分光光度计,上海元析仪器有限公司;E2695型高效液相色谱仪,美国沃特斯;U3000型高效液相色谱仪,美国赛默飞。
1.2 脱蛋白处理
取适量牛源粗品肝素,按固液比1∶10(g∶mL,下同)加水溶解,加入溶液体积1%的氯化钙,搅拌2 h,升温至90 ℃保持30 min后,降至室温;将溶液用阴离子树脂进行吸附,2%氯化钠溶液洗涤,15%氯化钠溶液洗脱,收集洗脱液,用1 BV(1倍体积)乙醇醇沉,沉淀烘干,即得牛源脱蛋白肝素。
1.3 脱色处理
1.3.1 双氧水工艺
取适量牛源脱蛋白肝素,按固液比1∶10加水溶解,加入3%的30%双氧水溶液,调节pH值至9~10,反应3 h,过滤;滤液中加入5%氯化钠溶液,用3 BV乙醇醇沉,沉淀烘干,即得牛肝素精品。
1.3.2 过氧乙酸工艺
取适量牛源脱蛋白肝素,按固液比1∶10加水溶解,加入6%的15%过氧乙酸溶液,反应3 h,过滤;后续操作同1.3.1。
1.3.3 高锰酸钾工艺
取适量牛源脱蛋白肝素,按固液比1∶10加水溶解,调节pH值至9~10,升温至80 ℃,加入溶液体积0.9%的高锰酸钾,反应3 h;冷却至室温,过滤;后续操作同1.3.1。
1.4 分析方法
1.4.1 脱色率的测定
将牛肝素精品的水溶液进行全波长扫描,发现在400 nm处有一个吸收峰,因此,选择检测波长为400 nm。通过测定样品脱色前后在400 nm处吸光度评价脱色效果,按式(1)计算脱色率:

(1)
1.4.2 效价及回收率的测定
采用羊血浆法测定效价及回收率。精密称量供试品(m)0.1 g,置于100 mL容量瓶中,用0.9%氯化钠溶液溶解,定容即为供试溶液。吸取一定量的供试溶液置于25 mL容量瓶中,用0.9%氯化钠溶液稀释至刻度,使溶液浓度约为8 IU·mL-1。用进样器分别吸取肝素钠标准溶液与供试稀释液,取液量每支试管递增10 μL,各5支试管,分别加入1.0 mL绵羊血浆、0.8 mL 0.25%氯化钙溶液,盖上玻璃塞,摇匀,于(37±1) ℃恒温水浴锅中保温1 h,记录开始保温、中间保温和结束保温时的温度,观察各试管中血浆的凝结程度。根据凝固点按式(2)计算效价,按式(3)计算回收率。

(2)

(3)
1.4.3 双糖的测定
取肝素酶Ⅰ、Ⅱ、Ⅲ,分别加入pH值7.0的磷酸钾缓冲溶液,制成0.4 U·mL-1的肝素酶溶液;按体积比1∶1∶1混合,得到混合肝素酶溶液。取超纯水20 μL,加入pH值7.0的醋酸钙溶液70 μL和混合肝素酶溶液100 μL,混匀,于25 ℃下放置48 h以上,作为空白溶液。
取肝素钠标准溶液、供试溶液适量,加入水,分别制成20 mg·mL-1的溶液;分别取20 μL上述溶液,加入pH 值7.0的醋酸钙溶液70 μL和混合肝素酶溶液100 μL,混匀,于25 ℃下放置48 h以上,即得酶解后溶液。
取空白溶液、酶解后溶液各10 μL,采用SAX-HPLC法测定双糖含量,以标准肝素双糖确定峰位置。
1.4.413CNMR分析
称取样品0.20 g,加入0.2 mL氘代水和0.8 mL水,再加入0.05 mL氘代甲醇,混匀,放入直径为5 mm的核磁管中。设定核磁共振波谱仪工作频率为125 MHz、采集时间为0.55 s、温度为40 ℃,采集13CNMR图谱,采集结束进行数据处理。
2 结果与讨论
2.1 不同氧化工艺的脱色效果
双氧水工艺、过氧乙酸工艺、高锰酸钾工艺的脱色率分别为92.0%、96.0%、95.9%,回收率分别为96.0%、91.3%、95.3%。
双氧水的脱色原理是双氧水在受热或光照条件下快速分解,产生初生态氧[O]而破坏有色物质[6];双氧水的氧化性较过氧乙酸、高锰酸钾的弱,脱色率最低,对肝素结构的破坏性也小,故回收率最高。过氧乙酸的脱色原理和双氧水类似,但反应更为剧烈,过氧乙酸分解可以释放出[O]或过羟基自由基,可有效破坏发色基团,从而破坏有色物质,因此,过氧乙酸工艺的脱色率较高;但由于其对肝素结构的破坏作用也强于另外两种氧化剂,导致回收率最低。高锰酸钾也是一种强氧化剂,通过氧化还原反应,Mn(Ⅶ)可将发色基团氧化,起到脱色作用;高锰酸钾工艺的脱色率和回收率均高于95.0%,对牛肝素的脱色效果最好。
2.2 不同氧化工艺对牛肝素结构的影响(表1)
由表1可知,经双氧水氧化后,牛肝素的双糖分布与氧化前基本一致,说明双氧水对牛肝素结构的影响较小;经过氧乙酸氧化后,ΔGlyser含量显著降低,ΔGlyser ox1含量明显升高,其它结构双糖含量与氧化前差异不大;经高锰酸钾氧化后,ΔGlyser含量显著降低,ΔGlyser ox1和ΔGlyser ox2含量均有一定提高,ΔⅣSgal和ΔⅡSgal含量也有略微提高。这是由于,ΔGlyser存在于几乎所有肝素粗品中的-GlcA β1-3 Gal β1-3 Gal β1-4 Xyl β1-0-Ser序列[7],用于表征牛肝素连接域的丝氨酸,丝氨酸会诱发美拉德反应,影响牛肝素的稳定性,导致牛肝素颜色变深;ΔGlyser经过氧乙酸氧化后形成ΔGlyser ox1结构,经高锰酸钾氧化后形成ΔGlyser ox1和ΔGlyser ox2两种结构。ΔⅣSgal和ΔⅡSgal结构源于-IdoA(2S)-GlcNS(6S)-和-IdoA(2S)-GlcNS-在碱性条件下2-O-脱硫[8],高锰酸钾反应时的高温加速了该反应,导致ΔⅣSgal和ΔⅡSgal含量略微提高。

表1 不同氧化工艺精制的牛肝素的双糖分布Tab.1 Disaccharide distribution of bovine heparin refined by different oxidation processes
ΔGlyser、ΔGlyser ox1和ΔGlyser ox2的结构式见图1。丝氨酸在13CNMR图谱的δ57.4处(图2)。
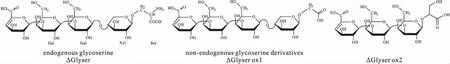
图1 ΔGlyser、ΔGlyser ox1和ΔGlyser ox2的结构式Fig.1 Structural formulas of ΔGlyser,ΔGlyser ox1,and ΔGlyser ox2

图2 不同氧化工艺精制的牛肝素的13CNMR图谱Fig.2 13CNMR spectra of bovine heparin refined by different oxidation processes
ΔGlyser ox1和ΔGlyser ox2两种氧化结构不会诱发美拉德反应,可维持牛肝素的稳定,延缓颜色变深。为了验证该观点,将3种氧化工艺精制的牛肝素制成注射液,在(25±2) ℃、75%±5%湿度条件下进行加速实验,记录400 nm处吸光度(A400)的变化,结果见图3。

图3 牛肝素注射液的颜色随放置时间的变化Fig.3 Color change of bovine heparin injection with storage time
由图3可知,随着放置时间的延长,3种牛肝素注射液的颜色均逐渐变深,但是双氧水工艺精制的牛肝素注射液的颜色变深速度明显快于其它两种氧化工艺,过氧乙酸工艺精制的牛肝素注射液的颜色变深速度略快于高锰酸钾工艺。说明,将牛肝素的ΔGlyser结构氧化为ΔGlyser ox1和ΔGlyser ox2结构,可以延缓牛肝素颜色变深。
3 结论
将牛源粗品肝素经脱蛋白处理后,分别采用双氧水工艺、过氧乙酸工艺、高锰酸钾工艺等3种氧化工艺精制牛肝素,研究了不同氧化工艺对牛肝素脱色效果和结构的影响。结果表明,双氧水工艺、过氧乙酸工艺、高锰酸钾工艺的脱色率分别为92.0%、96.0%、95.9%,回收率分别为96.0%、91.3%、95.3%;经双氧水氧化后,牛肝素的双糖结构变化不大;经过氧乙酸氧化后,ΔGlyser被氧化为ΔGlyser ox1;经高锰酸钾氧化后,ΔGlyser被氧化为ΔGlyser ox1和ΔGlyser ox2;将精制的牛肝素制成注射液后,双氧水工艺牛肝素注射液的颜色变深速度最快,其次依次为过氧乙酸工艺、高锰酸钾工艺。综合评价,高锰酸钾工艺为牛肝素的最佳脱色工艺。
