利用具有过水解活性的乙酰基木聚糖酯酶催化制备过氧乙酸
2020-10-15陶惟一羊亚平
袁 琪,陶惟一,羊亚平,李 霜
(1.南京工业大学 生物与制药工程学院,江苏 南京 211800;2.江苏亚邦强生药业有限公司,江苏 金坛 213100)
过氧乙酸具有强氧化性,是一种广谱、高效、环保型消毒剂,其工作质量浓度为1.0~5.0 g/L[1],但由于其对金属、织物和石材的强烈腐蚀性,限制了过氧乙酸的使用范畴。
传统工业法生产过氧乙酸,是用冰醋酸和高质量浓度H2O2(300 g/L)为底物,以硫酸为催化剂,在常温下反应24~48 h可获得150~200 g/L的过氧乙酸溶液,使用时将其稀释至工作浓度[2]。由于15%~20%的过氧乙酸及其底物中的高浓度H2O2均不稳定,导致过氧乙酸在运输和储存过程中易发生爆炸,安全隐患极大[3]。
近年来,利用生物酶催化乙酸酯的过水解反应来制备过氧乙酸得到了学术界和产业界的广泛关注[4-8]。酶法制备过氧乙酸的优点在于反应迅速、温和,不需要高浓度过H2O2等底物,可以解决运输和储存等问题。而商业化酶催化产生过氧乙酸的浓度较低(0.007~0.07%,质量分数)[9],达不到最低消毒浓度(0.1%)。
笔者所在课题组的田倩倩等[10]发现来源于枯草芽孢杆菌(Bacillussubtilis)CICC 20034的乙酰基木聚糖酯酶(AXE)具有良好的过水解催化活力,游离酶和固定化酶可催化甘油三乙酸酯和H2O2反应,获得浓度高达150 mmol/L的过氧乙酸,但是酶的用量较大。酶制剂AXE是酶法制备过氧乙酸的重要成本之一。因此,本文中,笔者重点探讨降低酶制剂用量,合成更有成本优势的过氧乙酸,并考察酶法制备过氧乙酸的稳定性及金属腐蚀性,以期为后期开发提供基础数据。
1 材料与方法
1.1 材料
出发菌株为大肠杆菌(Escherichiacoli)BL21/pET-CAH[10]。蛋白胨、酵母粉,OXOID公司;NaCl、乳糖、NaHPO4、Na2HPO4、NaOH、甘油三乙酸酯、30%H2O2、戊二醛,国药集团化学试剂有限公司。
ZQQZY-75AN型恒温振荡培养箱,上海知楚仪器有限公司;3-30K型低温高速离心机,Sigma公司;MD190型酶标仪,Molecular Devices公司;AH100B型超高压破碎仪,ATS Engineering 公司;SW-CJ-1CU型生物净化工作台,苏净安泰AIRTECH公司;GI54DWS型灭菌锅,ZEALWAY公司;DHG-907385型恒温鼓风干燥箱,新苗公司;GNP-9160型恒温培养箱,上海精宏实验设备有限公司;BS 124 S型万分之一天平,Sartorius公司;DK-8D型恒温水浴锅,上海精宏实验设备有限公司。
1.2 方法
1.2.1 AXE游离酶的制备
1)种子培养。出发菌株为大肠杆菌(Escherichiacoli)BL21/pET-CAH[11],LB培养基:酵母粉5 g/L、蛋白胨10 g/L、NaCl 10 g/L;培养条件:250 mL的三角瓶,装液量为50 mL,培养温度为37 ℃,摇床转速为200 r/min,培养时间为12 h。
2)发酵培养。培养基组成:酵母粉25 g/L、蛋白胨15 g/L、NaCl 10 g/L、甘油0.1%(体积分数)、葡萄糖2 g/L、乳糖2 g/L。5L发酵罐发酵培养:装液量为3 L,接种量为3.3%(体积分数),发酵温度为30 ℃,搅拌速度为200 r/min,通气量2 vvm,pH 7.0,发酵时间为16 h[9]。
3)粗酶液的提取。将发酵液离心,收集菌泥悬浮于0.1 mol/L的PBS缓冲液(浓缩12倍),采用高压细胞破碎法,压力加至600 Pa以上,破碎菌液,液体变得透明黏稠即破碎完全。将细胞破碎液再次离心去掉细胞碎片杂质,上清液即为游离粗酶液,4 ℃保存。
1.2.2 AXE酶活测定
参照酯酶的酶活测定方法[11],使用对硝基苯酚乙酸酯(p-NPA)为底物,进行酶活测定。1个酶活单位(U)定义:在一定反应条件下,每分钟释放1.0 μmol/L乙酸对硝基苯酚(p-NP)所需的酶量。重组菌E.coliBL21/pET-CAH发酵16 h,浓缩破胞后获得粗酶液的酶活性达3 480 U/mL。
1.2.3 蛋白含量测定
参照文献[12]测定粗酶的蛋白含量。测得浓缩酶的蛋白含量为7.92 mg/mL。
1.2.4 游离酶的固定化
参照文献[9],先将丙烯氨基树脂MI-BS1进行戊二醛活化,然后将蛋白含量为0.1 g的粗酶液加入50 mL 100 mol/L的Tris-HCl 缓冲溶液(pH 7.4),与10 g活化后的树脂混合,在35 ℃下反应6 h,将含有固定化酶的树脂进行过滤干燥备用。经丙烯氨基树脂MI-BS1固定化后,固定化酶的酶活为350 U/g树脂。
1.2.5 AXE酶催化甘油三乙酸酯过水解反应制备过氧乙酸
设置50 mL反应体系,以40 mmol/L的磷酸盐(pH 7.8)为缓冲液,底物H2O2浓度为1.0 mol/L或0.35 mol/L,甘油三乙酸酯浓度分别为0.3 mol/L或0.1 mol/L;先将甘油三乙酸酯和磷酸盐缓冲液振荡均匀,再加入H2O2振荡均匀,最后加入不同量的AXE酶液(游离酶)或固定化酶,室温振荡5 min,迅速加入MnO2终止反应,离心取上清测过氧乙酸含量[13]。
1.2.6 化学催化法制备过氧乙酸
购买市售AB液包装的过氧乙酸产品,其中A液为高浓度冰醋酸和浓硫酸,B液为30%H2O2。使用时按说明书进行1∶ 1体积比混合,25 ℃静置24~48 h。
1.2.7 过氧乙酸含量的测定
过氧乙酸含量的测定参照文献[14]进行。
1.2.8 酶法/化学催化法过氧乙酸稳定性比较
分别用酶法和化学法制备过氧乙酸,用无菌水调整至相同质量浓度(10和3.5 g/L),25 ℃放置一周,每天测过氧乙酸质量浓度[3,15]。
1.2.9 酶法/化学催化法过氧乙酸腐蚀性比较
分别用酶法和化学法制备过氧乙酸,调整过氧乙酸质量浓度至3.5 g/L,浸泡碳钢、不锈钢、铝和铜金属片,每天换液并称4种金属片的质量,连续一周。
2 结果与讨论
2.1 不同反应体系中过氧乙酸含量的测定
2.1.1 游离酶催化三乙酸甘油酯底物制备过氧乙酸
由于底物H2O2具有强氧化性,能导致酶发生变性,破坏酶的活性,常用的医用双氧水消毒剂的工作质量浓度为30 g/L左右,因此设定反应体系中H2O2最高浓度为1 mol/L(34 g/L)。考虑到甘油三乙酸酯的过水解反应需要过量的H2O2,因此,将H2O2和甘油三乙酸酯的摩尔比设为10∶ 3;此时,反应体系中含有65 g/L(0.3 mol/L)甘油三乙酸酯,考察不同游离酶用量对反应的影响,结果如图1所示。
由图1可知:当粗酶的添加量(蛋白质质量浓度)为1.0 g/L时,室温反应5 min即可获得高达11.6 g/L(152 mmol/L)的过氧乙酸,底物甘油三乙酸酯的过水解反应占比为16.7%;进一步增加酶的用量,不能再提高产物过氧乙酸的产量。

图1 高浓度反应体系下AXE用量对过氧乙酸浓度的影响
该反应体系中,底物H2O2为34 g/L,相当于其作为消毒剂使用的工作浓度,是可接受的安全范围;底物甘油三乙酸酯可作为日用化学品定香剂使用,具有微弱果香气味;反应条件温和,反应速度快,仅反应5 min即可达到高于消毒剂使用浓度的过氧乙酸。因此,利用酶法催化过氧乙酸的合成具有安全和快速的特点。
考虑到H2O2对AXE酶的氧化毒性,降低H2O2浓度将有利于酶活性功能的发挥。将反应体系中H2O2降至12 g/L(0.35 mol/L),底物甘油三乙酸酯降至22 g/L(0.1 mol/L),减少AXE游离酶的使用量,结果如图2所示。
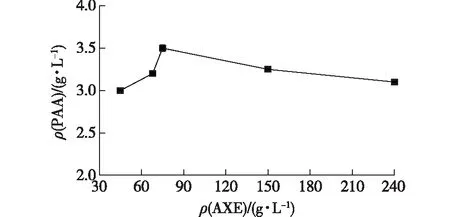
图2 低浓度反应体系下AXE用量对过氧乙酸浓度的影响
由图2可知:当AXE粗酶液的添加量为75 mg/L时,反应5 min产生过氧乙酸质量浓度最高达到3.5 g/L;AXE粗酶液的添加量为45 mg/L时,反应5 min产生的过氧乙酸也可以达到3.0 g/L左右。这一数据表明,在含有低浓度H2O2的反应体系中,AXE酶催化甘油三乙酸酯的过水解反应占比仍能达到15.3%。该反应体系中的过氧乙酸(3.0~3.5 g/L)已满足消毒使用的有效剂量,相比高浓度H2O2的反应体系,达到相同工作质量浓度(3 g/L)的过氧乙酸所需的用酶量可大幅降低近80%,有效节约制备成本。
2.1.2 固定化酶催化甘油三乙酸酯底物制备过氧乙酸
考虑到酶在过氧乙酸制备中占据了较大成本,采用固定化酶催化制备过氧乙酸可进一步降低酶的成本。此前,Tao等[9]采用固定化酶用量为1 g/mL时,可获得浓度达142.5 mmol/L的过氧乙酸(11 g/L),固定化酶重复使用10批次仍可获得95.5 mmol/L过氧乙酸(7.3 g/L)。将反应体系中H2O2和甘油三乙酸酯的质量浓度分别降低到12 g/L(0.35 mol/L)和22 g/L(0.1 mol/L)时,固定化酶用量分别为50和100 mg/mL,结果如图3所示。

图3 固定化酶反应批次
由图3可知:固定化酶用量为100 mg/mL时,过氧乙酸可达到3.9 g/L,固定化酶重复利用5批次时,过氧乙酸产量依然可达2.4 g/L;降低固定化酶使用量到50 mg/mL时,过氧乙酸可达到3.6 g/L,固定化酶重复利用5批次后,过氧乙酸为1.8 g/L。因此,固定化酶用量为50 mg/mL是更为经济的用量。
2.2 酶法制备与市售过氧乙酸的稳定性
将游离酶、固定化酶和化学反应法制备的过氧乙酸溶液质量浓度分别设置为10和3.5 g/L,在室温条件下静置一周,每24 h测一次过氧乙酸的含量,结果如图4和图5所示。
由图4和图5可知:二元反应法制备的过氧乙酸,每天分解约10%~15%;高浓度游离酶制备的过氧乙酸溶液最不稳定,10 g/L过氧乙酸室温放置24 h后浓度降低50%,48 h后过氧乙酸浓度降低75%左右,64 h后过氧乙酸全部分解,可能与溶液中含有高浓度蛋白质有关。过氧乙酸具有强氧化性,使得蛋白质被氧化导致变性失活的同时也导致过氧乙酸自身的不稳定。利用游离酶制备过氧乙酸体系中,10 g/L的过氧乙酸反应体系中酶的用量远大于3.5 g/L的反应体系,使得其稳定性最差;而固定化酶反应体系中,反应结束后固定化酶的树脂被取出,过氧乙酸溶液中仅残留少量游离蛋白质,产物过氧乙酸的稳定性更好。75 mg/L游离酶制备3.5 g/L过氧乙酸,其稳定性得到大幅提升,与固定化酶催化制备的过氧乙酸体系的稳定性基本一致,表明过氧乙酸溶液中蛋白质类有机物是影响溶液稳定的关键因素。
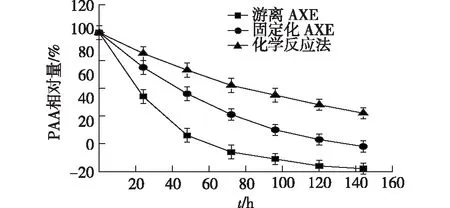
图4 过氧乙酸(10 g/L)稳定性

图5 过氧乙酸的稳定性(3.5 g/L)
2.3 酶法制备和市售过氧乙酸的腐蚀性
将固定化酶制备过氧乙酸和市售过氧乙酸的质量浓度均用无菌水调整至3.5 g/L,测得两种过氧乙酸溶液的pH分别为4.45和1.98,表明市售过氧乙酸中由于含有浓硫酸催化剂,在同等工作浓度下的pH更低。以铜、不锈钢、碳钢和铝片为检测材料,浸泡上述4种金属片,每天换液一次,称质量考察二者对金属材料的腐蚀性,结果如图6所示。
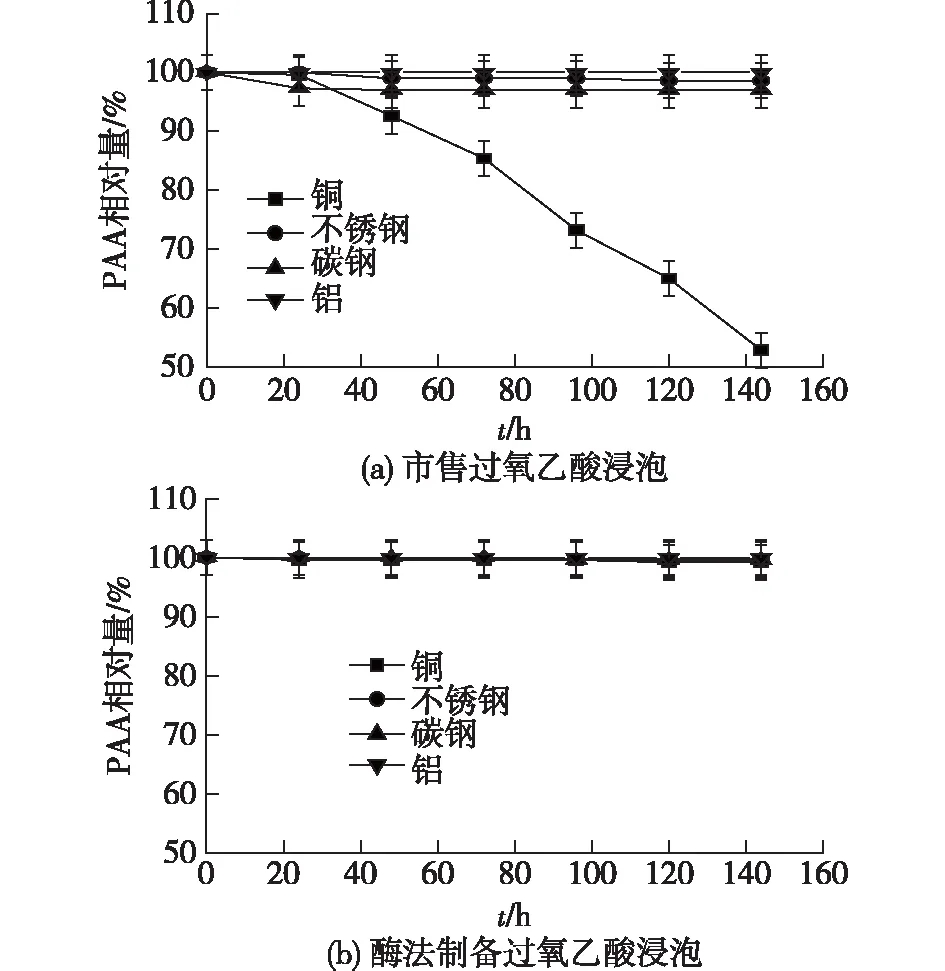
图6 过氧乙酸溶液浸泡4种金属片质量变化
由图6可知:市售的化学法制备过氧乙酸对铜和碳钢的腐蚀性较强,使铜片5 d内质量下降30%,达到重度腐蚀,使碳钢质量下降5%,形成轻度腐蚀;用酶法制备的过氧乙酸对这4种金属基本无腐蚀作用。
图7为过氧乙酸金属浸泡液的结果。由图7可以直观看出,化学法制备的过氧乙酸对金属材料的腐蚀程度远远大于酶法制备的过氧乙酸。

图7 过氧乙酸浸泡四种金属片
3 结论
制备同等总量的低浓度过氧乙酸可大幅节约酶用量且增加了过氧乙酸的稳定性。游离酶和固定化酶的用量分别为75 mg/L和50 g/L时,即可催化22 g/L(0.1 mol/L)甘油三乙酸酯和12 g/L(0.35 mol/L)H2O2发生过水解反应,获得3.5 g/L的过氧乙酸,酶的用量分别降低了80%和90%;该浓度下的过氧乙酸在25 ℃下每天分解率约为20%,同等条件下化学法制备的过氧乙酸每天分解约15%。
酶法制备的过氧乙酸消毒溶液对金属腐蚀性更低。3.5 g/L的酶法制备和市售过氧乙酸,其pH分别为4.45和1.98;该浓度下的市售过氧乙酸溶液对铜达到重度腐蚀,对碳钢形成轻度腐蚀;而该浓度下酶法制备的过氧乙酸均无腐蚀性。
以酶法生产过氧乙酸,能够解决传统生产工艺和运输、储存过程的高危险性问题,并降低金属腐蚀性,拓展应用领域。但由于该方法目前还不成熟,酶制剂的制备成本及稳定性等工艺问题有待进一步深入研究。
