天然气胺法脱碳吸收反应热实验研究
2022-11-16唐建峰姚宝龙刘倩玉花亦怀许义飞
唐建峰, 姚宝龙, 刘倩玉, 花亦怀, 桑 伟, 陈 静, 许义飞
(1.中国石油大学(华东) 储运与建筑工程学院,山东 青岛 266580;2.山东省油气储运安全省级重点实验室,山东 青岛 266580;3.中海石油气电集团有限责任公司 技术研发中心,北京 100027;4.同圆设计集团股份有限公司 青岛分公司,山东 青岛 266580)
胺法脱碳工艺因其高效和经济性成为目前天然气预处理工艺中应用最为普遍的脱碳技术之一[1]。吸收剂的性能优劣直接影响到工艺装置的处理效果,因此开发高性能的醇胺吸收剂对于天然气脱碳工艺的设计与优化至关重要。醇胺溶液吸收CO2后成为富液,在再生塔中进行高温再生,使其中的CO2脱除出来,经过再生处理后的醇胺溶液可以再次利用。有研究指出,工厂运营成本中大约80%用于溶液的再生[2],脱碳溶液的吸收反应热越高,对应的再生能耗也越大。因此测定醇胺溶液的吸收反应热对于高效吸收剂筛选、脱碳工艺及参数优化具有重要意义。
在研究醇胺溶液吸收CO2反应热的初期,学者们以理论研究为主,理论研究多采用吉布斯-亥姆霍兹方程(见式(1))利用相平衡数据对醇胺溶液吸收CO2过程的反应热(ΔHabs)进行计算:
(1)
式中:pCO2为CO2的分压,MPa;R为理想气体常数,8.314 J/(mol·K);T为温度,K;αCO2为CO2负载量,mol CO2/(mol amine)。
采用该方法计算吸收热,其准确性依赖于气-液平衡数据的准确性,当气-液平衡数据的误差达到2%~3%时,该式计算得到的吸收热误差会达到20%~30%[3]。因此采用直接测量法进行吸收反应热的测量有助于丰富胺法脱碳的热力学基础数据,优化胺法脱碳热力学理论模型。Kim等[4]在采用量热仪CPA122测定了不同温度、不同胺液体积分数下CO2在乙醇胺(MEA)溶液中的吸收热和CO2分压(pCO2),讨论了在基于pCO2的实验数据下利用吉布斯-亥姆霍兹方程估算溶液吸收焓的应用。Oscarson等[5]使用自制等温量热仪测定了混合气体CO2/CH4在N-甲基二乙醇胺(MDEA)和二乙醇胺(DEA)溶液中的反应热,发现影响测得热量的最重要因素是温度和气体进料流中CO2分压。Øystein等[6]利用量热仪分别研究了MDEA和N,N-二甲基乙醇胺(DMMEA)水溶液吸收CO2的反应热。实验分别在胺浓度为2、4.2 mol/L以及温度313、353和393 K下进行。研究结果表明,在低负荷和低胺浓度下,温度对反应热的影响更明显。
国内学者也对胺法脱碳工艺中吸收反应热的测量做了大量工作,付鑫等[7]基于能量守恒的原理结合低温水滴定的思路测定氨水吸收CO2的反应热,通过向反应后溶液中滴入0 ℃的蒸馏水使之降温到初始值,计算加入冷却水的量,结合水的比热容确定反应放出的热量,利用该方法对质量分数为12%的氨水溶液吸收CO2的反应热进行了测量,得到的实验结果与理论值的相对误差不超过4%。马嘉慧等[8]利用量热系统测量了MEA溶液吸收CO2的反应热、解吸热以及吸收量,研究了CO2负载、压力、温度等因素对反应热、解吸热及吸收量的影响,并且发现活化剂的添加有效降低了单一MEA溶液的吸收反应热。孟晓峰等[9]采用C80反应热测试仪探究了温度、胺浓度、CO2负载对羟乙基乙二胺(AEEA)溶液吸收反应热的影响规律。
单组分吸收剂各有优点,传统伯胺、仲胺吸收容量大,但再生能耗较高;叔胺再生能耗低,反应速率较慢,无法同时兼具吸收容量高、吸收速率快、再生能耗低等优点,因此混合醇胺溶液逐渐成为国内外高效吸收剂开发的研究热点。个别学者对MDEA+哌嗪(PZ)、MEA+3,3′-二氨基二丙胺(DPTA)、MDEA+DPTA、MDEA+2-氨基-2-甲基-1-丙醇(AMP)、MDEA+六亚甲基二胺(HMDA)、MEA+MDEA以及AEEA+二乙烯三胺(DETA)等二元醇胺溶液在低压下的热力学性质[10-16]进行了实验研究。
目前国内外对于吸收反应热的研究多集中于低压的碳捕集领域,尚未系统探究在高压条件下各影响因素对吸收反应热的影响。笔者针对前期研究吸收性能较好的MDEA、PZ、AMP溶液,采用自主设计的吸收反应热测量系统,探究CO2负载、醇胺种类、总胺质量分数、吸收温度、吸收压力以及加入添加剂后对吸收反应热的影响,掌握各影响因素对吸收反应热的影响规律及原因,为操作参数优化及节能降耗提供依据。
1 实验部分
1.1 原料和试剂
原料气为氮气(N2)和二氧化碳(CO2),纯度均为99.995%,青岛瑞丰气体有限公司产品;N-甲基二乙醇胺(C5H13NO2,MDEA)、哌嗪(C4H10N2,PZ),均为分析纯,上海麦克林生化科技有限公司产品;2-氨基-2-甲基-1-丙醇(C4H11NO,AMP)、乙醇胺(C2H7NO,MEA)、二乙醇胺(C4H11NO2,DEA)、三乙醇胺(C6H15NO3,TEA),均为分析纯,上海展云化工有限公司产品;二次蒸馏去离子水,实验室自制。
1.2 二元复配胺液和三元复配胺液的制备
多元复配胺液是指在主体胺液中通过添加适当比例的活化剂构成。实验制备了2种二元复配胺液以及4种三元复配胺液,复配胺液质量均为200 g,其中MDEA为溶剂,PZ、AMP、MEA、DEA、TEA为活化剂。
分别以PZ(质量分数分别为2%、4%、6%)和AMP(质量分数分别为2%、4%、6%)为活化剂制得MDEA+PZ和MDEA+AMP二元复配胺液,过程如下:分别称取4、8、12 g活化剂添加至烧杯中,缓慢向烧杯中加入MDEA溶剂至80 g,最后加入去离子水至200 g,充分搅拌均匀。
以38%MDEA+2%PZ的二元复配胺液为基础,向其中添加第3种活化剂(AMP、MEA或DEA)构成三元复配胺液。其制备过程如下:称取4 g PZ添加至烧杯中,缓慢向烧杯中加入MDEA溶剂至80 g,之后再分别缓慢滴入4 g AMP、MEA或DEA,最后加入去离子水至200 g,充分搅拌均匀,制得38%MDEA+2%PZ+2%AMP、38%MDEA+2%PZ+2%MEA和38%MDEA+2%PZ+2%DEA三元复配胺液。
19%MDEA+2%PZ+19%TEA三元复配胺液的制备过程如下:称取4 g PZ添加至烧杯中,缓慢向烧杯中加入TEA溶剂至42 g,之后再缓慢加入MDEA溶剂至80 g,最后加入去离子水至200 g,充分搅拌均匀。
近代以降,中国社会对于儒家思想的态度经历了翻天覆地的变化,而关于孔孟等儒家之“武”却始终未引发足够的重视。郭沫若《十批判书》说孔子“是文士,关于军事也没有学过”[13](P93),冯友兰在《儒家论兵》中也说到:“有些人看见这个题目,也许就要呵呵大笑。他们心里想儒家是讲仁义礼乐底人,怎么也能谈兵?”[14](P597)近几十年来的当代中国文化,对于体育、军事、身体素质、实践能力的重视也仍远远不够。即便《论语》《孟子》中已经足够明确地表达了孔孟的“武德”观念,也已被我们的阐释传统和大众文化过滤掉,而常常将古圣先贤想象为“十指不沾阳春水”以及袖手清谈的“道德花瓶”。
1.3 胺液饱和吸收容量测定
胺液中CO2含量通过酸解实验进行测定,取3 mL 待测胺液,使用稀硫酸对已吸收至饱和的胺液中的CO2进行置换,通过排水法对CO2体积进行测定。每组胺液样品均进行3次重复酸解实验,取3次测量结果的平均值,通过上述操作,得到每3 mL 胺液中溶解的CO2体积。
1.4 天然气胺法脱碳吸收反应热实验测量系统
为准确测量高压天然气胺法脱碳过程中的吸收反应热,基于绝热量热法原理,自主设计了一套天然气胺法脱碳吸收反应热测量系统。该测量系统主要由绝热反应量热器、进气预热调压系统、反应器磁力搅拌、加热系统、抽真空系统以及传感器数据采集与控制系统组成。天然气胺法脱碳吸收反应热测量实验系统流程示意图如图1所示。
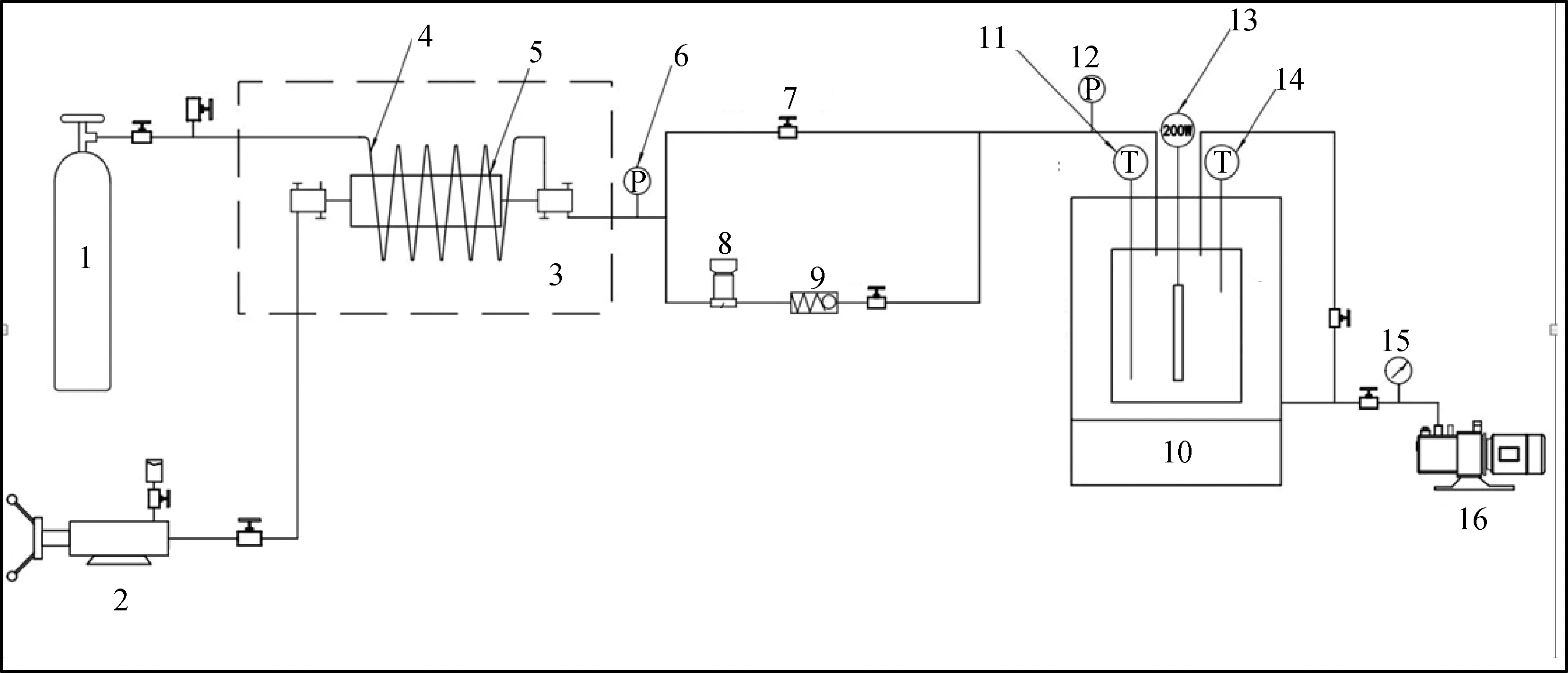
图1 天然气胺法脱碳吸收反应热实验流程图Fig.1 Experimental flow chart of absorption reaction heat for natural gas decarbonization by amine method1—High pressure cylinder; 2—Hand pump; 3—Constant temperature water bath; 4—Preheating coil; 5—Buffer tank; 6, 12—Pressure sensor;7—High pressure ball valve; 8—Regulating valve; 9—Check valve; 10—Magnetic stirrer; 11, 14—Temperature sensor;13—Constant power heating rod; 15—Vacuum meter; 16—Vacuum pump
1.5 吸收反应热计算方法
吸收反应热分为吸收反应的积分热和差分热2种,积分热(ΔQint)定义为整个吸收过程中总放热量与总CO2负载量的比值(见式(2)),kJ/mol;差分热(ΔQdiff)定义为分段通入CO2时产生的热量与分段吸收的CO2负载量的比值(见式(3)),kJ/mol[17]。
(2)
(3)
式(2)和式(3)中:Qabs,i为每次通入CO2时产生的热量,kJ;αCO2,i为每次通入CO2后的液相CO2负载量,mol CO2/(mol amine);Qabs为反应放出的热量,kJ;αCO2为CO2负载量,mol CO2/(mol amine)。
针对1.4节中设计搭建的天然气胺法脱碳吸收反应热实验测量系统,吸收反应过程中产生的热量有2个去向,一个是醇胺溶液的温升,另一个是反应量热器的温升。因此,反应过程中放热量的具体计算方法如式(4)所示。
(4)
CO2负载量(αCO2)通过恒定容积法计算,其计算公式如式(5)所示。
(5)
2 结果与讨论
2.1 实验误差分析
为了验证天然气胺法脱碳吸收反应热测量系统的精度是否达到要求,笔者测量了多组纯水在不同温度下的比热容数据,通过与美国国家标准与技术研究院(National Institute of Standards and Technology,NIST)所开发的REFPROP(Version9.1)软件计算得到的纯水比热容数据作为标准值进行对比,分析计算出天然气胺法脱碳吸收反应热测量系统的热当量,结果如表1所示。

表1 纯水定压比热容(Cp)实验结果Table 1 Experimental results of specific heat capacity atconstant pressure (Cp) of pure water
由表1可知,系统热当量随着实验温度和压力的升高基本不变,均在1.22 kJ/K左右。系统稳定性良好,将计算得到的系统热当量代入后续定压比热容的实验计算中,验证实验准确性,其结果如表2所示。
从表2可以看出,引入系统热当量之后有效提高了实验精度,测得的纯水定压比热容与标准值平均误差为0.90%,出现的最大误差为1.65%。30%MDEA比热容与标准值[18]偏差也均在5%以下,经过修正后的实验系统精度较高。
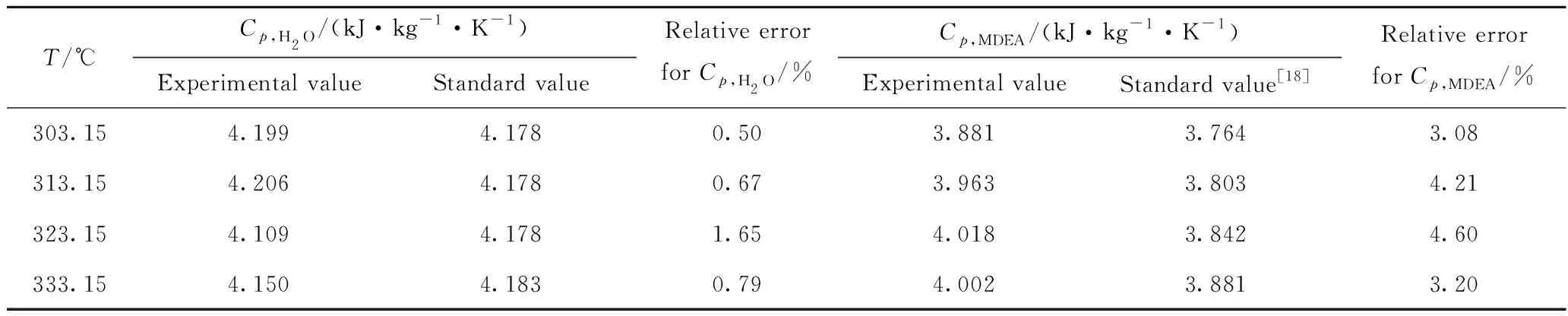
表2 修正后纯水比热容(Cp,H2O)、30%MDEA比热容(Cp,MDEA)与标准值的偏差Table 2 Deviation between the corrected values of specific heat capacity ofpure water (Cp,H2O) and 30%MDEA (Cp,MDEA) and the standard values
2.2 不同影响因素下吸收反应热随CO2负载量的变化规律
2.2.1 醇胺种类对吸收反应热的影响
课题组前期针对不同种类的醇胺溶液的饱和吸收容量进行了研究[19-20],实验结果表明,MDEA溶液的饱和吸收容量为37 mL CO2/(mL amine),而PZ和AMP溶液的饱和吸收容量分别为40和47 mL CO2/(mL amine),均大于MDEA溶液。
对上述3种胺液的吸收反应热进行实验测量,结果如图2所示。MDEA的吸收反应热在50~55 kJ/(mol CO2)之间,而PZ和AMP的吸收反应热在65~70 kJ/(mol CO2)之间,MDEA的吸反应热明显小于PZ和AMP。因此,综合考虑PZ和AMP较适合作为添加剂使用,而MDEA适合作为主体胺液使用。
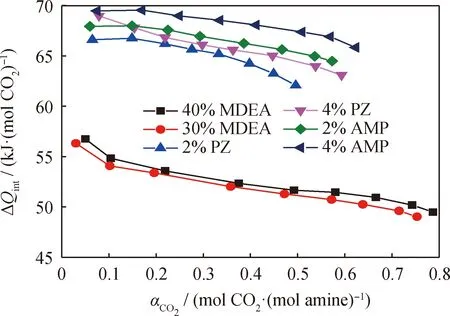
图2 不同CO2负载量(αCO2)下,醇胺种类对吸收反应热(ΔQint)的影响Fig.2 Effects of different alcohol amines on absorptionreaction heat (ΔQint) at different CO2 loads (αCO2)T=303.15 K; p=1.0 MPa
醇胺分子结构内有1个胺基和至少1个羟基,羟基可降低醇胺蒸气压,增加醇胺分子在水中的溶解度;胺基使水溶液呈碱性,促进对酸性组分的吸收。图3为MDEA、PZ、AMP的分子结构示意图。由图3可以看出,MDEA作为叔胺,其N原子上没有活泼氢原子相连,CO2在MDEA溶液中的反应并不像在伯胺或仲胺水溶液中生成稳定的胺基甲酸盐,而是生成亚稳态的碳酸氢盐,因此CO2与MDEA溶液的反应可以看作是物理溶解过程,MDEA分子在此过程中充当了催化剂促进了水分子的解离[21]。而从AMP及PZ的分子结构式可以看出,其N原子上均有活泼氢原子相连,因此与CO2反应时均直接参与反应,反应速率比MDEA溶液要快得多。且AMP为空间位阻胺,而PZ的结构中同样存在空间位阻,两者反应机理相似,均与CO2反应生成碳酸氢盐[22]。
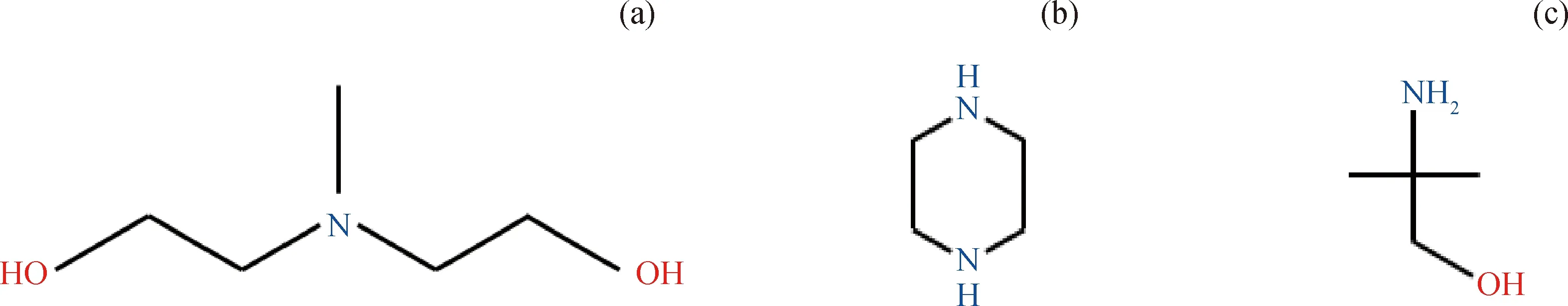
图3 MDEA、PZ和AMP分子结构示意图Fig.3 Schematic diagram for molecular structures of MDEA, PZ and AMP(a) MDEA; (b) PZ; (c) AMP
2.2.2 CO2负载量对吸收反应热的影响
在CO2分压为1 MPa下分段通入CO2进行MDEA、PZ以及AMP的吸收实验,并测定其每次通入CO2的积分热(ΔQint)和差分热(ΔQdiff),实验结果如图4所示。
由图4可知,随着CO2负载的升高,各吸收剂吸收CO2的积分热与差分热均呈现下降趋势,且差分热相对于积分热的下降幅度更大。醇胺溶液吸收CO2的反应过程并不是一步完成的,吸收剂的初始状态不同,导致各步反应的进程发生改变,从而导致每次通气时产生的热量不同。由于实验过程中每次通入CO2时醇胺溶液吸收剂的初始状态不同,后续通入CO2时溶液内已有部分酸气负荷,因此后续每次通气后的吸收反应热相比前一次通气也有所下降,故差分热下降更为明显。
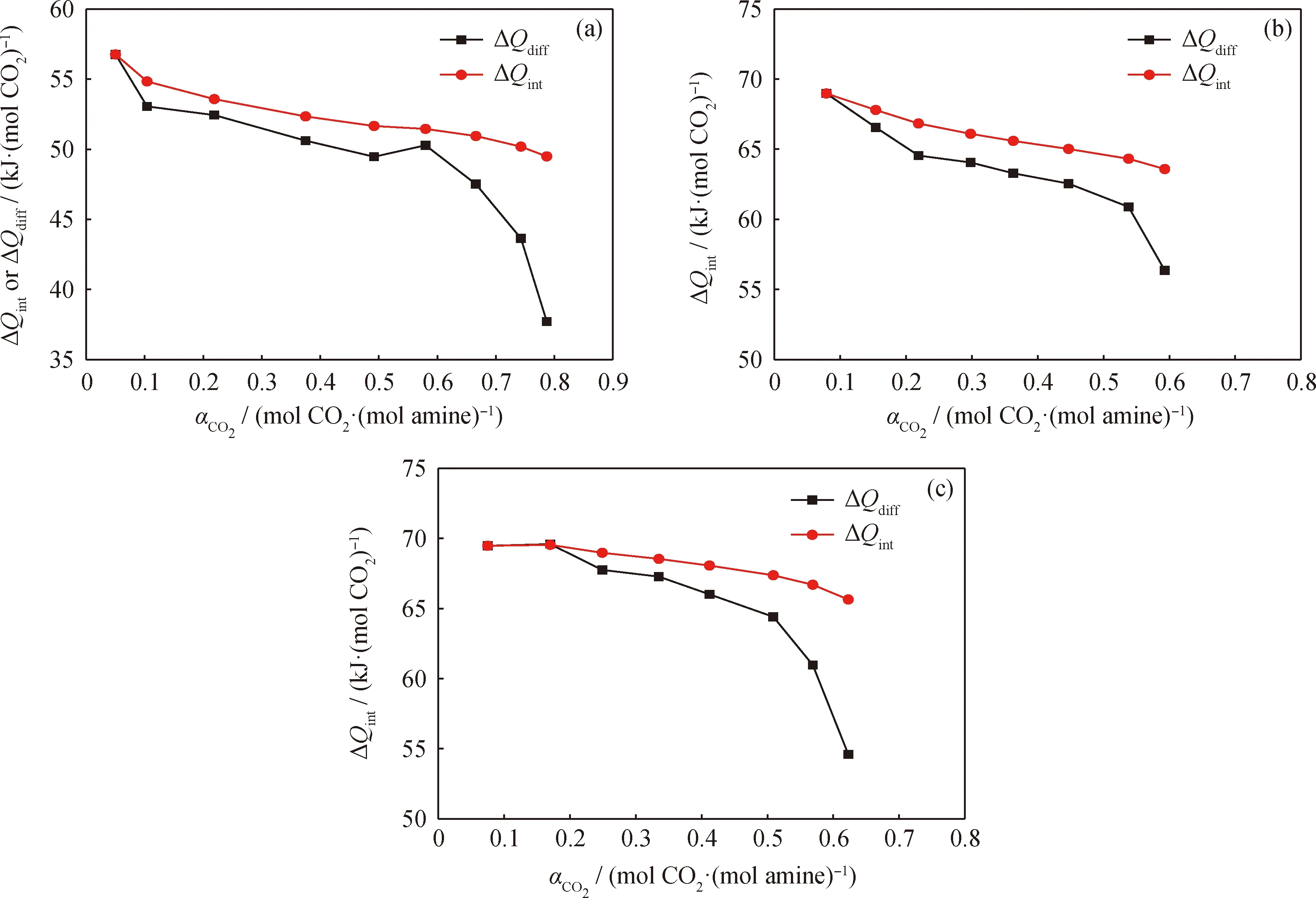
图4 CO2负载量(αCO2)对不同胺液吸收反应热(ΔQint、ΔQdiff)的影响Fig.4 Effects of CO2 loading (αCO2) on absorption reaction heat (ΔQint or ΔQdiff) of different amine solutions(a) MDEA; (b) PZ; (c) AMPT=303.15 K; p=1.0 MPa
2.2.3 总胺质量分数对吸收反应热的影响
图5为总胺质量分数对MDEA、PZ、AMP吸收反应热的影响。由图5可知,随着总胺质量分数的增加,吸收反应热整体呈增加趋势,MDEA吸收反应热受总胺质量分数的影响比PZ和AMP小。主要因为MDEA吸收CO2的反应中MDEA不直接参与反应,其主要作用为催化剂,催化水分子解离,过程比较平缓,小幅度增加MDEA质量分数对其反应过程影响不大。而PZ和AMP分子直接参加化学反应,因此其总胺质量分数变化对整个反应进程影响较大。

图5 总胺质量分数对MDEA、PZ、AMP吸收反应热(ΔQint)的影响Fig.5 Effects of total amine mass fraction on the absorption reaction heat (ΔQint) of MDEA, PZ and AMP(a) MDEA; (b) PZ; (c) AMPT=303.15 K; p=1.0 MPa
2.2.4 吸收压力对吸收反应热的影响
图6为吸收压力对MDEA、PZ、AMP吸收反应热的影响。由图6(a)可以看出,吸收压力对MDEA的反应热影响较小,其初始压力主要影响了反应的前半段,醇胺溶液吸收CO2包括了物理溶解和化学反应2个过程,初始压力的改变会影响物理溶解量的大小,初始压力越大,其物理溶解量也越大。随着反应的进行,化学吸收逐渐占据主导,CO2的物理溶解带来的影响逐渐降低。MDEA溶液吸收CO2的第一步为水分子的解离,水分子失去质子后与CO2发生反应,吸收压力的增加只影响了气相空间内CO2的状态,使得单位体积内CO2分子数量增多,但水分子的解离速率并未发生显著改变,因此MDEA的吸收反应热受压力的影响不大。由图6(b)和(c)可以看出,吸收压力对PZ和AMP的反应热影响主要在CO2负载量低于0.2 mol CO2/(mol amine)时,由于PZ溶液和AMP溶液吸收CO2时是CO2直接与分子的官能团进行结合,初始压力的改变使得气相空间单位体积内的CO2分子数量发生改变,从而迅速影响反应进程。总体而言,吸收压力对吸收反应热的影响较小。
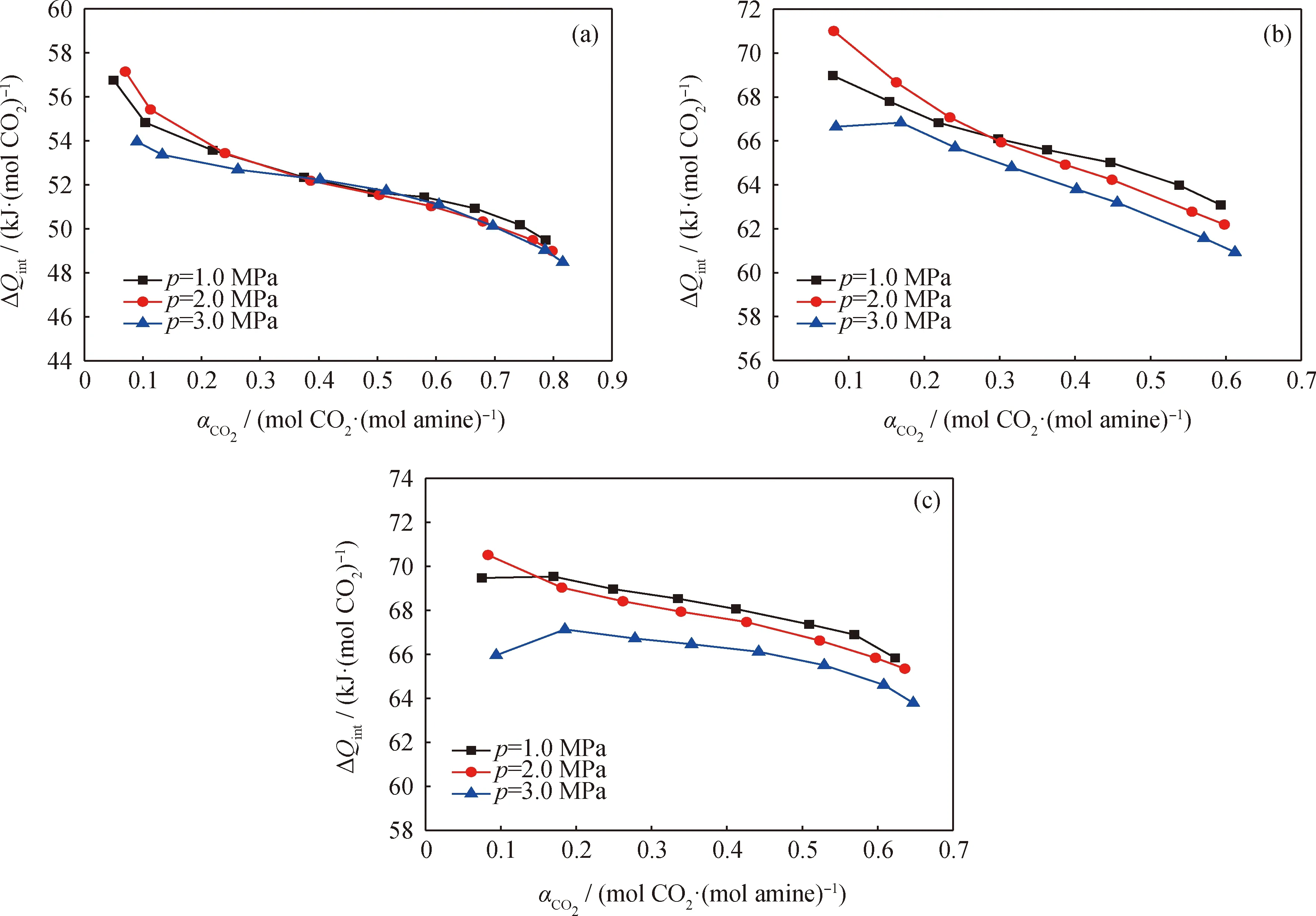
图6 吸收压力(p)对MDEA、PZ、AMP吸收反应热(ΔQint)的影响Fig.6 Effects of absorption pressure (p) on absorption reaction heat (ΔQint) of MDEA, PZ and AMP(a) MDEA; (b)PZ; (c) AMPT=303.15K; w(MDEA)=40%; w(PZ)=4%; w(AMP)=4%
2.2.5 吸收温度对吸收反应热的影响
醇胺溶液吸收CO2是一个放热反应,即实际的吸收过程中温度是一个变值,一般称醇胺溶液进入吸收塔时的温度为吸收温度,但该温度只是吸收温度的初始值[23]。因此,选取工厂贫液常见的吸收温度303.15~343.15K以及半贫液常见初始吸收温度343.15 K,在CO2分压为1.0 MPa下进行不同吸收温度下MDEA、PZ以及AMP的吸收实验测定其吸收反应热,测得的积分热结果如图7所示。
由图7可知,温度对不同种类的醇胺溶液的反应热影响规律不同。由于醇胺溶液吸收CO2并不是一步完成的,而是一个多步反应过程,因此吸收温度的改变主要影响放热量较大的反应步骤。

图7 吸收温度(T)对MDEA、PZ、AMP吸收反应热(ΔQint)的影响Fig.7 Effects of absorption temperature (T) on absorption reaction heat (ΔQint) of MDEA, PZ and AMP(a) MDEA; (b) PZ; (c) AMPp=1.0 MPa; w(MDEA)=40%; w(PZ)=4%; w(AMP)=4%
MDEA溶液吸收CO2主要以物理溶解为主,反应温度升高,CO2分子较易从气-液相界面向气相逃逸,显著影响了CO2的平衡溶解度[24]。由图7(a)可以看出,对于MDEA溶液,随着吸收温度的升高,吸收反应热逐渐增加,在温度较高时的影响较明显。343.15 K下MDEA吸收CO2在CO2负载量为0.4 mol CO2/(mol amine)时已达到最大吸收能力,吸收能力比303.15K和323.15 K下降显著。另一方面,醇胺溶液吸收CO2为放热反应,温度升高,反应平衡向着逆方向移动,导致反应热下降迅速。由图7(b)可以看出,吸收温度对PZ吸收CO2的吸收反应热而言影响不大,随着吸收温度的增加呈现先增加后减小的趋势,吸收温度在323.15 K下的吸收反应热最大。对于AMP溶液来说,吸收温度越高,吸收反应热越高。
2.3 二元复配胺液的吸收反应热变化规律
2.3.1 活化剂PZ对MDEA溶液吸收反应热的影响
固定总胺质量分数为40%,对PZ添加质量分数分别为2%、4%以及6%的复配胺液的吸收反应热进行测量,结果如图8所示。
PZ是典型的环状有机胺,吸收速率较快。在MDEA溶液中加入一定的PZ能够明显提高MDEA的反应速率。由于PZ本身也会与CO2发生反应,会改变原有单一MDEA与CO2的反应路径,从而影响其反应热。前期研究结果表明,PZ的吸收速率虽高,但是吸收容量较低,少量添加即可起到增加吸收速率的作用,大量添加反而会降低醇胺溶液的吸收性能。
由图8可知,与单一MDEA和单一PZ溶液的吸收反应热相比,MDEA+PZ二元复配胺液的吸收反应热介于两者之间,且较接近于单一PZ溶液的吸收反应热。PZ添加质量分数为2%、4%、6%时,二元复配胺液的吸收反应热相较于MDEA溶液提升了5~10 kJ/(mol CO2)。总体而言,添加不同浓度PZ后,吸收反应热由大到小的顺序依次为36%MDEA+4%PZ、34%MDEA+6%PZ、38%MDEA+2%PZ。
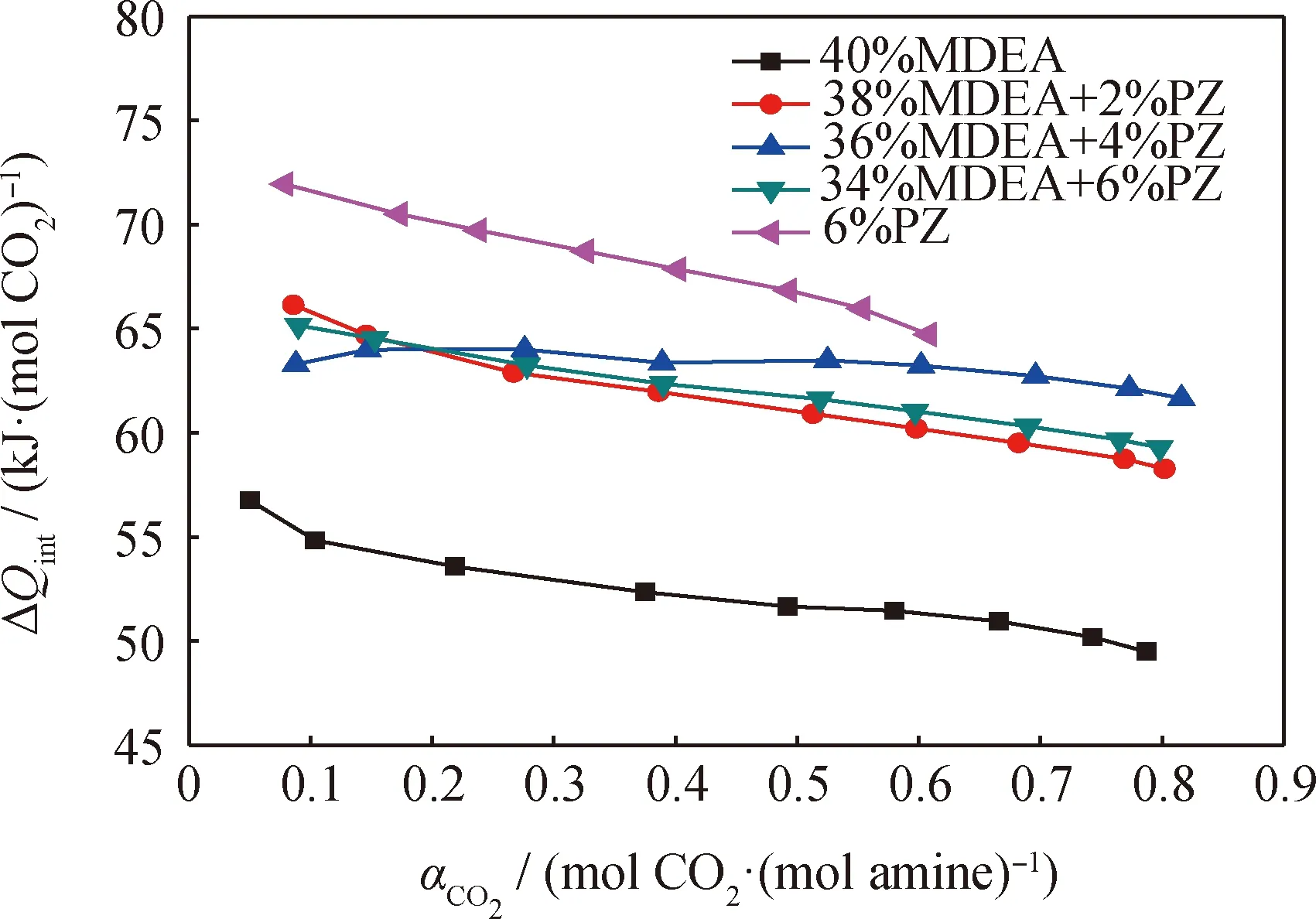
图8 活化剂PZ对MDEA溶液吸收反应热(ΔQint)的影响Fig.8 Effect of the activator PZ on absorptionreaction heat (ΔQint) of MDEA solutionT=303.15 K; p=1.0 MPa; w(Amine)=40%
2.3.2 活化剂AMP对MDEA溶液吸收反应热的影响
固定总胺质量分数为40%,对AMP添加质量分数分别为2%、4%以及6%的复配胺液进行吸收反应热测量,结果如图9所示。

图9 活化剂AMP对MDEA溶液吸收反应热(ΔQint)的影响Fig.9 Effect of the activator AMP on absorptionreaction heat (ΔQint) of MDEA solutionT=303.15 K; p=1.0 MPa; w(Amine)=40%
AMP是一种常见的空间位阻胺,由于其与氮原子相连的碳原子上存在庞大的取代基而产生空间位阻效应,会影响与CO2形成的氨基甲酸脂的稳定性,故具有吸收速率快、吸收容量大的特点。由图9 可以看出,与单一MDEA和单一AMP溶液的吸收热相比,MDEA+AMP二元复配胺液的吸收反应热介于两者之间且更接近于单一AMP的吸收反应热,当AMP添加质量分数为2%、4%、6%时,二元复配胺液的吸收反应热相较于单一MDEA溶液提升了10~12 kJ/(mol CO2)。总体来看,吸收反应热由大到小的顺序依次为34%MDEA+6%AMP、36%MDEA+4%AMP、38%MDEA+2%AMP。相对于单组分的MDEA溶液,活化剂AMP的加入会增加其吸收反应热,而且活化剂AMP的添加量越大,整体吸收反应热越高。
2.4 三元复配胺液的吸收反应热变化规律
由二元复配胺液吸收反应热结果可知,复配胺液在反应过程中并不是2种胺液吸收反应的累加,存在交互作用,反应过程较为复杂。对三元复配胺液的吸收反应热进行研究可以从热力学角度帮助分析三元复配胺液吸收CO2过程中的交互作用。
在吸收反应热较小的二元复配胺液38%MDEA+2%PZ的基础上分别添加第3种胺液AMP、MEA、DEA以及TEA组成三元复配体系。对比研究不同三元复配胺液吸收CO2的吸收反应热变化规律,探究第3种胺液的添加对吸收反应热的影响,结果如图10所示。
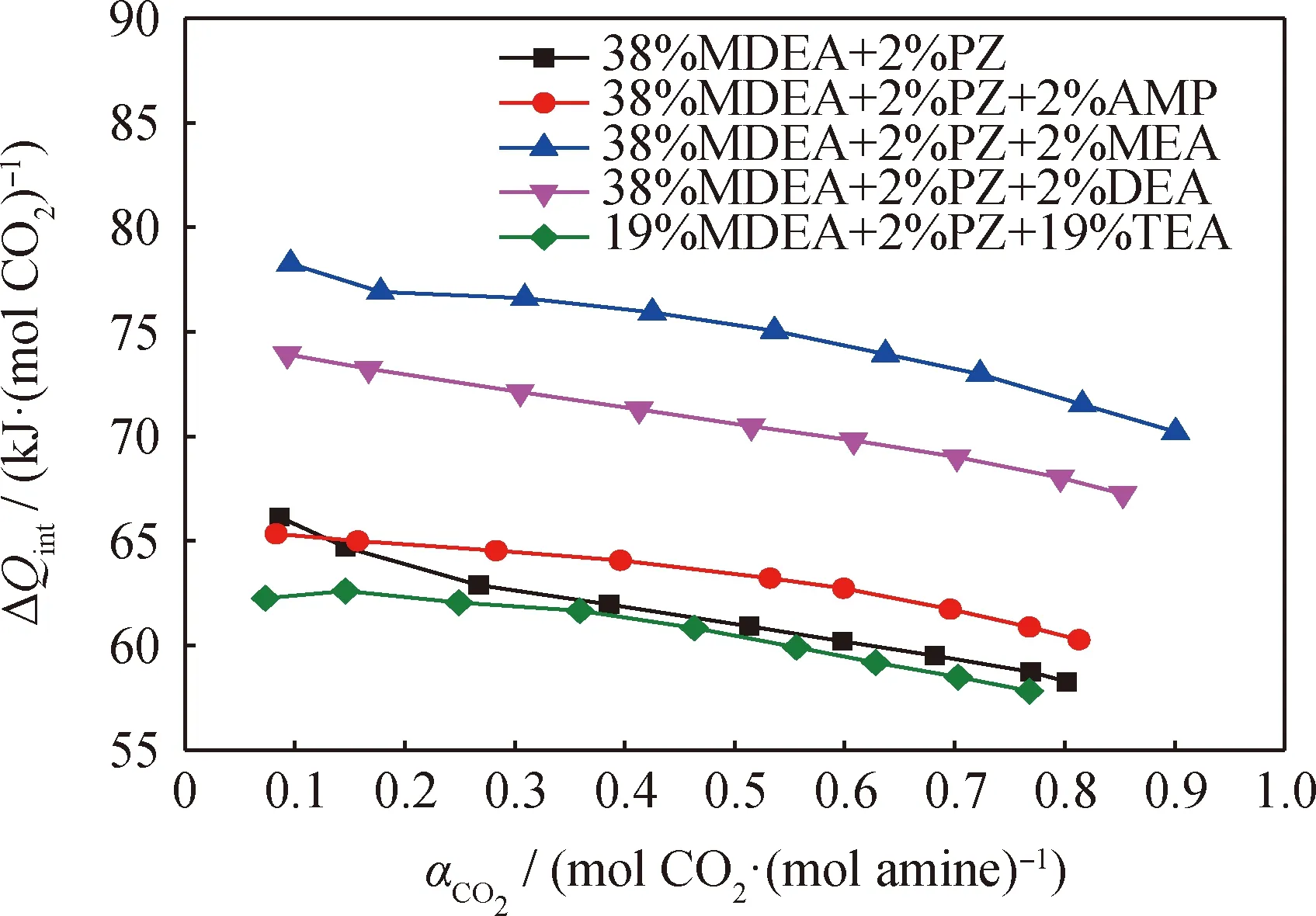
图10 三元复配胺液的吸收反应热(ΔQint)Fig.10 Absorption reaction heat (ΔQint) of ternarycompound amine solutionT=303.15 K; p=1.0 MPa
由图10可知,三元复配体系中,胺液对CO2的吸收反应热由大到小的顺序依次为38%MDEA+2%PZ+2%MEA、38%MDEA+2%PZ+2%DEA、38%MDEA+2%PZ+2%AMP、38%MDEA+2%PZ、19%MDEA+2%PZ+19%TEA。添加MEA和DEA后的吸收反应热明显增加,添加AMP和TEA后的吸收反应热与原二元复配胺液相近,且添加TEA后的吸收反应热稍低。
添加MEA和DEA后溶液吸收反应热明显增大,最高分别达到了78和73 kJ/(mol CO2),主要因为MEA为伯胺,DEA为仲胺,两者都是先与CO2反应生成两性离子,两性离子与溶液中的各类物质发生去质子化反应生成氨基甲酸盐,其实质上是CO2与伯胺或仲胺中活泼的氢原子发生了反应。从图10还可以看到,MEA比DEA的整个吸收过程更为剧烈,反应放热量更大。添加第3种胺液AMP后使吸收反应热有小幅度的升高,因为AMP和PZ同为位阻胺,其反应机理类似,因此添加AMP后并不会明显改变整个吸收过程的反应途径以及生成产物,两者的吸收反应热相差不大。添加TEA后吸收反应热有小幅度的降低,因为TEA与MDEA相似,两者都属于叔胺,本身的吸收反应热较小,加入TEA不会改变原有二元复配胺液的反应途径,因此对整体吸收反应热的影响不大。
3 结 论
探究了醇胺种类、总胺质量分数、CO2负载量、吸收压力以及吸收温度等因素对醇胺溶液的吸收反应热影响规律,研究了以MDEA为主体吸收剂的二元及三元复配胺液吸收反应热,考察了活化剂对吸收反应热的影响。结论如下:
(1)MDEA溶液的吸收反应热在50~55 kJ/mol CO2之间,而PZ溶液和AMP溶液的吸收反应热在65~70 kJ/(mol CO2)之间;从CO2负载量来看,PZ和AMP的最大吸收能力均低于MDEA。
(2)在相同的温度条件下,各吸收剂的吸收反应热随CO2负载量的增加而下降;随总胺浓度的增大而增大。PZ与AMP溶液吸收反应热随着吸收压力的升高而降低,MDEA溶液吸收反应热受压力的影响并不明显。其他条件相同时,温度对不同种类吸收剂的吸收反应热影响并不相同,但溶液的最大吸收能力随着温度的升高均有所降低。
(3)以MDEA为主体吸收剂的二元复配胺液的吸收反应热介于单一的主吸收剂和活化剂之间。随着活化剂含量的增加,MDEA+PZ二元复配胺液的吸收反应热先增加后减小,MDEA+AMP二元复配胺液的吸收反应热逐渐增加,活化剂AMP的加入对吸收反应热的影响比PZ略大。
(4)在二元复配胺液38%MDEA+2%PZ基础上,分别添加第3种胺液AMP、MEA、DEA以及TEA构成三元复配体系,分别添加MEA和DEA后的三元复配体系的吸收反应热明显增加,分别添加AMP和TEA后的三元复配体系的吸收反应热与二元复配胺液38%MDEA+2%PZ相近,且添加TEA后的吸收反应热稍有降低。
