醇胺溶液吸收CO2的反应原理及实验研究
2015-11-03苏雪梅
苏雪梅
(广西工业职业技术学院,广西 南宁 530001)
醇胺溶液吸收CO2的反应原理及实验研究
苏雪梅
(广西工业职业技术学院,广西 南宁 530001)
阐述了醇胺溶液吸收CO2的反应原理;以一乙醇胺(MEA)、二乙醇胺(DEA)、甲基二乙醇胺(MDEA)为研究对象,考察了醇胺溶液的浓度、种类对CO2的吸收速率和吸收总量的影响,并比较了不同复配体系的吸收性能。结果表明,相同条件下吸收效果MEA>DEA>MDEA,而在MEA溶液中加入一定量的MDEA溶液可以明显提高溶液的吸收性能。
醇胺溶液;二氧化碳;吸收;反应原理
作为目前最为重要的能源与环境问题之一,CO2捕集技术一直备受关注。目前世界上捕集CO2的方法包括物理法、化学法、物理—化学法、膜分离法、膜吸收法等,其中化学法具有吸收效果好、吸收量大、技术成熟等优点,在工业上得到广泛的应用。目前工业上脱除CO2技术的研究热点是化学吸收法,其中一类重要的吸收剂就是醇胺溶液。研究一种对CO2吸收速率快、吸收容量大、再生能耗低的新型复合胺吸收液就显得尤为重要。
本文以工业上常用的一乙醇胺(MEA)、二乙醇胺(DEA)、甲基二乙醇胺(MDEA)为研究对象,分别考察了吸收剂种类、浓度等对CO2吸收速率和吸收性能的影响,同时重点研究了二元复合胺溶液体系的吸收特性,并与相同浓度的纯溶液进行了对比,同时进行反应机理的分析,所得结果可为CO2吸收剂的复配提供可靠的实验依据。
1 醇胺的分类及反应机理
根据醇胺分子的结构,其与氨基(NH2)的氮原子相接的碳原子的个数仅有一个时,称为一级醇胺(伯胺);若氮原子与2个碳原子相接而失去一个氢原子,称为二级醇胺(仲胺);若氮原子与3个碳原子相接而失去2个氢原子,则为三级醇胺(叔胺)[1]。每种醇胺与CO2的反应机理是不同的。
1.1一级醇胺吸收CO2的反应机理
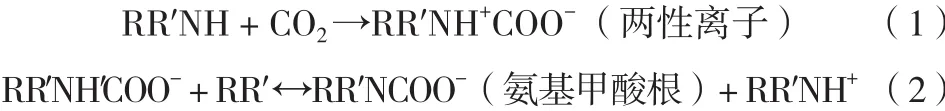
由反应方程式分析可知,一级醇胺与CO2反应时,由于受热力学限制,每1mol一级醇胺仅能够吸收0.5mol的CO2。常用的一级醇胺有MEA、DGA等,特点是吸收CO2速率快。
1.2二级醇胺吸收CO2的反应机理
二级醇胺与CO2的反应机理与一级醇胺相同,但因其缺少一个氢原子,故在反应速度上比一级醇胺要慢些。二级醇胺有DEA、DIPA等。
1.3三级醇胺吸收CO2的反应机理
三级醇胺由于结构中的氮原子失去了2个氢原子,没有多余的氢原子,不会与CO2生成氨基甲酸根。但其水溶液仍可吸收CO2,其反应机理是在反应过程中作为CO2水解的催化剂,使CO2生成碳酸氢根。反应式如下:
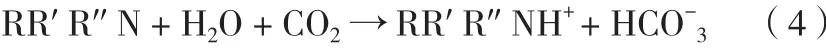
从反应式可知,三级醇胺与一、二级醇胺吸收CO2的机理不同,其吸收CO2不受热力学的限制,每1mol三级醇胺能够吸收1mol的CO2。三级醇胺包括TEA、MDEA等,特点是吸收CO2速率慢,但吸收容量大。
1.4复合胺吸收机理
根据以上分析,几乎每种醇胺溶液都有各自的优缺点,如一级醇胺吸收速率快,但吸收容量小;而三级醇胺刚好相反,其吸收速率慢,但吸收容量大。因此,人们开始研究复合胺,希望通过两种或多种醇胺的优势互补,达到更好的吸收效果。复合胺的吸收机理与单一醇胺不同,并非单纯两种醇胺各自反应,它们之间是相互作用的,过程比较复杂[2]。张亚萍[3]、顾光临[4]、盖群英[5-6]等人的研究表明,复合胺溶液体系在吸收过程中存在交互作用,在一定程度上增强了吸收CO2的能力。
2 实验部分
2.1实验试剂及实验流程
实验试剂包括一乙醇胺(MEA)、二乙醇胺(DEA)、甲基二乙醇胺(MDEA),均为分析纯试剂,蒸馏水为医用蒸馏水。
实验的流程如图1所示。实验在25℃、常压下进行,反应温度设定为40℃,在烧瓶中加入配制好的300mL吸收剂溶液,通入200mL·min-1混合气体进行反应。为保证实验安全,实验中未采用易燃易爆的沼气,而是以N2和CO2混合气体来模拟实际沼气组分(其中CO2含量占35%)。反应过程中以1200r·min-1的速率进行搅拌,使反应均匀。

图1 CO2吸收实验流程
2.2单组分溶液吸收性能研究
2.2.1溶液浓度对吸收速率的影响
对3种不同的醇胺溶液在0.1、0.3、0.5mol·L-1浓度下对CO2的吸收速率随时间的变化进行了实验测试,结果如图2、3、4所示。
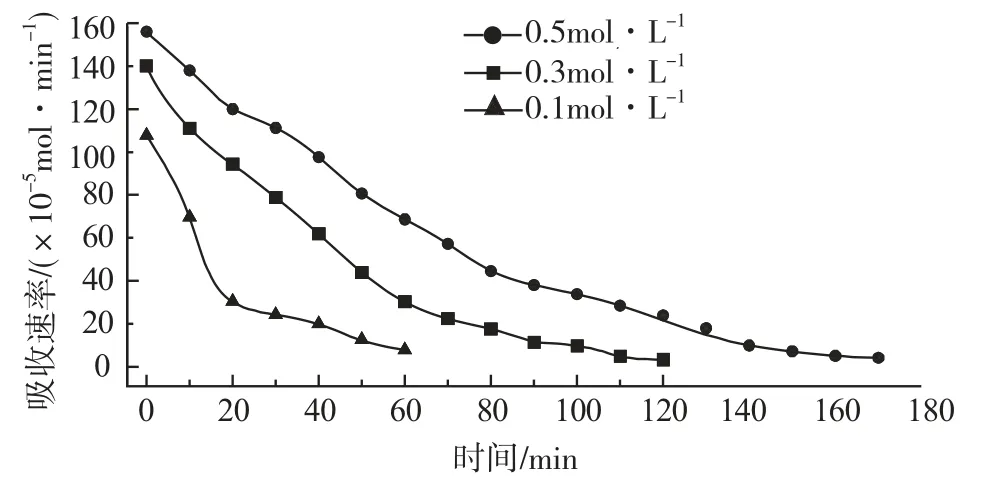
图2 MEA溶液的吸收速率
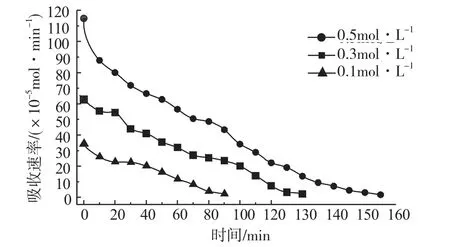
图3 DEA溶液的吸收速率

图4 MDEA溶液的吸收速率
从图2、3、4可以看出,对于MEA、DEA和MDEA这3种溶液,不同浓度溶液对混合气中CO2的吸收具有相似的规律,即浓度越高,吸收速率越快,吸收效果越好。原因是在吸收的开始阶段,吸收液中活性成分的浓度高,吸收迅速,而随着吸收的不断进行,活性逐渐下降,吸收速率减慢,直至最后达到饱和,吸收停止。
2.2.2溶液种类对吸收速率的影响
分析图2、3、4中的数据可以发现,在相同浓度下,MEA的吸收速率最快,其次是DEA,MDEA溶液吸收CO2的速率最慢,但其速率下降较前两者都要缓慢,达到饱和的时间最长。
2.2.3溶液浓度及种类对吸收总量的影响
实验考察了3种不同的醇胺溶液在0.1、0.3和0.5mol·L-1浓度下对CO2的吸收总量,结果如图5所示。

图5 3种溶液的吸收总量对比
图5是3种溶液的吸收总量比较图。可以看出,对每一种吸收液来说,都具有浓度越高,吸收总量越大的规律,即高浓度的吸收剂在吸收容量上面有明显优势,高浓度的胺溶液要达到吸收饱和所用的时间更长,说明高浓度吸收液有更强的吸收能力。原因正是由于浓度越高,其吸收速率越快,吸收时间越长,从而吸收总量也就越大。
对不同种类的醇胺溶液来说,MEA的吸收总量表现最优;作为三级醇胺的MDEA溶液,其吸收总量必须在较高浓度(0.5mol·L-1)条件下才体现出来。原因是虽然MDEA溶液的吸收速率小,但下降缓慢,吸收时间长。在低浓度(0.1mol·L-1和0.3mol·L-1)条件下,太小的吸收速率被认为吸收结束;而在高浓度下,MDEA溶液吸收时间长的优势就可以体现出来,能够以较小的吸收速率维持很长的时间,从而吸收总量逐渐接近吸收时间较短的MEA溶液。
2.3二元复合溶液吸收性能实验
不同种类的醇胺溶液各有优缺点,将不同种类的醇胺溶液混合起来,希望配制的复合胺溶液可以融合不同醇胺溶液的吸收优势,已成为现阶段研究的热点。根据查阅参考文献以及本实验结果可知,MEA的吸收速率快,但吸收时间较短,如果能在其中混入其他类型的醇胺,将其他醇胺的优势与MEA的高吸收速率结合起来,吸收效果将会大大提高。本实验在MEA中添加其他种类的醇胺,对双组分混合吸收液的吸收性能进行了实验研究。
2.3.1双组分混合溶液吸收速率的实验研究
图6为同等浓度的二元复合醇胺溶液与0.3mol·L-1的MEA溶液吸收速率对比图。从图6中可以看出,MEA与DEA的复合溶液较纯MEA溶液差别不大,总体上来说,其吸收CO2的速率和吸收时间均稍有提高,但不明显;而添加了MDEA的复合溶液,其吸收速率与纯MEA溶液相比有了较大的提高,吸收时间更是有了明显的延长,比MEA溶液的吸收时间延长了1/4左右。
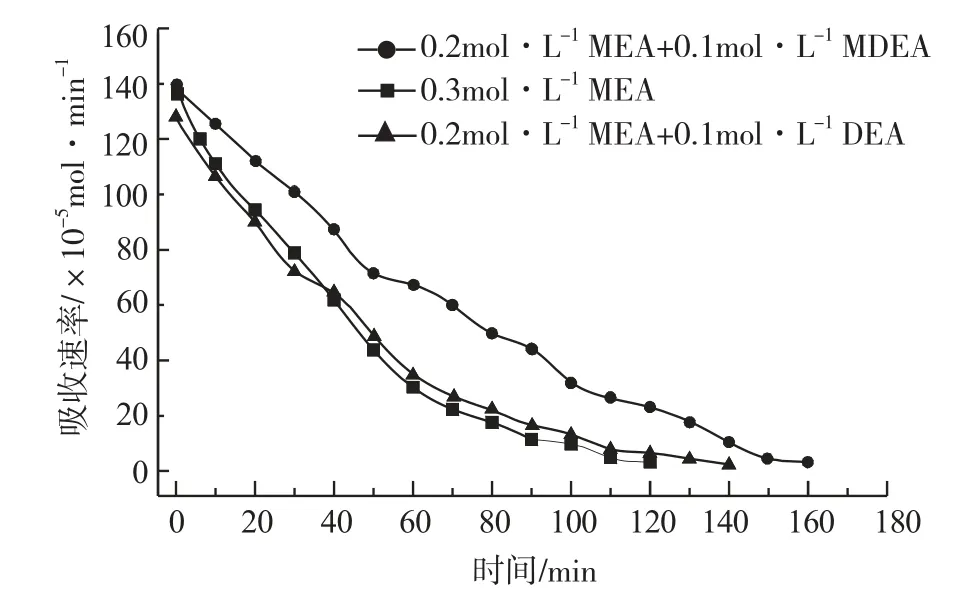
图6 MEA与二元复合溶液的吸收速率对比
2.3.2双组分混合溶液吸收总量的实验研究
图7为同等浓度的二元复合醇胺溶液与0.3mol·L-1的MEA溶液吸收总量对比图。从图7中可以看出,与同等浓度的纯MEA相比较,(MEA+DEA)二元复合溶液③较MEA溶液④吸收总量差别不大,仅有很微小的提高;但与0.2mol·L-1的MEA与0.1mol·L-1的DEA吸收总量之和①相比,则有明显提高,这说明复合溶液的吸收总量不单纯是两种纯溶液吸收总量的简单加和;相同的结果在(MEA+MDEA)二元复合溶液中得到验证(②、⑤)。但0.2mol·L-1的MEA加入0.1mol·L-1的MDEA后,其二元复合溶液的吸收总量⑤明显增大,比0.3mol·L-1的MEA溶液吸收总量③高出1/5左右,说明MDEA吸收时间长的优势可以结合在MEA上面,两者的正作用很明显。

图7 MEA与二元复合溶液的吸收总量对比
3 结论
通过实验考察了3种不同醇胺溶液及其二元复合溶液对CO2的吸收性能,得出以下结论:
1)MEA、DEA、MDEA摩尔浓度越大,其吸收速率越快,吸收总量越大;
2)相同摩尔浓度的溶液,吸收速率排序为MEA>DEA>MDEA;
3)实验考察了相同摩尔浓度的(MEA+DEA)二元复合溶液及(MEA+MDEA)二元复合溶液吸收CO2的效果,后者无论是吸收速率还是吸收总量均比前者及MEA的单组分溶液有显著提高。
[1] A Chakma. An energy efficicnt mixed solvent for the scparation of CO2[J]. Energy Convers., 1995, 36(6/9): 427-430.
[2] Aroonwilas A, Tontiwachwuthikul P. High-efficiency Structured packing for CO2absorption using 2-amine-2-methy-1-propanol.M.A.Sc.Thesis[D]. Regina: University of Regina, 1996.
[3] 张亚萍,等.混合醇胺溶液吸收烟气中的CO2[J]. 化工生产与技术,2012,19(1):22-24.
[4] 顾光临,等.乙醇胺为主体的CO2吸收剂的复配研究[J].北京化工大学学报:自然科学版,2010,37(3):20-24.
[5] 盖群英,等.醇胺溶液吸收与解吸CO2的研究[J]. 环境污染与防治,2008,30(6):62-65.
[6] 盖群英,等.有机醇胺溶液吸收二氧化碳的研究[J]. 现代化工,2007,27(11):395-397.
Reaction Theory and Experimental Study on Absorption of CO2into Alcohol Amines
SU Xue-mei
(Guangxi Vocational Technical Institute of Industry, Nanning 530001, China)
s:In this paper, reaction theory of alcohol amine solutions to absorb CO2were described; absorption rate and capacity of CO2into MEA, DEA, MDEA and their mixture solutions were investigated. The results showed that absorbing effect was MEA>DEA>MDEA under the same conditions, and adding proper quantity of MDEA into MEA solution could evidently improve the absorption properties of the whole solutions.
alcohol amines; carbon dioxide; absorption; reaction theory
TQ 028.1+4
A
1671-9905(2015)12-0007-03
广西高校科研资助项目(桂教科研2013YB327)
苏雪梅(1968-),女,广西人,副教授/高级工程师/注册安全工程师/安全评价师,从事化工教学与科研工作。电话:13086713149,E-mail:1274301723@qq.com
2015-10-09
