泼尼松联合西替利嗪对过敏性紫癜患儿炎症反应及免疫指标的影响
2022-11-10武海江孙永法陈清
武海江,孙永法,陈清
郑州大学附属洛阳中心医院儿科,洛阳 471009
过敏性紫癜(Henoch-Schönlein purpura,HSP)与免疫功能的异常有关,多由粉尘、药物等过敏性因素引起,免疫因子所介导的免疫球蛋白在血管壁沉积后可导致血管炎,甚至损伤机体肾功能[1-2]。因此,临床药物治疗HSP患儿应注重改善患儿免疫功能。泼尼松是一种合成的糖皮质激素,可抑制免疫复合物生成、减少结缔组织增生进而发挥抗过敏、抗炎等作用,缓解临床症状,还可减轻肾脏负担、抑制血栓素的生成、减少血管痉挛的发生,临床常用于HSP的治疗[3]。HSP多发于免疫力相对更低的儿童群体,而长期应用泼尼松可能会增加不良反应和感染的发生风险,加重患儿的身心负担,且有研究发现,单一应用泼尼松治疗HSP患儿时,疾病控制效果不够理想,提示需要联合其他药物以提高疗效[4]。西替利嗪是一种抗组胺类药物,可有效阻断H1受体、抑制嗜酸性粒细胞的活化和趋化、阻断变态反应的迟发相与速发相进而降低血管通透性、缓解HSP症状,且起效快、持效久、安全性高[5]。有研究表明,西替利嗪联合糖皮质激素可有效减轻过敏性疾病患儿的症状[6]。基于此,本研究探讨了泼尼松联合西替利嗪对HSP患儿炎症反应及免疫指标的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2018年6月~2021年6月来本院就诊的84例HSP患儿为研究对象,按照随机数字表法分为对照组和观察组,每组42例。对照组:男性24例,女性18例;年龄6~14岁,平均年龄(9.36±0.92)岁;病程2~16天,平均病程(9.55±1.01)天;疾病类型:单纯型18例,肾型6例,腹型12例,关节型6例。观察组:男性22例,女性20例;年龄6~14岁,平均年龄(9.43±0.87)岁;病程3~15天,平均病程(9.62±0.98)天;疾病类型:单纯型20例,肾型5例,腹型9例,关节型8例。两组一般资料比较无统计学差异(P>0.05),具有可比性。本研究经本院医学伦理委员会审核通过[伦理批号:伦审(2018025)号],患儿家属均签署同意书。
纳入标准:①符合《诸福棠实用儿科学》[7]中HSP诊断标准者。②有皮肤紫癜、胃肠道症状、关节症状者。③机体凝血、出血时间正常者。④年龄<14岁者。排除标准:①合并其他皮肤病者。②合并其他免疫功能障碍疾病者。③合并感染性疾病或恶性肿瘤者。④严重肝肾功能障碍者。⑤对试验药物过敏者。⑥依从性差、不能完成治疗者。⑦近1个月内服用激素者。
1.2 治疗方法
根据HSP患儿具体情况,实施纠正水电解质、营养支持治疗和对症治疗,存在关节症状、发热症状的患儿口服吲哚美辛片(上海金不换兰考制药有限公司,国药准字 H41021631,规格 25mg),1.5mg/(kg·d),分3次服用,存在腹痛症状的患儿口服消旋山莨菪碱片(杭州民生药业股份有限公司,国药准字H33021706,规格5mg),0.1mg/kg,tid。
对照组在常规治疗基础上给予醋酸泼尼松片(华中药业股份有限公司,国药准字H42021526,规格5mg)口服,体重<30kg的患儿,5mg/次,bid,1日最大剂量为10mg;体重≥30kg的患儿,10mg/次,bid,1日最大剂量为30mg。观察组在对照组治疗基础上加用盐酸西替利嗪片(扬子江药业集团有限公司,国药准字H19980059,规格10毫克)口服,年龄<12岁者,5mg/次,qd;年龄≥12岁者,10 mg/次,qd。两组均连续治疗2周。
1.3 观察指标
①症状缓解时间。记录并比较两组患儿皮肤紫癜缓解(皮肤、黏膜瘀点瘀斑消退)时间、胃肠道症状(腹痛、呕吐、便血等)缓解时间、关节症状(关节肿胀、疼痛)缓解时间。②炎症因子。于治疗前后采集患儿空腹肘部静脉血3ml,采用Thermo ST16离心机(美国赛默飞公司,r=16cm),以2000r/min离心10min。采用酶联免疫吸附法检测白细胞介素-6(interleukin-6,IL-6)、IL-8、肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)水平。③免疫功能指标。于治疗前后采集患儿空腹肘部静脉血3ml,以3000r/min离心10min,取血清,用免疫比浊法测定免疫球蛋白A(immunoglobulin A,IgA)、IgM、IgG水平。④不良反应发生率。记录治疗期间两组恶心呕吐、胃肠不适、头痛等不良反应发生情况。⑤复发率。于治疗结束后随访6个月,患儿若再次出现皮肤紫癜、胃肠道症状、关节症状等症状且血小板、白细胞计数、抗溶血性链球菌素O等指标升高,则判定为复发,统计两组患儿复发率。
1.4 统计学方法
采用SPSS 25.0软件对数据进行处理和分析。计数资料以n(%)表示,行χ2检验,若期望值<5,采用连续校正χ2检验;计量资料均经Shapiro-Wilk正态性检验,正态分布计量资料以x±s表示,组间用独立样本t检验,组内用配对样本t检验,方差不齐采用校正t检验。P<0.05为具有统计学差异。
2 结果
2.1 症状缓解时间
观察组皮肤紫癜、胃肠道症状、关节症状等的缓解时间均短于对照组(P<0.05)。见表1。
表1 两组症状缓解时间比较 n=42,x±s,天
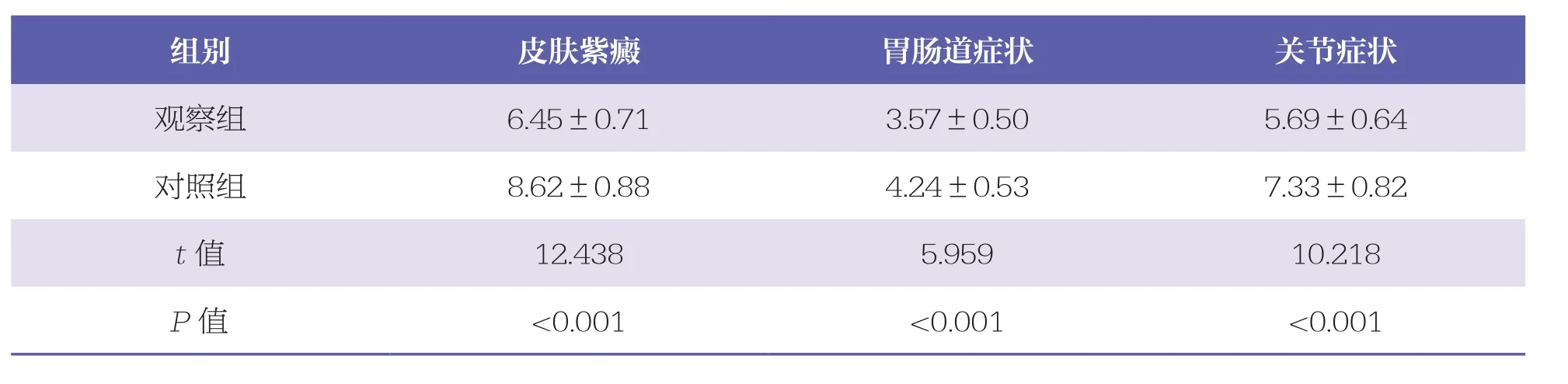
表1 两组症状缓解时间比较 n=42,x±s,天
组别 皮肤紫癜 胃肠道症状 关节症状观察组 6.45±0.71 3.57±0.50 5.69±0.64对照组 8.62±0.88 4.24±0.53 7.33±0.82 t值 12.438 5.959 10.218 P值 <0.001 <0.001 <0.001
2.2 炎症因子
治疗前,两组血清IL-6、IL-8、TNF-α水平比较无统计学差异(P>0.05);治疗后,两组各指标水平均降低,且观察组低于对照组(P<0.05)。见表2。
表2 两组炎症因子水平比较 n=42,x±s,ng/L

表2 两组炎症因子水平比较 n=42,x±s,ng/L
与同组治疗前比较,a:P<0.05。下同
IL-6 IL-8 TNF-α治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 31.45±3.79 19.56±2.13a 62.79±6.78 37.57±4.06a 4.57±0.63 2.85±0.35a对照组 31.66±3.52 23.89±2.75a 61.57±6.33 41.88±4.57a 4.61±0.46 3.47±0.42a t值 0.263 8.067 0.852 4.569 0.332 7.349 P值 0.793 <0.001 0.397 <0.001 0.741 <0.001组别
2.3 免疫功能指标
治疗前,两组血清IgA、IgM、IgG水平比较无统计学差异(P>0.05);治疗后,两组各指标水平均降低,且观察组低于对照组(P<0.05)。见表3。
表3 两组免疫功能指标比较 n=42,x±s,g/L
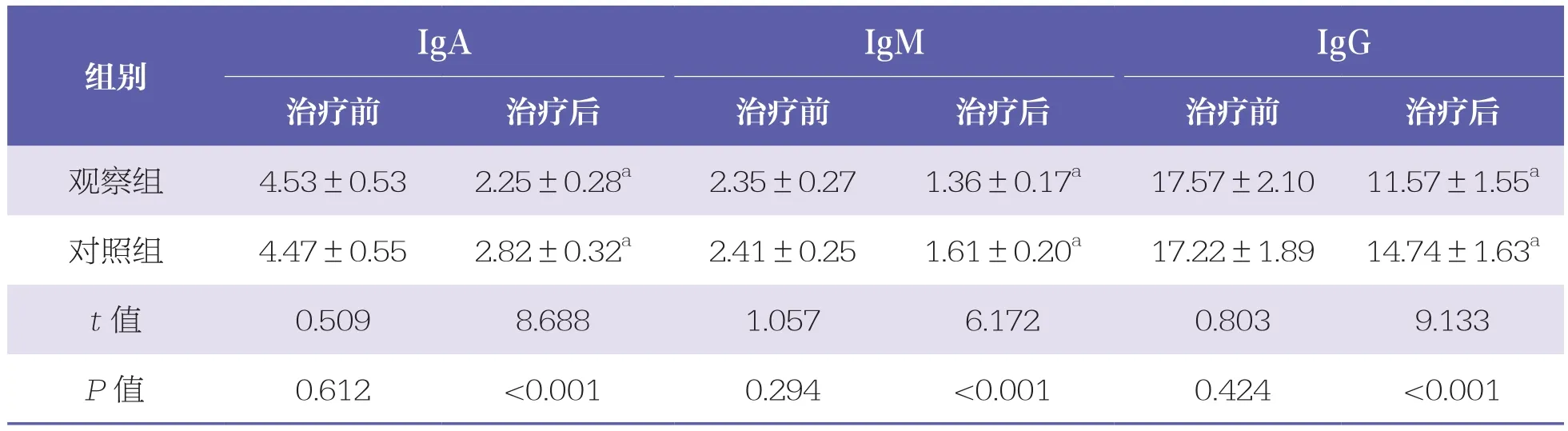
表3 两组免疫功能指标比较 n=42,x±s,g/L
IgA IgM IgG治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 4.53±0.53 2.25±0.28a 2.35±0.27 1.36±0.17a 17.57±2.10 11.57±1.55a对照组 4.47±0.55 2.82±0.32a 2.41±0.25 1.61±0.20a 17.22±1.89 14.74±1.63a t值 0.509 8.688 1.057 6.172 0.803 9.133 P值 0.612 <0.001 0.294 <0.001 0.424 <0.001组别
2.4 不良反应发生率
治疗期间两组不良反应发生率比较无统计学差异(P>0.05)。见表4。

表4 两组治疗期间不良反应发生率比较 n=42,n(%)
2.5 复发率
治疗完成后随访6个月,观察组复发率(2例,4.76%)低于对照组(6例,14.29%),但组间比较无统计学差异(χ2=1.243,P=0.265)。
3 讨论
作为儿童常见的血管炎,HSP具有易反复发作、迁延不愈的特点,若治疗不当可使病情发展,甚至导致患儿全身多脏器损伤[8],探索有效的HSP治疗方案具有重要意义。HSP发生与免疫细胞活化、细胞因子活化介导的免疫功能紊乱有关,因此临床治疗中应注意调节患儿的免疫功能。
目前,临床上治疗HSP多采用糖皮质激素、免疫抑制剂等药物进行对症治疗。泼尼松是一种糖皮质激素,可调节机体T淋巴细胞亚群、抑制免疫球蛋白生成,从而缓解免疫反应[9]。但泼尼松难以遏制HSP带来的损伤(尤其是肾损伤),且HSP患儿长期使用泼尼松容易产生耐药性,可能影响疗效、增加不良反应发生风险[10]。西替利嗪作为第2代抗组胺药,可阻断H1受体、抑制嗜酸性粒细胞生成、减少变态反应,且对过敏反应后期产生的损伤具有遏制作用[11]。本研究结果显示,泼尼松联合西替利嗪可有效缩短HSP患儿的皮肤紫癜、胃肠道症状、关节症状等的缓解时间,其原因可能为:西替利嗪通过强效的嗜酸性粒细胞抑制作用,阻滞嗜酸性粒细胞的活化与趋化,减轻变态反应、炎症反应,降低小血管通透性,从而缓解过敏性反应,缩短皮肤紫癜、胃肠道症状、关节症状的缓解时间[12];泼尼松可抑制血栓素的生成,减轻患儿的皮肤紫癜、胃肠道症状等各种症状;两种药物通过不同机制发挥协同作用,可进一步改善患儿临床症状。
HSP是血管炎症的一种,其发生与微炎症状态有关,且疾病进展过程中伴随炎症反应[13]。IL-6、IL-8、TNF-α均为常见的炎症反应指标,其中IL-6可通过促进HSP患儿的B淋巴细胞分化及活化、刺激T淋巴细胞增殖、诱发细胞毒性反应进而加重炎症反应;IL-8属于趋化性炎症因子,HSP急性期可被大量释放,其水平升高可提示血管炎性损伤的发生;TNF-α由巨噬细胞、单核细胞等分泌,并能对巨噬细胞产生刺激、促进花生四烯酸的生成、造成细胞坏死进而加重炎性损伤[14]。本研究中,治疗后两组血清IL-6、IL-8、TNF-α水平均降低,且观察组低于对照组,提示泼尼松、西替利嗪均能减轻HSP患儿的炎症反应,且联用疗效更佳。分析原因可能为:泼尼松通过降低细胞膜与毛细血管壁的通透性,减少炎性渗出,抑制毒性物质的生成,从而减轻炎症反应[15];同时泼尼松进入机体后结合转运蛋白,转运至机体各个部位,消除沉积的复合物,发挥较强的抗炎作用。而西替利嗪是一种羟嗪代谢产物,能抑制嗜酸性粒细胞主导的炎症细胞浸润及聚集,缓解机体炎症反应[16]。
炎症反应和自身免疫损伤会加重HSP患儿的免疫失衡,导致T淋巴细胞活性增强、免疫球蛋白沉积,并促进IgA、IgM、IgG等免疫复合物生成,造成IgA、IgM、IgG水平升高[17]。IgA、IgM、IgG沉积于小血管壁会加重血管炎症性反应,损伤血管壁组织,引起关节症状、胃肠道症状等[18]。本研究中,泼尼松联合西替利嗪可有效降低IgA、IgM、IgG水平,改善HSP患儿的免疫功能。分析原因可能为:泼尼松经机体吸收后能发挥调节免疫作用,直接抑制免疫复合物生成[19];西替利嗪可通过抑制炎症因子分泌,促进Th1/Th2失衡的快速恢复 ,同时可减少IgA、IgM、IgG等免疫球蛋白沉积[20]。
泼尼松联合西替利嗪治疗HSP患儿安全性较高,其原因可能为:常规给药剂量下,泼尼松不易引起不良反应,若剂量过大或长期应用可能会增加恶心、呕吐等不良反应[21];西替利嗪无潜在的心脏毒性,对中枢抑制小,且无明显抗胆碱的特点,安全性较高[22]。此外,泼尼松联合西替利嗪治疗可有效提高疗效、加快症状缓解,进而避免长期用药所导致的不良反应。
HSP是一种自身免疫疾病,多数患儿常出现病情反复、复发的现象。研究证实,HSP患儿发生复发或病情反复的风险可达71.79%,处于较高水平[23]。病情反复的患儿可因变应性血管炎而增加机体中免疫复合物的积聚,并进一步加重肾脏损害,诱发间质性肾炎,甚至引起慢性肾功能不全,对患儿的预后产生负面影响。因此,优化治疗方案、提升疗效以减少HSP患儿复发风险尤为重要。本研究中,泼尼松联合西替利嗪可有效减轻HSP患儿炎症反应、降低炎症对变态反应性血管炎的刺激,还可改善患儿免疫功能,改善预后,进而降低复发风险[24-25]。但观察组复发率虽然低于对照组,两组比较却无统计学差异,这可能是由于本研究样本量较小,后续应扩大样本量、延长观察时间进一步论证。
综上所述,泼尼松联合西替利嗪治疗可有效减轻HSP患儿的炎症反应、调节免疫指标、加快症状缓解,且安全性较高。
