奥希替尼致罕见的中毒性表皮坏死松解症1例
2022-11-03刘秀坤
刘秀坤,马 雷,陈 雷,沈 芳
0 引言
奥希替尼为第3代不可逆的酪氨酸激酶抑制剂(Tyrosine kinase inhibitor,TKI),可抑制表皮生长因子受体(Epidermal growth factor receptor,EGFR)特异性突变的非小细胞肺癌(Non-small-cell lung cancer,NSCLC)肿瘤的生长,被批准作为EGFR突变的晚期NSCLC的一线治疗药物。其导致的皮肤毒性很常见[1-2],但导致的中毒性表皮坏死松解症(Toxic epidermal necrolysis,TEN)罕见,现报道1例奥西替尼导致的TEN。
1 病例资料
患者,女,58岁,因“确诊左肺鳞癌1月余,全身多发皮疹1周”于2021年4月18日收治入院。患者入院前1月余因咳嗽、咳痰及头痛在我院确诊左肺鳞癌伴脑转移和骨转移,头部姑息性放疗1疗程出院。肺癌基因检测显示EGFR 19外显子非移码缺失性突变,在医生与患者家属充分沟通的情况下,于2021年3月29日开始口服奥希替尼靶向治疗,每次80 mg,每日1次。服用约14 d后,患者颈部、胸部首先出现红斑,伴明显瘙痒,后皮损进行性加重,予口服西替利嗪及外用卤米松乳膏效果不佳,为进一步诊治收住我院呼吸科。患者既往有腰椎间盘突出病史,无食物药物过敏史。
入院查体:体温36.5 ℃,脉搏119次/min,呼吸20次/min,血压138/91 mmHg。神志清,精神差,口腔黏膜糜烂,面部、颈部、前胸、后背、手臂、大腿、腹股沟等弥漫性多形性红斑,无水疱。两肺叩诊音清,双肺呼吸音低,未闻及明显干湿性啰音。心律齐,各瓣膜区听诊区未闻及病理性杂音,腹软,无压痛,肝脾肋下未触及,双下肢无水肿。辅助检查:2021年2月胸部CT提示左肺尖占位伴主动脉弓左前旁、左锁骨下小淋巴结转移。2021年3月病理(左肺)结合HE及免疫组化染色结果显示为鳞状细胞癌。头颅MR和骨骼ECT提示颅内和多发骨转移。入院诊断:左肺鳞癌(T4N3M1c)ⅣB期;腰椎间盘突出。
治疗经过:结合患者用药史及临床表现,考虑患者皮损为药物性皮损。完善相关检查,予卤米松乳膏外用和对症支持治疗。4月19日辅助检查示:WBC 4.96×109/L,EO 6.9%,ALT 75 U/L,AST 37 U/L,ALP 273 U/L,UREA 2.3 mmol/L,CREA 57 μmol/L。4月20日,患者躯干部皮肤广泛红斑伴有水疱,部分水疱破裂,疼痛。皮肤科会诊,加用泼尼松片(25 mg qd)、枸地氯雷他定和依巴斯汀口服,头孢尼西抗感染,氢化可的松乳膏外用。4月21日,患者发热,体温最高39.7 ℃,伴畏寒、寒战,送血培养,予退热对症处理及莫匹罗星软膏外用。停用奥希替尼。4月22日,患者躯干、颈部、四肢及会阴部红斑较前进一步扩大,红斑基础上有松弛性水疱、大疱,疱壁薄、疱液浑浊。背部、臀部可见大面积表皮剥脱、坏死,尼氏征阳性(见图1 A、1B)。渗出明显,全身痒痛难忍。皮肤科再次会诊,考虑患者为TEN。患者体重65 kg,参考Stevens-Johnson综合征(SJS)/中毒性表皮坏死松解症诊疗专家共识[3],对于中重度SJS/TEN患者,可给予糖皮质激素1.5~2 mg/(kg·d),起始量(泼尼松当量),免疫球蛋白推荐剂量400 mg/(kg·d)。泼尼松片调整为注射用甲泼尼龙琥珀酸钠(60 mg q12h,连续6 d)。4月23日,患者体温恢复正常,但皮损进一步加重。WBC 2.27×109/L,EO 0,肝肾功无明显异常。因患者经济因素,治疗上加用小剂量免疫球蛋白(2.5 g qd,连续6 d)。人体的皮肤表面有大量的表皮葡萄球菌,该患者患有肺癌,机体免疫力差,表皮广泛剥脱,皮肤屏障破坏,极易发生感染并重症化,医生予利奈唑胺(0.6 g q12h)和头孢哌酮舒巴坦(3 g q12h)控制感染,并请烧伤科协助换药。4月24日,患者大面积表皮剥脱,伴有渗出,疼痛明显,继续皮肤换药和盐酸布桂嗪止痛。换药方式主要是清创、氯己定消毒,待皮肤稍干燥,先用表皮生长因子溶液喷在创面上,再用混合的磺胺嘧啶银和湿润烧伤膏涂抹,接着凡士林纱布覆盖创面,最后用纱布、棉垫和绷带固定。4月28日,皮损较前减轻,甲泼尼龙逐渐减量(60 mg qd,连续5 d)。最终患者经全身治疗及多次换药处理后,创面逐渐愈合(见图1C、D),住院26 d后患者好转出院。
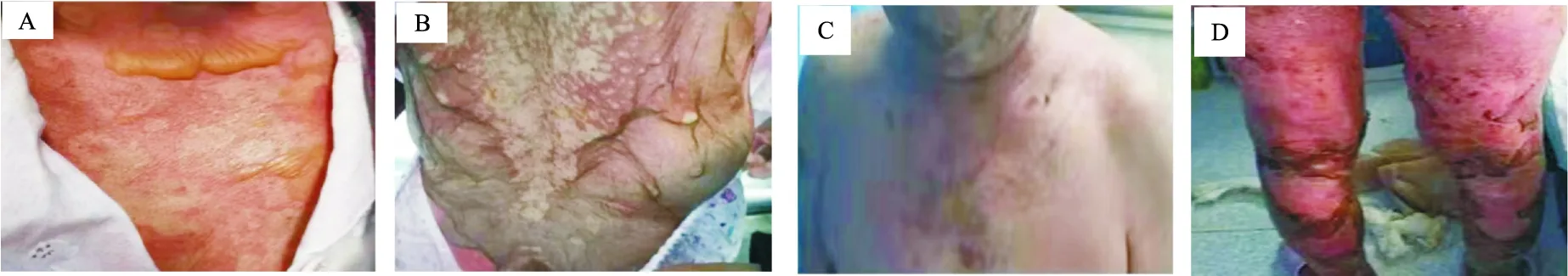
图1 患者治疗前后皮损情况注:A.颈部、胸部弥漫性暗红色斑片,其上可见松弛性水疱、大疱,疱壁薄、疱液浑浊;B.背部、臀部大面积表皮坏死松解、脱落,糜烂面基底潮红,渗出明显;C.颈部、胸部皮损已完全消退,可见少许色素沉着;D.双下肢皮肤糜烂面已痊愈,遗留片状暗褐色鳞屑
2 讨论
肺癌是男性发病率和死亡率第1位的癌症,是女性发病率第3位和死亡率第2位的癌症[4]。NSCLC约占肺癌的85%,主要包括腺癌、鳞状细胞癌和大细胞癌,由于早期症状不典型,大多数患者确诊时已属于中晚期,失去了手术机会。在亚洲,有约50%的NSCLC患者发生EGFR基因突变[5]。针对EGFR基因突变的靶向治疗得到了迅速发展。奥希替尼是第3代EGFR-TKI,适用于具有EGFR外显子19缺失或外显子21(L858R)置换突变的局部晚期或转移性NSCLC成人患者的一线治疗。与第1、第2代EGFR-TKI相比,不仅疗效显著,而且安全性和耐受性更好[6]。皮肤不良反应是奥希替尼常见的不良反应,包括痤疮样皮疹、皮肤干燥、瘙痒和甲沟炎等。研究显示,接受奥希替尼治疗的患者中,皮肤不良反应大多数是轻微的(1或2级),3~4级皮疹不超过1%[2]。目前奥希替尼引起TEN的报道罕见,国内仅报道了2例奥希替尼导致的TEN[7-8],国外仅日本报道1例[9]。本患者为肺鳞癌伴脑转移及多发骨转移,先行头部姑息性放疗1疗程,在基因检测示EGFR19外显子非移码缺失性突变后口服奥希替尼。服药约14 d后出现多发红斑,并进行性加重。研究显示,使用EGFR-TKI治疗的患者,皮疹通常出现在EGFR-TKI治疗开始的2周内,因此,该患者用药与皮疹有合理的时间关系[10-11]。该药说明书记载皮疹发生率为47%,而且国内外也有奥希替尼致TEN的个别报道,日本药品和医疗器械管理局早在2019年就警示奥希替尼相关TEN、SJS和多形性红斑的不良反应[12],因此本患者不良反应符合奥希替尼已知的不良反应。停药和经过治疗后,患者症状减轻。患者发病前仅服用奥希替尼,TEN难以用其他病因来解释。依据《药品不良反应报告和检测工作手册》关联性评价标准[13],奥希替尼与TEN的关联性评价结果为“很可能”,属于严重不良反应。
TEN与SJS同属严重的皮肤过敏反应,其表现类似,特征是表皮和黏膜脱落,但皮损分布不同。当表皮受累面积>体表面积的30%,则认为是TEN。该患者表皮受累面积已达体表面积的60%,属于TEN。TEN严重威胁患者生命,死亡率高达14.8%,95%的TEN为药物导致[14]。奥希替尼导致SJS/TEN的机制尚不明确,由于EGFR在皮肤上皮细胞中高度表达,EGFR-TKI阻断表皮生长因子信号通路会干扰正常表皮的发育,导致异常的增殖、迁移和分化,引起皮肤黏膜毒性反应[15-17]。Li等[18]分析认为,EGFR-TKI的致死性皮肤毒性机制可能与表皮层损伤破坏皮肤物理屏障、毛囊损伤、皮肤稳态破坏、炎症和宿主免疫激活,以及放射治疗有关。EGFR-TKI相关的 SJS/TEN 的发病机制还可能与其干扰了表皮分化和再上皮化,最终导致皮肤广泛破坏有关[19]。此外,EGFR-TKI相关SJS/TEN的报道主要来自亚洲国家,种族和遗传在其潜在的机制中也可能发挥作用[9]。EGFR-TKI诱导的 SJS/TEN机制需要进一步阐明。
目前药物导致的TEN尚缺乏明确的高级别循证医学证据,最佳治疗方案仍然存在争议。该患者经过停用可疑药物,全身使用糖皮质激素、免疫球蛋白,防治感染和对症支持治疗,精心的皮肤创面护理,衣服和床单清洁消毒等综合治疗,获得痊愈。另外,该患者的成功治疗还得益于多学科的协作以及患者与家属的理解和配合。
综上,本文报道了1例奥希替尼导致的TEN病例,目前在国内属于第3例报道。临床治疗中应密切关注,做好用药宣教,早发现,早诊断,早治疗。
