蔪艾精油凝胶缓释系统的透皮效果评价
2022-10-27兰晓霞葛宝健李瑞欣钱晓明曾原
兰晓霞 葛宝健 李瑞欣 钱晓明 曾原
艾是菊科多年生草本植物,主要包括挥发油类、黄酮类、桉叶烷类、三萜类、多糖类和微量元素等多种活性成分[1-2]。据报道,艾叶精油具有镇痛镇静、抗氧化、抗真菌、抗炎、抑菌、抗过敏等药理作用[3-5]。就不同种类艾草中的精油含量而言,蕲艾中精油含量要比湖南产艾叶精油含量高25%左右[6-7]。临床用于艾灸的艾条或艾绒在使用过程中会产生和排放大量烟雾,不仅存在烫灼伤、呼吸道刺激、火灾等安全隐患,大量烟尘亦使治疗环境被污染[8-9]。因此,本研究将蕲艾精油通过低温3D 打印法制备成凝胶缓释系统,既可使艾草精油在制备过程中减少挥发,以最大程度避免损失并保持其活性,又能充分利用艾草精油具有抗菌性、促进创面愈合的优点,并且可以克服传统艾灸存在的安全隐患及污染治疗环境等问题。本研究旨在评价不同时间和温度下,艾草精油凝胶缓释系统的透皮吸收效果。
1 材料与方法
1.1 仪器与材料
气相色谱仪(型号:7890B,美国安捷伦科技公司),火焰离子化检测器(flame ionization detector,FID)(型号:7890A,美国安捷伦科技公司),进样针(型号:10 μL,美国安捷伦科技公司),色谱柱(柱型号:HP-FFAP,30 mm×0.32 mm×0.25 μm),药物透皮扩散试验仪(型号:RYJ-6B,上海黄海药检仪器有限公司)。
桉叶油醇(95.0%,分析对照品,CAS:470-82-6,C10H18O,密度0.9225%,上海麦克林生化科技有限公司),无水乙醇(99.5%,药用级,上海麦克林生化科技有限公司),0.9%氯化钠生理盐水(国药准字:H42020475,规格:0.9%,武汉滨湖双鹤药业有限公司),超纯水。课题组研制的“一种通过低温3D 打印法制备的艾草精油凝胶缓释系统”(已申报发明专利)。
SPF 级12 周SD 雄性大鼠[SCKX(京)2019-0008,北京华阜康生物科技股份有限公司]。
1.2 方法
1.2.1 低温3D 打印蕲艾精油凝胶缓释系统的制备
将聚乙烯醇溶解于90 ~100℃的水中,配制成聚乙烯醇水溶液,于乳化剂水溶液中混入艾草精油制作成乳化配制混合液,然后将降至常温的聚乙烯醇水溶液加入上述混合液搅拌均匀,再装入低温3D 打印机料筒,进行低温3D打印,将打印制备的凝胶重复3 ~5 次冷冻和解冻循环后,获得蕲艾精油凝胶缓释系统。
1.2.2 皮肤制备
SPF 级12 周SD 雄性大鼠,体质量200 ~260 g,10%水合氯醛腹(0.3 mL/kg)行腹腔麻醉,背部皮肤备皮,保证皮肤完整无破损,剪取腰背部皮肤组织约4 cm2,将取下的皮肤平铺于干净的玻璃板上,角质层朝下,剔除多余的皮下结缔组织,再用0.9%生理盐水冲洗干净,展平后置于低温冰箱保存备用(-25℃)。实验前放置于常温中,自然解冻,并用0.9%生理盐水浸泡30 min。
1.2.3 析出实验
将蕲艾精油凝胶缓释系统分别完全浸没在5.5 mL 的20%乙醇生理盐水中,于32℃、35℃、37℃、40℃、42℃,分别恒温浸泡1、2、3、4 和5 h 后,搅拌均匀后用冻存管分别收集浸泡液50 μL,置于-40℃液氮环境冻存备用。
1.2.4 透皮实验
采用药物透皮吸收扩散试验仪(型号:RYJ-6B,上海黄海药检仪器有限公司)进行透皮实验。剪取3 cm2皮肤组织,按照给药池、蕲艾精油凝胶缓释系统、离体大鼠皮肤(角质层一侧朝向给药室)、接收池的顺序依次固定。在给药池和接收池分别加入5.5 mL 的20%乙醇生理盐水,排空接收池空气,使蕲艾精油凝胶缓释系统直接接触给药池液体。实验水浴温度分别设定为30℃、32℃、35℃、37℃、40℃、42℃,200 r/h 恒速搅拌,每个温度分别于不同的透皮时间点(1、2、3、4 和5 h)收集接受池液体50 μL,用冻存管封存,置于-40℃液氮中冻存待测。
1.2.5 气相色谱分析
本实验以桉叶油醇(95%,分析对照品,CAS:470-82-6,C10H18O)为外标物,定位蕲艾挥发油中桉叶油醇的出峰位置。具体步骤:1)取出冻存液,常温冻融后充分摇匀进行气相色谱分析,所有样品冻存时间不超过48 h,防止蔪艾精油有效成分挥发。2)标准溶液配制:称取87.5 mg 桉叶油醇标准品,超声溶解于100 mL 的20%乙醇生理盐水中,配置浓度为831 μg/mL 标准溶液,气相色谱分析测定出峰位置并绘制桉叶油醇的面积-浓度标准曲线(图1)。3)待测样品中桉叶油醇的峰面积(图2),根据标准曲线查得样品中桉叶油醇的浓度(μg/mL)。4)通过对比相同实验条件下析出浸泡液和接收液中桉叶油醇的含量,分析该条件下蕲艾精油凝胶缓释系统的透皮率,透皮率=(透皮吸收液中桉油醇的含量/相同温度相同时间浸泡析出液中桉油醇的含量)×100%。
2 结果
2.1 蕲艾精油凝胶缓释系统析出实验
以20%乙醇生理盐水为溶剂,蕲艾精油凝胶缓释系统随着浸泡时间的延长,桉叶油醇的浓度逐渐降低。就浸泡温度而言,浸泡作用时间相同时,35℃~40℃时蕲艾精油凝胶缓释系统的桉叶油醇析出效果较佳,尤以37℃浸泡液中桉叶油醇的浓度最高。综合温度和浸泡时间,蕲艾精油凝胶缓释系统于37℃恒温浸泡2 h 时,浸泡液中桉叶油醇的浓度浓度最高,为18.6 μg/mL(表1、图3)。蕲艾精油凝胶缓释系统于37℃恒温浸泡2 h 的气相色谱图谱见图4。

表1 不同时间和温度蕲艾精油凝胶缓释系统浸泡析出液中桉叶油醇的浓度(μg/mL)
2.2 透皮实验
在药物透收扩散试验仪(RYJ-6B)的给药池和接收池均加入20%乙醇生理盐水5.5 mL,于32℃、35℃、37℃、40℃、42℃时,恒速200 r/min 分别搅拌1、2、3、4、5 h,收集接收池溶液进行气相色谱测定,气相色谱测定结果见(表 2、图 5)。可以看出蕲艾精油凝胶缓释系统接收池中桉叶油醇的浓度在透皮实验2 h 时浓度最高,之后随着透皮时间的延长逐渐下降。透皮时间相同时,32 ~37℃时该缓释系统的透皮接收液中桉叶油醇的浓度逐渐上升,37℃时接收液中桉叶油醇的浓度最高,而随着温度的上升,接收液中桉叶油醇的浓度又呈下降趋势,呈现倒“U”型趋势。综合透皮的时间和温度因素,蕲艾精油凝胶缓释系统在37℃透皮作用2 h 时,接收液中桉叶油醇的浓度最高,为11.1 μg/mL。该缓释系统于37℃透皮2 h 时接收池溶液的气相色谱图见(图6)。
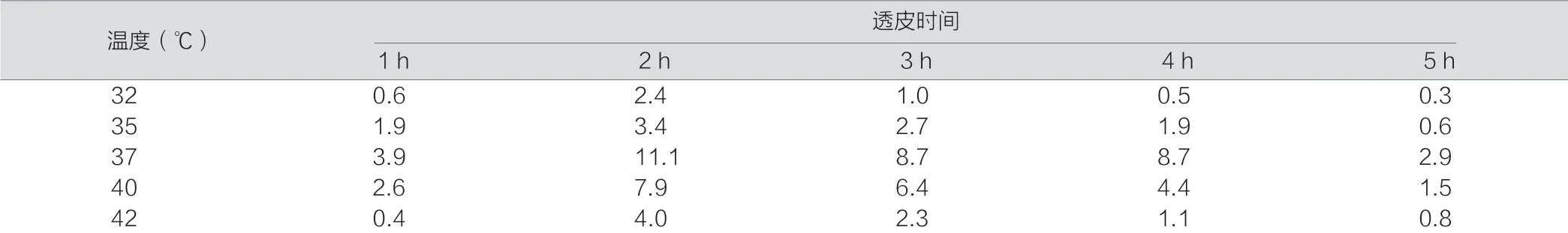
表2 蕲艾精油凝胶缓释系统不同时间和温度时透皮接收液中桉油醇浓度(μg/mL)
2.3 蕲艾精油凝胶缓释系统的透皮率
蕲艾精油凝胶缓释系统的透皮率随温度和作用时间的延长,均呈倒“U”型变化。即温度相同时,随着透皮作用时间的延长,蕲艾精油凝胶缓释系统的透皮率从1 h 开始上升,至2 h 透皮率达最高,之后随着时间的延长透皮效果稳步下降(图7);而透皮作用时间相同时,从32℃开始,随着温度的升高,药物透皮率稳步升高,至37℃透皮效果最好,37 ~42℃时,透皮率逐渐下降(图8)。综合上述结果,在37℃透皮2 h 时,蕲艾精油凝胶缓释系统的透皮率可达59.48%,透皮效果最佳(表3)。

表3 蕲艾精油凝胶缓释系统不同时间和温度的透皮率(%)
3 讨论
3.1 蕲艾精油凝胶缓释系统
艾是我国传统中医药学常用的草本植物,其中蕲艾是具有代表性的品种之一,植株具有浓烈香气,全草入药,有温经散寒、止血安胎等传统功效。有研究通过水蒸气蒸馏法对多个不同产地艾叶进行挥发油提取,发现蕲艾叶的挥发油及桉油精的含量最高[9]。
随着现代材料科学以及生物学技术的发展,艾草精油的提取技术不断改进。王曼笛等[10]发现以纤维素纳米晶为稳定剂制备的Pickering 乳液对艾草精油有很好的缓释作用。翟媛媛等[11]以艾草精油为芯材,以明胶、壳聚糖为芯材制备微胶囊,可以让艾草精油具有良好的缓释性能。
本研究采用自主研发通过低温3D 打印法制备精油凝胶缓释系统,该系统常温下向空气中缓慢释放艾草精油,能够减少艾草精油在制备过程中挥发造成的损失,在使用过程中消除了传统艾灸造成的烟雾和的安全隐患,可通过非接触的方式促进创面愈合,避免了常规水凝胶贴膏剂对创面的刺激。
3.2 气相色谱的测定条件
本研究蕲艾精油析出液的气相色谱测定条件为:柱温60℃,保持2 min,20℃/min 升到120℃,保持3 min,进样口200℃,检测器250℃,氮气流量1 mL/min,氢气流量40 mL/min,空气流量400 mL/min,分流比1 ∶1。为了保证测量结果的重复性,每次实验进样3 次,每次进样量为1 μL,取3 次测量结果平均值为最终测定结果。根据相同的色谱条件下峰面积与桉叶油醇含量成正比的原理[12-13],制订桉叶油醇的峰面积-浓度标准曲线,该标准曲线的R2=0.998,说明曲线的拟合效果为优。根据待测样品气相色谱图峰面积,由标准曲线计算得出待测样本中桉叶油醇的浓度。
3.3 蕲艾精油凝胶缓释系统透皮效果
艾灸药理主要通过药物、温热与近红外光辐射发挥作用[14-15]。本研究主要研究32℃、35℃、37℃、40℃、42℃5 个较高温度下,蕲艾精油凝胶缓释系统的精油成分透皮吸收效果。朱乃甫等[14]发现艾叶精油的透皮吸收效果在透皮作用时间相同时,随着温度的升高,艾叶精油的透皮率大大增加;而温度固定时,透皮作用时间越长,艾叶精油的透皮率越高。其作用机制主要与分子热运动增加、皮肤通道打开、局部血管扩张有关。本研究选择浸泡时间和透皮作用时间分别为1、2、3、4、5 h 时间点来分析蕲艾精油凝胶缓释系统的透皮效果。结果显示,蕲艾精油凝胶缓释系统的透皮率在同一温度下随着透皮时间的变化呈先上升后下降的趋势,在同样透皮时间下,随着水浴温度的升高也呈现先上升后下降的趋势。这与前期研究结论存在差异[14]。这可能是因为在艾叶精油含量一定的情况下,其透皮释放过程是存在峰值变化的,如果持续增加精油的含量来研究温度和时间对艾叶精油透皮作用的影响,其结论是与前期研究相符的[14]。尹彬彬[15]研究艾叶精油的提取实验发现,浸泡时间与艾叶精油得量呈现先下降后逐渐上升然后下降的趋势,认为增加浸泡时间并不能有效提高精油含量随着析出量的增加,艾草中的精油含量降低,这与本研究结论一致。所以,在艾叶精油含量固定的情况下,综合透皮作用时间和温度因素,本课题组研发的蕲艾精油凝胶缓释系统在37℃、透皮2 h 时药物透皮率最大,透皮吸收效果最佳,建议临床应用时,按时更换蕲艾精油凝胶缓释系统,以保证艾叶精油的持续性和高透过作用。
3.4 本研究的应用前景
现有研究认为,高温促进蕲艾精油的透皮吸收主要有三种机制:1)分子的热运动速度随着温度的升高而增快,利于促进精油成分的运动过程。2)皮肤通道间隙随着温度提高可以增加、变大,皮肤的渗透性能增强。3)局部的皮下组织血管随着温度升高发生扩张,血液循环有效加快,促进药物吸收。本研究证实了温度和时间因素对蕲艾精油凝胶缓释系统透皮率的影响,表面温度、时间与艾草精油透皮率均呈倒“U”型变化,证实蕲艾精油凝胶缓释系统在临床透皮应用的最佳温度是37℃,最佳作用时间是2 h。
本研究虽然事先评估了冻存液存放时间对桉叶油醇检测量的影响,确定了冻存液的气相色谱检测时间不超过48 h。但由于样品中桉叶油醇的痕量特点,建议尽可能选择新鲜的接收液或浸泡液进行气相色谱检测,进一步提高结果的准确性。
本实验通过将蕲艾精油凝胶缓释系统浸泡于20%乙醇生理盐水中,研究32℃、35℃、37℃、40℃、42℃,分别恒温浸泡1、2、3、4、5 h 后的析出率,然后用SPF 大鼠模拟人体皮肤,研究蕲艾精油凝胶缓释系统在不同温度的透皮率,该实验条件与临床实用场景相近,便于将基于本缓释系统的产品直接应用于临床实验研究。本课题组研制的蕲艾精油凝胶缓释系统可在常温下向空气中释放艾草精油,但本研究在研究透皮率时,未评估向空气释放后蕲艾精油凝胶缓释系统精油含量的衰减。
本研究前期实验观察到本缓释系统可以通过非接触促进创面或者感染创面的愈合,提示下一步可研究缓释系统通过非接触促进创面或者感染创面愈合的效果,综合分析缓释系统的最佳使用条件。
