眼动脉灌注化学治疗儿童视网膜母细胞瘤
2022-10-25吴长华孙佳丽
王 亮,吴长华,孙佳丽,宋 丹,李 静,张 鑫,郭 磊
(山东大学附属儿童医院血管瘤与介入血管外科,山东 济南 250022)
视网膜母细胞瘤(retinoblastoma, RB)是儿童原发性眼内恶性肿瘤[1],发病率为1∶16 000~1∶18 000[2],我国每年新增患儿约1 100~1 500例[3]。对部分早期RB可采用局部治疗,但对多数患儿则需采用联合治疗。眼动脉灌注化学治疗(intra-arterial chemotherapy, IAC)对中晚期及复发RB疗效较佳,能有效降低化疗药物所致全身不良反应,已逐渐成为一线治疗方法[4-5]。本研究观察IAC治疗儿童RB的效果及其安全性。
1 资料与方法
1.1 一般资料 回顾性分析2017年3月—2020年6月238例于山东大学附属儿童医院接受IAC的RB患儿,男146例、女92例,年龄0.6~99.7个月、中位年龄21.9个月,体质量4.5~45.0 kg、中位体质量12.00 kg;均为单发RB, 136例病灶位于左眼、102例位于右眼;其中182例因白瞳症、36例因斜视就诊,10例为查体发现眼部异常,其余10例则因频繁眨眼、眼球肿胀、屈光异常、视物黑影及视力低下等就诊;72例于本次IAC前曾接受全身化疗、眼局部治疗及IAC等(表1),另外166例未曾接受RB相关治疗;根据国际眼内RB分级标准(A~E期),238例中,C期12例、D期164例、E期62例。本研究通过医院伦理委员会批准;治疗前监护人均签署知情同意书。
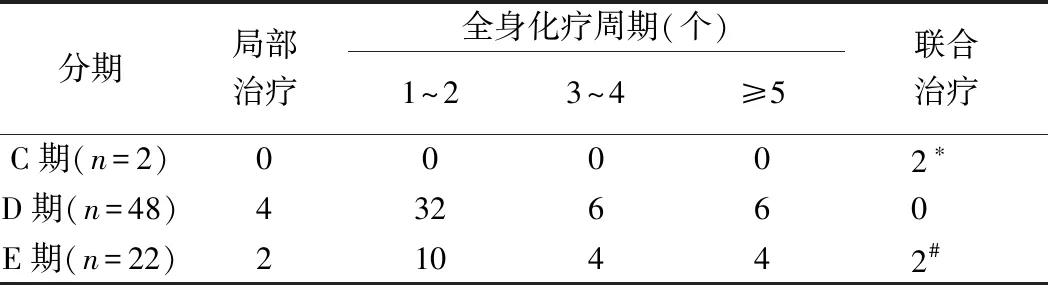
表1 72例患儿既往RB相关治疗方案(例)
1.2 IAC IAC前先行眼底检查(图1A)、眼眶平扫+增强MRI、颅脑平扫MRI及颈部淋巴结超声检查,以明确眼部肿瘤情况,并排除眼外转移。对患儿行全身麻醉,常规以羟甲唑啉喷鼻、去氧肾上腺素湿敷患侧额部及眼睑。采用 Seldinger技术穿刺股动脉并置管,行全身肝素化(肝素75 U/kg体质量);以4F超滑Cobra导管(Terumo)行患侧颈总动脉侧位造影(图2A),并于路图引导下采用1.7F ev3 45°微导管(Micro Therapeutics)超选择性插管至眼动脉开口并行眼动脉造影,观察眼动脉及脉络膜(图2B);之后以2 ml/min流率、按照≤0.5 mg/kg体质量灌注化疗药物美法仑(美法仑∶生理盐水=1 mg∶6 ml),灌注过程中注意观察微导管位置,如发现其离开眼动脉开口处则及时加以纠正后继续灌注。
对出现玻璃体种植者以美法仑联合拓扑替康或卡铂进行灌注;对IAC反应欠佳及临床风险较高者采用美法仑、拓扑替康及卡铂三联治疗方案;遇眼动脉插管困难时,采用颈内动脉球囊阻断法行快速化疗药物灌注(图2C),自球囊开始阻断至灌注结束时间应<4 min;对颈总动脉造影显示眼动脉不清患儿行同侧脑膜中动脉造影,待脉络膜清晰显影后行脑膜中动脉IAC(图2D);对合并渗出性视网膜脱离(retinal detachment, RD)等中晚期RB患儿,行激光光凝术/冷冻术/玻璃体腔注药术等联合治疗。
1.3 疗效评价 IAC期间每2个月复查MRI;记录每次IAC后相关不良反应,包括局部反应(如额部红斑、眼睑水肿、上睑下垂、玻璃体积血等)和全身反应(如消化道反应、骨髓抑制等),并于3~5周后复查眼底检查;如发现RB肿瘤仍存在活性(图1B),则继续行IAC;发现RB肿瘤完全钙化(图1C)或无活性时结束IAC。
2 结果
IAC前,12例C期RB患儿均未见其他明显眼底表现;164例D期RB患儿中,4例合并单纯玻璃体混浊(vitreous opacity, VO),48例合并单纯RD,4例合并单纯玻璃体积血(vitreous hemorrhage, VH),8例合并RD+VH,4例合并VO+VH,2例合并RD+VO;62例E期患儿中,12例合并单纯RD,7例合并单纯VO,2例合并单纯VH,13例合并RD+VO,12例合并RD+VH,2例合并VO+VH,2例合并VO+RD+VH。
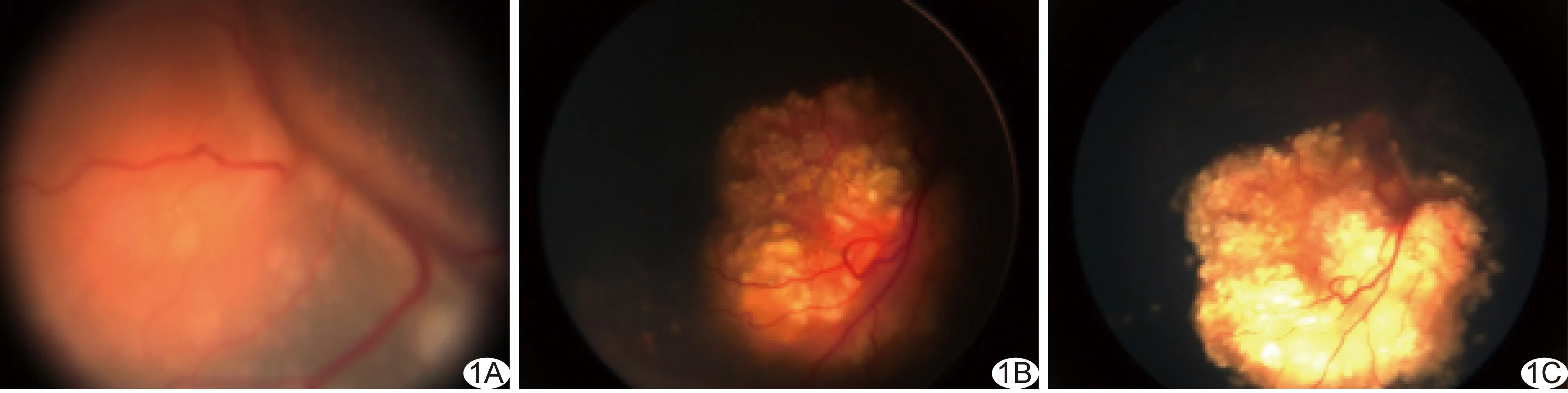
图1 RB眼底检查图 A.IAC前眼底图示巨大肿瘤; B.首次IAC后1个月,眼底图示肿瘤大部分钙化; C.第3次IAC后1个月,眼底图示肿瘤完全钙化
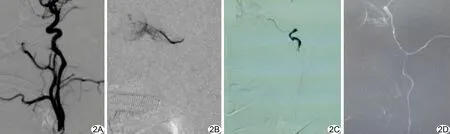
图2 造影图示眼动脉IAC A.右侧颈总动脉侧位造影图; B.以微导管超选择插管至右眼动脉开口处后,造影显示眼环; C.以球囊导管阻断左眼动脉远端颈内动脉,于其近端造影显示眼环; D.右侧脑膜中动脉造影显示眼环
238例患儿共接受692次IAC(其中92例联合眼局部治疗),每例1~6次、中位次数3次;其中682次经颈内动脉行眼动脉超选择插管(4次插管失败,后行颈内动脉球囊阻断灌注化疗),成功率99.41%(678/682),10次经脑膜中动脉灌注;140次采用美法仑单药灌注,472次采用美法仑联合拓扑替康,20次采用美法仑联合卡铂,60次采用三联治疗。插管过程中,18例出现36次支气管痉挛样反应(均为颈内动脉-眼动脉超选择插管),表现为呼吸道阻力增加及呼吸末CO2迅速下降,继而出现血氧饱和度降低、心率升高及血压降低等;予肾上腺素后症状缓解。
692次IAC中,68次(9.83%,68/692)出现骨髓抑制,其中轻、中度(Ⅰ、Ⅱ、Ⅲ级)48次(6.94%,48/692)自行好转,重度(Ⅳ级)20次(2.89%,20/692)均行粒细胞集落刺激因子治疗后好转;出现消化道反应80次(11.56%,80/692),主要表现为呕吐,约1~5次/日,予甲磺酸多拉司琼治疗后好转。238例中,IAC后86例出现眼睑水肿,58例出现VH,42例眼球内陷(6例因内陷明显而后选择摘除眼球),30例见额部红斑,RD及上睑下垂各4例。
IAC结束后共随访2~43个月,平均(25.31±8.86)个月。随访期间,36例接受眼球摘除,202例(84.87%,202/238)患眼保留;保眼率在C期患儿中为100%(12/12),D期84.15%(138/164),E期83.87%(52/62),首次接受治疗患儿保眼率86.75%(144/166),既往曾接受相关治疗保眼率80.56%(58/72)。随访期间所有患儿均未见明确新发转移。
3 讨论
GOBIN等[6]尝试于眼动脉插管灌注化疗药物,即以IAC治疗RB,成功率达98.46%(255/259)。IAC本质为局部化疗,主要通过介入技术直接将化疗药物灌注至肿瘤供血血管,已广泛用于治疗恶性肿瘤[7-8]。据报道[9],首次接受IAC的单侧眼内RB患儿的保眼率为78.7%;且有学者[5]认为IAC对复发RB疗效同样显著。
STATHOPOULOS等[10]报道,IAC时将微导管插管至眼动脉开口处或通过颈外动脉途径灌药可降低脉络膜并发症风险;QUINN等[11]建议,IAC时若超选择插管至眼动脉失败,可采用球囊导管阻断颈内动脉远端或经脑膜中动脉途径灌注化疗药物。本研究采用同样方法行眼动脉IAC,228例患儿于超选择眼动脉插管后造影见脉络膜显影, 10例未见脉络膜显影,后于超选择插管至颈外动脉-脑膜中动脉后造影见脉络膜显影;IAC后RB患儿总保眼率达84.87%(202/238),且首次接受IAC者的保眼率(86.75%)略大于此前曾接受相关治疗者(80.56%),分析原因,可能主要在于本组对中晚期RB患儿加用其他方法联合治疗,且部分患儿经本次IAC治疗后瘤体大部分已灭活,后仅需接受玻璃体切割术而提高了保眼率。
本研究IAC插管过程中,18例共出现36次支气管痉挛样反应,且多发生于第2次及其后IAC中,常出现于微导管/微导丝刺激眼动脉附近区域或眼动脉定位造影时,而未见于药物灌注过程中,与既往研究[6]相符;且均于接受肾上腺素治疗后缓解,之后亦未见明显相关不良反应。
IAC后全身不良反应包括骨髓抑制及胃肠道反应等,程度较全身化疗后不良反应为轻,且多为自限性,即可于治疗结束后自行恢复。有学者[12]指出,IAC后全身不良反应发生率均不足20%。本组患儿IAC后消化道反应及骨髓抑制发生率分别为11.56%及9.83%。IAC后局部不良反应包括眼周水肿和充血、上睑下垂、局部睫毛脱落及前额红斑等,主要与眼动脉分支有关,可通过羟甲唑啉喷鼻、去氧肾上腺素湿敷患侧额部或眼睑等收缩局部血管等方法加以预防。此外,药物刺激肿瘤滋养血管或肿瘤钙化收缩过快可导致VH[13],可通过降低术中灌注药物浓度、减缓灌注速度等降低其发生率。眼球内陷与IAC后眼球及眶周灌注减少导致眼球及球后脂肪萎缩有关[14];RD则为肿瘤钙化收缩牵拉网膜或视网膜下渗出、积液所致,可于肿瘤灭活后行玻璃体+肿瘤切除及视网膜修复术一并处理。本组患儿IAC后86例出现眼睑水肿,58例出现VH,眼球内陷42例,额部红斑30例,RD及上睑下垂各4例。
综上,眼动脉IAC治疗儿童RB安全、有效,保眼率较高而不良反应较少。但本研究随访时间较短,可能存在偏倚,有待累积更多病例进一步观察。