碳纳米钯的生物合成及其催化性能研究
2022-10-24叶明磊石先阳
叶明磊,石先阳
碳纳米钯的生物合成及其催化性能研究
叶明磊,石先阳*
(安徽大学 资源与环境工程学院,合肥 230000)
将奥奈达希瓦氏菌(MR-1)原位还原形成的零价纳米钯颗粒负载在碳纳米管(CNTs)表面,制备了Pd/CNTs纳米复合材料。用TEM、XPS等多种手段对材料进行了表征,并用对硝基苯酚(4-NP)的还原降解反应评价了Pd/CNTs的催化性能。表征结果表明,钯纳米颗粒(直径2~3 nm)较均匀地分散在CNTs表面;钯负载在CNTs上会造成其拉曼峰强的增大和特征峰的偏移,且结晶度和颗粒数目随着负载量的增加而增加。性能评价表明,Pd/CNTs对4-NP还原降解具有较高催化性能,较其催化效率较单一的CNTs降解效率提高了6.3倍;在pH = 10的条件下,5% Pd/CNTs催化18 min可将4-NP降解99.5%,经6个反应循环后对4-NP的去除率仍保持在95.2%。
化学催化;细菌还原;碳纳米钯;表征;催化性能
对硝基苯酚(4-NP)是一种毒性高、生物降解难的污染物,其在水体中可通过食物链富集效应而对人体健康和环境产生不利影响。含4-NP废水的高效处理日趋受到关注[1]。4-氨基苯酚(4-AP)作为4-NP的还原产物,具有毒性相对低、易降解的特点,在工业生产中可作为止痛剂和退热剂合成的中间体。通过将4-NP转化为4-AP可以实现4-NP的高效处理与资源化利用[2-3],这其中的关键是需要高效的催化剂。
现有将4-NP转化为4-AP的催化剂存在催化效率不高的缺陷。纳米催化剂可有效地降解许多结构稳定的有机污染物,使其变为无毒、无害小分子无机物[4]。以比表面积大和孔分布均匀的碳纳米管(CNTs)为催化剂的载体,具有卓越的化学稳定性和良好的电子传输性能[5]。另一方面,具有表面效应、量子尺寸效应、小尺寸效应和宏观量子隧道效应等多重特殊性质的贵金属纳米颗粒(NMNPs)也呈现出独特的电子和催化性能[6-7]。研究表明,NMNPs与CNTs形成的复合材料兼具二者单体的优良性能[8]。
相对于纳米材料的化学法合成[9-10],采用具有还原能力微生物原位合成的纳米材料具有反应条件温和、可避免有毒有害的副产物的产生、反应的过程易操控等优点[11-14]。奥奈达希瓦氏菌(,)的还原能力优于其它大部分还原微生物,在合成零价贵金属纳米颗粒方面具有优势[15-17]。厌氧环境下,可将细胞内的碳源进行氧化,其所产生的电子可通过细胞周质以及细胞膜上的色素(OmcA和MtrC)所组成的电子呼吸通道传递至膜外的受体上[18-21]。经合成的钯,其加氢、脱卤和还原金属等多种催化活性优于纯化学合成的钯纳米颗粒[22-25]。
本文以MR-1为生物还原剂,将原位还原形成的零价纳米钯颗粒负载在碳纳米管表面,制备出Pd/CNTs纳米复合材料,探究其结构与性能。以4-NP为目标物,考察Pd/CNTs催化剂催化性能,并探究4-NP还原生成4-AP的反应动力学过程。
1 实验
1.1 试剂
碳纳米管(CNTs)、乙醇(C2H5OH)、醋酸钠(NaAc)、二水合硝酸钯(Pd(NO3)2·2H2O)、聚乙烯吡咯烷酮(PVP K30)、乙二醇(EG)、十二烷基苯磺酸钠(SDBS)等均为市售分析纯试剂,水为超纯水。
1.2 细菌培养
MR-1的培养采用Luria-Bertani (LB)培养基和厌氧培养基。其中LB培养基的配比为:1 L纯水中含有10 g酵母粉、10 g NaCl、10 g蛋白胨。pH为7.6的厌氧培养基成分为:NaCl 0.465 g/L、微量元素储备液5 mL、4-羟乙基哌嗪乙磺酸(HEPES) 4.766 g/L、乳酸钠2.242 g/L、MgSO4·7H2O 0.024 g/L、(NH4)2SO40.255 g/L。
将MR-1菌种接种到100 mL液体LB培养基中。在30°C、150 r/min的摇床中避光培养24 h。菌液经6000 r/min离心5 min后弃去其上清液,菌体用厌氧培养基洗3遍后重悬,备用。
1.3 CNTs的预处理
CNTs通过酸化处理去除杂质并使其表面能嫁接亲水基团。将1 g CNTs分散到体积为80 mL的浓硫酸/浓硝酸=3/1 (/)的溶液中,80°C搅拌6 h。经过酸化后的CNTs离心分离后用超纯水洗涤至中性,并在烘箱温度为105°C的条件下烘干,最后将所合成的黑色材料于玛瑙钵体中磨碎备用。
1.4 Pd/CNTs纳米复合材料的制备
将0.1287 g Pd(NO3)2·2H2O加至25 mL 2% SDBS溶液中,磁力搅拌混合均匀;再加入0.3 g PVP和0.8846 g CNTs,连续搅拌3 h。在无菌环境中用2.5 mL注射器将2 mL上述溶液注入装有50 mL厌氧培养基的若干血清瓶中,加入MR-1悬浮液(5×106CFU/mL)后,于30°C、150 r/min摇床中避光连续培养48 h。混合液经5000 r/min离心10 min去除菌体,然后在10000 r/min离心6~9 min,所得产物用去离子水洗涤再离心,重复3次。最后将产物放入65°C的烘箱内干燥24 h后取出,在玛瑙钵内充分研磨,所获得的黑色颗粒用于分析表征。
1.5 分析表征
Pd/CNTs纳米复合材料的形貌、元素组成和晶体结构等分别借助透射电子显微镜(TEM,JEOL JEM-2100),X射线衍射仪(XRD,Rigaku SmartLab 9kW),场发射扫描电子显微镜(SEM,Hitachi S-4800),X射线能量色散光谱仪(EDX,EDAX Octane Super)和X射线光电子能谱(XPS,Thermo Fisher EscaLab 250Xi)检测。吸收光谱用紫外-可见分光光度计(UV-Vis,Perkin-Elmer Lambda 900)测定。
1.6 Pd/CNTs催化降解性能测试
取5 mg Pd/CNTs粉末于50 mL 33.4 mg/L 4-NP溶液中,超声5 min后磁力搅拌0.5 h,使其达到吸附平衡。以足量的硼氢化钠(0.1 mol/L 25 mL)为还原剂进行催化降解实验,每间隔1 min取样2 mL,在10000 r/min条件下离心取上清液测吸光度。实验流程如图1所示。

图1 实验流程图
2 结果与讨论
2.1 材料的形貌和晶体结构
采用SEM、TEM和高分辨率TEM (HRTEM)对CNTs和Pd/CNTs的结构与形貌简写表征,如图2所示。由图2(a)可见,CNTs是一个典型的纳米管结构,管径约40 nm,长度约为1000~2000 nm。采用生物还原法制备的球形、尺寸较小的附于CNTs表面的钯颗粒,其平均直径约为2~3 nm,Pd/CNTs较均匀地分散在CNTs表面(图2(b))。图2(c)中显示出Pd和C的强烈能谱信号,这表明Pd/CNTs主要由C和Pd组成的;C和Pd的质量分数分别为47.87%和32.15%(图中Cu元素峰是由于测试中以Cu网基材背景所致[30])。HRTEM照片(图2(d))显示了PdNPs和CNTs之间的界面区域具有较清晰的晶格条纹,这说明其具有较高的结晶度,晶体已基本形成,负载在CNTs上的PdNPs的晶格间距为0.126 nm。

(a). CNTs-TEM; (b). Pd/CNTs-TEM; (c). Pd/CNTs-EDX; (d) Pd/CNTs-HRTEM
纳米颗粒能被修饰在CNTs上(图2(a))可以解释为:回流处理后的CNTs对PdNPs的生长和分布有利,经HNO3处理产生的大量活性位点(如-OH、-COOH等),这些缺陷点(活性位点)有利于Pd2+的附着;SDBS被裹附在CNTs壁上,因Pd2+带正电,很容易地被吸引在CNTs壁上,经MR-1原位还原形成PdNPs。EDX谱(图2(c))证实Pd/CNTs复合催化剂中仅存在C、Pd和O等3种元素,分别来自于CNTs和PdNPs,表明成功合成了Pd/CNTs复合催化剂。
2.2 Pd/CNTs的XPS分析
为了解Pd/CNTs纳米复合材料的表面化学组成和元素化学态,通过XPS对复合材料进行表征,如图3所示。XPS全谱显示出Pd/CNTs由C、O、N和Pd共4种元素组成(图3(a))。负载在CNTs上的钯在337.9和343.2 eV处的Pd 3d特征峰分别对应于Pd 3d5/2和Pd 3d3/2的结合能(图3(b))。表明所合成的Pd/CNTs纳米复合材料中的钯是以Pd0的形式出现,且两峰的间距为5.3 eV,这证实了钯在Pd/CNTs纳米复合材料中仅存在Pd0这一种形态。

(a). Pd/CNTs; (b). Pd 3d
2.3 Pd/CNTs的Raman光谱
Raman光谱是碳材料检测和表征最常用的手段之一,主要用于表征包括CNTs、石墨等碳材料中的sp2和sp3杂化碳原子。图4为几种不同负载比的Pd/CNTs和纯化后的CNTs的Raman光谱。

图4 CNTs和Pd/CNTs的拉曼光谱。
图4中,CNTs在500~3200 cm-1内有2个特征峰。1341 cm-1是纯化后的CNTs的第一个特征峰,在1341 cm-1处出现的特征峰是碳材料无序诱导的拉曼特征,代表布里渊区K点的A1g声子模式,通常称之为D峰;在1576 cm-1处可以观察到第二个特征峰,在1576 cm-1处出现的特征峰对应于布里渊区域中心的E2g声子震动,是C-C间伸缩振动而产生的,称为G峰。在拉曼光谱中测得的Pd/CNTs的D峰和G峰的强度比明显要低于CNTs,说明钯纳米粒子对复合材料而言,起到减弱表面拉曼效应的作用,且与纯CNTs相比,根据D峰测定结果,2% Pd/CNTs的特征峰偏移了8 cm-1,5% Pd/CNTs的特征峰偏移了11 cm-1,8% Pd/CNTs的特征峰偏移了4 cm-1,10% Pd/CNTs的的特征峰偏移了9 cm-1。负载了钯纳米颗粒的CNTs的1341 cm-1处特征峰发生的细微移动为4~11 cm-1,这说明CNTs上负载钯后会使得多晶CNTs晶体缺陷变少。而在1576 cm-1处的G峰,即CNTs的石墨化结构的波段处,观察到的峰虽未发生偏移,但负载量的增加使峰强不断变大,在负载量为10%时,峰强最大。在2834 cm-1处,整体呈现出随负载量增加而峰强增加的趋势。Raman光谱的变化表明钯负载在CNTs上会造成其峰强增加和特征峰的偏移,并且偏移度在钯负载在CNTs后相对于纯CNTs产生了细微增加[26-27]。
2.4 Pd/CNTs的催化性能
在催化剂作用下,NaBH4将4-NP还原为4-AP:

通过加入的亲核试剂BH4-,电子从BH4-电子供体传递到4-NP离子后通过用氨基取代硝基中的氧,将4-NP还原为4-AP,从而实现对4-NP的还原。采用紫外-可见分光光度计对4-NP溶液在190~500 nm的范围内进行扫描,监测Pd/CNTs的催化性能,结果如图5所示。
4-NP最大吸收波长位于400 nm处(图5(a))。由图5(a)可见,随反应时间增加,4-NP溶液的最大吸收峰逐渐降低;当反应进行到21 min时,5% Pd/CNTs所对应的4-NP在400 nm处的紫外吸收峰几近消失,溶液也近似变为无色,此时4-NP的降解效率为98.5%。空白对照组4-NP的浓度基本没有变化,加入CNTs的降解效率为13.5%,负载钯后的复合材料较单独CNTs催化效率提高了6.3倍。
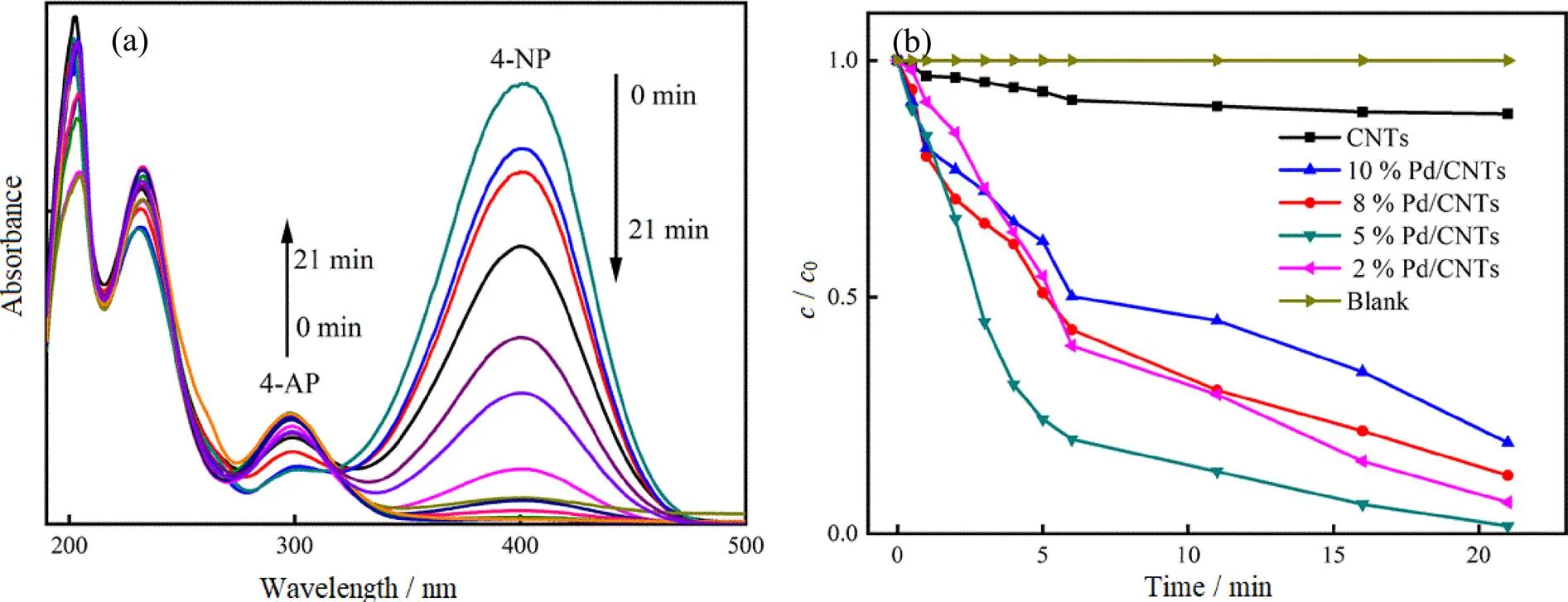
(a). 紫外-可见吸收图谱(UV-Vis spectra), 5% Pd/CNTs; (b). 降解曲线(Degradation curve)
根据图5(b)在不同负载量Pd/CNTs作用下的4-NP的催化降解降解曲线,其最佳的负载量为5%Pd/CNTs,并依此进行后续实验。
2.5 不同pH值下Pd/CNTs对4-NP的催化降解
Pd/CNTs对4-NP进行降解的过程中,pH值会对纳米复合物和污染物的表面状态、电荷特性、表面电势以及聚集特性产生影响,并且在催化反应过程中形成自由基·OH和·O2- [28-30],从而影响Pd/CNTs纳米复合物降解4-NP的效率。因此,通过改变溶液的pH值,评估了生物合成的5% Pd/CNTs纳米复合材料对4-NP催化降解效率,如图6所示。

图6 pH值对5% Pd/CNTs催化降解4-NP速率的影响
图6显示,在pH =10时,Pd/CNTs纳米复合材料降解4-NP的速率最高,当反应时间达到18min时,反应趋于平稳,约为99.5%。当pH值为6~9时,4-NP表面的自由电子更有可能与·NO2上的氧原子一起沉淀,从而阻止4-NP分子与催化剂表面接触,导致·OH和·O2-的形成困难,降低了催化活性。随着pH值的增加,更多的亲水基团被暴露出来,离子间相互作用显著增强,并且在pH值为10时达到了最大值[31]。这归功于NaBH4分解对H+原位生成的促进作用,污染物去除效率更高。当pH值从10上升至12时,4-NP的降解率逐渐降低。这是因为在碱性条件下,去除4-NP时产生的CO2转化为CO32-和HCO3-,而CO32-的增加使得HCO3-增加,HCO3-则降低了纳米复合材料的吸附性能和催化活性,从而阻碍了反应溶液中4-NP的降解[32]。同时,催化剂表面上许多·OH生成的纳米复合物与4-NP之间的范德华力和静电相互作用显著减弱。这也导致了4-NP的去除率进一步降低[33]。所以在强碱或弱酸环境下,纳米复合材料对4-NP的催化活性均未提高。
2.6 Pd/CNTs的重复使用稳定性
使用Pd/CNTs纳米复合材料降解4-NP的优点之一是材料易于从反应混合物中分离出来,可重复使用性是评价催化剂效果重要指标之一。一次催化反应(18 min)结束后,从反应混合物中离心分离回收催化剂,在去离子水中洗涤并在烘箱中干燥,将催化剂再次投入下一反应循环使用,评估Pd/CNTs的重复使用性能。连续6个反应循环的降解率数据列于表1。根据表1结果,循环使用6次后,4-NP的降解率仍保持在95.2%,表明Pd/CNTs是一种较稳定的化学催化剂。
表1 5% Pd/CNTs对4-NP的重复使用催化降解率(pH=10)

Tab.1 Catalytic degradation rate of repeated use of 4-NP by 5% Pd/CNTs nanocomposites (pH=10)
3 结论
1) 用MR-1在CNTs表面原位还原Pd2+合成了Pd/CNTs纳米复合材料。表征结果表明,近似球形的纳米钯(PdNPs,粒径2~3 nm)以稳定的方式固定在CNT载体表面上。
2) Pd/CNTs纳米复合材料对4-NP的NaBH4还原降解具有较高的催化性能。在中性环境下,反应进行到21 min时,对初始浓度为33.4 mg/L的对硝基苯酚的降解效率为98.5%,较纯CNTs效率提高了6.3倍。反应宜在弱酸或碱性环境下进行,pH=10时催化性能最佳。钯负载量为5%的Pd/CNTs催化性能较优。
3) 在pH = 10的条件下,5% Pd/CNTs纳米复合材料对4-NP还原降解效率在18 min时达到了基本完成反应,催化效率为99.5%,经6个反应循环后对4-NP的去除率仍保持在95.2%。
[1] 陈晓伟, 刘璐. MoS2上Cu2O的担载及催化性能研究[J]. 哈尔滨师范大学自然科学学报, 2021, 37(3): 66-70.
CHEN X W, LIU L. Cu2O supported on MoS2and catalytic performance on Cu2O/MoS2[J]. Natural Science Journal of Harbin Normal University, 2021, 37(3): 66-70.
[2] EICHENBAUM G, JOHNSON M, KIRKLAND D, et al. Assessment of the genotoxic and carcinogenic risks of pnitrophenol when it is present as an impurity in a drug product[J]. Regulatory Toxicology and Pharmacology, 2009, 55(1): 33-42.
[3] HERVÉS P, PÉREZ-LORENZO M, LIZ-MARZÁN L M, et al. Catalysis by metallic nanoparticles in aqueous solution: Model re-actions [J]. Chemical Society Reviews, 2012, 41(17): 5577-5587.
[4] 李蓉. 含铁类水滑石催化高效液相氧化有机废水研究[D]. 西安: 西安工业大学, 2019.
LI R. Study on high performance liquid phase oxidation of organic wastewater catalyzed by iron-containing hydro- talcites[D]. Xi’an: Xi’an Technological University, 2019.
[5] WU B H, KUANG Y J, ZHANG X H, et al. Noble metal nanoparticles/carbon nanotubes nanohybrids: Synthesis and applications[J]. Nano Today, 2011, 6(1): 75-90.
[6] 王微. 生物法制备纳米钯催化剂及其在铬解毒与产氢中的应用[D]. 北京: 中国地质大学, 2020.
WANG W. Nanoscale palladium catalyst synthesis and its application in chromium detoxification and hydrogen production[D]. Beijing: China University of Geosciences, 2020.
[7] QIN X, XU J, ZHU Z, et al. Co78Si8B14metallic glass: A highly efficient and ultra-sustainable Fenton-like catalyst in degrading wastewater under universal pH conditions[J]. Journal of Materials Science & Technology, 2022(18): 105.
[8] CUI J Y, ZHU N W, KANG N X, et al. Biorecovery mechanism of palladium as nanoparticles by Enterococcus faecalis: From biosorption to bioreduction[J]. Chemical Engineering Journal, 2017, 328: 1051-1057.
[9] 苏文, 杨辉, 董腾达, 等. 纳米硒制备方法研究进展[J]. 食品工业, 2021, 42(1): 280-284.
SU W, YANG H, DONG T D, et al. Progress on the Preparation Methods of Nano-selenium[J]. Food Industry, 2021, 42(1): 280-284.
[10] 牛珠玉, 陈元彩, 胡勇有. 恶臭假单胞菌原位还原Pd(0) NPs对微生物电子传递性能及活性的影响[J]. 环境科学学报, 2018, 38(6): 2320-2326.
NIU Z Y, CHEN Y C, HU Y Y. The study about the influence of-reduced Pd(0) NPs toward bacteria electron transfer and bacteria activity[J]. Acta Scientiae Circumstantiae, 2018, 38(6): 2320-2326.
[11] FRAGOON A, MAMOUN A, FRAH L, et al. Biosynthesis of gold nanoparticle by fenugreek seed (trigonella foenum) extract[C]. International Conference on Computing, 2016, 1(5): 50-55.
[12] ASSUNCAO A, COSTA M C, CARLIER J D. Application of urea-agarose gel electrophoresis to select non-redundant 16S rRNAs for taxonomic studies: Palladium(II) removal bacteria[J]. Applied Microbiology and Biotechnology, 2016, 100: 2721-2735.
[13] 马晓波, 雷育斌, 王明娜, 等. 希瓦氏菌介导纳米材料生物合成及其环境应用[J]. 环境科学与技术, 2014, 37(12): 253-257.
MA X B, LEI Y B, WANG M N, et al. Biosynthesis of nanomaterials bystrainand its application in environment restoration[J]. Environmental Science &Technology, 2014, 37(12): 253-257.
[14] COURTNEY J, DEPLANCHE K, REES N V, et al. Biomanufacture of nano-Pd(0) by Escherichia coli and electrochemical activity of bio-Pd(0) made at the expense of H2and formate as electron donors[J]. Biotechnology Letters, 2016, 38(11): 1903-1910.
[15] KIM D H, KANALY R A, HUR H G. Biological accumulation of tellurium nanorod structures via reduction of tellurite byMR-1[J]. Bioresource Technology, 2012, 125(4): 127-131.
[16] XU H, TAN L, CUI H, et al. Characterization of Pd(Ⅱ) biosorption in aqueous solution by Shewanella oneidensis MR-1[J]. Journal of Molecular Liquids, 2018, 255: 333.
[17] PALLIYARAYIL A, JAYAKUMAR K S, KUMAR N S. A facile green tea assisted synthesis of palladium nano- particles usingrecovered palladium from spent palladium impregnated carbon[J]. Johnson Matthey Technology Review, 2018, 62(1): 60-73.
[18] CLARKE T A, EDWARDS M J, GATES A J, et al. Structure of a bacterial cell surface decaheme electron conduit[J]. Proceedings of the National Academy of Sciences of the United States of America, 2011, 108(23): 9384-9389.
[19] VON CANSTEIN H, OGAWA J, SHIMIZU S, et al. Secretion of flavins byspecies and their role in extracellular electron transfer[J]. Applied and Environ- mental Microbiology, 2018, 74: 615-623.
[20] 李春晓. 非贵金属纳米复合材料微生物合成及其催化性能研究[D]. 合肥: 安徽大学, 2020.
LI C X. Study on Biosynthesis and catalytic performance of non-precious metal nanocomposites[D]. Hefei: Anhui University, 2020.
[21] 谈碧玉, 石先阳. Ag2S/rGO纳米复合材料的细菌还原制备及光电性能研究[J]. 贵金属, 2021, 42(3): 1-9.
TAN B Y, SHI X Y. Study on bacterial reduction preparation and photoelectric properties of Ag2S/rGO nanocomposites [J]. Precious Metals, 2021, 42(3): 1-9.
[22] FONSECA B M, PAQUETE C M, NETO S E, et al. Mind the gap: Cytochrome interactions reveal electron pathways across the periplasm of Shewanella oneidensis MR-1[J]. Biochemical Journal, 2013, 449(1): 101-108.
[23] 张金风. Pd及PdPt双金属纳米颗粒的制备及其电催化性能研究[D]. 上海: 上海交通大学, 2015.
ZHANG J F. The synthesis of pd and pdpt bimetallic nanparticles and the study of their electrocatalytic perfor- mance[D]. Shanghai: Shanghai Jiao Tong University, 2015.
[24] CELEBI M, YURDERI M, BULUT A, et al. Palladium nanoparticles supported on amine-functionalized SiO2for the catalvtic hexavalent chromium reduction[J]. Applied Catalysis B-Environmental, 2016, 180: 53-64.
[25] FREDRICKSON J K, ROMINE M F, BELIAEV A S, et al. Towards environmental systems biology of Shewanella[J]. Nature Reviews Microbiology, 2008, 6(8): 592-603.
[26] DE GUSSEME B, HENNEBEL T, VANHAECKE L, et al. Biogenic palladium enhances diatrizoate removal from hospital wastewater in a microbial electrolysis cell[J]. Environmental Science and Technology, 2011, 45(13): 5737-5745.
[27] YASUHIRO K, KAORI O, NORIZOH S, et al. Bio- reductive deposition of platinum nanoparticleson the bacteriumalgae[J]. Journal of Biotechnology, 2007, 128: 648-653.
[28] LIZAMA C, FREER J, BAEZA J, MANSILLA H D. Optimized photodegradation of Reactive Blue 19 on TiO2and ZnO suspensions[J]. Catalysis Today, 2002, 76: 235.
[29] KHALIK W F, ONG S A, HO L N, et al. Influence of supporting electrolyte in electricity generation and degradation of organic pollutants in photocatalytic fuel cell [J]. Environmental Science and Pollution Research, 2016, 23: 16716-16721.
[30] SAKTHIVEL S, NEPPOLIAN B, SHANKAR M V, et al. Solar photocatalytic degradation of azo dye: Comparison of photocatalytic efficiency of ZnO and TiO2[J]. Solar Energy Mat erial and Solar Cells, 2003, 77: 65-82.
[31] SAAR R A, WEBER J H. Comparison of spectrofluoro- metry and ion-selective electrode potentiometry for deter- mination of complexes between fulvic acid and heavy-metal ions[J]. Analytical Chemistry, 2002, 52: 2095-2100.
[32] ZHANG W B, XIAO X M, AN T C, et al. Kinetics, degradation pathway and reaction mechanism of advanced oxidation of 4-nitrophenol in water by a UV/H2O2process [J]. Journal of Chemical Technology and Biotechnology, 2003, 78: 788-794.
[33] WANG R Z, YANG S K, FANG J, et al. Characterizing the interaction between antibiotics and humic acid by fluorescence quenching method[J]. International Journal of Environmental Research and Public Health, 2018, 15: 1458-1471.
Study on biosynthesis and catalytic performance of Pd/CNTs
YE Ming-lei, SHI Xian-yang*
(School of Resources and Environmental Engineering, Anhui University, Hefei 230000, China)
Pd/CNTs nanocomposites were prepared by in situ reduction of zero-valent Pd nanoparticles formed byMR-1 on the surface of carbon nanotubes (CNTs). The materials were characterized by TEM, XPS and other means, and the catalytic performance of Pd/CNTs was evaluated by the reductive degradation of 4-nitrophenol (4-NP). The characterization results showed that palladium nanoparticles (2~3 nm in diameter) were well dispersed on the CNTs surface. Palladium loading on CNTs will increase the Raman peak strength and shift the characteristic peak, and the crystallinity and particle number will increase with the increase of loading amount. The performance evaluation showed that Pd/CNTs had high catalytic performance for 4-NP reduction degradation, which was 6.3 times higher than that of CNTs alone. Under the condition of pH=10, 5% Pd/CNTs can degrade 99.5% of 4-NP in 18 min, and the removal rate of 4-NP remains at 95.2% after six reaction cycles.
chemocatalysis; bacteria reduction; Pd/CNTs; characterization;catalytic performance
O643.3
A
1004-0676(2022)03-0014-07
2022-02-25
国家自然科学基金项目(51278001)
叶明磊,男,硕士研究生。研究方向:纳米复合材料的生物合成及其应用。E-mail:330926142@qq.com
石先阳,男,教授。研究方向:污染控制与功能材料。E-mail:shixi381@163.com
