吹扫捕集/气相色谱-质谱联用法同时测定食品接触材料及制品中9种苯系物的迁移量
2022-10-22阿文伟黄华军陈燕芬钟怀宁郑建国
阿文伟, 曾 铭, 黄华军, 曾 莹, 董 犇, 李 丹, 陈燕芬, 钟怀宁, 郑建国
(广州海关技术中心 国家食品接触材料检测重点实验室(广东), 广东 广州 510623)
苯及其衍生物称为苯系物, 是极为重要的一类化工原料。常见的苯系物有苯、甲苯、乙苯、异丙苯、丙苯、苯乙烯、烯丙苯、α-甲基苯乙烯、苯乙炔等, 其中苯是目前公认的一级致癌物, 其他几种苯系物对人的神经、造血机能和心血管系统均有明显的毒性和抑制作用[1-2]。苯系物常用作制备塑料、橡胶、纤维等各类日用化工产品的助剂, 因此广泛应用于饮料瓶、果盘和保鲜袋等食品接触材料领域的塑料制品可能含有苯系物, 如饮料瓶、矿泉水瓶、牛奶瓶等包装[3-5]。近年来研究发现, 当含有上述苯系物的塑料制品用作食品接触材料时, 苯系物可能会迁移到所包装的食品中, 通过饮食、呼吸等方式进入人体, 即使在较低浓度下, 也会对人体的造血、免疫与神经系统带来一定损害[6], 进而危害消费者的身体健康。
由于苯系物具有含量低、易挥发等特点, 因此样品前处理方法显得十分关键。目前, 针对苯系物通用的样品预处理技术主要有静态顶空法[7-8]、吹扫捕集法(动态顶空法)[9-11]和固相微萃取法[12-13]等, 其中静态顶空法的效率低、灵敏度和富集效率不高。而吹扫捕集技术适用于挥发性及半挥发性有机物, 此技术无需使用有机试剂, 能够大幅降低对环境带来的二次污染, 加之其富集效率极高、基体干扰小等优点较为突出, 对痕量组分的富集和分析有明显优势。苯系物常见的检测方法以气相色谱-质谱联用法[12, 14-15]、气相色谱法[16-17]等为主, 但上述方法主要针对饮用水、饮料、水体[15, 18]、土壤[19-20]、空气[21-22]等基质。而有关食品接触材料及其制品中苯系物迁移量检测方法的研究尚未见报道。因此, 亟需开展食品接触用塑料中苯系物检测方法的相关研究, 以监测潜在的风险, 确保食品接触材料的质量安全。
吹扫捕集/气相色谱-质谱联用法具有灵敏度高、富集效率强、选择性好和检出限低等优点。本文利用该方法对食品接触材料及制品中苯、甲苯、乙苯、异丙苯等9种苯系物在4%乙酸(AcOH)、10%乙醇(EtOH)和橄榄油模拟物中的迁移量进行研究, 采用选择离子监测(SIM)模式建立了一种适合常见食品模拟物中苯系物迁移量的检测方法。该方法的建立可为食品接触材料相关领域风险监测提供一定的科学依据。
1 实验部分
1.1 仪器与试剂
8890 GC/5977B气相色谱-质谱联用仪(美国Agilent公司);Atomx XYZ吹扫捕集进样器(美国Tekmar公司);HP-INNOWax毛细管色谱柱(30 m×320μm×0. 50μm, 美国Agilent公司);ME204电子天平(瑞士梅特勒-托利多仪器公司);电子移液枪(量程10~200μL, 德国Brand公司);Milli-Q超纯水系统(美国Millipore公司);9种标准物质:苯、甲苯、乙苯、异丙苯、丙基苯、苯乙烯、烯丙苯、α-甲基苯乙烯、苯乙炔均购自Dr. Ehrenstorfer公司;无水乙醇、乙酸、甲醇(HPLC级, Fisher Chemical公司);橄榄油(Macklin公司)。
1.2 标准溶液的配制
1.2.1 标准储备溶液与标准中间溶液以甲醇为溶剂配制9种苯系物质量浓度均为1 000 mg/L的单标储备溶液, 然后用甲醇稀释成质量浓度分别为10、8. 0、6. 0、5. 0、4. 0、3. 0、2. 0、1. 0、0. 50、0. 30、0. 15 mg/L的9种苯系物混合标准中间溶液。
1.2.2 4%乙酸、10%乙醇食品模拟物标准工作溶液准确吸取质量浓度为1. 0、2. 0、4. 0、6. 0、8. 0、10 mg/L的9种苯系物混合标准中间溶液各25μL于50 mL容量瓶中, 用4%乙酸定容, 摇匀后得到9种苯系物质量浓度分别为0. 50、1. 0、2. 0、3. 0、4. 0、5. 0μg/L的标准工作溶液, 移取40 mL标准工作溶液于顶空瓶中上机待测。采用相同方法配制10%乙醇食品模拟物的同样质量浓度系列的9种苯系物标准工作溶液。
1.2.3 橄榄油食品模拟物标准工作溶液准确称取20. 0 g橄榄油于40 mL顶空瓶中, 分别吸取质量浓度为0. 50、1. 0、2. 0、3. 0、4. 0、5. 0 mg/L的9种苯系物混合标准中间溶液20μL于40 mL顶空瓶中, 摇匀, 得到9种苯系物含量分别为0. 50、1. 0、2. 0、3. 0、4. 0、5. 0μg/kg的标准工作溶液。
1.2.4 迁移实验结合样品预期接触食品情况, 确定4%(体积分数, 下同)乙酸、10%乙醇和橄榄油作为食品模拟物, 按照GB 31604. 1-2015[23]进行迁移实验。
1.2.5 条件优化准确移取25μL质量浓度为6. 0 mg/L的9种苯系物混合标准中间溶液于50 mL容量瓶中, 加入蒸馏水定容后摇匀, 配制成质量浓度为3. 0μg/L的标准工作溶液, 依据9种苯系物的加标回收率进行吹扫时间、流量和温度等条件的优化。每个样品平行测试2次, 并设置相同处理过程的空白实验。
1.3 浸泡液的处理
对于4%乙酸和10%乙醇食品模拟物:准确量取迁移实验中得到的食品模拟物40 mL, 添加25μL甲醇, 摇匀后待测;对于橄榄油食品模拟物:准确称取20. 0 g迁移实验中得到的橄榄油模拟物, 添加20μL甲醇, 摇匀后待测。
1.4 吹扫捕集条件
4%乙酸和10%乙醇食品模拟物的关键吹扫条件如下:吹扫温度、流速和时间分别为恒温20℃、40 mL/min和5 min;预脱附温度和脱附温度分别为220、225℃;脱附和烘烤时间分别为2、3 min;烘烤温度为250℃。
橄榄油食品模拟物的关键吹扫条件如下:吹扫温度、流速和时间分别为恒温20℃、40 mL/min和5 min;样品杯温度为80℃;预加热时间为10 min;预脱附温度和脱附温度分别为220、225℃;脱附和烘烤时间分别为2、3 min;烘烤温度为250℃。
1.5 色谱条件
色谱柱:HP-INNOWax毛细管色谱柱(30 m×320μm×0. 50μm);进样口温度:250℃;进样方式:分流进样(分流比50∶1);载气流量(载气为氦气):1. 0 mL/min。升温程序:40℃持续4 min, 以10℃/min升至80℃, 保持0 min;以5℃/min升至120℃, 保持0 min;然后以80℃/min升至250℃, 保持3 min。
1.6 质谱条件
电子电离(EI)方式, 电子能量为70 eV;离子源、四极杆、质谱接口温度分别为230、150、250℃;溶剂延迟时间为2. 0 min;采用SIM模式作为采集方式。9种苯系物的检测参数见表1。
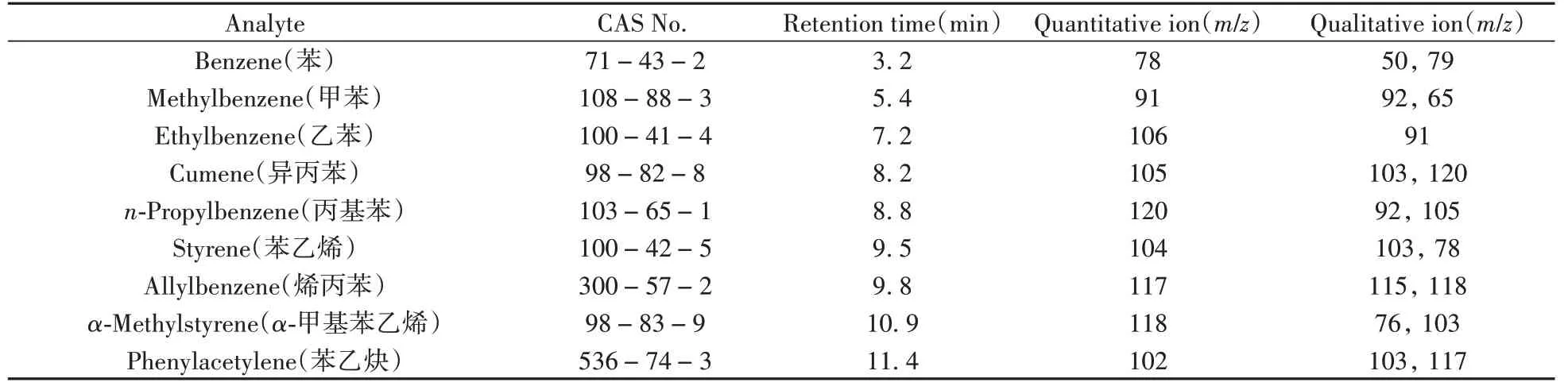
表1 9种苯系物的气相色谱-质谱检测条件Table 1 Analytical conditions of 9 kinds of benzeneseries by GC-MS
2 结果与讨论
2.1 吹扫捕集条件的优化
2.1.1 吹扫时间的影响考察了吹扫时间(3、5、8、11 min)对9种苯系物加标回收率的影响(图1)。由图1可知, 9种苯系物的回收率均可在较短时间内达到75. 0%以上, 继续延长吹扫时间, 9种苯系物的响应虽有提高, 但从食品模拟物中吹扫出来的乙醇、水分等物质会明显增加。综合考虑检测效率及基线噪声, 选择最佳吹扫时间为5 min。

图1 吹扫时间对9种苯系物加标回收率的影响Fig. 1 Effect of purge time on the spiked recoveries of 9 benzeneseries
2.1.2 吹扫流速的影响考察了吹扫流速(20、40、60、80 mL/min)对9种苯系物加标回收率的影响(图2)。由图2可知, 随着吹扫流速从20 mL/min增至40 mL/min, 9种苯系物的回收率从73. 0%提高到93. 0%以上, 但继续增加吹扫流速时, 气体流速太快反而使得捕集阱的富集效率降低。因此, 选择最佳吹扫流速为40 mL/min。
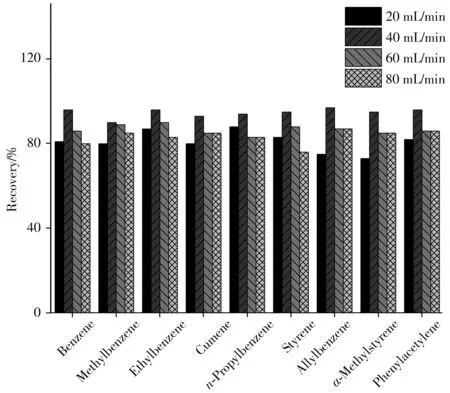
图2 吹扫流速对9种苯系物加标回收率的影响Fig. 2 Effect of purge flow on the spiked recoveries of 9 benzeneseries
2.1.3 吹扫温度的影响考察了吹扫温度(20、40、60、80℃)对9种苯系物回收率的影响(图3)。由图3可知, 吹扫温度从20℃升至80℃时, 9种苯系物的加标回收率均在85. 0%左右, 变化不明显。考虑到仪器能效, 选择最佳吹扫温度为20℃。
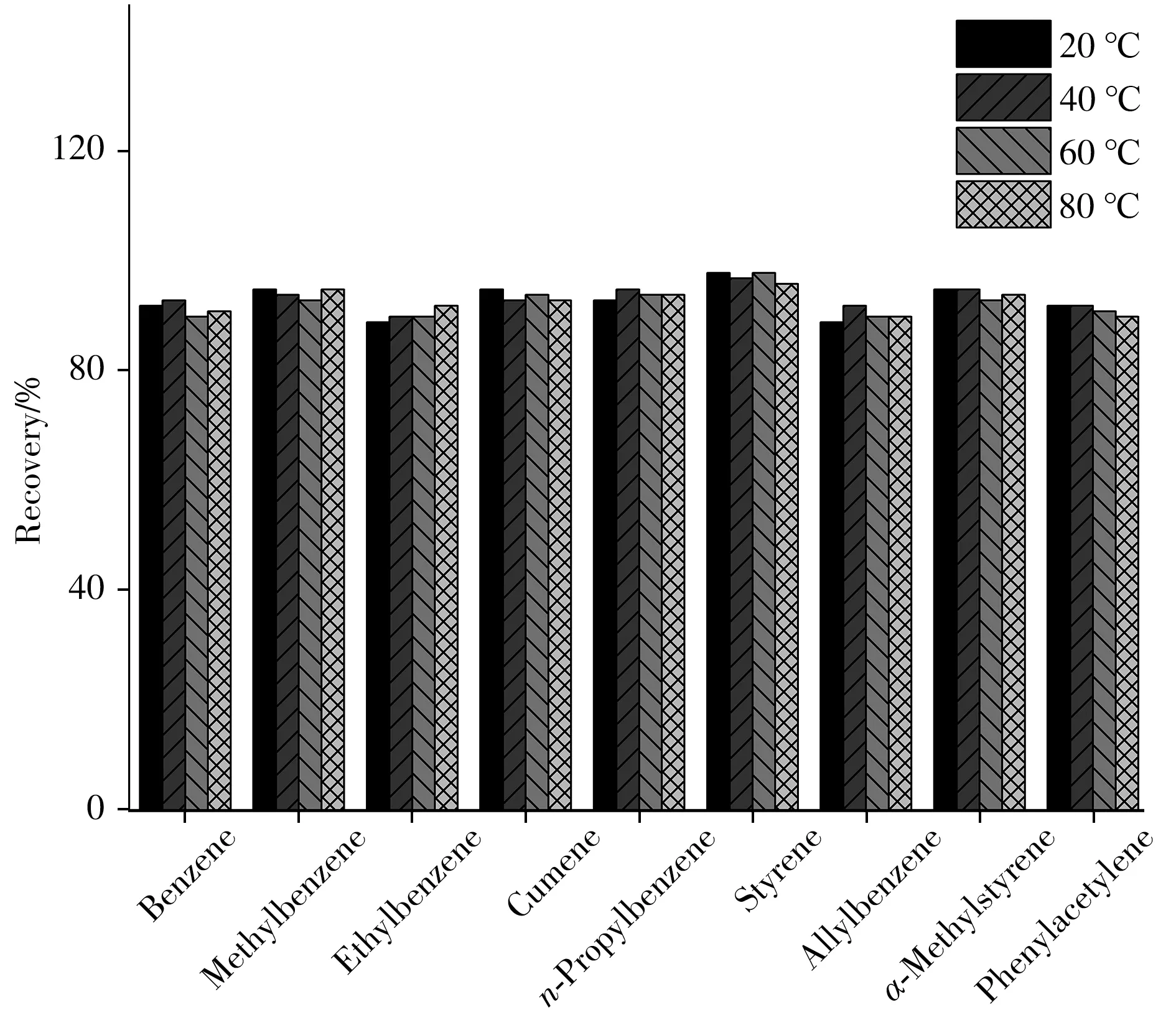
图3 不同吹扫温度对9种苯系物加标回收率的影响Fig. 3 Effect of purge temperature on the spiked recoveries of 9 benzeneseries
2.2 分流比的确定
实验考察了不分流及不同分流比(10∶1、30∶1、50∶1、100∶1)进样时对9种苯系物分离效果的影响。结果表明, 采用不分流或分流比较小时进样, 易造成峰形变差和拖尾;而分流比太大时, 实际检测到的组分量减小, 导致各组分的峰面积逐渐减小, 积分时易引起较大误差。因此, 选择分流比为50∶1。
2.3 色谱柱的选择
考察了9种苯系物 在HP-INNOWax(30 m×320μm×0. 50μm)极性毛细管色谱柱、DB-5MS(30 m×250μm×0. 25μm)中等极性毛细管色谱柱、DB-1(30 m×250μm×0. 25μm)弱极性毛细管色谱柱上的分离效果。结果表明, 9种苯系物在HPINNOWax毛细管色谱柱上的分离效果较好(见图4), 可满足实际检测需求, 这也与文献报道的苯系物多采用强极性色谱柱进行分离一致[24]。因此, 选择HP-INNOWax(30 m×320μm×0. 50μm)极性毛细管色谱柱以获得更好的分离效果。
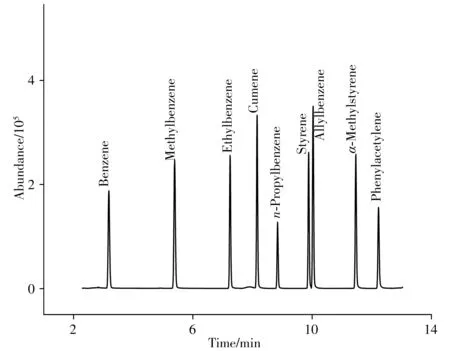
图4 9种苯系物标准溶液(1. 0 mg/L)的选择离子监测色谱图Fig. 4 SIM chromatogram of 9 benzeneseries(1. 0 mg/L)
2.4 线性范围、检出限及定量下限
将相应的食品模拟物系列标准工作溶液按照优化的仪器条件上机进行测定, 取2次测定的平均值完成相关计算。以9种苯系物的峰面积(y)和对应的含量(x, μg/kg或μg/L)绘制标准工作曲线。结果表明, 9种苯系物在0. 50~5. 0μg/kg或0. 50~5. 0μg/L范围内具有良好的线性关系, 相关系数(r2)均不小于0. 995(表2)。取未检出9种苯系物的塑料片材样品作为空白样品进行迁移实验, 取浸泡液进行相应浓度的加标实验, 计算目标峰的信噪比(S/N), 并进行实际验证。进一步结合信噪比S/N≥3和S/N≥10确定检出限和定量下限。结果显示, 9种苯系物的检出限均为0. 15μg/kg, 定量下限均为0. 50μg/kg。
2.5 加标回收率及相对标准偏差
在待测样品的迁移测试过程中, 采用实际塑料片材样品在3种食品模拟物(4%乙酸、10%乙醇和橄榄油)中进行加标实验, 分别在经不同空白样品浸泡的食品模拟物中添加0. 50、2. 0、4. 0μg/kg 3个不同含量的9种苯系物, 每个加标水平单独测定6次(见表2)。由表2可知, 9种苯系物的加标回收率为78. 5%~107%, 相对标准偏差(RSD, n=6)为1. 1%~9. 2%, 表明本方法的准确度与精密度满足分析要求。
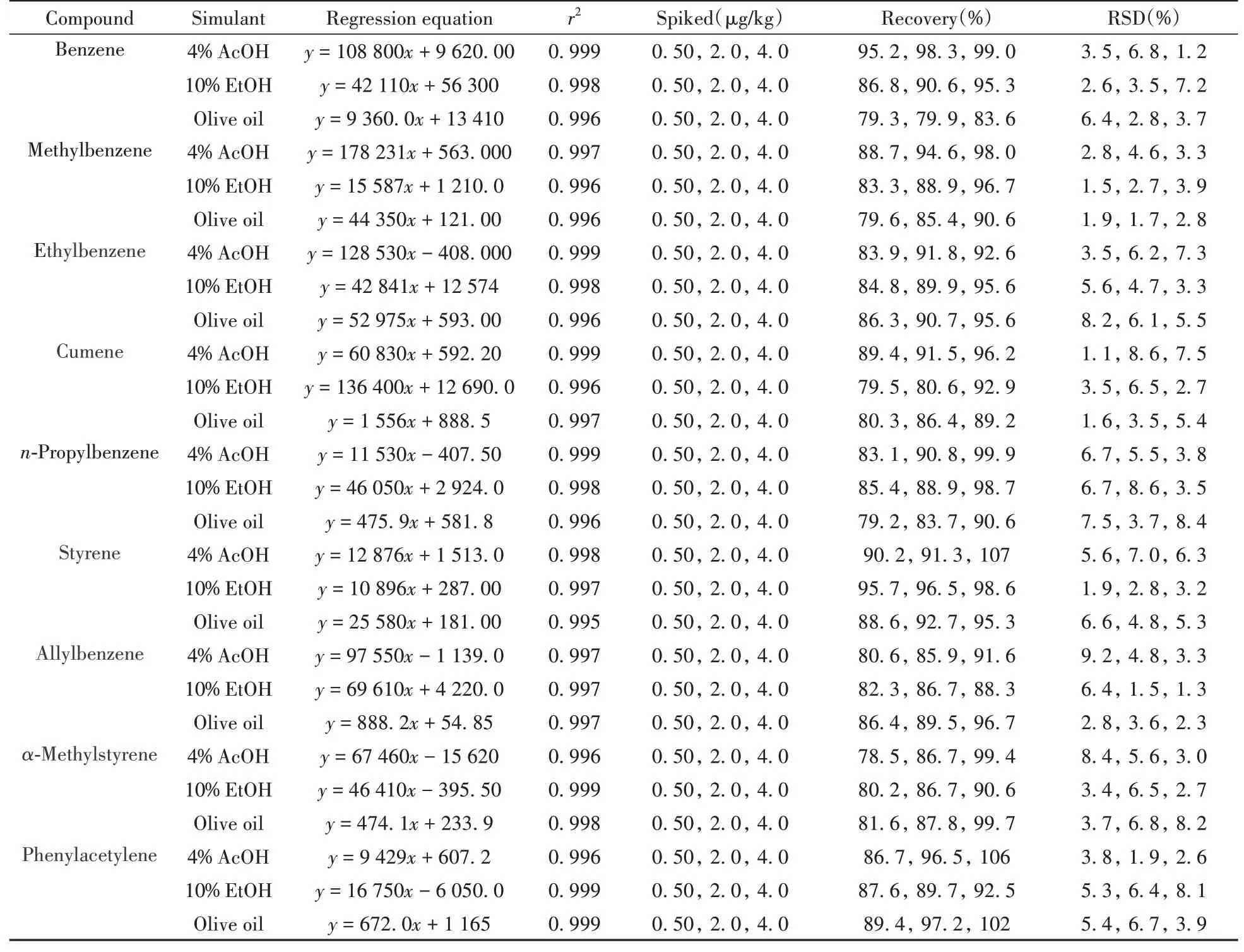
表2 9种苯系物的线性参数、回收率及相对标准偏差Table 2 Linear parameters, recoveries and RSDs of 9 kinds of benzeneseries
2.6 实际样品测定
采用本方法对15批材质为耐冲击性聚苯乙烯(HIPS)的食品接触用塑料片材样品进行检测。结果表明, 以4%乙酸、10%乙醇和橄榄油作为食品模拟物时, 有7批样品中均检出异丙苯和α-甲基苯乙烯, 迁移量为0. 53~2. 9μg/kg;13批样品中均检出苯乙烯和乙苯, 迁移量为0. 82~11. 3μg/kg。阳性样品在4%乙酸模拟物中的迁移量较小, 而在10%乙醇和橄榄油模拟物中的迁移量较高, 可能是由于苯系物不溶于水, 易溶于油脂、乙醇等有机溶剂所致。
3 结 论
本文建立了吹扫捕集/气相色谱-质谱联用测定食品接触材料及制品中9种苯系物迁移量的检测方法, 9种苯系物在0. 50~5. 0μg/kg或0. 50~5. 0μg/L范围内具有良好的线性关系, 检出限均为0. 15μg/kg, 加标回收率为78. 5%~107%, RSD为1. 1%~9. 2%。研究结果表明, 本方法具有操作方便、精确度好、灵敏度高、抗基质干扰效果好等优点, 可应用于食品接触材料及其制品中9种苯系物迁移量的日常检测和风险监测。
